одновременно не означают аминомехил,
подвергают взаимодействию с соответствующим алкилирующим или ацилирующим агентом в соотношении 2:1 с последующим выделением целевого продукта в свободнгом виде или в соли..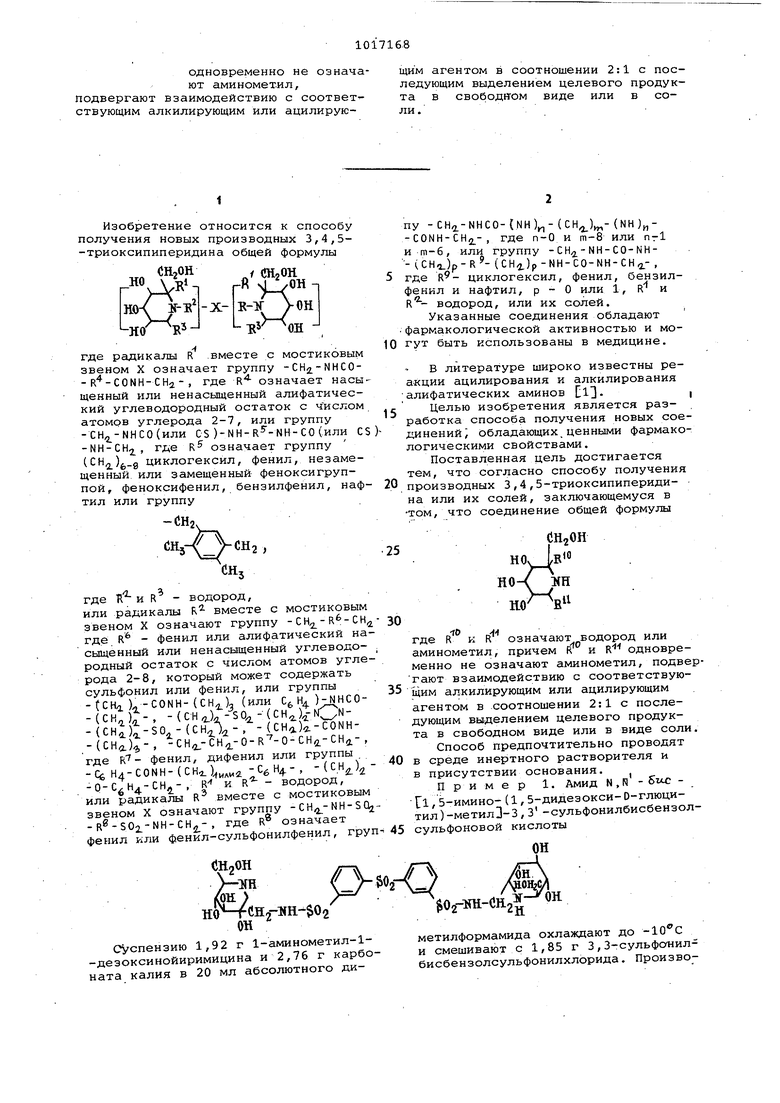



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 3,4,5-триоксипиперидина | 1981 |
|
SU1050563A3 |
| Способ получения производных 3,4,5-триоксипиридина или их солей | 1978 |
|
SU917697A3 |
| Способ получения производных 3,4,5-триоксипиперидина | 1982 |
|
SU1087074A3 |
| ИМИНОСАХАР В КРИСТАЛЛИЧЕСКОЙ ФОРМЕ | 2014 |
|
RU2678085C2 |
| Способ получения производных 3,4,5-тригидроксипиперидина | 1981 |
|
SU1014471A3 |
| Миглустат N-бутил-1,5-дидезокси-1,5-имино-D-глюцит | 2019 |
|
RU2743694C1 |
| ПРОИЗВОДНЫЕ ПИРИДОБЕНЗОКСАДИАЗИНКАРБОНОВОЙ КИСЛОТЫ, СМЕСЬ ИХ ИЗОМЕРОВ ИЛИ ОТДЕЛЬНЫЕ ИЗОМЕРЫ, ИХ ФАРМАЦЕВТИЧЕСКИ ИСПОЛЬЗУЕМЫЕ ГИДРАТЫ И СОЛИ, А ТАКЖЕ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ НА ИХ ОСНОВЕ | 1995 |
|
RU2138504C1 |
| Способ получения производных фенилгуанидина | 1973 |
|
SU489315A3 |
| ПРОИЗВОДНЫЕ 7-ИЗОИНДОЛИНИЛХИНОЛОНА И 7-ИЗОИНДОЛИНИЛНАФТИРИДОНА | 1993 |
|
RU2111964C1 |
| ПРОИЗВОДНЫЕ ПИРИДОБЕНЗОКСАДИАЗИНА, СМЕСЬ ИХ ИЗОМЕРОВ ИЛИ ОТДЕЛЬНЫЕ ИЗОМЕРЫ, ИХ ГИДРАТЫ И СОЛИ | 1994 |
|
RU2131430C1 |
Способ получения производных 3,4,5-триоксипиперидина общей формулы CHjOH G120H гЛ - ц гТ )R«« 1 10 но L s oH-J- CHj- JHj-Ce-ira-tCHilj e - J:H 2-CH2-$02- JH2- iH2-3f - CHj-dH -co-iTR-tCHj)}- , где R - фенил, дифбнил или группы (c.l -Ct,-, tC и R - водород, . или радикалы R вместе с мостиковым звеном X означают группу - CH -NH-SOj - R -SOi-NH- , где R . означает .фенил или фенилсульфонилфенил, группу -CH NHCO- (НН)„-(СН4)„-(МН)„-СОННСН,-, где п-0 и т-В или п-1 и т-6, или группу -Ctt -WH-CO-NH- . -(CHi)(CH)p-NH-CO-NH-CH -, где R. - циклогексил, фенил, бензилфенил и нафтил, р-0 или 1, (Г и R где радикалы R вместе с мостиковым звеном X означают группу - СH -NH-CO-R -CO-NH-CH -, где R - насыщенный или ненасыщенный алифатический углеводородный остаток с числом атомов углерода группу .-ЫН-СО(или CS)-NH-R -NH-CO(или CS)-NH-CHa-, где R - (СН)б-8. W логексил, фенил, незамещенный или за мещенный феноксигруппой, феноксифёнил, бензилфенил, нафтил или груп-№., / где R и а - ввдород, СО или радикалы R вместе с мостнковым е звеном X означают группу . где фенил или алифатический насыщенный или ненасыщенный углеводеродный остаток с числсян атомов углерода 2-8, который может содержать сульфонил или фенил, или группы -CHj-CH -o-CbHt- Hj-, jH4HH-«0-(jH2-6H2 , HiH2-CH2-$Of (JH2-funf o-H -o-CHj-CHj-, водород, или их солей, отличающийся тем, что соединение общей формулы 10 j . где R и R - водород или аминометил, причем R и R

Изобретение относится к способу получения новых производных 3,4,5-триоксипиперидина общей формулы Jll20H /ШгОН , rft 4J yOH-n -Х- В- вз -1 L -gy д где радикалы R .вместе с мостиковым звеном X означает группу -CH2.-NHCO- R -CONH-CH.2 - , где R означает насы щенный или ненасыщенный алифатический углеводородный остаток с числом атомов углерода 2-7, или группу -СН,2 -ННСО(или CS )-МН-Н -ЫН-СО(или C -NH-CHj, где К5 означает группу (СН2)д циклогексил, фенил, незамещенный или замещенный феноксигруппой, феноксифенил, бензилфенил, наф тил или группу где 1 и R - водород, или радикалы R вместе с мостиковым звеном X означают группу - где R - фенил или алифатический на сыщенный или ненасыщенный углеводородный остаток с числом атомов угле рода 2-8, который может содержать сульфонил или фенил, или группы -tCHaL-CONH-CCH) (или )-ДНСО-(CH)J-, -(сн).(сн ьОн-(CHi);;-SO,.-(, -(CHak-CONH.-(СНа)-, ,L-0-R-0-CH,i-CH4-, где фенил, дифенил или группы -Сб Н4-СОМН-(СН-г.идиа -СбЧ, -(СН,) -Q-C/Н -СНл-, R и R водород, или радикалы R вместе с мостиковым звеном X означают группу -CH -NH-SO -R -SOi-NH-CHj.-, где R означает фенил или фенил-сульфонилфенил, гру ((он ,- Н-$02 ОН суспензию 1,92 г 1-аминометил-1-дезоксинойиримицина и 2,76 г карбо ната калия в 20 мл абсолютного дипу -CH,2.-NHCO-(NH)-{CH,j)-(NH)-CONH-CH,j,.-, где п-0 и т-8 или nrl и m-б, или группу -CH,.-NH-СО-NH- (CHt)p-R- (CHi)p-NH-CO-NH-CH2.-, где циклогексил, фенил, бензилфенил и нафтил, р - О или 1, R и R - водород, или их солей. Указанные соединения обладают фармакологической активностью и могут быть использованы в медицине. В литературе широко известны реакции ацилирования и алкилирования алифатических аминов Cl.| Целью изобретения является разработка способа получения новых соединений; обладающих,ценными фармакологическими свойствами. Поставленная цель достигается тем, что согласно способу получения производных 3,4 ,5-триоксипиперидина или их солей, заключающемуся в том, что соединение общей формулы -(.мн где R к R означают водород или аминометил, причем R и R одновременно не означают аминометил, подвергают взаимодействию с соответствующим алкилирующим или адилирующим агентом в соотношении 2:1 с последующим выделением целевого продукта в свободном виде или в виде соли. Способ предпочтительно проводят в среде инертного растворителя и в присутствии основания. Пример 1. Амид N , R - STXC TI ,5-имино- (1, 5-дидезокси- 0-глюцитил)-метилЗ-3,3 -сульфонилбисбензолсульфоновой кислоты Ог-ж-СНг метилформамида охлаждают до -10 С и смешивают с 1,85 г 3,3-сульфанилбисбензолсульфонилхлорида. Производят перемешивание в течение ночи, отсасывают от вьшелившейся соли и сгущают. Остаток/ полученный от упаривания, растворяют в небольшом количестве воды и подают на колонну длиной 120 см и диаметром 4 см, содержаШУЮ в качестве неподвижной фазы целлюлозу и в качестве подвижной фазы ацетон, Элюируют водным ацетоном при возрастаю1цем от 10 до 30% содержания воды. Получаемые фракции исследуют тонкослойной хроматографией. HOHjfi Щ-УП- 50-KH-( 11Н 5,3 г 2-Аминометил-2-оксиметил-3,4,5-триоксипиперидиндигидрохлорида растворяют в 40 мл 1 н. латрового щелока и разбавляют 80 мл метанола. Охлаждают до и по каплям размешивают с раствором из 1,59 мл гексаметилемдиизоцианата в 20 мл уксусного эфира. Перемешивают 18 ч, сгуща ют, поглощают абсолютным метанолом и отфильтровывают от неорганической соли. Фильтрат подают в концентрированном виде на колонну длиной 120 см и диаметром 4 см, содержащую в качестве подвижной фазы целлюлозу и в качестве подвижной фазы ацетон. Элюируют водным ацетоном, при возрас
HOHgC CH2-lfH-CO-(CH2)j-CO-lllbCR2 JSHjOH
Т янrofVoK
м
5,3 г Дигидрохлорида 2-аминомети-2-оксиметил-З,4,5-триоксипиперидина растворяют в смеси из 20 мл воды и 60 мл метанола и смешивают с 8,4 мл триэтиламина. При ледяном охлалсдении добавляют затем каплями . раствор 2,13 мл дихлорида себациновой кислоты в 30 мл уксусного эфира. Перемешивают 3 ч при комнатной температуре, сгущают и в виде водного раствора, фильтруют через колонну ДЛИНОЙ 25 см и диаметром 3 см, содержащую ионит амберлит 1R 400 (ОН -форма). Промывают тщательно водой. Остаток, получаемый от упаривания, подают на колонку длиной 120 см и диаметром 4 см, содержащую в качестве неподвижной фазы целлюлозу и в качестве подвижной фазы ацетон. Элюируют сначала ацетоном, а затем водным ацетоном при возрастающем от 10 до 30% содержании воды. Получаемые фракции исследуют тонкослойной хроматографией. Фракции, содержащие целевой продукт, объединяют и сгущают. Полу
Фракции, содержащие желаемый продукт, объединяют и сгущают.
Получают 0,9 г (24,8%) бесцветной пены со значением 0,57 (силикагельные плиты 60 F 254). Растворитель: смесь метанола, хлороформа и 25%-ного аммиака в соотнсшении 90:60:60. R{ 1-сик1инометил-1-дезоксинойиримицина 0,26.
Пример 2. Бисмочевина N,N -5uc- 5-(1,5-имино-1,5-дидeзoкcи-D-глюцитил)-мeтил -гексаметилена
чают 0,9 г (15,8%) продукта в виде твердой пены с Rf 0,48. Растворитель: смесь метанола, хлороформа и 25%-ного аммиака в соотнсмпении 3:2:2.,
Пример 4. Диамид N,N -вас-Gl-c - (If 5-дидезокси-1,5-имино-0-глюцит-ил)-метил3-себациновой кислоты.
-ян
(Сек
lffi60t K2) Н
он
к смеси 0,5 г 1-аминометил-1-дезоксинойиримицина в 6 мл метанола, 2 мл воды и 0,36 мл триэтиламина добавляют каплями при 0,28 мл
дихлорангидрида себациновой кислоты и 4 мл уксусного эфира. Перемешивают 2 ч при комнатной температуре и отсасывают осадок. Промывают дрпрлнительно уксусным эфиром и сушат.
Твердое вещество растворяют в смеси -HH-CO H СИ2 mr. тающем от 10 до 30% содержании воды. Отдельные фракции проверяют тонкослойной хроматографией на содержание целево го продук та. Фракции, содержащие целевой продукт, объединяют и сгущают. Получают 450 мг (9,4%) продукта в виде бесцветной пены с R 0,33. Растворитель: смесь метанола, хлороформа и -25%-ного аммиака в соотношении 3:2:2. Rf 2-аминометил-2-оксиметил-3,4,5-триоксипиперидина 0,315. , Пример 3. Диамид N,N - Гис- 15-(1,5-ИМИНО-1,5-дидезокси-D-глюцитил )-метил -себациновой кислоты
из диметилформамида и воды (3:1) и осаждают ацетоном.
Выход 0,5 г (42%) продукта с т.пл. 247-250°С, R{ 0,53 на силика гельных плитах (Nr.60,F 254 фирмы Мерк, ОРГ; растворитель: смесь метанола, хлороформа и водного аммиака в соотношении. 3:2:2), R для 1-аминометил-1-дезоксинойиримицина 0,28.
Пример 5. 1,4- N , N-dTuc-(1,5-дидезокси-1,5-имино-0-глюцит)ил -бутен-2
к смеси 2 г 1-дезоксинойиримицина -и 12 мл воды и 12 мл димётилформа/мида добавляют 2 г и каплями при О С добавляют 1,3 т-ntfycLUC-., -дибромбутен-2 в 5 мл диметилформамида.
Температуру медленно повышают до комнатной и мешают 3 ч при комнатной температуре. Затем разбавляют зр мл воды, соли отделяют и водный фильтрат сгущают. Остаток подают на наполненную целлюлозой колонну. Элюируют сначала смесью ацетона и воды в соотношении 9:1, затем смесью ацетона и воды с соотношении 8:2 и, наконец, смесью ацетона и воды в соотношении 7:3. Полученные фракции исследуют тонкослойной хроматографией (растворитель: смесь метанола, хлороформа и водного аммиака в соотношении 3:2:2). Фракции, содержащие целевой продукт, объединяют и сгущают.
Выход 0,9 г (38,4%) продукта с значением Rf 0,35 (на силикагельных плитах Nr.GOF 254 фирмы Мерк, ФРГ;
растворитель: смесь метанола, хлороформа и аодного аммиака в соотношении ). R для 1-дезоксинойиримицина 0,51.I
Пример 6. ji, э -CN.N -б-кс-(1,5-дидезокси-1,5-имино-0-глюцит)-илЗ-диэтилсульфон
ен2он -dHj-CHj-- $02-СН2- %-ir
Ш1
5 ох
6,52 г (40 ммоль) 1-Дезоксиной иримицина растворяют в смеси 60 мл этанола и 30 мл воды и после добав0 л1ения одной капли концентрированного натрового щелока охлаждают до 0-5 С. Добавляют 2,3 мл ( квлоль) дивинилсульфона и затем перемешивают 48 ч при комнатной температуре.
5 Сгущают, растворяют в небольшом количестве воды и подают на колонну длиной 120 см и диаметром 6 см, содержащую в качестве неподвижной фазы целлюлозу и вкачестве подвижQ ной фазы ацетон. Элюируют водным ацетбном при возрастающем от 10 до 25% содержании вода,
Получаемые фракции исследуются - : тонкослойной хроматографией. После .ч отделения побочных фракций получают желаемое соединение элюированием смесью Из ацетона и воды в соотношении 7:3. Фракции,. содержгицие чистый продукт, объединяют и сгущают. Получают 4,6 г (42,5%) бесцветнсэй пены с
0 R 0,33 (растворитель: смесь метанола, хлороформа и 25%-ного аммиака в соотношении 3:2:2); R{ для 1-дезоксинойиримицина 0,52.
Пример 7. Бистиомочевина
5 N , N-бисСз-(1,5-ИМИНО-1,5-дидезокси-0-глюцитил)-метилЗ-гексаметилена
HOHjd CHj-iJrH-CS-KH-lCHaV lbCS-NH-CHa CiiaOH шшгХ4
но
он
5,3 г Дигидрохлорида 2-аминометил-2-оксиметил-З,4,5-триоксипиперидина растворяют в смеси 180 4Л метанола и 60 мл воды и последобавт ления 5,6 мл триэтиламина добавляют по каплям при раствор 2,0 г гексаметилендииэотиоцианата в 60 мл . уксусного эфира. Перемешивают 24 ч при комнатной температуре, сгущают и рартворяют в небольшом количестве смеси метанола и воды в соотношений 8:1. Фильтруют через короткую коЩГ -ОН
он
лонну, содержащую ионит амберлит
1R 400 ОН-формы, и тщательно промывают смесью метанола и воды в соотношении 8:1. Фильтрат сгущают, растворяют в небольшом количестве смеси метанола и воды (8-:1) и подают на
колонну длиной 100 см.и диаметром 4 см, содержащую в качестве неподвижной фазы целлюлозу и в качестве подвижной фазы ацетон. Элюируют сначала смесью ацетона и воды в соот
ношении 9:1, затем смесью ацетона и
воды в соотношении 8,5:1,5 и, наконец, смесью ацетона и воды в соотношении 8:2. Получае1«яе фракции исследуют тонкослойной хрсялатографией на силикагёльных плитах (растворитель: смесь метанола, хлорофохжа и 25%-ного аммиака в .соотнсж ении 3:2:2, Фракции с чнСяым продуктом объединяют и С1 }щают. Подучают 1,4 г (27,5% j продукта со значением Rf О, 56. R$ 2-аминеяаетил-2-оксиме тил-3,4,5-триоксипиперкдив дигидрохлорида 0,34. Растворитель смесь метанола, хлороформа и 25%-ного акмиака зз кОличественн соотношении 3::2:2.
Призер 8. l,6-tN, . - (1,, 5- дидезокси-1,5-ймино 0-глюцит) -илЗ- н-гексаи
енгШ
1Г-Й15Г№ К2
т
т
К смеси 5 г 1-деэоксинойиримидина в 50 мл диметилформамида при 20 С добавляют 2,5 г К,СО и 4 г 1,б-дибрсмгексана. Нагревают до . 100 С и перемешивают 15 ч с последую1цим удалением диметилформамида в вакууме. Остаток подают на колонну, наполненную целлюлозой. Элюируют сначала смесью ацетона и вода в соотношении 9:1, затем смесью ацетона
и воды в соотн %1ении 8:2 и, наконец, смесью ацетова и водщ в соотнсяоении 7:3. Полученные фракции исследуют на снликагельвых плитах тонкослойной хромато1 рафией. Растворитель: смесь
метанола, хлоЕЮфОЕма и водного аммиака в соотносоёнии 3:2:2. Фракции, содержайщие желаемое соединеиие, объединяют нсгуц т. R 0,525 (на силикагелышх плитах Кг. 60 F 254 фирмы Мерк, {растворитель: метанола, хл юформа и водного еалвя ка в соотжмоевии 3:2; 2), R{ для 1-дезркеиЫ4 йирю« дана 0,53.
--шхоД:4,8% .-; - -.
П р н м ё р 9. ДигидаохлоЕЖд
N,S -ф1Сг11 2(1,5-имиио-1,5-дидезокси-В-ггвоиеитил }-метилЗ-венэоя-1 г 3 Ешсульфстдшша
Смесь 2,95 г 1-дезоксинойир«мицина с 5 г карбоната.калия и 2,9 г Бис- (2-бромэтокси )-бёнзола перет(лешивают 5 ч в 25 мл абсолютного да1 метилформамида при . Отсасывают в горячем состоянии-, фильтрат сгущают. Остаток, получаемый от упаривания, растворяют в небольшом количест не смеси метанола и воды (9:1) и очищают в колонне, наполненной целлюлозой с ацетоном. После перекристаллизации из воды получают 1,1 г (12,2%) бесцветных кристаллов с 226-228с.
Диалогично примергш 1-9 получают слёдухяа е соединения. При этом ft$ определяют описанным в примере 1 образом.,
П р и ме р 11. l,5-6w:CN,N -(1,5-ИМИНО-1,5-дидезокси-0-глюцитйл)-пентан(Ж
60
eHjon
2- ai2-eH2-eHf СН2-
&S Выход 14%, т.пл. 18&-187°С (из метанола J. Пример 12. Бисмочевина N, l-od- (1,5-дидезокси-1,5-им но-D-глюцитил)-метил -гексаметилен СЯ}«М«Н lir Clli-jrH-CO-KH-(H2)e-™- 2 вн- ...и 5 0,39, выход 18%., Пример 13. l,B-Suc- N,N -(1,5-имино-1,5-дидезокси-D-глюцитил )3 - н-октан CHjOH F VoHjOt -CHj-KJH le-CHjR 0,63, выход 21%.. П р и м ер 14. Диамид N,N -Suc -.5- (1,5-ИМИНО-1,5-дидезокси-D-глю цитил )-метилЗ-янтарной кислоты CHj-lfHHJe-tCHj jHJO-HH-Cttj CUjOH У-кн4 Л и ейон Rf 0,2; выход 17%. П р и м-е р 15. Диамид N,N -Es-(1,5-ИМИНО-1,5-дидезокси-D-глю тил )-метил -глутаровой кислоты ИОНг CHj-TJH-CO-iCHj j-CO-UH-CHj CHjOH У-ьнHN-XQH онон R 0,23, выход 13,4%., Пример 16. Диамид N,R -fttc -Г5-(1,5-ИМИНО-1,5-дидезокси-D-глю тил) -метил 3-адипиновой кислоты Л0и, (П-СО-(Мз), СНаО . R 0,3; выход 17%. Пример 17, Диамид N,N-6u (1,5-имино-1,5-дидезокси-D-глю цитил)-метил -пробковой кислоты НОН,С (Mj-3«tt-(0-(CHiV le-Htt- Hj. СНлОН ОН Rr 0,41; выход 18,5%. ЛЬЛЛ1 Л1 JL и , I р 18. Диамид N,N -бтад П ,р и м е 5- (1, 5-ИМИНО-1, 5-дидезокси- D-глюц тил)-метил -азелаиновой кислоты ОН.С СИ4-ИНгСО-(Нг1г 0-«И-СНл CHjOH -йл. г 0,47; выход 11,5%. и м е р l Mfli ,N - -исГ . ,,Н (1,5-дидезокси-1,5-иминo-D-глюцит)илj-П-ксилолR/ 0,53, т.пл. 280-281С (из меанола); выход 43,8%. , Пример 20. N, N -5 tcL5-(1,5имино-1,5-дидезокси-D-глюцитил)метилЗ-4,4-окси-бисфенилмочевина оя,с «iij-HR-CO-uiK вн-со-инчн, -TIH R 0,51, выход 18%. Пример .21. С,- ffcct5- (1,5имино-1,5-дидeзoкcи-D-глюдитил)метил -фенилен-1,4-Ьисмочевина OHjC СНв-ЯН-СО- Н-СО- Н- Н2 , - чОН Rr 0,3; выход 20%.. .| 1, V Пр И М е р 22. ЫЕ5-(1,5имино-1,5-дидезокси-D-глюцетил)метил -(4,6-диметилфенилен-1,3-меилен-бисмочевина) лон,с н,-1щ-С(ыга-€Нг eHv-BH-eo-HH-CH, «K,OH Rr 0,48, выход 26,7%. Пример 23. N,N - tccLs-(l,5иминo-l, 5-дидезокси-D-глюцитил )3 -диенил-метан-4,4-бисмрчевина OHjC ji, eHi/ V H-« -nH-CH ,«1цон Л 1/inr-iAtt Rr 0,55; выход 8%. . Пример 24. N.N - ticLl-ct(1,5-дидезокси-1,5-имино-D-глюциил)-метил -1,4-бисуреидоциклогексан CHgOHон l -|TjrЛ k / Ш)/-у/POHjC О СНгТЯШЮМКД /HHtfONHCHg - OH ОН Выход 18,2%, т.пл, (из из пропанола). , . Пример 25, N,N -5acCl-oL-(1,5-дидезокси-1,5-имино-О-глюцитил)-метил -4,4-бисуреидодифенилметан . он W«X// V мнсонн сн, НО -CHj-UHCOHH- J к . :. т. пл. 239С (из изопропанола) выход 47%. П р и м е р 26. N.N -SacCl-ot- (1,5-дидезокси-1, 5-имино-р-глюцитил)-метил -,3-фениленбисмочевина .инсокнсн CHj tttCOXHCHj3r--eH ва т. пл. 235с (из изопропанола) , вьлход 29,7%. Пример 27. N, Г1-06. -(1,5-дидезокси-1,5-имино-0-глюцитил)-метил 1-о,о -бисуреидо-м-ксилол мК/Ы тнкюянсн, сн jUHConHflHjV- т RI 0,28; выход 27,9%. Пример 28. N, .c,;i-ot-(1,5-дидезокси-1,.5-имино-0-глюцитил)}-метил -1, 5-бисуреидонафталин CHjOH J i«iо , ,1ГНСОИН -11НС011НСН2
т.пл. (из метанола/ , выход
60,6%.14
Пример 29. N,N - 5iic l-ci-(1,5-дидезокси-1,5-имино-О-глюцитил)-метил -1,4-фениленбисмочевина
JLMH кон
HO -fCHoiiHConH-C Укнеоинсн-тН он Rr 0,21, выход 29,4%. л,:7,чо .. . им е р 30. Диамид N,N .. X л гч ЛЛиАКЛ -(1,5-дидезокси-1,5-имино-О-глюцит-ил -пропионовая кислота;) -тримети -irCH2«fjCe«H{CHj),NHCeCH2 H2- - 0 Ш онон
Х.пл. (из изопропанола) (разл.), Rr 0,25; выход 36,9%., Пример 35. .Диамид N,N .c -l5-(1,5-ИМИНО-1,5-дидeзoкcи-0-глюцитил)-мeтилЗ-фyмapoвoй кислоты
ИОНг jJHjSHiSO Н У-Ж
МН ИCOSHCH.
H0 -fНК Н
Rr 0,45, т.пл. 254°С (из кзопропа ла;, выход 19,5%. Пример 31. Бисамид N,N -(1езоксинойиримицинил- -пропионил)1-фениленаvnjvji / VnHCOCn-Cn, J-ij-(;HjCH2 ioKHо« Ri0,53j выход 9,7%. Пример 32. N, N - 5u.c (1дезоксинойиримидинилэтилсульфонилтил)Д -пиперидин ™/-Л r-CH,CHi$e,,-i(VeH,CHiMiCH,«H,-«-KOH он«н Т.пл. (.из изопропанола) 175с разл.)у выход 48,8%. , .oji У у ч U f . , Пример 33. N.N -L3,3-(l,4фенилен)-$ис (2-пропенил) -ди(1-деоксинойиримицин) CHjOH.-, J--Tf-CH2- iH fiH-/ (iH2-Tf 011 Г( Oftей т.пл. (из изопропанола) 258-260 с разл.); выход 35%. Пример 34. 1,,(1,5-дидезокси-1,5-имино-D-глюат)илЗ-бутин-2CHj- ( RO 0,19; выход 18,6%. , Пр.имер 36. Диамид N,N -JucL5- (1, 5-ИМИНО-1,5-дидезокси-1Э-глюитил)-метил -3-гексендикарбоновой ислоты В«Н,С .СИ,11И«ОСН.-СН СН-СН2Св11ИСН, .СН.вН У-тлщгл «
Т.пл. (из этанола) (разл.) выход 7%.I
Пример 42. Бензиламид 4,4-fuc { 2-CN- (l, 5-дидезокси-l, 5-имино-D-ГЛЮЦИТ)-ил -этокси}-бензойной кислоты65
НО
ОН Т.пл. 185 С (из изопропанола); выход 38%. Показатель вращения 008,6. Свойства производных 3,4,5-триоксипиперидина определяют в опыте. В пробирке можно определить энзимоингибиторную активность вещест ва путем сравнения активности растворенного кишечного комплекса дисахаридазы в присутствии или в отсутствие ингибитора. В качестве су страта, при помощи которого определяют специфичность теста ингибиров ния, используют практически свобод ную от глюкозы сахарозу (глюкоза, 100 ч/мм). Определение активности энзима основывается на спектрофотометрическом определении выделенной глюкозы посредством дегидро назы глюкозы и никотинамид-адеин-ди нуклеотида в качестве софактора. Одной единицей ингибитора сахарозы (SIE) считают такую активност ингибирования, при которой в определенной исходной смеси восстанавливается заданная сахаролитическая активность на одну единицу (единица Сахаров SE), единицей сахарозы считают активность энзимов, при которой в заданных условиях расщепляется 1 мк моль глюкозы..определяемой тестом, и фруктозы, не охваченной тестом. Кишечный комплекс дисахарйдазы получают из слизистой оболочки тонкого свинного кишечника путем триптического переваривания, осаждения из 66% этанола при , поглощения осадка в 100 мМ фосфатного буфера, рН 7,0 и в заключение диализом против буфера. В 10 мк.л пробного раствора доба ляют 100 мк.л {разбавленного комплек са дисахарйдазы в О,1 М малеинатног буфера, рН 6,25 и предварительно ин кубируют при 37 С в течение 10 мин Комплекс дисахарйдазы следует разбавить с таким расчетом, чтобы активность составила 0,1 SE/мл. Затем проводят сахаролитическую реакцию путем добавки 100 мкл раствора 0,4 М сахарозы (SERVA 35579) в 0,1 М малеинатного буфера, рН 6,25, которую прекращают по истечении 20 мин инкубирования при , путем добавки 1 мл. смеси из глюко- зы, гидрогеназы и реактива (1 флакон лиофилированной смеси глюкозы и дегидрогеназы (МЕРК 14053) и 331,7 мг смеси из -никотинамида, аденина и динуклеотида (свободная кислота Берингер, степень чистоты 1, растворенных в 250 мл 0,5 М трис буфера, рН 7,6). Для доказательства наличия глюкозы инкубируют в течение 30 мин при З7с и затем при 340 нм фотометрируют в отношении реактива (с энзимом, однако без сахарозы} Расчет тормозящей активности ингибиторов затрудняется тем, что уже незначительные изменения в системе теста, например, незначительно варьирующий в отдельных случаях общий Объем, имеет такое влияние на результат, которым нельзя пренебречь. Этих затруднений избегают тем, что при каждом определении одновременно используют стандарт; в качестве стандарта служит ингибитор сахарозы формулы ./8 который имеет специфическую активность торможения 77 700 и при взятых количествах 10 до 20 мг в тесте приводит к специфицированному выше порядку величин. При известной разнице экстинкции при 340 нм общего объема и заторможенной стандартом смеси, можно из разницы экстинкции и заторможенной пробным раствором смеси с учетом взятого количества ингибитора, известным образом высчитать его ТОЕ «ЭЗЯщую активность, которая выражается в единицах ингибитора сахарозы на грамл (SIE/r).. Специфическая, тормозящая сахарозу, активность 1-дезоксинойиримицин465000 SIE/r Соединение из примера 21 582800 51Е/г Соединение из примера 33 1103300 SIE/r Соединение из примера 41 730400 SIE/r Соединение из примера 43 924600 SIE/r
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Бюллер К., Пирсон Д | |||
| Органические синтезы | |||
| М | |||
| , Мир, 1973, т | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ получения целлюлозы из стеблей хлопчатника | 1912 |
|
SU504A1 |
| Переносный ветряный двигатель | 1922 |
|
SU384A1 |
Авторы
Даты
1983-05-07—Публикация
1980-05-28—Подача