Изобретение относится к металлургии цветных и редких металлов, в частности к широко используемому методу получения хлорида кальция, .свободного от гипохлорида кальция, в процессах утилизации и обезвреживания хлорсодержащих газов, сбросов различных производств известным молоком Са (ОН). Известен реактив для разложения гипохлорита кальция Са (СЮ) , кото рый представляет собой водный или солянокислый раствор хлорида никеля хлорида меди (I) и хлорида железа (1 ВЗЯТЫХ в соотношении 1:1:3 (в пересчете на ГИДРООКИ.СИ) l . Недостатком реактива является ег нестабильность во времени, снижение эффективности при хранении, поэтому он применяется только свежеприготов ленным во избежание образования гидроокисей до введения в раствор хлористого кальция. Кроме того, в состав реактива входят дорогостоящие хлориды никеля и меди. По суще ствующей технологии составляющие реактива в виде гидроокисей отфильт ровываются вместе с песками от раствора хлористого кальция и сбрасываются в отвальное пЬле, т.е. ценные компоненты безвозвратно теря ются. Существенным недостатком яйля ется и токсичность соединений меди и никеля, которые относятся к чрезвычайно опасным и опасным веществам их использование приводит к загрязнению окружающей среды. Цель изобретения - повышение ста бильности реактива. Указанная цель достигается тем, что реактив для разложения гипохлорита кальция в.растворах хлорида кальция, содержащий хлорид железа (l дополнительно содержит хлорид железа (U) и хлорид калия при следующих соотношениях ингредиентов, мол. Хлорид железа (Ш) 9-31 Хлорид калия4-9 Хлорид железа (it) Остальное При этом хлориды никеля и меди исключаются полностью. Реактив получают в компактном виде (сплав солей) и он может храниться ( в гер метичной упаковке) длительное время Кроме того, в способе получения реактива для разложения гипохлорита кальция в растворах хлорида кальция .процесс осуществляют хлорированием 432 железа при 650i5 C и подаче хлора со скоростью 0,20-0,25 л/ч см , конденсацию паров ведут на хлориде калия крупностью 1,6-2,8 мм при 600-650°С. Пример 1. Опыты по определению устойчивости гипохлорита кальция ведут в растворе известкового молока после его хлорирования, концентрация гипохлорита кальция в котором определяется по содержанию активного хлора и составляет 3,7 г/л. В ходе опытов берут две параллельные пробы исследуемого раствора по 15 мл. В одну из них добавляют реактив для разложения гипохлорита кальция, выдерживают 1 мин и анализируют на содержание Са (ClOj . Результаты опытов приведены в табл. 1. . Из таблицы видно, что практически полное разложение гипохлорита кальция может быть осуществлено реактивом 2 и 3. Степень разложения Са (С10)2 чистым хлорным железом невелика - 16,5% даже при концентрации Fe CBj - 7,55 г/л. Превышение содержания хлорида калия (вьш1е 10%) нежелательно, так как это приведет к изменению состава электролита и его дополнительной корректировке при электролитическом получении кальция. Таким образом, наиболее оптимальным для разложения гипохлорита кальция является реактив следующего состава, мол.%: Fe ,31, Fe С 60-87; КС1 4-9. Эффективность известного реактива резко падает при его 1зыдержке. Так, степень разложения гипохлорита кальция реактивом, приготовленным за 24 ч до опыта, снижается с 99,2 до 43% (опыт 7, табл. 1). Изменения же стабильности данного реактива не наблюдалось в течение года. Реактив полученный по способу-прототипу, не обеспечивает достаточной степени разложения гипохлорита кальция (опыт 8, табл. 1). Пример 2. Железный лом хлорируют при 650 С в кварцевой ячейке 30 мм, соединенной с кварцевым стаканом 45 мм. Нижняя часть стакана является сборником стекающей солевой смеси, а отделенная от нее ложным дном верхняя часть заполнена хлористым калием. Высота столба соли составляет 100-120 мм, Температуру сборника и нижней части поддерживают при заданном значении постоянной в пределах 12®С. Образующийся пЛав солей анали зируют на содержание хлоридов железа (11) и (110. .Результаты опытов в зависимости от крупности КС1 и температур (при скорости подачи хлора в хлоратор 0,2 л/ч см ) приведены в табл. 2. Из табл. 2 видно, что смесь требуемого состава может быть получена на солевой насадке крупностью 2,81,6 мм при температуре 600-650 0. Снижение температуры и увеличение крупности КС1 приводят к резкому уменьшению содержания хлорида железа (Ц) в смеси. Увеличение температуры и снижение крупности солевой насадки уменьшают содержания хлорид железа (110 в полученной смеси. Это можно объяснить тем, что с увеличе нием поверхности конденсации и температуры вероятность термическог разложения хлорида железа (110 возрастает. Таким образом, изменение установленных значений - температур и крупности КС1 приведет к отклонен от граничных значений ингредиентов объекта-вещества. Результаты опытов по определению влияния скорости подачи хлора в хло ратор на состав образующейся солево смеси при и крупности КС1 2,8 мм приведены в табл. 3. Из табл. 3 видно, что оптимальной скоростью подачи хлора в хлоратор является 0,20-0,25 л/ч см. Температура хлорирования железного лома 650i5 C. Изменение температуры (понижение или повьщ1ение) приводит к изменению соотношения хлорида железа (II иШ) в паровой фазе. Так, например, увеличение до 700-750с приводит к снижению содержания хлорида железа (Ш) в 1,5 раза за счет диссоциации на хлорид железа (II) и хлор. Снижение температуры хлорирования приводит к преимущественному образованию хлорида железа (llfi. Таким образом, при хлорировании железного лома со скоростью подачи хлора в хлоратор 0,20-0,25 л/ч.см с конденсацией образующихся хлоридов железа на солевой насадке из хлорида калия крупностью2,8-1,6 мм, нагретой до 600-650 С, можно получить реактив для разложения гипохлоритй кальция. Предлагаемый способ обеспечит получение наиболее простого по составу реактива, приготовление которого может быть организовано непосредстУ венно на предприятии-потребителе из отходов производства. Исключаются потери ценных компонентов - никеля и меди, обезвреживаются сточные воды. Кроме того, полученный реактив значительно более стабилен и удобен в обращении. Таблица
1084243
8 Продолжение табл. 1


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРИДА КАЛЬЦИЯ | 2003 |
|
RU2255899C1 |
| СПОСОБ ОБЕЗВРЕЖИВАНИЯ ПУЛЬПЫ ГИПОХЛОРИТА КАЛЬЦИЯ | 2018 |
|
RU2687455C1 |
| аСЕССЮЗНАЯ I | 1973 |
|
SU361213A1 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕТРАХЛОРИДОВ РЕДКИХ МЕТАЛЛОВ С ИСПОЛЬЗОВАНИЕМ СЕРЫ | 2019 |
|
RU2797475C2 |
| СПОСОБ ПРОИЗВОДСТВА ТЕТРАХЛОРСИЛАНА | 2010 |
|
RU2450969C1 |
| Способ пуска солевого хлоратора | 1981 |
|
SU956588A1 |
| СПОСОБ ПЕРЕРАБОТКИ ТИТАНСОДЕРЖАЩЕГО СЫРЬЯ | 2008 |
|
RU2379365C1 |
| Способ получения хлорида кальция | 1982 |
|
SU1081126A1 |
| СПОСОБ ПОДГОТОВКИ ХЛОРМАГНИЕВОГО СЫРЬЯ К ПРОЦЕССУ ЭЛЕКТРОЛИТИЧЕСКОГО ПОЛУЧЕНИЯ МАГНИЯ И ХЛОРА | 2008 |
|
RU2376393C1 |
| Способ получения безводного хлорида хрома | 1982 |
|
SU1159888A1 |
1. Реактив для разложения гипохлорита кальция в растворах хлорида кальция, содержащий хлорид железа (Ш, отличающийся I . 1 J|3 . .. v ;лй( сл тем, что, с целью повышения стабильности реактива, он дополнительно содержит хлорид (И) и хлорид калия при следующих соотношениях ингредиентов, мол.%: Хлорид железа (llJ Хлорид калия4-9 Хлорид железа (П) Остальное 2. Способ получения реактива для разложения гипохлорита кальция в растворах хлорида кальция хлорированием железа с конденсацией паров на хлориде калия, отличающийся тем, что, с целью повышения степени разложения гипоё хлорита кальция, хлорирование осуществляют при 650i5°C и подаче (Л хлора со скоростью 0,20-0,25, л/ч.см, а конденсацию паров ведут на хлориде калия крупностью 1,6-2,8 мм при 600-650 С.
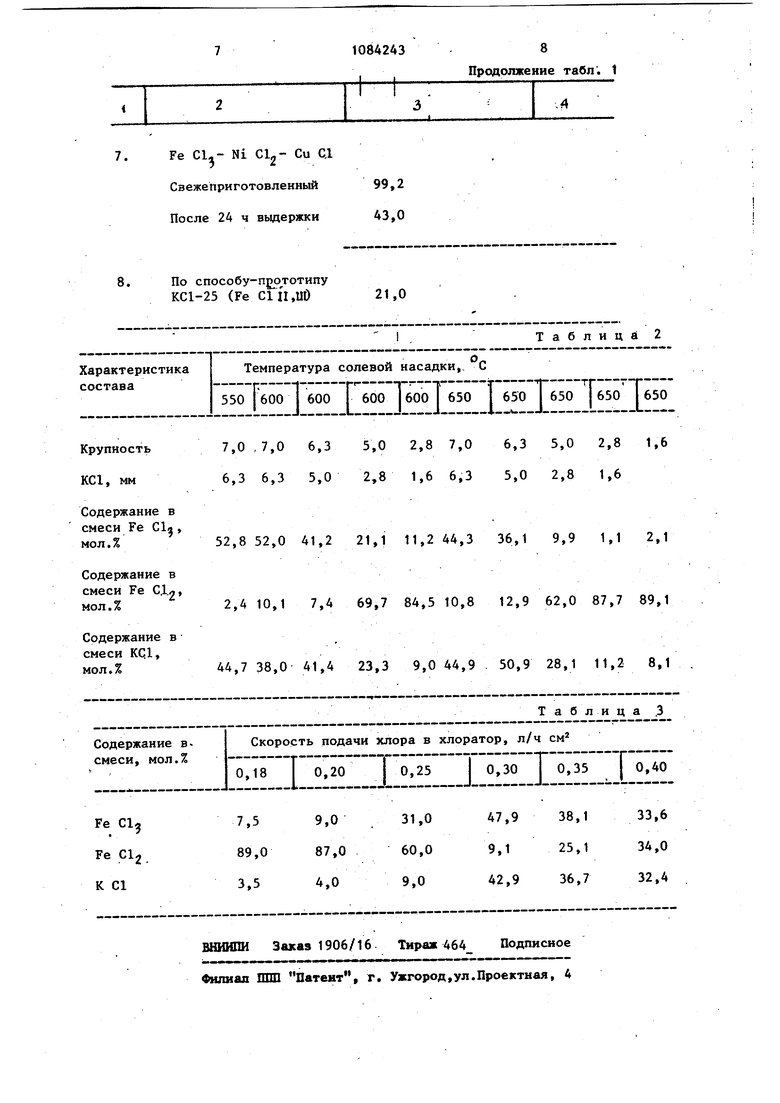
Свежеприготовленный 99,2 После 24 ч выдержки 43,0
В. По способу-п ртотипу
КС1-25 (Fe Clfl.uD21,0 Характеристика Температура состава 550 600 I 600 7,0 ,7,06,35,0 Крупность 6.36,35,02,8 КС1, мм Содержание в смеси Fe Cl-, мол. % 52,8 52,041,221,1 Содержание в смеси Fe СДл 2.410,17,469,7 мол.% Содержание в смеси КС1, 44,7 38,041,423,3 мол.%
Таблица 2 солевой насадки,, С Г 600 ТбОО I 650 | 650 Тб50 |650 Гб50 2,87,06,35,02,81,6 1,66,35,02,81,6 1,244,336,19,91,12,1 4,510,812,962,087,789,1 9,044,9, 50,928,111,28,1
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Доронин Н.А | |||
| Кальций | |||
| М., Госатомиздат, 1962, с | |||
| Видоизменение прибора для получения стереоскопических впечатлений от двух изображений различного масштаба | 1919 |
|
SU54A1 |
Авторы
Даты
1984-04-07—Публикация
1981-11-09—Подача