.. Изобретение относится к новому биологически активному химическому соединению - к циклическому пентапептиду - аналогу энкефалина, обладающему анальгетической активностью, который может найти применение в медицине .
Энкефапин - природный агонист опиг атного рецептора в мозгу, был вьщелен и идентифицирован в виде смеси двух Г1ентапептидов:Н-Туг-С1у-С1у-РЬе-МесОН (метионин-энкефалин) и H-Tyr-Gly Gly-Phe-Leu-OH (лейцин-энкефалин). Оба пептида проявляют морфиноподобную активность в опытах на специфиче ских моделях опиатного рецептора, а также подавляют стереоспецифическое связьшание с рецептором опиатного антагониста налоксона в гомогенатах мозга. Met-и Leu-энкефалины показывают анальгезию в течение 5-15 мин при внутрижелудочковом введении в мозг мыши. Известны циклические аналоги эн кефалина, включающие в цикл 18, 15 атомных группировок (см.табл.), од нако они показьшают полное отсутствие специфической активности энкефа лина. Наиболее близким по химической структуре является циклический аналог энкефалина (7)(см.табл.1), однако анальгетическая активность это го соединения не исследована. Целью настоящего изобретения является расширение арсенала средств воздействия на живой организм, создание аналогов энкефалина, обладающих анальгетической активностью. Поставленная цель достигается описываемым циклическим пентапептидом формулы: Tyr-D-Orn-Gly-Phe-Asnобладающим анальгетической активностью. Синтез пептида осуществляют известными методами пептидной химии в растворе согласно приведенной схе ме с использованием активированньпс эфиров трет-бутилоксикарбониламинок лот /, S -Аминофункцию D-орнитина за щищают бензилоксйкарбонильной группой, гидроксил тирозина - трет-бутилоксикарбонильной группой. На чертеже приведена схема синте Пример. Для синтеза аналога энкефалина 1 используют аминокислот и их производные фирмы Reanal (Ве грия). Всё аминокислоты, кроме DОрнитина, имеют L-конфигураЦию. Тем пературу плавления веществ определя в капилляре (без коррекции). Индиви дуальность промежуточных соединений контролируют с помощью тех на пластинках Silufol LVi54 (ЧССР). Для хроматографии аналога энкефалина применяют стеклянные пластинки с закрепленным слоем силикагеля SilikaGel 60-F-254 фирмы Merck (ФРГ). Используют следующие Системы растворителей: хлороформ - этанол - уксусная кислота (АсОН), 85:10:5 (А), н - бутанол - пиридин - АсОН - , 15:10: :3:6 (B)i н-бутанол - АсОН - Н,0, 4:1:1 (С), хлороформ - метанол - АсОНН О, 30:20:4:6 (Д), 60:18:2:3 (Е), н-бутанол - пиридин - АсОН - Н,0, 15:12:3:10 (F). Удельное оптическое вращение пептидов измеряют на поляриметре Perkin Elmir 141 М (ФРГ). Кислотный гидролиз проводят при 120С в течение 24 ч. Аминокислотный состав определяют на анализаторе Jeol-3, соединений данные элементного анализа удовлетворительно совпадают с вычисленным содержанием C,H,N. Молекулярный вес циклопептида определен масс-спектрометрически на приборе СН-5 Varian МАТ (США) при температуре приблизительно 250 С и ионизирующем напряжении 70 эВ. N-трет-бутилоксикарбонил-Глицил-фенилаланин (9). 6,6 г (40 ммоль) L-фенилаланина растворяют в 40 мл 1 н,раствора гидроокиси натрия, добавляют 3,34 г бикарбоната натрия, 50 мл диметилформамида (ДМФА) и 16,94 г (40 ммоль) пентахлорфенилового эфира трет-бутилоксикарбонил-глицина, растворенного в 20 мл ДМФА. Смесь перемешивают в течение нескольких часов. После завершения реакции (хроматографический контроль) реакционную массу разбавляют этилацетатом и водой (до разделения слоев), охлаждают до О и подкисляют 0,5 н. соляной кислотой до рН 3. Этилацетатный слой отделяют, водную фазу экстрагируют повторно. Объединенный этилацетатный слой промьшают водой,насьпденным раствором хлористого натрия и сушат над безводным сульфатом натрия.Кристаллический осадок, полученный после отгонки растворителя, перекристаллизовьшают из этилацетата с небольшой добавкой петролейного эфира. Вькод дипептида (9 ) 11,4 г (88%). Т.пл. 133- 35С,И +15,7 (с 1, ДМФА), Rf 0,73 (А), Rf 0,80 (Д). М -трет-бутилоксикарбонил, N °.бензилоксикарбонил-В-орнитил-глицил-фенилапанин (11). 10,9 г (33,8 ммоль) дипептида (9 растворяют в 50 мл 70%-ного раствора трифторуксусной кислоты (TFA) в дихлорметане и выдерживают 30 мин. Растворитель отгоняют, остаток расти рают с эфиром,, отфильтровьшают, промывают эфиром на фильтре и сушат в вакууме над гидроокисью калия. Получают 10,4 г (91%) трифторацетата дипептвда (10), Rf 0,63 (Д). 5,2 г (15,5 ммоль) трифторацетата (10) растворяют в 50 мл ДМФА, охлаждают до 0°С и при охлаждении до бавляют. 2,, 65 мл (15,5 ммоль) диизопропи этиламина в 5 мл ДМФА и 8,2 г (15,5 ммол пентафторфенилового эфираТг-трет-бут ,локсикарбонил, N -бензилоксикарбонил -D-орнитина, растворенного в 15 мл ДМФА. Реакционную массу перемешивают несколько часов и после завершения реакции обрабатывают аналогично соединению 9. Продукт, полученный после отгонки растворителя, очищают на колонке с силикагелем фирмы Merck. , Элюирование проводят в системе: хлороформ-этанол-этилацетат-АсОН-Н О, 285:5:8:2:0,25. Соответствующие i. фракции собирают, упаривают и сушат в вакууме. Получают 5,9 г (67%) масла защи- щенного трипептида (11) с Rf 0,65 (А), Rf 0,72 (В). N,О-ди-трет-бутилоксикарбонил-тирозил-N -бензилокси-карбонил-D-орнитида-глицил-фенилаланин (13). 20,0 г (35 ммоль) трипептида (11) растворяют в 100 мл 50%-ного раствора TFA в дихлорметане и выдерживают в течение 20 мин. Растворитель отгоняют, остаток растирают с эфиром. Образовавшийся осадок отфильтровывают, вновь промывают эфиром и высушивают в вакууме над - гидроокисью ка-ЛИЯ. Получают 19,2 г (94%) трифторацетата трипептида: (12) cRf 0,62(Д) 18,1 г (31 ммоль) трифторацетйта трипептида (12) растворяют в 100 мл ДМФА, охлаждают до , добавляют при перемешивании 5,3 мл (31 ммоль) диизопропилэтиламина в 10 мл ДМФА и 16,6 г (31.ммоль)« пентафторфенилового эфира N, О-дис-Вос-Ъ-тирозина. Реакционную массу перемешивают 1,52 ч (хроматографический контроль) и после завершения реакции обрабаты17 вают аналогично соединению 9. Продукт , полученный после отгона этилацетата размешивают с эфиром и охлаждают. Вьтавший осадок отфильтровывают, промывают эфиром и сушат в эксикаторе. Выход 16,0 (62%) защищенного тетрапептида (13) с Rf 0,75 (А), Rf 0,55 (В, Merck ) + 5,6 (с 1, ДМФА). К,0-ди-трет-бутилоксикарбонилтирозш1- н-(Ы -бензилоксикарбонил-аспарагил) -D-орнитил-глицил-фенилаланин (15). К 18 г (22 ммоль) защищенного тетрапептида (13) в 150 мл метанола, 15 мл АсОН и 20.мл добавляют палладиевую и гидрируют в течение нескольких часов. Катализатор отфильтровывают, фильтрат упаривают. Остаток растирают с эфиром и фильтруют, затем дважды переосаждают из спирта эфиром, вновь промывают эфиром и сушат в вакууме над гидроокисью калия, Получают 13,8 г (91%) тетрапептида (14) с Rf 0,15 (А) Rf 0,72 (Д, Merck )i Rf 0,77 (F, Merck), 5,1 г (6,8 ммоль) тетрапептида (14) растворяют в 100 мл ДМФА и при перемешивании и охлаждении добавляют 1,16 мл (6,8 ммоль). диизопропилэтиламина в 3 мл ДМФА и 3,3 г (6,8ммоль) нитрофенилового эфира N -бензилоксикарбонил-Ь-аспарагина, растворенного в 15 мл ДМФА. Через 2-3 ч реакционную массу обрабатывают аналогично соединению. 9. Продукт, полученный после отгонки растворителяj очищают на колонке с силикагелем фирмы Merck. Элюирование проводят в системе: хлороформ - этанол - этилацетат - АсОН - , 185:5:8:2:0,25. Соответствующие фракции собирают, упаривают и сушат в вакууме, Получают 4,6 г (70%) с Rf 0,72 (А); Rf 0,83 (Д); +8,2 (С 1, ДМФА). N,0-ди-трет-бутилоксикарбонилтирозил-цикло(-Н-В-орнитил-глицил-фенилаланил-.аспарагинил) (17), К 700 мг (0,73 ммоль)защищенного пентапептида (15) в 60 мл метанола, 4 мл АсОН и 1 мл воды добавляют палладиевую чернь и гидрируют в течение 2-3 ч. Катализатор отфильтровывают, фильтрат упаривают. Остаток растирают с эфиром и сушат в вакууме над гидроокисью калия. Получают Г 560, мг (94%) пентапептида (Ю) с Rf 0,07 (А), Rf 0,70 (Д) . 800 мг (0,98 ммоль) пентапептида (10) растворяют в 800 мл очищенного даФА, охлаждают до -20)С, прибавляют .триэтиламин в ДМФА до рН 7,2 и затем медленно прикапывают 0,63 мл (2,94 ммоль) дифенилфосфорилазида в ЗО мл ДМФА. Раствор перемешивают в течение «7 дней и поддерживают рН около 7 периодическим добавлением триэтиламина к реакционной массе. По завершении реакции растворитель отгоняют при 40°С, к остатку добавляют 1,5-2 мл этилацетата и небольшое количество эфира. Выпавший осад отфильтровывают, промывают эфиром, сушат в вакууме, получают 415 мг бе лого порошка защищенного циклическо го пентапептида (17). Ввиду плохой растворимости (17)очистку не проводят.
Химические сдвиги Н циклического пентапептида Тирозил-цикло (-N -D-орнитил-глйцил-фенилаланил-асиарагинк оС ). 415 мг (0,52 ммоль) защищенного циклического пентапептида (17) растворяют в Го мл 70%-ного раствора TIA в хлористом метилене и выдерживают 30 мин. Растворитель отгоняют, остаток растирают с эфиром и сушат в вакууме. Полученный продукт очищают высокоэффективной жидкостной хроматографией на хроматографе Du Pont-830 Элюирование осуществляют смесью: этанол -0,1 М ацетат аммония, 13:87. Соответствующие фракции собирают и лиофилизируют. Выход: 120 мг (38%) циклопентапептида энкефалина (1), +36 (с 0,5, AcOH)i Rf 0,62 (В, Merck), Rf 0,78 (Д, Merck)} аминокислотный состав: Туг 0,93, Gly 1,00; Phe 0,91; Orn 0,95; Asn 0,98.


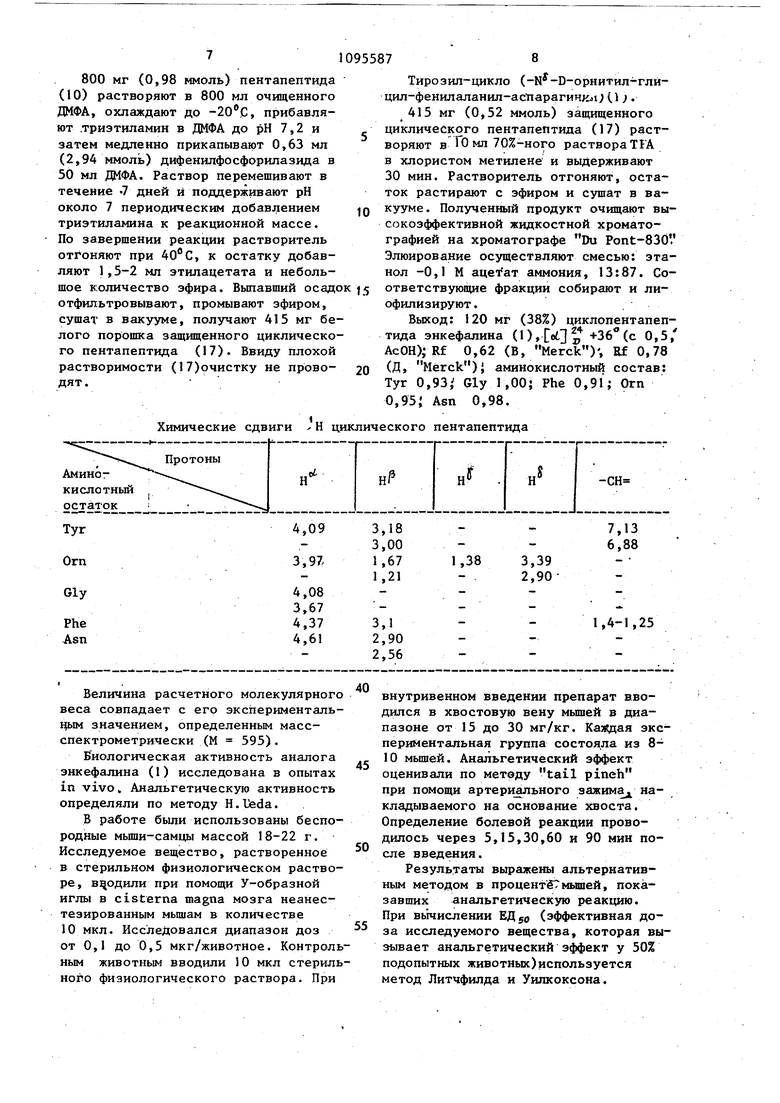


Циклический пентапептид формулы Tyr-D-Orn-Gly-Phe-Asnобладающий анальгетической активностью. т СП СП 00 
3,67 4,37 4,61
Величина расчетного молекулярного веса совпадает с его экспериментальЧым значением, определенным массспектрометрически (М 595).
Биологическая активность аналога энкефалина (1) исследована в опытах in vivo. Анальгетическую активность определяли по методу H.Ueda.
В работе были использованы беспородные мьш1и-самцы массой 18-22 г. Исследуемое вещество, растворенное в стерильном физиологическом растворе, вводили при помощи У-образной иглы в cisterna magna мозга неанестезированным мьпиам в количестве 10 мкл. Исследовался диапазон доз от 0,1 до 0,5 мкг/животное. Контрольным животным вводили 10 мкл стерильного физиологического раствора. При
1,4-1,25
2,90
2,56
внутривенном введении препарат вводился в хвостовую вену мьш1ей в диапазоне от 15 до 30 мг/кг. Казадая экспериментальная группа состояла из 810 мьш1ей. Анальгетический эффект оценивали по методу tail pineh при помощи артери ьного зажима накладываемого на основание хвоста. Определение болевой реакции проводилось через 5,15,30,60 и 90 мин после введения.
Результаты выражены альтернативным методом в процент1 мьшей, показавших анальгетическую реакцию. При вьЬгислении ЕД50 (эффективная доза исследуемого вещества, которая вызывает анальгетический эффект у 50% подопытных животных)используется метод Литчфилда и Уилкоксона.
Анальгетическая активность исследуемых соединений приведена в табл, 2 и 3. .
Цикло-(К°-В-Огп, А8п5)-энкефалин. 1 обладает выраженной анальгетической активностью. Максимальный эффект наблюдается на 5-ой минуте после введения. Анальгетическая активность нового аналога энкефалина 10 значитель- JQ но превьшает активность природных энефалинов (2,3) и в 4 раза превышает активность морфина в молярных соотношениях при интрацистернальном введении мышам (см.табл.2). 5
Цикло-(N°-D-Orn, Asn)-энкефалин (1) в отличие от природных энкефалинов активен при внутривенном введении. Он обладает 60% активности морина при внутривенном введении (см. 20 табя.З).
Цикпоаналог энкефалина 1 показывает более прод рлжитепьный анальгетичеАналоги энкефалина Линейные
Цикле-(N -D-Orn 1- При ЕД 2- В работе использовался морфинский эффект, чем природные энкефалины. Продолжительность анальгезии
нового аналога, (I) сопоставима ,с продолжительностью анальгетического
эффекта морфина при обоих способах введения и составляет 60 мин.(см. табл. 2,3)
Эффективная доза описываемого соединения (ЁДдо) при внутркйенном введении составляет 30 мкмоль/кг, или 22 мг/кг. При введении в дозе 500 мг/кг не наблюдается токсических эффектов, следовательно терапевтический индекс данного соединения составляет величину, большую, чем
500
22 (
22). что является без22 .
опасным интервалом для терапевтического средства.
Полученные результаты позволяют предполагать использование описываемого соединения в медицине.
Таблица 1 природные энкефалины. Анальгетическая активность цикло-(К -D-Orn , Asn ) -энкефалина при интрацистериальном введении мышам (метод tail pineh) Таблица 2 гидрохлорид производства Ташкентского ХФЗ.
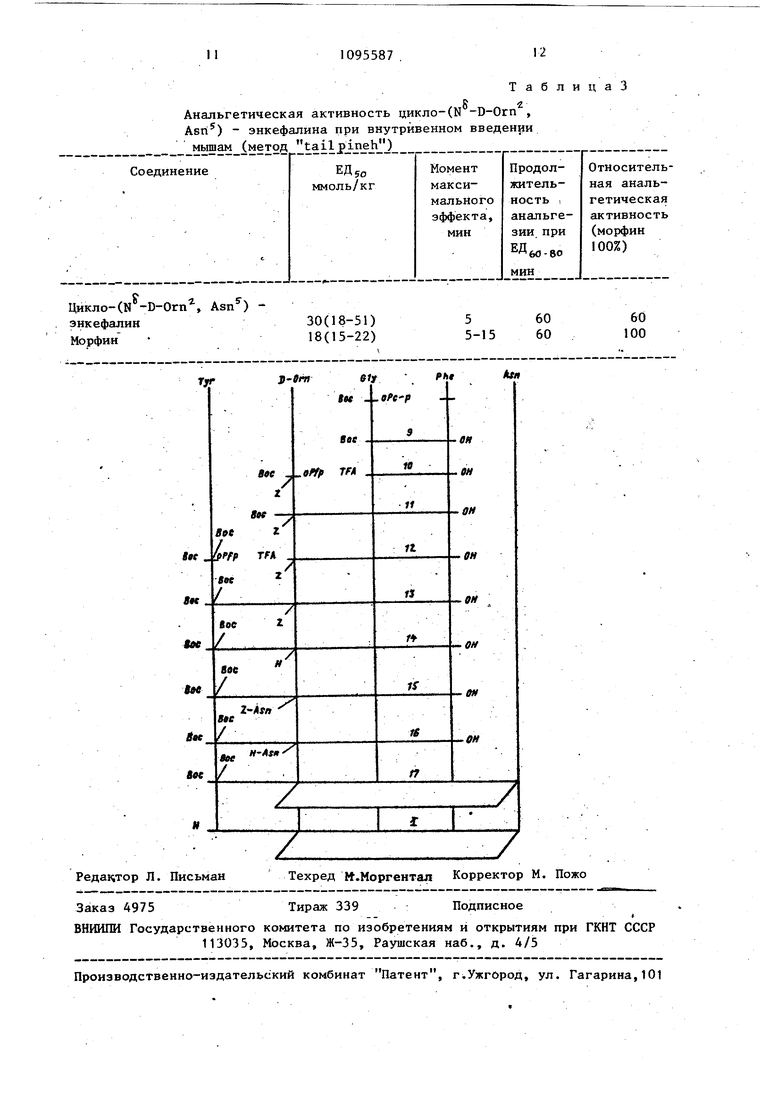
Анальгетическая активность цикло-(Ы -D-Orn , Asri) - энкефалина при внутривенном введении
Цикло-(Н -D-Orn Asn) энкефалин30(18-51)
Морфин 18(15-22)
ТаблицаЗ
60
60 60
5 5-15 100
| Hughes J., Smith T.W., Rosterlitz H.W., Fothergill L.A., Morgan B.A., Morris H.R | |||
| Сплав для отливки колец для сальниковых набивок | 1922 |
|
SU1975A1 |
| Buescher H.H., Hill R.C., Romer D., Cardinaux F., Closse A., .Hauser D., Pless J | |||
| Планшайба для точной расточки лекал и выработок | 1922 |
|
SU1976A1 |
| Hudson D., Sharpe R., Szelke M., Methionine enkephalin and isosteric analogues | |||
| Int | |||
| J | |||
| Peptide Protein Res | |||
| Способ получения фтористых солей | 1914 |
|
SU1980A1 |
| Kessler H., Holzemann G., CycloLeu -Enkephalin Angew | |||
| Chem | |||
| Int | |||
| Ed | |||
| Engl., 1981, 20, № i, 124 | |||
| pi Maio J | |||
| Schiller P.W | |||
| A cyclic enkephalin analog with high in vitro opTate activity, Proc | |||
| Natl | |||
| Sci | |||
| USA, 1980, V | |||
| Спускная труба при плотине | 0 |
|
SU77A1 |
Авторы
Даты
1989-08-30—Публикация
1982-11-24—Подача