Изо етение относится к новым бкологически активным соединениям аналогам энкефалина, обладающим анальгетической активностью, которые могут найти применение в медицине.
Энкефалин - природный антагонист опиатного рецептора в мозгу, был выделен и : тздентифицирован в виде смеси двух пентапептидов: H-Tyr-Gly-Gly-Phe-Met-OH (метионинэнкефапин) и H-Tyr-Gly-Gly-Phe-LeuOH (лейцилэнкефапин). Оба пептида проявляют морфиноподобную активность в опытах на специфических моделях опиатного рецептора, а также подавляют стереоО
специфическое связывание с рецептором, опиатного антагониста налрксона в го05могенатах мозга. СО 00
Met- и Leu- энкефалина показывают анальгезию в течение 5-15 мин при внутрижелудочковом введении в мозг мыши.
Наиболее близким к описываемому соединению является аналог энкефалина (D-Arg) - энкефапин, содержащий во втором положении D-изомер амино- ; кислоты с основными свойствами, проявлякнций анапьгетическую активность при внутримозговом введении и не обла дающий анальгезией при внутривенной введении. Цель изобретения - поиск новых пеп тидных производных аналогов энкефа.лина, обладающих более высокой ана ьгетической активностью, чем известные природные знкефалины или их синтетические аналоги. Поставленная цель достигается опис ваемыми аналогами энкефалина общей формулы Tyr-DOrn-GVy-Phe-y X- Описываемые соединения синтезируют известными методами пептидной химии в растворе согласно приведенной схемы с использованием активированных эфиров трет-бутилоксикарбониламинокислот. Для синтеза аналогов энкефалина ( 1) используют аминокислоты и их производные фирмы Reanal (Венгрия). Все аминокислоты, кроме D-opнитина, имеют L-конфигурацию. Температуру плавления веществ определяли в капиллярах (без коррекции). Индивидуальность промежуточных соединений контролировали с помоисью ТСХ на пласт тинках Silufо1 (ЧССР),.Для хроматографии аналогов энкефалина применяли стеклянные пластинки с закрепленным слоем силикагеля Silika Gel 60 F-254 фирмы Merck (ФРГ). Использовали следующие системы растворителей хлоррФорм - этанол - уксусная кислота (АсОН) 85:10:5 (А); н-бутанол-пиридин-АсОН5-Н О 15:10:3:6 (Б); н-бутанол -/АсОН - 4:1:1 (В); хлороформ-метанол-АсОН-Н О 30:20:4:6 (В); 60:18:2:3 (Г); н-бутанол-пиридин-АсОН-Н О 15:12:3:10 (D). Удельнов оптическое вращение пептидов измеряют на поляриметре Perkin Elmer 14Ш (США). Кислотный гидролиз проводят при 120С в течение 24 ч. Амин кислотный состав определяют па йнали заторе 1во1-3. Для всех соединений дантш элемен ного анализа удовлетворительно совпадают с вычисленным содержанием С, Н и др.. Пример 1. N-трет-бутилоксикарбонилглицилфенилапанин (4). 11 6,6 г (АО ммоль) L-фенилаланина (2) растворяют в 40 мл 1 н.раствора гидроокиси натрия, добавляют 3,34 г бикарбоната натрия, 50 Ил диметилформаМИДа (ДМФА) и 16,94г (40 ммоль) пентахлорфенилового эфира трет-бутилоксикарбонилглицина (3), растворенного в 20 мл ДМФА. Смесь перемешивают в течение нескольких часов. После завершения реакции (хроматографический контроль) реакционную массу разбавляют этилацетатом и водой (до разделения слоев), охлаждают до и подкисляют 0,5 н. соляной кислотой до рН 3. Этилацетатный слой отделяют, водную фазу экстрагируют повторно. Объединенный этилацетатный слой промывают водой, насыщенной раствором хлористого натрия, и сушат над безводным сульфатом натрия. Кристаллический осадок, полученный после отгонки растворителя, перекристаллизовывают из этилацетата с небольшой добавкой петролейного эфира. Выход дипептида (4) - 11,4 г (88%); т.пл. ПЗ-ПЗ С; + 15,7(с. 1 ДМФА); Rf 0,73 (А); 0,80 (В). Ы-трет-бутилоксикарбонилу .N -бен Рбонил-В-орнитилглицилфенилаланин (7). 10,9 г (33,8 ммоль) дипептида (4) растворяют в 50 мл 70%-ного раствора трифторуксусной кислоты (TFA) в дихлорметане и вьщерживают 30 мин. Растворитель отгоняют, остаток растирают с эфиром, отфильтровывают, промывают эфиром на фильтре и сушат в вакууме над гидроокисью калия. Получают 10,4 г (91%) трифторацетатй дипептида (5), Rf 0,63 (В). 5,2 г (15,5 ммоль) трифторацета- та (5) растворяют в 50 мл ДМФА, охлаждают до и при охлаждении добавляют 2,65 4п (15,5 ммоль) диизопропилэтиламина в 5 мл ДМФА и 8,2 г (15,5 моль) пентафторфенилового эфира N -трет-бутилоксикарбонил, N бензилоксикарбонил-О-орнитика (6), растворенного в 15 мл ДМФА. Рейкционкую массу перемешивают несколько часов и после завершения реакции обрабатывают аналогично соединению .4. Про. дукт, полученный после отгонки растворителя, очищают на колонке с силикагелем фирмы Merck. Элюироваиие проводят в системехлороформ-этаяолэтнлацетат-AcOH-HjiO 285:5:8:2:0,25. Соответствующие фракции собирают, упаривают и сушат в вакууме. Получают 5,9 г (67%) масла защищенного трипептида (7) с Rf 0,65 (А) 0,72 (Б). N,0-ди-тpeт-бyтилokcикapбoнилтирозил-К -бензилокси-карбонил-П-орнитилглицилфенилаланин (10). 20.0г (35 ммоль) трипептида (7) растворяют в 100 мл 50% раствора три фторуксусной кислоты в дихлорметане и выдерживают в течение 20 мин. Раст воритель отгоняют, остаток растирают с эфиром,, Образовавшийся осадок отфильтровывают, вновь промывают эфиро и высушивают в вакууме над гидроокис калия. , - - , . Получают 19,2 г (94%) трифторацетата трипептида (8) с Rf 0,62 (Д). 18.1г (31 ммоль) трифторацетата трипептида (8 растворяют в 100 мл , охлаждают до добавляют при перемешивании 5,3 мл (31 ммоль) диизопропилэтиламина в 10 мл ДМФА и 16,6 г (31 ммоль) пентафторфенилового эфира Н,0-ди-Вос-Ь-тирозина (9). Реакционную массу- перемешивают 1,5-2 часа (хроматографический контроль) и после завершения реакции обрабатывают аналогично соединению 4 Продукт, полученный после отгона этилацетата, размешивают с эфиром и охлаждают. Выпавший осадок отфильтро вывают, промывают эфиром и сушат в эксикаторе. Выход 16,0 г (62%) запощенного тетрапептида (10); Rf 0,75 (А), 0,55 (Б Merck); + 5,6 (с.IjДМФА) N-0-ди-трет-бутилоксикарбонилтирозил- К -(М -бензилоксикарбонил-. пролин)J D-орнитилглицилфенилаланин ( К 18 г (2,2 моль) защищенного тет рапептида (10) в 150 мл метанола, 15 мл АсОН и 20 мл воды добавляют палладиевую чернь и гидрируют в тече ние нескольких часов. Катализатор от фильтровывают, фильтрат упаривают. Остаток растирают с эфиром и фильтру ют, затем дважды переосаждают из спирта эфиром, вновь промывают эфиром и сушат в вакууме над гидроокисью калия. Получают 13,8 г (91%) тетрапептида ( 1 1 ) с Rf 0,15 (А); Rf 0,72 (В, Merck). 5,1 г (6,8 ммоль) тетрапептида (II) растворяют в 100 мл ДМФА и при перемешивании и охлаждении добавляют 1,16 МП (6,8 ммоль) диизопропилэтиламина в 3 мл ДМФА и 2,8 г (6,8 ммоль) пентафторфенилового эфира Ы-бензилоксикарбонил-Ъ-пролина растворенного в 15 мл ДМФА. Через 2-3 ч реакцигнную массу обрабатывают аналогично соединению 9. Продукт, полученный после отгонки растворителя, очищают на колонке с силикагелем фирмы Merck. Элюирование проводят в системе хлороформ-этанол-этилацеTaT-AcOK-Hj,0 185:5:8 2:0,25. Соответствующие фракции собирают, упаривают и сушат в вакууме. Получают 4,3 т (68%) защищенного пентапептида (12) 17° (с. 1, ДМФА); Rf 0,79 (В. Merck); 0,65 (Г. Merck)Ы,0-ди-трет-бутилоксикарбонилтиро-., (Ы -бензилоксикарбонил-лейцил) D-орнитилглицилфенилаланин (13). Из 5,1 г (6,8 ммоль) тетрапептида (11) п 3,5 г (6,8 ммоль) пентахлорфенилового эфира Ы-бензилоксикарбонилL-лейцина получают пентапептид (13) аналогично соединению 12. Выход 4,8 г (74%) белого порошка защищенного пентапептида(13) ( -5 (с. 1,ДМФА); Rf 0,80 (А); 0,84 (В). N-0-ди-трет-бутилоксикарбонилтирозш1- Ы -(N -бензилоксикарбонилacпapaгинил)J-D-орнитилглицилфенилаланин (14). Из 5,1 г (6,8 ммоль) тетрапептида (П) и 3,3 г (6,8 ммоль) нитрофенилового эфира N-бензилоксикарбонил-oi аспарагина получают пентапептид (14) аналогично соединению 12. Выход 4,7 г (70%) белого порошка защищенного пентапептида (14); + + 8,2(с.1, ДMФA);Rf 0,83 (Б). л Тирозил-(Н -пропил)-0-орнитилглищшфенилаланин (1). К 300 мг (0,32 ммоль) защищенного пентапептида .12 п 20 мл метанола, 2 мл АсОН и 0,5 мл воды добавляют палладиевую чернь и гидрируют в течение 2-3 ч. Катализатор отфильтровывают, фильтрат упаривают. Остаток растирают с эфиром и сушат в вакууме над гидроокисью калия. Полученный продукт растворяют в 5 мл 70%-ного раствора TFA в хлористом метилене и выдерживают в течение 30 мин. Растворитель отгоняют и остаток растирают с эфиром. Образовавшийся осадок отфильтровывают, повторно промывают эфиром и су- шат в. вакууме. Полученный продукт очищают высокоэффективной жидкостной хроматографией на хроматографе Du Pont-830. Элюированне осуществляют смесью этанол- О, I н.раствора ацетата аммония 20:80. Соответствующие фракции собирают и лиофилизуют. Вы- ход 70 г (37%) разветвленного пентапептида аналога энкефалина (I)} Coijg-f 41 (с, 1; 0,2 и АсОН); Rf 0,30 (Б) 0,74 (В), аминокислотый состав:. Gly 1,00; Туг 0,93; Phe 1 ,10; Oru 0,93; Pro 1,03. «
Пример 2. Тирозил-(Ы -лейцш1)-Б-ррнитш1глицш1фенилаланин (1°)
700 мг (0,73 ммоль) защищенного пентапептида (13) обрабатывают аналогично соединению 1а. Получают 205 мг (А6%) разветвленного пентапептида аналога энкефалина (1); foijf + 52 (с. 1; 0,2н. АсЦН); Rf 0,60 (Б), 0,50 (В), аминокислотный состав: Gly 1,00, Туг 0,95, Phe 1,26, Orn 0,98, Leu 1 ,05.
Примерз. Тирозш1-(М -аспарагинил)-В -орнитилглицилфенилаланин (I).
700 Mt- (0,73 ммоль) защищенного пентапептида (14) обрабатывают аналогично соединению l. Получают 270 мг (60%) разветвленного пентапептида аналога энкефалина (1); Ijyi + 37(с. 1; 0,2 н АсОН); Rf ,0,42 (В); Rf 0,8 (Д),аминокислотный состав: Gly 1,00; Туг 0,89; Phe 1,13; Orn 0,97; Asn 1,09.
П р и м е р 4. 0-ди-трет-бутилоксикарбонил-тирозил-Ы-(Ы-бензилоксикарбонш1-пролил)-Б-орнитил-глицил-фенилаланииамид (15).
К раствору 0,50 г (0,54 ммоль) соединения (12) в 3 мл ДМФА добавляю 0,08 г (0,54 ммоль) аммониевой соли L-окси бензотриазола и 0,11 г (0,54 ммоль) дициклогексилкарбодиими да. Реакционную смесь оставляют на ночь, отфильтровывают и обрабатывают аналогично соединению 4. Получают 0,46 г (91%) запущенного амида пентапептида 15 с Rg 0,48 (А.Мерк).
Тирозил-(N -пролил)-D-орнитилглицилфенилапанинамид (I )..
К 0,28 г (0,30 ммоль) защищенного пептапептида (15) в 20 мл метанола, 2 МП АсОН и 0,5 мол воды добавляют палладиевую чернь и гидрируют в течение 2-3 ч. Катализатор отфильтровывают, фильтрат упаривают. Остаток растирают с эфиром и сушат в вакууме
над гидроокисью калия. Полученный продукт растворяют в 5 мл 70% раствора TFA в хлористом метилене -и выдерживают в течение 30 мин. Растворитель отгоняют и остаток растирают в с эфиром. Образовавщийся осадок отфильтровывают, повторно промывают эфиром и сушат в вакууме. Полученный продукт очищают высокоэффективной жидкостной хроматографией на колонке Zorbax-Co. Элюирование осуществляют смесью этанола и 0,1 М раствора ацет та аммония 5:95. Соответствующие фраи ции собирают и лиофилизуют. 90 мг (50%) разветвленного амида пентапептида (1) ; foiU +20(с.1; О,2 н АсОН); Rf О,53 (В), 0,22 (В, Мерк), аминокислотный состав,%: Туг 0,86; Gly 1,00; Phe 0,91; Orn 0,92; Pro 1,08.
Проведены испытания биологической активности описываемых соединений
).
Анальгетическую активность опредеяли по методу H.Ueda et. al.
В работе бьши использованы беспородные мыши-самцы массой 18-22 г. сследй емое вещество, растворенное в стерильном физиологическом растворе, вводили при помощи У-образной иглы в isterna mague мозга неанестезированым мьщ1ам в количестве 10 мкл. Исслеовался диапазон доз от 0,25 до , . 10 мкг/животнс е для (l) , от 0,25 о 100 . мкг/животное для аналогов энкефалина (1) и (I) и от 0,05 до. 0,5 мкг/животное для (1). Контрольным животным вводили 10 мкл стерильного физиологического раствора. При внутривенном введении препарат вводился в хвостовую вену мьшей в диапазоне доз от 10 до 100 мг/кг( для соединения I от 15 до 25 мкг/кг). Каждая экспериментальная группа состояла из 8-10 . Анальгетическую активность оценивали по методу Buescher при помощи артериального зажима, накладываемого на основание хвоста, бпределение болевой реакции проводилось через 5,15,30,60 и 90 мин йоеле введения и затем каждые 30 мин до исчезновения анальгетической реакции.
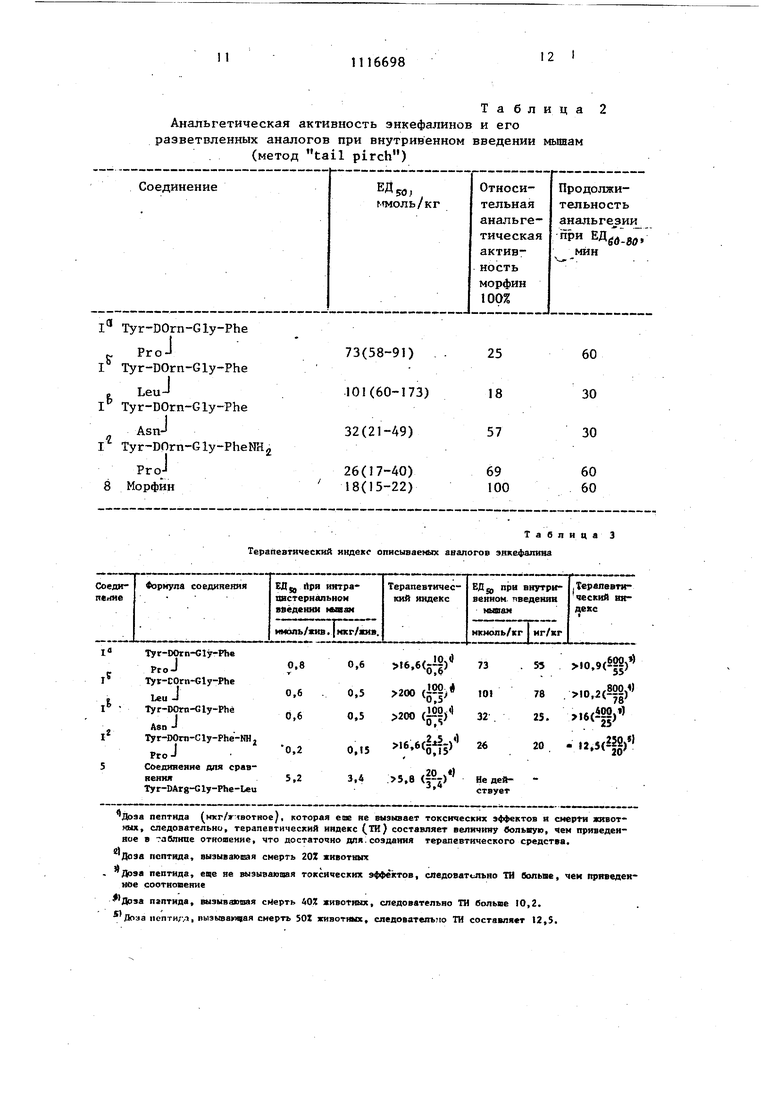
Результаты выражены альтернативным методом (процент мьш1ей, показавптх анальгетическую реакцию). При вычислении КД (эффективная доза исследуемого вещества, которая вызы 111вает анальгетический эффект у 50% подопытных животных) использован метод Литчфилда и Уилкоксона. Анальгетическая активность исследуемых соединений приведена в табл. и 2. Синтезированные аналоги энкефалина с разветвленной пептидной цепью () обладают выраженной аиальгети ческой активностью. Максимальный эффект наблюдается на 5-15 (I ,1), либо на 5-30 мин (I,) после введения. Анальгетическая активность аналогов () значительно превышает активность природных энкефалинов (соединения 6,7 в таблице 1) активность (Е-Аг§)-Ьеигэнкефалина (соединение 5, табл.1). Анальгетический эффект новых аналогов энкефалина ( в 1,5-2 раза и (I) в 6 раз выше анальгетического эффекта морфина в молярных соотношениях при интрацистер напьном введении мышам (см.табл.1). По продолжительности анальгетического действия соединение I превосходит мо соединение I - в 1,5 ра фин в 3 раза, за, В отличие от природных энкефалинов и от соединения, взятого для сравнения..0 и при внутривенном введении. Анальгетическая активность энкефалинов при интрацистернальном введении .№Ш1ам (метод tail pirch) эти аналоги активны при внутривенном введении (см.табп.2). Аналоги энкефалина обладают анальгетической активностью в интервале от 18 до 69% анапьгетического эффекта морфина при внутривенном введении мьш1ам. Сравнение терапевтических индексов и широты терапевтического действия описываемых соединений (таблицы 3 и 4) с теми же параметрами их ближайшего структурного аналога. Tyr-DArg-Gly- . -Phe-Leu показывает, что описываемые соединения малотоксичнь и превосхо,7 дят известное соединение по широте терапевтического действия и терапевтическому индексу при интрацистернальном введении мышам. Описываемые соединения проявляют. высокую активность при внутривенном введении мьш1ам, известное соединение, взятое для сравнения, при таком.способе введения неактивно. I. Проведенные исследования показали, что описываемые соединения малотоксичны и превосходят по анальгетической активности известные соединения, при этом их. активность сохраняется Таблица





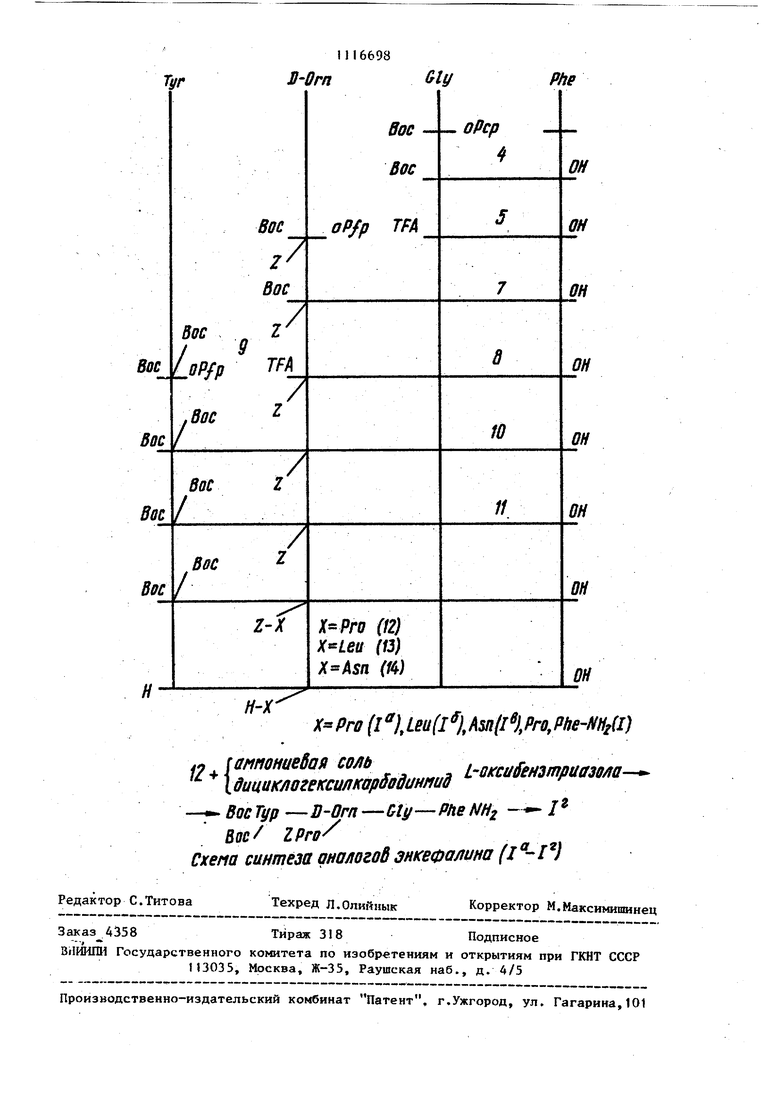
Аналоги энкефалина ойцей форму Tyr-DOrn-Gly-Phe-y X-J У ОН ОН ОН Pro Leu , где Asn Pro NH, обладающие анальгетической активностью. (Л
)
при Данные по активности (ЕД;, приведены из литературного источника (3) . .
Анальгетическая активность энкефалинов и его разветвленных аналогов при внутривенном введении мышам (метод tail pitch)
доэа пептида (нкг/г-1вотное), которая еше не вызывает токсических эффектов и снерги животных, следоаательни, терапевтический индекс (.ТИ) составляет величину больвую, чем приведеивое в тавЯнпе отношение, что достаточно дня:создания терапевтического средства.
доэа пептида, выэываю|Еая смерть 20Z животных
Даэа пептида, еце не вызывающая токсических эффектов, следовательно ТИ больве, чей пряведеяяое соотновение
Доза пгптида, вызывающая сйерть 402 животиых, следовательно ТИ больве 10,2. Доза пепти/-.я, вызывающая смерть 50t животных, следовательно ТИ составляет 12,5.
Т а б л и ц а 2
Терапевтическая широта действия описываемых аналогов Доза пептидов (мкг/животное), которые еще
ности, следовательно, терапевтическая широта (Till) превьшает приведенные в таблице отношения.
Доза соединения 11, вызывающая смерть 20% животных.
Максимальные исследованные дозы, которые еще не вызывали токсических эффектов, следовательно, ТШ превьшает приведенные отношения.
Доза соединения, вызывающая смерть30% животныхДоза соединения I г, вызывающая смерть 50% животных.
Т а б л и ц а 4
энкефалина не вызывают признаков токсич1116698
ЛОгп&1у
Туг
Phe
| Hughes J | |||
| и др | |||
| Identification of tvo related pentapeptides .from the bravi wittapotent opiate agonist activity Nature, 1973, 253, pp.577579 | |||
| Buescher Й | |||
| и др | |||
| Evidence for analge il activity of enkephalin in the Nature | |||
| Планшайба для точной расточки лекал и выработок | 1922 |
|
SU1976A1 |
| Kubota M | |||
| и др | |||
| Enkephalin ano logs containing the olipeptidi unit Tyr-Arg (Kyotorphin), Chem | |||
| Pharm | |||
| Bull., 1980, 28, 8, pp.2580-2586. | |||
Авторы
Даты
1990-10-07—Публикация
1982-11-24—Подача