CD 05
ел О1
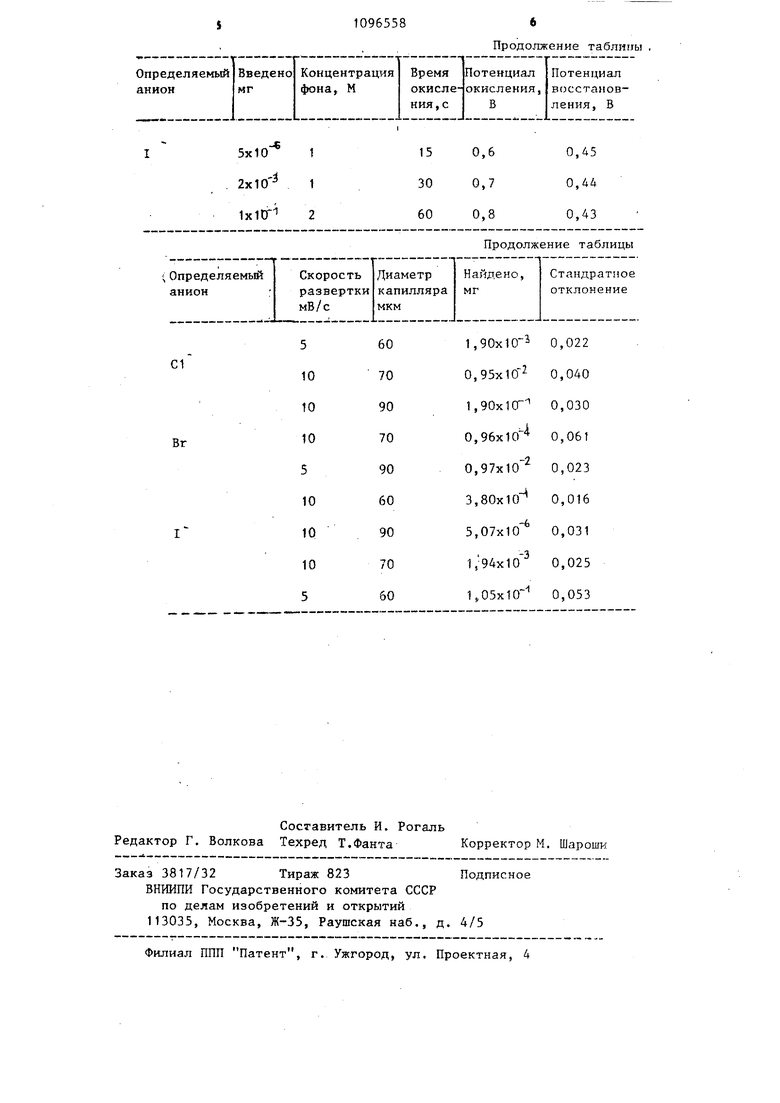
00 Изобретение относится к электрохимическим методам анализа, в част ности к определению галогенид-ионов на твердом электроде, и может быть использовано в аналитической практи ке, например в химической промышленности, для контроля сточных вод, в анализе биологических объектов. Известен способ осциллополярогра фического определения СЕ, Вп( D ионов на серебряном электроде с использованием метода накопления и од ноциклической вольтамперометрии, эаключакйцийся в том, что при злектр окислении серебряного электрода на его поверхности образуется пленк галогенидов серебра, которую растворяют при определенных потенциалах восстановления, при этом получаемый сигнал пропорционален концентрации ионозированных галогенов Г1 3 Недостатком этого способа являет необходимость перемешивания анализируемого раствора, сложной обработки электрода, предварительной подготовки и очистки его, Точность результатов в значительной степени зависит от стабильности работы элек рода. Наиболее близким по технической сущности к пpeд.лaгaeмo ry является способ вольтамперометрического ,опре деления хлорид,-бромид- и иодидионов, заключающийся в электрохимическом окислении галогенидов на твер дом электроде 2, Определение проводят по токам окисления галогенид-ионов на смешан юм фоне сульфата калия и серной кислоты,-При этом наблюдается один пик окисления Вг ионов (,,0 В) и несколько пиков окисления 3 -конов, из которых только первые два (0,5 и ,7 В) пригодны для аналитических целей. Определение проводят по первому пику или по сумме первого и второго пиков. Для малых концентраций иодид-ионов определение по сум ме пиков в присутствии брошщ-ионов или смеси их с хлорид-ионами невозможно. Диапазон определяемых концентраций, узок и составляет для иодид-ианов интервал от 10 до 10 М а .для бромид-ионов - от 10 до 10 М Метод не позволяет определять хлорид ионы, так как в этих условиях волна нк окисления не наблюдается. Целью изобретения является повышение селективности определения. 582 Поставленная цель достигается тем, что согласно способу вольтамперометрического опред 2ления хлорид-,бромиди иодид-иоиов, заключающемуся в электрохимическом окислении галогенидов на твердом электроде, электрохимическое окисление галогенидов проводят На фоне 5-6 М серной кислоты для хлорид-ионов и 1-2 М серной кислоты д,пя бромид- и иодид-ионов, определяя выделившиеся галогены по площадке вольтамперограмм их восстановления, причем в качестве твердого электрода используют электрод из углеродного моноволокна в капилляре с диаметром превышающим диаметр электрода не более, чем в 3 раза. Использование условий ограниченного объема капиллярной полости при внутреннем диаметре капилляра только в два-три раза большем, чем диаметр самого электрода, позволяет добиться полного электрохимического превращения галогенидов из восстановленной формы в окисленную и, наоборот Регистрируемая в этих условиях вольтамперограмма имеет пикообраэную форму из-за полного истощения раствора. Площадь пккообразной вольтамперограмФарадея соответствует количеству гагюгенид-конов. Объем капиллярной полости рассчитывают по геометрическим размераи: капилляра и электрода. Точность определения зависит от полноты окисления галогенид-ионов и последующего их восстановления. Это достигается соблюдением следующих экспериментально подобранных условий. Электроокисление галогенид-ионов на электроде из углеродного моноволокна, позволяющее работать при высоких положителыи.гя потенциалах (порядка 2 В), до образования свободных галогенов (одкоэлектронный процесс) ведут при следующих оптимальных потенциалах для иодид-ионов - от 0,6 до 0,8 В, для бромид-ионов от 1,1 до ,3 В, для хлорид-ионов от 1,8 до 2,0 В в течение 15-60 с,, что позволяет определять любой из названных галогенов в присутствии других, более электроположительных:, т.е. иодид в присутствии любых количеств бромид- и хлоридионов, бромид в присутствии любых количеств хлорид-ионов, хлорид-ионы в присутствии бромид-ионов. Однако Больтамперограмма хлорид-ионов в этих условиях регистрируется в области выделения кислорода, поэтому опре деление их концентрации по анодным токам становится невозможнь М. Для обеспечения возможности определения всех галогенидов, исключая фторидионы, предложено использовать результаты, получаемые при катодной развертке потенциала, непосредственно после их окисления. В этом случае восстановление свободных галогенов обр азовавшихся при электроокислении, идет также количественно, что регистрируется вольтамперометрически в области потенциалов от 0,5 до 0,9 В для хлорид-ионов, от 0,5 до 0,9 для бромид-ионов и от 0,3 до 0,6 для иодид-ионов. При этом скорость катодной развертки потенциала лежит в пределах от 5 до 10 мВ/с что обеспечивает получение симметри ных вольтамперограмм с площадями, выраженными в кулонах, соответствую щими количествам восстанавливаемых галогенов. Концентрация серной кисл ты, используемой в качестве фона, влияет на результаты определений, поэтому были найдены оптимальные ее значения в каждом конкретном случае для хлорид-ионов - 5-6 М/л, для бромид- и иодид-ионов - 1-2 М. Указанные условия позволили определять хлорид-ионы в интервале концентраций от 2x10 до 2x10 М, бром-ионы - в интервале от до 4х1(Т М, иодид-ионы - в интервале от 5х10 до lOV:. Кулонометрический способ (вольтамперометрия в тонком слое) определения галогенид-ионов позволяет существенно сократить время анализа потому что отпадает необходимость в построении калибровочного графика Электрод из углеродного моноволокна не нуждается в дополнительной подготовке, что также сокращает время анализа. Способ осуществляется следующим образом. Определения проведены на искусственньк растворах с известной концентрацией, которые вводили в термостатированную электрохимическую ячейку (25+0,1°С). Электродом сравнения служил хлорсеребряный, вспомогательным - стеклоуглеродный. Индикаторный электрод из углеродного моноволокна диаметром 30 мкм помещали в капилляр с внутренним диаметром 60-90 мкм объемом 1,Ах10 см, в котором проводили сначала электрохимическое окисление, а затем восстановление галоге- . нид-ионов. Растворенный кислород удаляли пропусканием через раствор электролитического водорода. Регистрировали по пять вольтамперограмм для каждой концентрации галогенидионов на универсальном полярографе ПУ-1 в постояннотоковом 3-х электродном режиме непосредственно после стадии электроокисления. Количество галогенид-ионов определяли по площади вольтамперограммы, полученной при катодной развертке потенциала. Результаты определений (число определений () приведены в таблице. Использование предлагаемого способа определения галогенид-ионов обеспечивает по сравнению с известными способами следующие преимущества.: расширение диапазона определяемых концентраций 5x10 -4х10 1, возможность определять хлорид-ионы, сокращение времени анализа из-за отсутствия необходимости построения калибровочного графика.

СПОСОБ ВОЛЬТАКПЕРОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ Х.ПОРИД-БРОМИД- М ИОДИД-ИОНОВ, заключающийся в электрохимическом окислении галогенидов на твердом электроде, отличающийся тем, что, с целью повышения селективности определения, электрохимическое окисление галогенидов проводят на фоне 5-6 М серной кислоты для хлорид-ионов и 1-2 М серной кислоты для бромид- и иодидионов, определяя выделившиеся свободные галогены по площадке вольтамперограмм их восстановлением, причем в качестве твердого электрода испольg зуют электрод из углеродного моноволокна в капилляре с диаметром, . превьппающим диаметр электрода не более чем в 3 раза.
2x10З
5 -2
6
1x10
1
г1
5 1
2x10
1x10г
1x10.
2 2
,-1
4x10
0,71 0,70
0,69 0,71
0,70 0,69
Продолжение таблипы
Продолжение таблицы
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Гороховский В.М | |||
| и др | |||
| 0сциллополярографическое определение ионов СГ , Bt, 3 на серебряном электроде.- Журнал аналитической химии, 1966, т.21, №1, 86 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Voltanmiefrie determination of iodide and bromide at the rotating pyrolytic graphite electrode.-I.Electroanal | |||
| Chem.,12, 416, 1966, 12, №5/6, 416 (прототип). | |||
Авторы
Даты
1984-06-07—Публикация
1983-01-03—Подача