со
а
N3 Изобретение относится к нсчюму производному изохииолнна,.а именно к 6,7-диэтокси-1(А-этоксн-3-оксибензил)-3,4-дигидроизохинолину форму ьтСгНэО ОС2Н5 обладающему действием на сердечнососудистую систему. Наиболее близким к предлагаемому соединению по химической структуре и биологическому действию является ;6,7-ДИЭТОКСИ-1-(З-этокси-4-оксибензил)-3, 4-дигидроизохинолин О. Указанное соединение является метаболитом Дротаверина, обладает анти ангинозным действием (действие в расчете на папаверин 1,28), повышает коронарный кровоток, уменьшает коронарную резистенцию и потребление кислорода левым желудочком сердца, повьппает миокардиальное потребление кислорода и, следовательно, улучшает оксигенизацию миокарда. Кроме того, соединение повьшгает порог фибрилляции (мерцания) предсердия и желудочка и обладает антиаритмическим дейст вием, однако оно уменьшает кровоток периферических сосудов (Arteria реmoralis, Carotis, ertibralis), а следовательно, повьш1ает их резистенцию, поэтому не применяется при периферических нарушениях циркуляции к-рови с целью улучшения кровоснабжения конечностей или головного мозга Цель изобретения - улучшение свойств производных изохинолина, обладающих действием на сердечно-сосудистую систему. Поставленная цель достигается тем что применяют 6,7-диэтокси-1-(4-эток си-3-оксибензил)-3,4-дигидроизохинолин формулы (1), обладающий ценными фармакологическими свойствами. Указанное соединение получают путем гидролиза в щелочной среде метил (З-бензилокси-4-этоксифенил) ацетата до З-бензилокси-4-этрксифенилуксусной кислоты, которую подвергаю взаимодействию с 3,4-диэтокси-р-фенилэтиламином в присутствии катионо 212 обменной синтетической смолы Варион КС, циклизации; полученного N-(3--бензилокси-4-этоксифенилацетил)-3,4-диэтокси- -фенилэтиламина в 6,7-диэтокси-1-(3-бензилокси-4-этоксибензил)-3,4-дигидроизохинолин с последующим гидрированием и выделением целевого продукта. Пример 1 , 3-Б,ензилокси-4-этоксифенилуксусная кислота. 20,0 г (66,6 ммоль) метил(3-бензилокси-4-зтоксифенил)ацетата в 100 мл 10%-ного раствора гидроксида натрия перемешивают в течение 2 ч при 110 С. После растворения исходного продукта раствор охлаждают до + 10 на бане лед - вода и подкисляют концентрированной соляной кислотой до рН 1. Вьтадающий в виде хлопьевидных (пушистых) белых кристаллов продукт отсасывают и промывают дистиллированной водой. Вещество высушивают в вакуум-эксикаторе. Сырой продукт очищают путем перекристаллизации из смеси растворителей бензол - петролейный эфир. Получают 17,9 г (93,8%) 3-бензилокси-4-этоксифенилуксусной кислоты с т. пл. 95-97 с. Вычислено, %: С 71,31; Н 6,33, C-j-jH „0 Найдено, %: С 71,18 Н 6,11. ИК-спектр (в виде таблеток с КВг): 1712 см-М С О). ЯМР-спектр (растворитель CjClj): 1,38 (триплет, ЗН, СНз-), 3,44 (синглет, 2Н, -CHj-COO-), 3,77 - 4,26 (квадруплет, 2Н, -CHj-)i 5,03 (синглет, 2Н, бензил, -CHj)i 6,47 - 7,57 (мультиплет, 8Н, ароматические Н); 9,86 (синглет, 1Н, -СООН). Пример 2. Ы-(3-Бензйлокси-4-этоксифенилацетш1)-3,4-диэтокси-р-фенилэтиламид. 6,30 г (22,0 ммоль) З-бензилокси-4-эток сифенилуксусной кислоты растворяют в 60 МП ксилола. Добавляют 4,80 г (22,9 ммоль) 3,4-диэтокси-/з-фенилэтиламина и 1 г катионообмеиной синтетической смолы Варион КС,которую промывают сначала 5 н,раствором соляной кислоты,затем водой.Смесь кипятят с насадкой для отделения воды вплоть до удаленияэквивалентного количества воды. По окончании нагревания горячий раствор фильтруют, фильтрат охлаждают и кристаллизуют. Выпавшее в осадок кристаллическое вещество обсасывают, промьшают петролейным эфиром и высушивают. Получают 8,20 г (78,0%) N-(3бензилокси-4-этоксифенилацетил)-3,4 -диэтоксифенилэтиламида с т.пл. 123 . Вычислено, 7с: С 72,92} Н 7,38/ N 2,93 Найдено, %: С 72,86, Н 7,59 N 2,89 ЯМР-спектр (растворитель CDCIj): 1,39 и 1,44 (триплет, 9Н, -CHj); 2,59 (триплет, 2Н, Аг ); 3,08-3,68 (мультиплет, 4Н, -CHj-C 0 -CHj- C-0)j 3,78-4,37 (мультиплет, 6Н, СНзСН -О); 5,04 (синглет, 2Н, бензил-СН -)i 5,40 (синглет, 1Н, -NH-)j 6,28 - 7,58 Хмультиплет, 11Н ароматические Н), Пример 3. Гидрохлорид 6,7-диэтокси-1-(3-бензилокси-4-этоксйбенэил)-3,4-дигидроизохинолина.
10,0 г (20,9 ммоль) N-(3-бeнзилoкcи-4-этoкcифeн maцeтил)-3,4-диэтокси-д-фенилэтиламида растворяют в 60 мл безводного хлороформа. Раствор охлаждают до О °С, после чего добавляют суспензию 5,60 г (26,8 ммоль) пятихлористого фосфора в 60 мл безводного хлороформа при О °С. Полученную смесь оставляют стоять в течение 30 мин при О °С, затем в течение 2 дней при комнатной температуре. Реакционную смесь разбавляют безводным эфиром. Выпавшее кристаллическое вещестяо отсасывают, промывают безводным эфиром и высушивают. Получают 9,65 г (92,9%) гидрохлорида 6,7-диэтокси-1-(3-бензилокси-4-этоксибензил)-3,4-дигидроизохинолина с т.пл. 209-210 С с разложением.
Вычислено, %: С 70,21; Н 6,90, N 2,82
.N
Найдено, %: С 69,80; Н 6,70; N 3,25
ИК-спектр (в виде таблеток с KBt) 1670 см-- (хС ).
Пример 4. Гидрохлорид 6,7диэтокси-1-(4-этокси-3-оксибензил)-3,4-дигидроизохинолина.
3,50 г (7,05 ммоль) 6,7-диэтокси-1-(3-бензилокси-4-этоксибензил)-3,4-дигидроизохинолина гидрохлорида растворяют в 100 мл метанола и раствор добавляют к используемой для гидрирования суспензии 1,50 г каталиПротивоангинное (антиангинозное) действие полученного соединения (Т) исследуют путем измерения подавления вызываемой Вазопрессином (2 IU/кг, внутривенно) острой коронарной недостаточности (соответствует Т-волновому сдвигу на электрокардиограмме) на подвергнутых наркозу с помощью 45 мг/кг (интраперитонеально) пентобарбитала крысах штамма CFY по методу Рарр и Szeheres.
Антиаритмическое действие исследуют на подвергнутых наркозу с помощью хлорадозы-уретана (500/300 мг/кг, интраперитонеально) кошках путем измерения изменения порога (предела) фибрилляций предсердий и желудочка по методу Szeheres и Рарр.
Обпще гемодинамические (сердечнососудистые действия) исследуют на подвергнутых наркозу с помощью пентобарбитала (35 мг/кг, внутривенно) собаках.
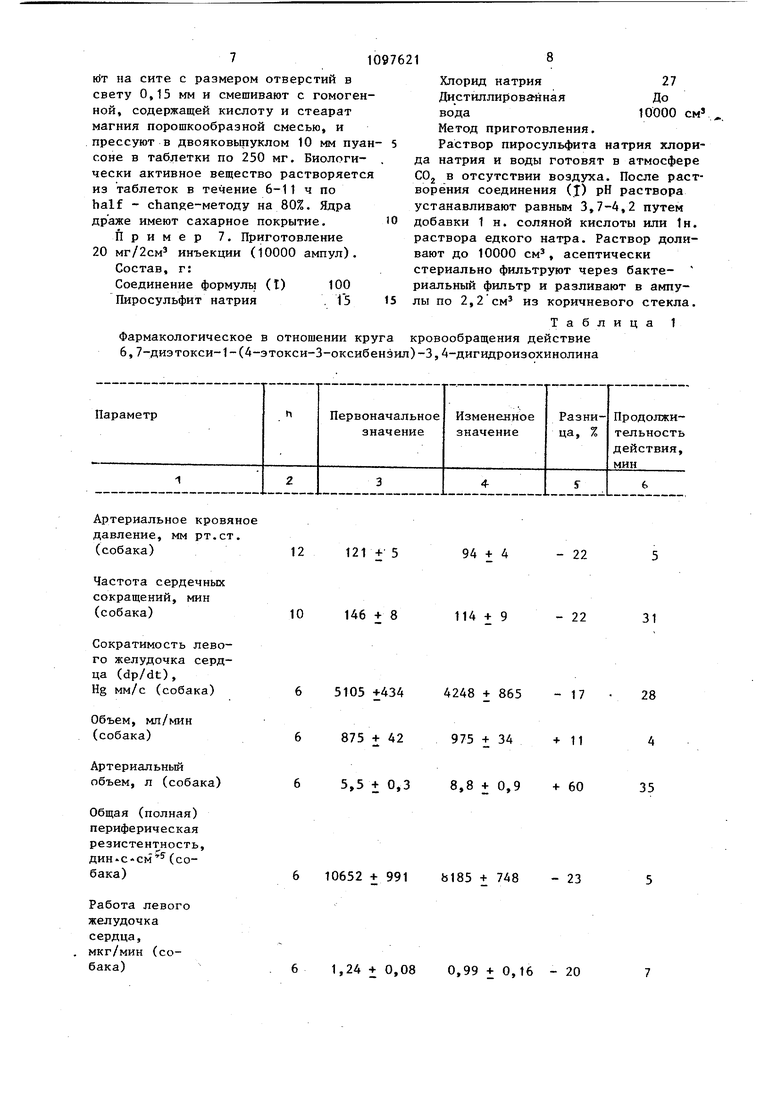
Соединение формулы (I) обладает значительным противоангинным (антиангинозным) действием (относительное действие в расчете на папаверин 1,40), и значительным антиаритмическим действием в отношении предсердия и желудочка, направленным против фибрилляции (табл. 1 и 2) и благоприятно влияет на некоторые параметры сердечно-сосудистой системы. Кроме того, соединение (I) по14затора, содержащего 10% палладия в виде палладия на активном угле в .20 мл метанола. Гидрирование осуществляют при нормал-ьном давлении и при комнатной температуре. Продукт поглощает теоретически рассчитанное количество водорода (169 мл) в течение примерно 10 мин. После прекращения гидрирования катализатор отфильтровывают и растворитель отгоняют в вакууме. В качестве остатка получают твердое вещество. Выход 2,80 г. Сьфой продукт Kpnc-t таллизуют из смеси метанола с эфиром. Получан5т 2,0 г (69,8%) 6,7-диэтокси-1-(4-этокси-3-оксибензил)-6,7-дигидроизохинолин гидрохлорида с т.пл. 223-225 с. Вычислено, %: С 65,09; Н 6,95; N 3,45 c H eCtNO Найдено, %: С 64.97; Н 6,99, N 3,66 S1097621 вьшает кровоток периферических сосудов (Arteria femoralis, Carotis Ver tebralis), следовательно,Уменьшается резистенция сосудов и улучшается эффективность работы сердца. В соответствии с антиангинозным действием повьппается коронарный кровоток, уменьшается коронарная резистенция и потребление кислорода левым желудочком сердца, повьш1ается доля миокардиального потребления кислорода (расход кислорода), в результате чего улучшается оксигенизация миокарда (сердечной мыощы). Таким образом, соединение формулы (I) является лекарственным средством для сердечно-сосудистых заболеваний, особенно Angina Pectoris, аритмий желудочка и предсердия, а также периферических циркуляционных потоков из-за уменьшенн го кровотока. Данные об острой токсичности 6,7 -диэтокси-1-(4-этокси-3-оксибензил) -3,4-дигидроизохинолина формулы (1) 24,92 мг/кг внутри- ; веяно для крысы 22,98 мг/кг внутривенно для 269,18 мг/кг перорально для мыши 164,89 мг/км перорально для мьшш ЛДр. 493 мг/кг перорально для крысы 625 мг/кг перорально для крысы Соединение формулы (I) в качеств биологически активного вещества может применяться в содержащих инертные, нетоксичные, твердые или жидки разбавители или носители препарата Препараты могут быть в твердой форме (например, таблетки, капсулы, др же) или в жидкой форме (например, раствор, суспензия, эмульсия).. Содержание биологически активног вещества в фармацевтических препара тах может изменяться в пределах 0,. Дневная доза может изменяться в широкой области и зависит от состояния, возраста и веса тела пациента, а также от готовой формы и активности биологически активного вещества. де го 10 из ра вор Пример 5. Приготовление сожащих 30 мг биологически активновещества таблеток (количество 00 шт.), Состав, г: Соединение формулы (I) 300 Кукурузный крахмал 530 Молочный сахар600 Желатин18 Дистиллированная вода 100 Этанол (96 об.%) 200 Пиросульфит натрия 2 Тальк30 Стеариновая кислота 20 Метод приготовления. Гомогенную порошкообразную смесь соединения (I), крахмала и сахасмачивают (в малых порциях) растом желатина, воды, этанола и пиросульфита натрия в кнет-машине для перемешивания, гранулируют на сите с размером отверстий в свету 0,3 мм и сушат при 40° С. Сухой гранулят повторно гранулируют на сите с размером отверстий в свету 0,15 мм, смешивают с гомогенной порошкообразной смесью талька и стеариновой кислоты и прессуют в двояковьшуклые таблетки по 150 мг с помощью пуансона размером 8 мм. Пример 6. Таблетки (драже) с пролонгированным.действием со 100 мг биологически активного вещества (10000 шт.).. Состав, г: Соединение формулы (1) 1000 Кристаллическая целлюлоза450 Молочный сахар . 765 Сополимер винилпирролидона с винилацетатом 180 Дистиллированая вода .150 Этанол (96 об.%) 350 Пиросульфит натрия 5 Коллоидальная кремниевая кислота25 Стеарат магния25 Стеарин 50 Метод приготовления. Гомогенную порошкообразную смесь из соединения (I), целлюлозы и сахара вместе с содержащей суспензионной смесью указанного сополимера, воды, этанола, стеарина и пиросульфита натрия-гранулируют в аппарате с повьш1енным давлением при 40 С по принципу псеЬдоожижения и высушивают. Высушенньй гранулят снова гранулиру7KJT на сите с размером отверстий в свету 0,15 мм и смешивают с гомоге ной, содержащей кислоту и стеарат магния порошкообразной смесью, и прессуют в двояковыпуклом 10 мм пуа соне в таблетки по 250 мг. Биологически активное вещество растворяетс из таблеток в течение 6-11 ч по half - change-методу на 80%. Ядра драже имеют сахарное покрытие. Пример 7. Приготовление 20 мг/2см инъекции (10000 ампул). Состав, г: Соединение формуль (I) 100 Пиросульфит натрия . 15 Фармакологическое в отношении к 6,7-диэтокси-1-(4-этокси-3-окси 1 27 Хлорид натрия До Дистиллированная 10000 см Метод приготовления. Раствор пиросульфита натрия хлорида натрия и воды готовят в атмосфере COj в отсутствии воздуха. После растворения соединения (J) рН раствора устанавливают равным 3,7-4,2 путем Добавки 1 н. соляной кислоты или 1н. раствора едкого натра. Раствор доливают до 10000 см, асептически стериально фильтруют через бактериальньй фильтр и разливают в ампулы по 2,2 см из коричневого стекла, Таблица 1 кровообращения действие )-3,4-дигидроизохинолина





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 1-(гидроксистирил)-5Н-2,3-бензодиазепина | 1987 |
|
SU1503681A3 |
| ПРОИЗВОДНЫЕ БЕНЗИЛАМИДА 4-ОКСИМАСЛЯНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЕ МЕСТНО-АНЕСТЕЗИРУЮЩУЮ, АНТИАРИТМИЧЕСКУЮ, АНТИАНГИАЛЬНУЮ И АНТИНЕКРОТИЧЕСКУЮ АКТИВНОСТЬ | 1988 |
|
SU1601984A1 |
| АНТИАРИТМИЧЕСКОЕ СРЕДСТВО | 1983 |
|
RU2068261C1 |
| ПРОИЗВОДНЫЕ 2-МЕРКАПТОБЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЕ ПРОТИВОИШЕМИЧЕСКОЙ, АНТИАРИТМИЧЕСКОЙ И ПРОТИВОФИБРИЛЛЯТОРНОЙ АКТИВНОСТЬЮ | 1995 |
|
RU2136667C1 |
| Соли производных 1,2,4-оксадиазолин-5-она проявляющие свойства регуляторов деятельности сердечно-сосудистой системы | 1980 |
|
SU1087519A1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИАРИТМИЧЕСКИМ, АНТИФИБРИЛЛЯТОРНЫМ, ПРОТИВОИШЕМИЧЕСКИМ ДЕЙСТВИЕМ, И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2011 |
|
RU2477130C1 |
| Способ моделирования острой ишемии миокарда | 1990 |
|
SU1803927A1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИАРИТМИЧЕСКИМИ И ГЕПАТОПРОТЕКТОРНЫМИ СВОЙСТВАМИ | 2011 |
|
RU2469720C1 |
| Способ определения функции изолированного сердца | 1980 |
|
SU1022696A1 |
| Способ искусственного кровообращения | 1987 |
|
SU1426592A1 |
6,7-Диэтокси-1-
Артериальное кровяное давление, мм рт.ст. (собака) 12 121-1- 5 Частота сердечных сокращений, мин (собака) 10 146 + 8 Сократимость левого желудочка сердца (dp/dt), Hg мм/с (собака) 6 5105 +434 Объем, мл/мин (собака) 6 875 4- 42 Артериальный объем, л (собака) 6 5,5 + 0,3 Общая (полная) периферическая резистентность, дин«с-см (собака) 6 10652 +991 Работа левого желудочка сердца, мкг/мин (собака) 6 1,24 + 0,0 94 -ь 4 114 + 9 248 -ь 865 - 17 975 -ь 34 +11 8,8 + 0,9 + 60 185 + 748 - 23 0,99 + 0,16 - 20 Коронарное протекание жидкости, мп/мин/100 г (собака) Коронарная резистентность, мм рт.ст./мл/ /мин/100 г 6 , 1,16 + 0 (собака) Потребление кислорода левым желудочком сердца, мл/мин/ЮО г, (собака) 6 11,6 + 0,09 Эффективность работы сердца, мкг/мп/ЮО г (собака) 6 0,11 + 0,02 Миокардиальная оксигенизация (Oj - предложение/О расход (собака) 6 1,70 + 0,07 Количество протекающей жидкости (крови) через А. femoral is, мл/мин 34 + 7 Резистенция A.femoralis, мм рт.ст./мл/мин (собака) 6 4,84 + 0,86 Количество протекающей жидкости через A.Carotis, мл/мин, (собака)70+7РезисТендая A.Carotis, мм рт.ст./мл/мин (собака) 6 2,33 + 0,23 Количество протекающей жидкости через А. Vertebralis, мл/мин (собака) 43 + 6 Резистенция A.Zertebralis, мм рт.ст./МП/ мин (собака) 6 3,28 + 0,33
10
1097621 Продолжение таблицы 1 95+5 29 9 ,76 + 0,06 - 34 ,2 + 1,2 - 29 ,16 +0,02 + 45 ,95 + 0,21 + 74 49 + 10 + 44 ,66 + 0,42 - 45 89+13 + 27 ,02 + 0,32 - 13 65 + 9 1,81 +, 0,17 - 45
11 Порог фибрилляции желудочка сердца, 62,07 + 0,10 m А, (кошка) Артериальное кровяное давление 6 139+5 мм рт.ст. (кошка) Порог фибрилляции предсердия, m А 6 0,73+0,10 (кошка)
Примечание . Доза 2 мг/кг внутривенно.
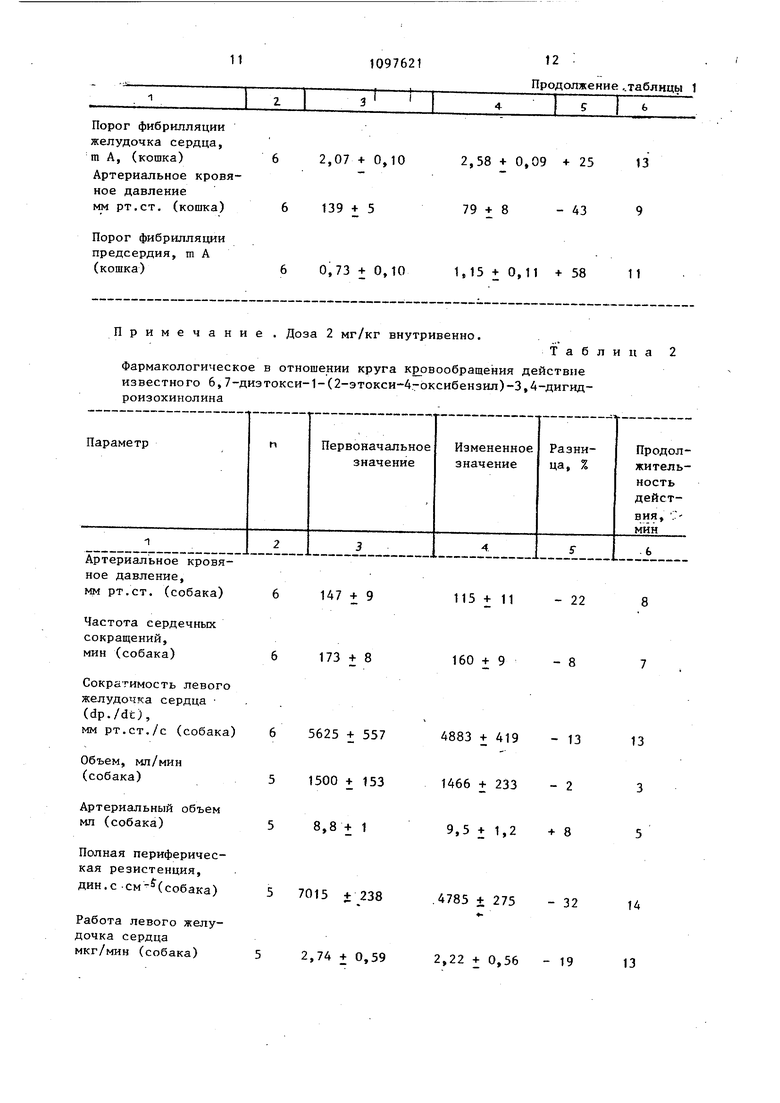
Фармакологическое в отношении круга кровообращения действие известного 6,7-диэтокси-1-(2-этокси-4-оксибензил)-3,4-дигидроизохинолинаАртериальное кровяное давление, мм рт.ст. (собака) 147 + 9 Частота сердечных сокращений, мин (собака) 173 + 8 Сократимость левого желудочка сердца (dp./dt), мм рт.ст./с (собака) 5625 + 557 Объем, мл/мин (собака) 1500 + 153 Артериальный объем мл (собака) 8,8 + 1 Полная периферическая резистенция, дин.с-см-(собака) 5 7015 Работа левого желудочка сердца мкг/мин (собака) 5 2,74 + 0,59
12
1097621 Продолжение ..таблицы 1
Таблица 2 2,58 + 0,09 + 2513 79+8 ,15+0,11 +5811 115+11 - 22 160 + 9 883 + 419 - 13 466 +233 - 2 9,5 +1,2 +8 785 + 275 - 32 ,22 + 0,56 - 19 13109752 t 1I 2 I 3 Коронарное протекание жидкости мл/мин/100 г (собака)5 73+13 Коронарная резистентность, мм рт.ст-./МП/мин/100 г (собака)5 1,03 + 0,10 Oj - потребление левым желудочком сердца, мл/мин/100 г (собака) 5 8,4 + 0,9 Эффективность работы сердца, мкг/мл/100 г (собака) 5 0,32 + 0,03 Миокардиальная оксигенизация, 0 - предложение /0 -потребление (собака) 5 1,62 -f 0,06 Количество протекающей жидкости (крови) через А. femoralis,. МП/мин (собака) 5 46+5 Резистенция А.femoral is, мм рт.ст./мл/мин (собака)5 3,48 + 0,45 Количество протекающей жидкости через A.Carotis, мл/мин (собака)5 91+9 Резистенция A.Carotis, мм рт.ст./мл/мин (собака)5 2,04 + 0,3 Количество протекающей жидкости через A.Zertebralis, МП/мин (собака)554+9 Резистенция А. lertebralis, ММ рт,ст./мл/мин (собака)53,22 +0,61 Порог фибрилляции Предсердия, m А (5ошка)50,52 + 0,07 , Продолжение таблшщ 2 1 . 86+13 -«-18 15 1,42 + 0,22 - 22 11 7,9 +1,9 - 6 9 0,28 + 0,05 - 13. 20 1,79 + 0,10 +10 18 42+5 -9 11 3,69 + 0,68 +6 18 80+10 -12 12 2,19 + 0,4 +7 15 0+7-77 5 + 0,32 + 1212 7 + 0,19+489
15 Порог фибрилляции желудочка сердца, т А. (кошка) 5 0,70 J; 0,10 Артериальное кровяное давление мм рт.ст. (кошка) 142 + 11
Примечание . Доза 1 мг/кг внутривенно.
16 :
1097621
i Продолжение, таблицы 2
12 1,00 + 0,18 . + 48 110+16 - 23
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Qualitative and Quantitative Determination.of Drotaverine Metabolite in Rat Bile.- European Journal of Drug Metabolism and Pharmacokinetics | |||
| Способ получения фтористых солей | 1914 |
|
SU1980A1 |
Авторы
Даты
1984-06-15—Публикация
1982-06-16—Подача