00
«-д
4 Изобретение относится к физикохимическим способам анализа в анали тической химии и может найти применение для определения Содержания глюкозы в крови и других биологичес ких жидкостях, в сельскохозяйственном производстве, пищевой промышлен ности. Известен способ определения концентрации глюкозы в крови in vivo с помощью электрода из благородного металла с последующим измерением то ка или потенциала окисления глюкозы используя в качестве основной реакции электрохимическое окисление глю козы на электродах-катализаторах из платиновой черни, стационарный ток, протекающий через этот элемент, про порционален концентрации глюкозы в анализируемой жидкости 113. Для очистки измерительного элект рода дополнительно используется пот циостатическое устройство, подающее очистительный импульс 1,5 В. Такой способ характеризуется быстрой дезактивацией платинового электрода-катализатора из-за высокой способности платины к прочной хемосорбции различных органических веществ, анионов и катионов, отсюда неконтролируемое падение тока во времени и выход датчика из строя. Максимальное время работы 2 мес., среднее - 2 недели. Точность измерений работающего датчика 7%. Для пр одоления этого недостатка требуется разработка различных сложных систем реактивации и непрерывной калибровки. Кроме того, низка величина токового сигнала с единицы поверхности катализатора. Система нечувствительна также к концентрации глюкозы менее 50 мг% и мало чувствительна к концентрациям более 500 мг% (0,0275 М), для которых зависимость тока от концентрации на платиновом электроде отклоняется от линейности и выходит на предел. Целью изобретения является повышение точности способа. Поставленная цель достигается тем что согласно способу определения концентрации глюкозы в крови in vivo с помощью электрода из благородного металла с последующим измерением тока или потенциала окисления глюкозы, электроокисление глюкозы проводят на золотом электроде при рН 9,5-14,0. Способ осуществляют следующим образом. Для проведения анализа на содержание глюкозы используют стандартное электрохимическое оборудование: трехэлектродную электрохимическую ячейку, осциллографический полярограф ПО-5122, рабочий электрод - золотая пластина 15 мм для малых концентраций или торец золотой проволоки для больших концентраций, вспомогательный электрод - никелевая сетка, электрод Сравнения - окиснортутный электрод в 1 М КОН. В качестве индикаторного электрода используют золото, так как оно является более селективным электродом-катализатором для электроокисления глюкозы, на котором большинство других органических веществ не окисляется. Золотой электрод в отличие от платинового практически не хемосорбирует большинство органических веществ и поэтому не отравляется, т.е. токи окисления глюкозы на нем стабильны в растворах, содержащих другие органические вещества. Система не предъявляет никаких специальных требований к противоэлектроду (катоду) и к электроду сравнения. Измерения можно проводить в режиме вольтамперометрии с обычной полярографической ячейкой с золотым электродом и при постоянном потенциале. Ток, протекающий в цепи при окислении глюкозы, прямо пропорционален ее концентрации в растворе. Выбор рабочего электрода-катализатора сделан на основании проведенных исследований электроокисления глюкозы в кислых, щелочных и нейтральных растворах на различных электроах из металлов I и VIII групп, стеклоуглероде и фталоцианинах кобальта и марганца. Величины токов окисления глюкозы на этих электродах приведены в табл.1 Таблица 1

| название | год | авторы | номер документа |
|---|---|---|---|
| АНОД ТОПЛИВНОГО ЭЛЕМЕНТА НА ОСНОВЕ МОЛИБДЕНОВЫХ БРОНЗ И ПЛАТИНЫ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2014 |
|
RU2564095C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЦИСТЕИНА В ВОДНЫХ РАСТВОРАХ МЕТОДОМ ЦИКЛИЧЕСКОЙ ВОЛЬТАМПЕРОМЕТРИИ НА ГРАФИТОВОМ ЭЛЕКТРОДЕ, МОДИФИЦИРОВАННОМ КОЛЛОИДНЫМИ ЧАСТИЦАМИ ЗОЛОТА | 2011 |
|
RU2463587C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПЛАТИНЫ В РУДАХ МЕТОДОМ ИНВЕРСИОННОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2010 |
|
RU2426108C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПЛАТИНЫ В ВОДНЫХ РАСТВОРАХ МЕТОДОМ ИНВЕРСИОННОЙ ВОЛЬТАМПЕРОМЕТРИИ ПО ПИКАМ СЕЛЕКТИВНОГО ЭЛЕКТРООКИСЛЕНИЯ ВИСМУТА ИЗ ИНТЕРМЕТАЛЛИЧЕСКОГО СОЕДИНЕНИЯ PtBi | 2009 |
|
RU2390011C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ВИСМУТА В ВОДНЫХ РАСТВОРАХ МЕТОДОМ ИНВЕРСИОННОЙ ВОЛЬТАМПЕРОМЕТРИИ ПО ПИКАМ СЕЛЕКТИВНОГО ЭЛЕКТРООКИСЛЕНИЯ ВИСМУТА ИЗ ИНТЕРМЕТАЛЛИЧЕСКОГО СОЕДИНЕНИЯ AuBi | 2011 |
|
RU2478944C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ОСМИЯ ИНВЕРСИОННО-ВОЛЬТАМПЕРОМЕТРИЧЕСКИМ МЕТОДОМ В ПРИРОДНОМ И ТЕХНОГЕННОМ СЫРЬЕ НА ГРАФИТОВОМ ЭЛЕКТРОДЕ, МОДИФИЦИРОВАННОМ ЗОЛОТОМ | 2012 |
|
RU2490624C1 |
| Способ кулонометрического определения иридия | 1981 |
|
SU1038870A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПЛАТИНЫ В ВОДНЫХ РАСТВОРАХ И ТЕХНОЛОГИЧЕСКИХ СЛИВАХ МЕТОДОМ ИНВЕРСИОННОЙ ВОЛЬТАМПЕРОМЕТРИИ | 2011 |
|
RU2467320C1 |
| Способ определения концентрации ингибиторов коррозии в пластовой воде (варианты) | 2024 |
|
RU2823917C1 |
| Способ приготовления электродов для количественного электрохимического определения 1,4-дигидроникотинамида аденин динуклеотида (NA DH) в растворе | 1988 |
|
SU1806187A3 |
СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ГЛЮКОЗЫ В КРОВИ IN VIVO с помощью электррда из благородного металла с последующим измерением тока или потенциала окисления глюкозы, отличающийся тем, что, с целью повышения точности способа, электроокисление глюкозы проводят на золотом электроде при рН 9,514,0.
0,2
О
О
О О О
0,02 0,08 О
Кобальт
Никель
Золото
Платина
Медь
Стеклоуглеро
Фталоцианины кобальта
Фталоцианины марганца Полученные результаты показывают что золотой электрод в щелочных рас ворах является лучшим электродомкатализатором для электроокисления глюкозы в щелочной среде. В щелочной среде золотой электро оказывается полностью нечувствитель ным к присутствию ионов хлора, даже в физиологической концентрации (1,610 MNaCl), что особенно важно при использовании этого метода для биологических жидкостей. Для получения воспроизводимых результатов проводится регенерация поверхности золотого электрода путем использования электрохимического способа наложения потенциодинамического импульса, состоящего из двух ступеней. На первой ступени проводят выдержку при потенциале окисления поверхности электрода Е 1,451,55 В в течение 2-5 с, при котором происходит окисление всех органических примесей, адсорбированных на поверхности электрода и покрытие поверхности электрода защитным слоем окисла, на второй - выдержку электро да при восстановительном потенциале Ej 0-0,02 В в течение 2-5 с, при котором происходит восстановление не окислившихся примесей и восстановление окисного слоя и чистая поверхность электрода оказывается в контакте с анализируемым раствором. Затем проводится выдержка при Е 0,05-0,06 В в течение 2-5 с для установления адсорбционного равновесия и диффузионного режима в приэлектрод ном слое. После этого на электрод на кладывается линейно возрастающий по1113744
Продолжение табл. 1
О
О
О
О
,008
5,8
49,0
,85
3,0
1,5
О
О
7,0
О
0,22
О 0,26 тенциал с достаточно медленной скоростью V 12,5 мВ/с. Для проведения анализа на содержание глюкозы в ячейку заливают строго определенный объем 1 М КОИ и вводят 0,1-2,5 мл жидкости, содержащей глюкозу, и, накладывая сложный потенциодинамический импульс, проводят активацию и записывают зависимость тока окисления от потенциала со скоростью 12,5 мВ/с. Измерения можно проводить в режиме измерения стационарного тока при постоянном потенциале (Е 1,0-1,1 В) При этом на электрод накладывают очистительный импульс, затем задают потенциал Е 1.0-1,1 В и измеряют ток при этом потенциале. Концентрацию глюкозы определяют по калибровочной кривой зависимость тока окисления от концентрации глюкозы. В области потенциалов окисления 1,0-1,1 В относительно водородного электрода в том же растворе ток окисления прямо пропорционален концентрации глюкозы в диапазоне концентраций 0,01 (5,5 10М) - 2000 мг% (0,11 М). При анализе сложных многокомпонентных жидкостей калибровочную кривую лучше строить по данным, полученным не для чистых растворов глюкозы, а для тех же жидкостей с разным количеством глюкозы, т.е. в присутствии всех компонентов данной жидкости. Это позволяет увеличить точность измерений . Измерения можно проводить на золотом электроде, отделенном от исследуемой жидкости проницаемой для глюкозы мембраной, но не проницаемой для других компонентов жидкости. При использовании такой полупроницаемой мембраны ток может приобрести диффузионный характер по отношению к глюкозе, и коэффициент диффузии определяется мембраной. Мембрана вносит дополнительное диффузионное сопротивление, снижая ток, но он остается достаточно большим и хорошо измеряемым. :,
Пример 1, Определение содержания глюкозы в потенциодинамическом режиме.
В трехэлектродную ячейку заливают раствор глюкозы (0,11 М)в 1М КОН (рН 13,6), подают на электрод трехступенчатый импульс Е 1,5 В, Е2 0,02 в и ЕЗ 0,05 В и выдерживают при каждом потенциале 5 с. От потенциала 0,05 В на полярографе ПО-5122 модель ОЗА при скорости развертки 12,5 мВ/с снимают потенциодинамическую кривую и фиксируют ток при потенциале максимального значения тока, т.е. при Р: 1,1 В.
По калибровочной кривой определяют содержание глюкозы.
В табл, 2 представлены результаты определения глюкозы на золотом электроде в 1м КОН в потенциодинамическом режиме.
Таблица2
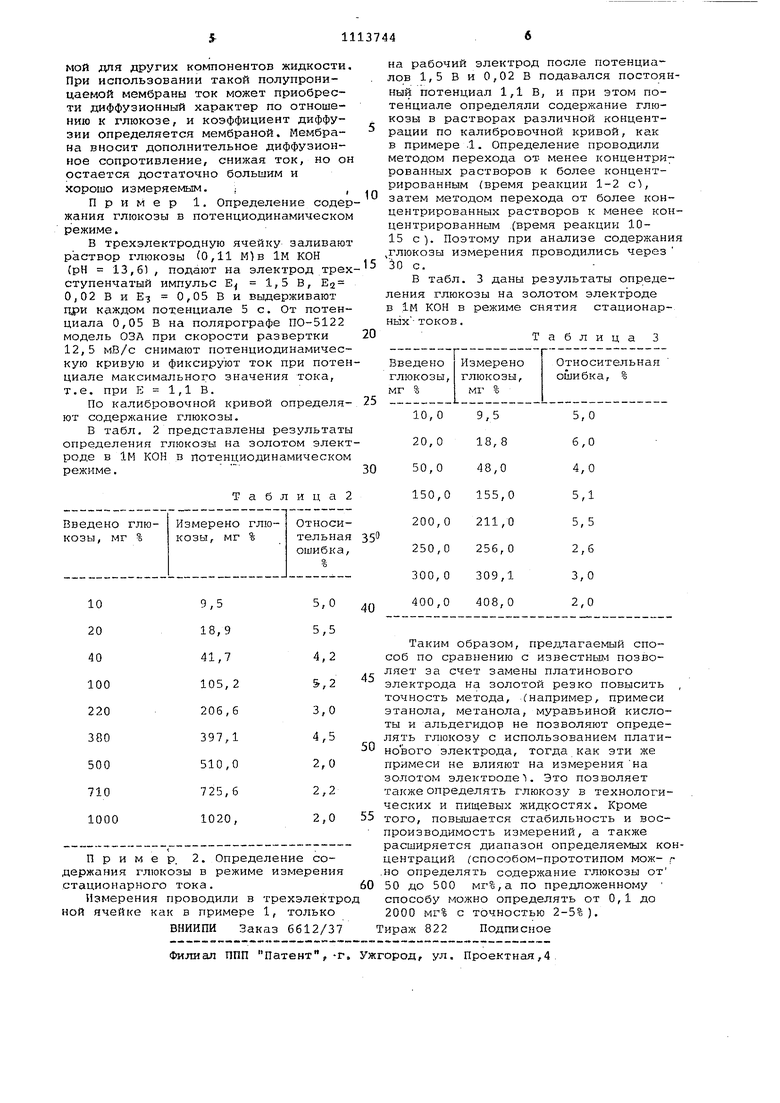
на рабочий электрод после потенциалов 1,5 В и 0,02 В подавался постоянный потенциал 1,1 В, и при этом потенциале определяли содержание глюкозы в растворах различной концентрации по калибровочной кривой, как в примере .1. Определение проводили методом перехода от- менее концентрированных растворов к более концентрированным (время реакции 1-2 с, затем методом перехода от более концентрированных растворов к менее концентрированным .(время реакции 1015 с). Поэтому при анализе содержани глюкозы измерения проводились через 30 с.
В табл. 3 даны результаты определения глюкозы на золотом электроде в 1м КОН в режиме снятия стационарных- токов,
Таблица 3
| , 1 | |||
| УСТАНОВКА ФС-525 ДЛЯ ПОЛУЧЕНИЯ КИСЛОРОДА И ВОДОРОДА | 1992 |
|
RU2019580C1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1984-09-15—Публикация
1982-11-30—Подача