11
Изобретение относится к физико химическим методам анализа и может найти применение в химической технологии, металлургии и других отраслях промьшленности.
Известен ионоселективный электрод на кадмий, которьш получают втиранием активного вещества (зкви-молярная смесь сульфидов кадмия и серебра) в гидрофобизированн-с.гй тефлоном, поливинилхлоридом или полиэтиленом графит ll .
Недостатками этого электрода являются необходимость предварительного вымачивания электрода перед измерениями в течение 1-2 сут и небольшой срок службы.
Известен кадмийселективный электрод на основе смеси сульфида сереб ра с 0,3-50 мол.% теллурида кадмия 2j .
Недостатки данного электрода меньшие стабильность и воспроизводимость потенциала, чем у электродов сульфидных систем.
Наиболее близким по технической сущности к предлагаемому является состав мембраны халькогенидного электрода для определения ионов кадмия, мембрана которого состоит из поликристаллической смеси сульфидов серебра и кадмия .
Известный состав характеризуется недостаточной протяженностью рабочей области рН в кислых средах и относительно невысокой селективностью к ионам щелочных металлов.
Цель изобретения - расширение рабочего диапазона рН и повышение селективности к щелочным катионам.
Поставленная цель достигается ем, что состав мембраны халькогеидного электрода для определения онов кадмия содержит смесь иодида адмия, сульфида серебра и сульфида ьппьяка, приведенную в стеклообразое состояние, при следующем соотноении компонентов, мол.%: Иодид кадмия 5-20 Сульфид серебра 32-63 Сульфид мышьяка 32-57 Предложенные концентрационные преелы определяются областью стеклообразования в системе иодид кадмия сульфид серебра - сульфид мьпиьяка и электродными характеристиками стекол.
25534 .2
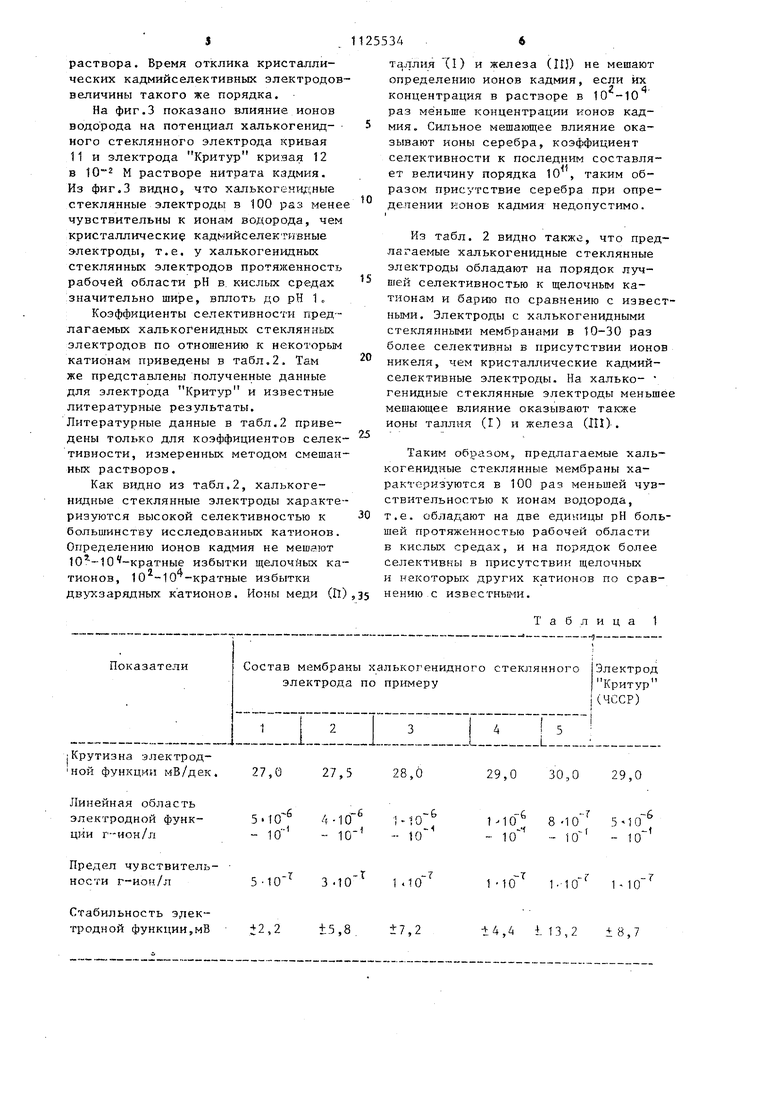
На фиг.1 изображена область стеклообразования в системе CdJ -Ag-SА8„3,; на фиг.2 - зависимость ЭДС электрохимической ячейки от логариф5 ма активности ионов кадмия в растворе, на фиг,3 - кривая, иллюстрирующая влияние ионов водорода на потенциал халькогенидного стеклянного электрода и электрода Критур в o растворе Cd(NO )2Области А иБ {фиг.1).- область стеклообразования в системе иодид кадмия - сульфид серебра - сульфид мышьяка. Стекла из области А, т.е. 5 сплавы, содержащие менее 5 и более 20 мол.% иодида кадмия, характеризуются неудовлетворительными электродными свойствам. Стекла, содержащие более 57 мол.% сульфида мьшь0 яка, обладают низкой электропроводностью, невысокой механической прочностью и химической устойчивостью, поэтому их применение в качестве мембранных материалов малоэффектив5 но.
Стекла из области Б с указанными концентрационными пределами обладают наилучшими электродными характеристиками. Составы стекол из области 0 Б (фиг„1, позиции 1-5) соответству,ют ппиведенным ниже npiiKepaM. .
Пример 1. Для получения 3 г стекла состава 5CdI -63AgjS-32As2 S (точка 1) берут 0,217 г иодида кад5 мия 1,850 г сульфида серебра,
0,933 г сульфида мьшьяка и помещают в кварцевую ампулу. Ампулу откачивают до остаточного давления воздуха
V
10 Па и проводят синтез при 1150 К
0- в течение 8 ч. Охлаждение осуществляют посредством закалки расплава со средней скоростью 100 град/с.
П р им е -р 2. Стекло состава 5CdJ238Ая2 S57AS2 S g (точка 2) син5 тезируют аналогично примеру 1, но для получения 3 г стекла берут 0,217 г иодида кадмия, 1,118 г сульфида серебра и 1,665 г сульфида мьшьяка.
0 Пример Зг Стекло состава
lOCdJj45Ag2S 45As2S (точка 3) синтезируют аналогично примеру 1, но для получения 3 г стекла берут Oj424 г иодида кадмия, 1,293 г суль5 Фида серебра и 1,283 г сульфида мышьяка.
Пример i. Стекло состава 20CdJ240Ap,;S40As S3 (точка 4) сии3
тезируют аналогично примеру 1, но для получения 3 г стекла берут 0,812 г иодида кадмия, 1,098 г сульфида серебра и 1,090 г сульфида мьшьяка.
Пример 5. Стекло состава ZOCdJj-aZAg S-ABASjS, (точка 5) синтезируют аналогично примеру 1, но для получения 3 г стекла берут 0,812 г иодида кадмия, 0,879 г сульфида серебра и 1,300 г сульфида мышьяка
КС1исследуAgCl насы- 1 М KNO емый
щенный где М - мембрана из халькогенидного стекла. Калибровочные растворы в концентрационной области от 10 до 10 гион кадмия/л готовят из нитрата кад мия. Растворы с концентрацией ионов кадмия от 10 до Ю г-ион/л готовят непосредственно перед измерениями в тефлоновой ячейке добавлением к известному объему дистиллированной воды или индифферентного электролита небольших калиброванных количест более концентрированных растворов нитрата кадмия. Для измерений коэффициентов селективности используют метод смешанных растворов, при кото ром концентрацию мешающего иона под держивают постоянной (чаще всего 1 г-ион/л), а концентрацию ионов кадмия от 1СГ°до г-ион/л) , Для определения коэффициентов селективности к сильномешающим катио нам(меди ( П ) , железа (lit) используют обратную процедуру. Закрепляют концентрацию ионов кадмия, а изменяю концентрацию мешающих ионов. Определение коэффициентов селективности к ионам серебра проводят по методу отдельных растворов. Рабочую область рН кадмийселективных электродов исследуют при постоянной концентрации ионов кадмия в среде с постоянной ионной силой ,0. Кислотность растворов изменяют добавлением азотной кислоты или гидроксида лития, рН растворов контролируют с помощью рН-метров, откалиброванных по стандартным буферным растворам. Измерение ЭДС электрохимической ячейки с исследуемыми электродами осуществляют при помощи цифровых вольтмет5344
Стекла разрезают на плоскопараллельные диски толщиной 1-Д мм. Полученные таким образом мембраны полируют до зеркального блеска на пасте ГОИ и вклеивают эпоксидным компаундом в поливинилхлоридный корпус электрода.
Для изучения электродных характеристик применяют следующую электрохимическую ячейку:
10- MgANO, Ю MgCdCNO)
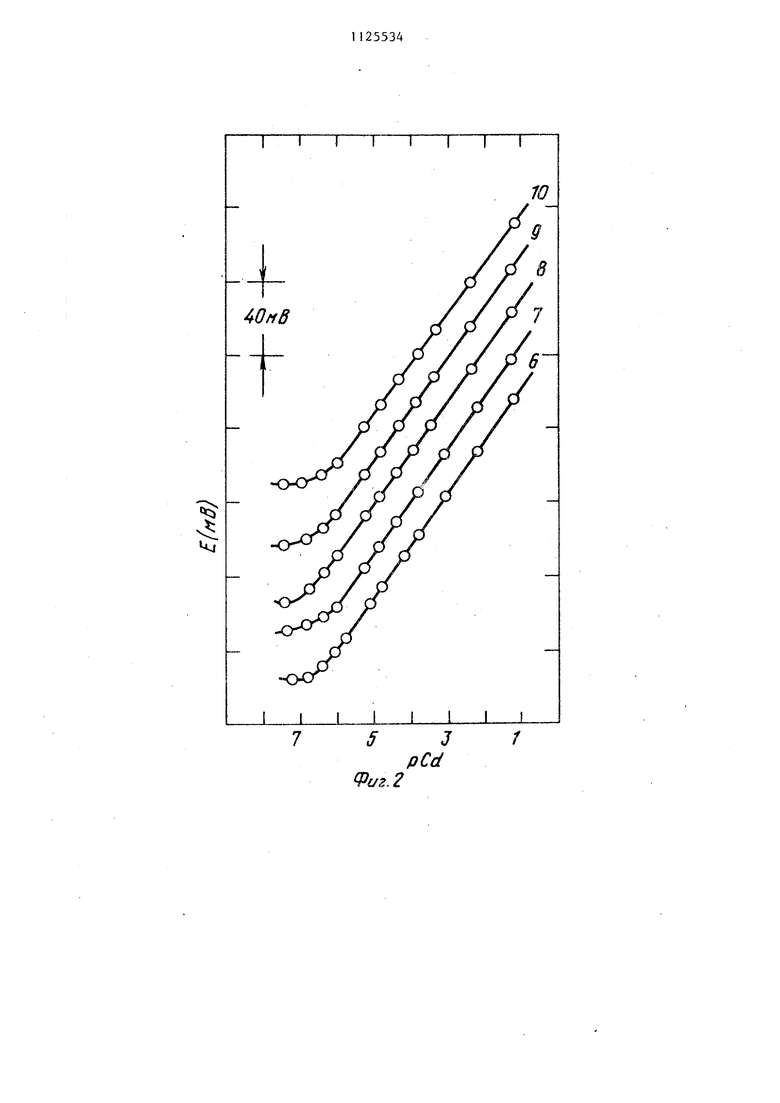
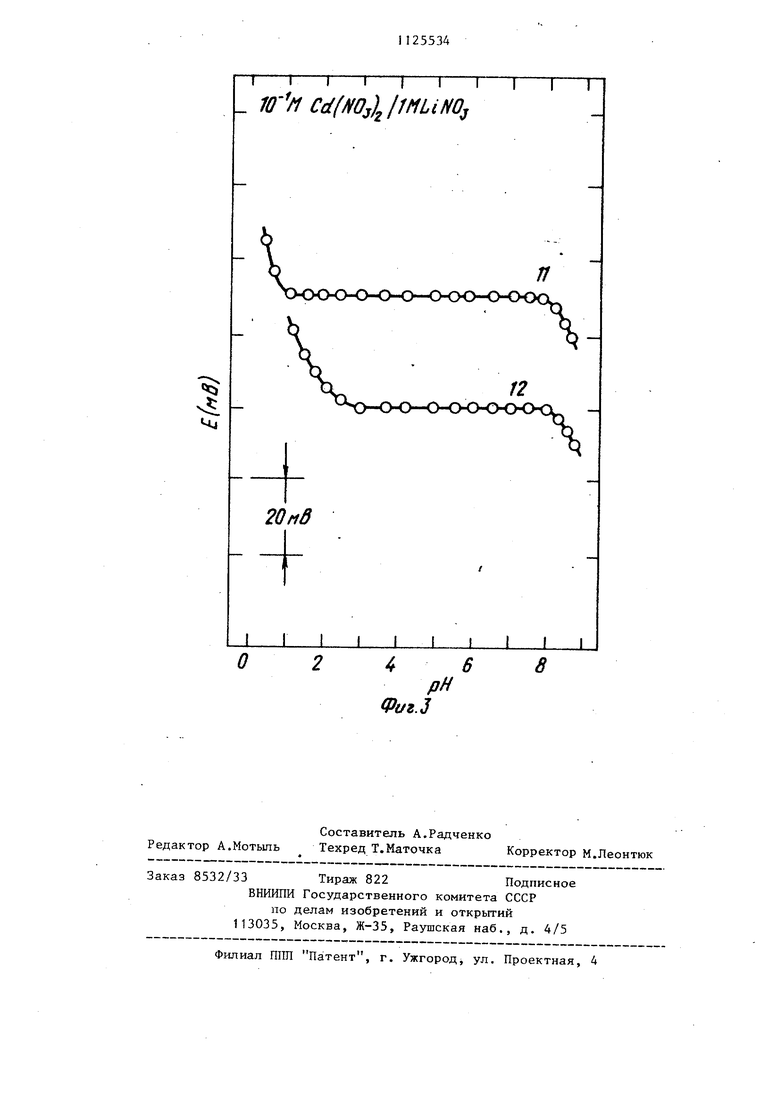
раствор ров (входное сопротивление 10 Ом) или иономеров. На фиг.2 показаны характерные за висимости ЭДС электрохимической ячейки от логарифма активности ионов кадмия в растворе, откуда видно, что все исследуемые электроды (позиции 6-10 соответствуют примерам 1-5) обладают высокой чувствительностью к ионам кадмия в растворе. В табл. 1 представлены величины угловых коэффициентов и протяженность линейной области электродной функции халькогенидных стеклянных электродов и коммерического кадмийселективного электрода Критур производсува ЧССР с поликристаллической мембраной состава сульфид кадмия сульфид серебра, который исследовался в тех же условиях, а также пределы чувс- вительнрсти полученных электродов и стабильность электродного потенциала в 1СГ.М растворе нитрата кадмия в течение 4 мес. работы. Из табл. 1 видно, что крутизна электродной функции составляет 2630 мВ/дек. в зависимости от состава стекла, т.е. близка или совпадает с теоретическим значением для двухзарядной электродной функции (29,6 мВ/дек.). По своей чувствительности, протяженности линейной области электродной функции и стабильности работы халькогенидные стеклянные электроды не уступают кристаллическому электроду Критур, а некоторые составы стекол даже превосходят последний. Время отклика халькогени/гных стеклянных электродов в растворах нитрата кадмия составляет 5-20 с в зависимости от концентрации исходного раствора. Время отклика кристаллических кадмийселективных электродов величины такого же порядка. На фиг.З показано влияние ионов водорода на потенциал халькогенидного стеклянного электрода кривая 11 и электрода Критур кривая 12 в 10 М растворе нитрата кадмия. Из фиг.З видноJ что халькогенщ ные стеклянные электроды в 100 раз мене чувствительны к ионам водорода, чем кристаллические кадмийселективные э-лектроды, т.е. у халькогенидных стеклянных электродов протяженность рабочей области рН в. кислых средах значительно шире, вплоть до рН 1, Коэффициенты селективности гфедлагаемых халькогенидных стеклянных электродов по отношению к некоторым катионам приведены в табл.2. Там же представлены полученные данные для электрода Критур и известные литературные результаты. Литературные данные в табл.2 приведены только для коэффициентов селек тивности, измеренных методом смешан ных растворов. Как видно из табл.2, халькогенидные стеклянные электроды характе ризуются высокой селективностью к большинству исследованных катионов. Определению ионов кадмия не мешают 10 -10 -кратные избытки щелочйых ка тионов, 10 -Ю -кратные избытки двухзарядньгх катионов. Ионы меди (П таллия (1) и железа (IIJ) не мешают определению ионов кадмия, если их концентрация в растворе в 10 -10 раз меньше концентрации ионов кадмия. Сильное мешающее влияние оказывают ионы серебра, коэффициент селективности к последним составляет величину порядка 10 , таким образом присутствие серебра при определении ионов кадмия недопустимо. Из табл. 2 видно также, что предлагаемые халькогенидные стеклянные электроды обладают на порядок лучшей селективностью к щелочным катионам и барию по сравнению с известными. Электроды с халькогенидными стеклянными мембранами в 10-30 раз более селективны в присутствии ионов никеля, чем кристаллические кадмийселективные электроды. На халько- генидные стеклянные электроды меньшее мешающее влияние оказывают также ионы таллия (Г) и железа (III)-. Таким образом,, предлагаемые халькогенидные стеклянные мембраны характеризуются в 100 раз меньшей чувствительностью к ионам водорода, т.е. обладают на две рН большей протяженностью рабочей области в кислых средах, и на порядок более селективны в присутствии щелочных и некоторых других катионов по сравнению.с известнььми.


| название | год | авторы | номер документа |
|---|---|---|---|
| Состав халькогенидной стеклянной мембраны электрода для определения ионов кадмия | 1989 |
|
SU1711055A1 |
| Состав халькогенидной стеклянной мембраны электрода для определения ионов свинца | 1983 |
|
SU1075135A1 |
| Состав мембраны халькогенидного стеклянного электрода для определения ионов меди (п) | 1983 |
|
SU1100553A1 |
| Состав мембраны халькогенидного стеклянного электрода для определения ионов железа ( @ ) | 1983 |
|
SU1125533A1 |
| Состав мембраны ионоселективного электрода для определения ионов ртути (II) | 1990 |
|
SU1718082A1 |
| Состав мембраны ионоселективного электрода для определения ионов брома | 1985 |
|
SU1260815A1 |
| СОСТАВ ХАЛЬКОГЕНИДНОЙ СТЕКЛЯННОЙ МЕМБРАНЫ ЭЛЕКТРОДА ДЛЯ ОПРЕДЕЛЕНИЯ ИОНОВ СВИНЦА | 1989 |
|
RU2034289C1 |
| СОСТАВ МЕМБРАНЫ ИОНОСЕЛЕКТИВНОГО ЭЛЕКТРОДА ДЛЯ ОПРЕДЕЛЕНИЯ ИОНОВ КАДМИЯ | 2010 |
|
RU2428683C1 |
| Кадмий-селективный электрод | 2019 |
|
RU2712920C1 |
| Состав халькогенидной стеклянной мембраны электрода для определения ионов свинца | 1988 |
|
SU1583820A1 |
СОСТАВ МЕМБРАНЫ ХАЛЬКОГЕНИДНОГО ЭЛЕКТРОДА ДЛЯ ОПРЕДЕЛЕНИЯ ИОНОВ КАДМИЯ, отличающийс я тем, что, с целью расширения рабочего диапазона рН и повышения селективности к щелочным катионам, он содержит смесь иодида кадмия, сульфида серебра и сульфида мьпльяка, приведенную в стеклообразное состояние, при следующем соотношении компонентов, мол.%: Иодид кадмия 5-20 Сульфид се$эебра 32-63 32-57 Сульфид мьшьяка CdJ. (Л N9 СЛ СЛ оо 4 20 40 6080 Фиг. Г
(Крутизна электродной функции мВ/дек. 27,027,5 Линейная область 5.10; 4-10 электродной функ- 10 - 10 ции Г--ИОН/Л
5-10 3-10
4 2 +58
. J J- I у i1 ЧО ЫО
±4,4 113,2 ±8,7 28,0 29,0 30,0 29,0 8-10 540 .- - - 10
Т а б ли ц а 2
pCd
иг.2
Т 1I
Wfl Cd() /fULi/ Oj
I I I I г
«
Ч.
8
pH
Фиг.З
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ химического окрашивания никеля | 1986 |
|
SU1382873A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Устройство станционной централизации и блокировочной сигнализации | 1915 |
|
SU1971A1 |
Авторы
Даты
1984-11-23—Публикация
1983-08-03—Подача