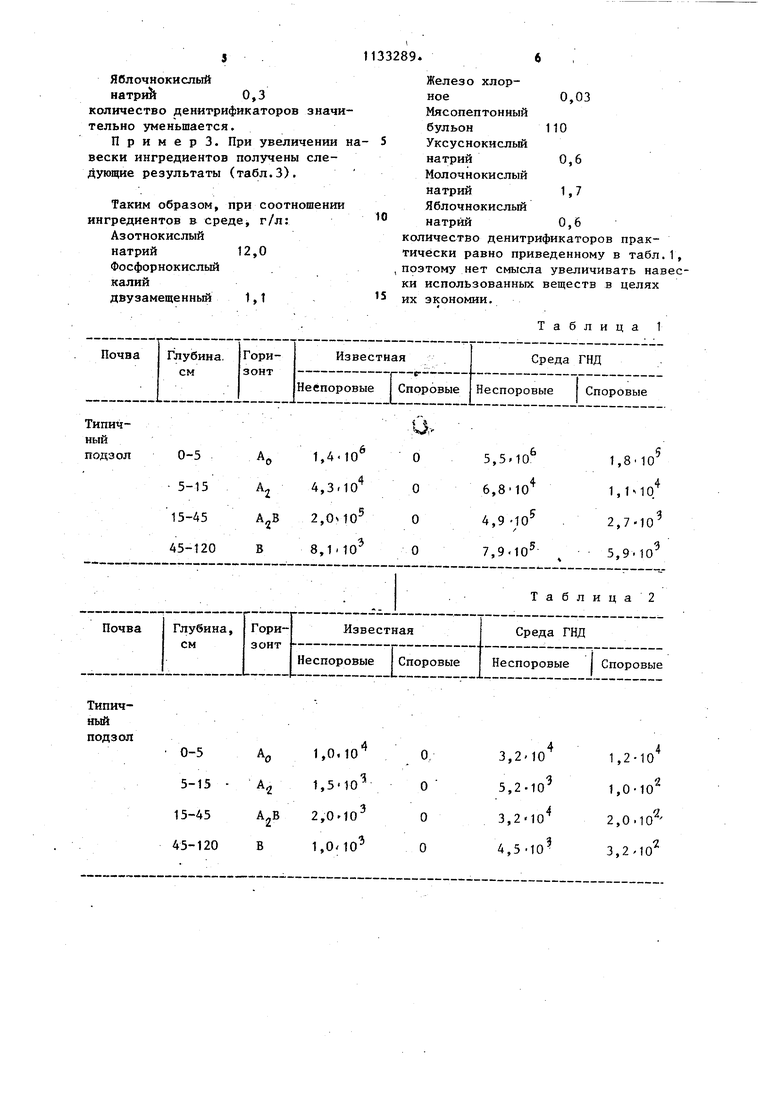
Изобретение относится к почвенно микробиологии и может быть использо вано для характеристики биологической активности и изучения азотного режима почв. Известно использование для обнаружения микроорганизмов, диссимилирующих нитраты, среды Гильтая, дл приготовления которой берут два рас вора,. Первый раствор содержит, г: азотнокислый калий 2,1; аспарагин 1 дистиллированная вода 250 мл. В сос тав второго раствора входят, г: Лимоннокисльм натрий 5,0; фосфорнокислый калий двузямещенный 2,0; сер нокислый марганец 2,0} хлорное железо следы; дистиллированная ..вода 500 мл. Оба.раствора сливают вместе, устанавливают рН 6,8-7,0 и объе доводят до 1 л. Подсчет проводят методом предельных; разведений, с до мощью которого, на среде Гильтая по мутности, изменению рН и газообразо ванию определяют количество денитри фикаторов iTОднако на известной среде невозм но разграничить на группы, диссимилирующие нитрат микроорганизмы, а т же вьшвить споровые формы. Целью изобретения является более полное выявление общего количества диссимилирующих нитраты микрооргани мов в. почве, а также обнаружение спорообразующих и восстанавливаклдих нитраты до нитритов микроорганизмо этой группы. Цель достигается тем, что питат ная среда для культивирования ;поч венных микроорганизмов, включающая азотнокислый калий, фобфорнокисльй калий двузамещенньй, хлорное желез и дистиллированную воду, сре;да доп нительно содержит мясопептонньШ бул он, уксуснокислый натрий, молочнокислый натрий, яблочнокислый натрий при следукщем соотношении компонен тов, г/л: Азотнокислый скалий8,0-12,0 Фосфорнокислый калий двузамещенный 0,9-1,0 0,01-0,03 Хлорное железо Мясопептонный 90-100 бульон Уксуснокислый 0,4-0,6 натрий- Молочнокислый 1,3-1,7 натрий Яблочнокислый натрий 0,4-0,6 Вода дистиллированнаяДо 1 л Значение рН среды доводят до 7,5-8,0. Среду разливают в пробирки по 10 мл, закрывают ватными пробка ми, стерилизуют при 0,5 атм давления пара и инкубируют в анаэробных или микроаэрофильных условиях. При. подборе среды, удовлетворяющей физиологические потребности большинства компонентов диссимилирующей нитраты микрофлоры почвы, приняты во внимание следующие сообра жения. Осуществление процессов биологической денитрификации в почве происходит за счет, использования боковых алифатических полипептидов молекул гумусовых веществ н качестве источника углерода и энергии. Следовательно, рекомендуемая среда ближе по составу к природной почвенной среде обитания диссимилирующих нитраты микроорганизмов, поскольку она приготовлена на основе разбавленного мясопептонного бульона. Кроме того, эта среда отличается от известной присутствием комплекса солей органических кислот, легко доступных для большинства.денитрификаторов, а также повышенной в пять раз концентрацией нитрата и более высоким содержанием железа, стимулирующего денитрификацию. Количество диссимилирующих нитра- . ты микроорганизмов, выросших на этой среде, подсчитываютметодом предельных разведений- по качественным реакциям на присутствие нитрата и нитрита. Таким образом, предлагаемая среда позволяет обнаружить различные группы диссимилирующих нитраты почвенных микроорганизмов, что дает возможность одновременно учеств количество обеих групп микроорганизмов, осуществляющих процессы нитратного дыхания, денитрифицирующие, а также микроорганизмы, восстанавливающие нитрат до нитрита. Кроме того, на предлагаемой среде развиваются и спорообразующие формы этих микроорганизмов. Предлагаемая среда обозначена ГНД (согласно ее назначению - выявлению микроорганизмов группы нитратного дыхания с учетом большего количества входящих в ее состав компонентов). Для обнаружений нитратов и нитритов всреде ГИД используют два ре актива в виде смеси веществ. Первой готовят растиранием 1 г сульфаниловой кислоты и- 2 г oL -нафтиламина ступке пестиком. Добавляют 100 г сульфата бария и 75 г лимонной кислоты, тщательно перемешивают все ко поненты. Второй реактив готовят из 10 г сернокислого марганца и 2 г цинковой пыпи, также тщательно растерных и перемешанных в ступке. В 0,5 - 2 мл культуральной среды проводят качественные реакции. Добавляют пять капель ледяной уксусно кислоты кончике скальпеля первьй реактив. Отсутствие красного, ок рашивания является показателем того что весь нитрат восстановился до га образных форм азота в процессе данитрификации. Появление кр-асного окрашивания свидетельствует о BOG-/ становлении нитратов -до нитритов. , С пробирками, в которых отмечался-., рост, но нитрит не бьщ обнаружен, л ступают следующим образом. Добавляю на кончике скальпеля второй реактив Отсутствие красного окрашивания означает, что весь добавленньн нитрат денитрифицировался. Появление красного окрашивания констатирует наличие незатронутого или остаточ ного нитрата. Эти пробирки при подсчете количества денитрификаторов, соответственно, принимаются или не принимаются во внимание. Подсчет диссимилирующих нитраты микроорганизмов производят через . три недели после посева. Количество различных групп микроорагнизмов осуществляющих процессы нитратного дыхания, устанавливают по таблице Мак-Креди. Для определения количества спорообразующих микроорганизмов обеих групп, денитрификаторов и восстанав ливающих нитраты до нитритов про- водят параллельный посев пастеризов ной суспензии почвы на средах известной и ГНД. Результаты исследований показали, что на известной ер де спорообразующие формы микроорганизмов, обладающих способностью к осуществлению процессов нитратного дыхания, не развиваются. Среда ГНД обеспечивает условия для развития этих -микроорганизмов. Пример 1. Используют среду состава, г/л: азотнокислый калий 10,Oj фосфорнокислый калий двузамещенныа 1,OJ хлорное железо 0,02f мясопептонный бульон ГОО; уксуснокислый натрий 0,5; молочнокислый натрий 1,5 яЭлочнокислый натрий 0,5, вода дистиллированная до 1 л. Устанавливают рН 7,5-8,0. Среду разливают по 10 мл в пробирки и стерилизуют.при 0,5 атм. Затем пробирки со средой инокулируют 1 мл почвенной суспензии соответствующих разведений. Инкубируют в ; анаэростате при 28®С в течение 3 нед |0тбирают пробирки со средой, где отмечается рост микроорганизмов (по мутности). Из этих пробирок оставляют 0,5-2 мл на анализ. Добавляют пять капель ледяной уксусной кислоты и 0,1 гпервого реактива. Пробирки, в котррых красное окрашивание присутствует, используют дня количественного подсчета микроорганизмов , восстанавливающих нитраты до нитритов. К культуральной жидкости пробирок с отсутствием красного окрашивания добавляют второй реактив. Отсутствие красного окрашивания свидетельствует о полном восстановленни нитрата до газообразных форм азота. Эти пробирки используют для количественнаго подсчета, денитрификаторов. Присутствие красного окрашивания указывает, на наличие нитрата в среде. Эти пробирки отбрасьшают. Количество микроорганизмов подсчитывают методом предельных разведений. . Полученные данные представлены в табл.1. П р и м е р 2. При уменьшении наески ингредиентов предлагаемой ере-, ы получены данные., представленные в табл.2. Таким образом, при соотношении нгредиентов в среде, г/л: Азотнокислый . ,;калий7,0 Фосфорнокисльй калий двузамещенный 0,8 Железо хлорное 0,009 Мясопептонный бульон 80 Уксуснокислый натрий 0,3 Молочнокислый натрий 1,2 Яблочнокислый натрий 0,3 количество денитрификаторов тельно уменьшается. Пример 3. При увелич вески ингредиентов получены дующие результаты (табл.3). Таким образом, при соотн ингредиентов в среде, г/л: Азотнокислый натрий 12,0 Фосфорнокислый калий двузамещенный 1,t Железо хлорное0,03 Мясопептонный бульон 110 Уксуснокислый натрий 0,6 Молочнокислый натрий 1,7 Яблочнокислый натрий 0,6 ичество денитрификаторов пракески равно приведенному в табл.1, тому нет смысла увеличивать навесиспользованных веществ в целях экономии. Таблица 1


| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ MICROCOCCUS VARIANS 8,0, ИСПОЛЬЗУЕМЫЙ ПРИ ПРОИЗВОДСТВЕ МЯСОПРОДУКТОВ | 1995 |
|
RU2091486C1 |
| СПОСОБ ПОЛУЧЕНИЯ БАКТЕРИАЛЬНОГО ПРЕПАРАТА ДЛЯ ПРИГОТОВЛЕНИЯ МЯСНЫХ ПРОДУКТОВ | 2004 |
|
RU2275423C2 |
| Способ обнаружения энтеробактерий в воде | 1988 |
|
SU1700468A1 |
| СОСТАВ ДЛЯ КУЛЬТИВИРОВАНИЯ ЭШЕРИХИЙ | 1997 |
|
RU2142505C1 |
| СИНТЕТИЧЕСКАЯ ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫРАЩИВАНИЯ МИКРООРГАНИЗМОВ | 2014 |
|
RU2547932C1 |
| ДВУХФАЗНАЯ ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ВЫДЕЛЕНИЯ БРУЦЕЛЛЕЗНОГО МИКРОБА | 2007 |
|
RU2346052C1 |
| Питательная среда для выращивания посевного материала асSINомYсеS RecIFeNSIS VaR еLYтIсUS 2435 | 1981 |
|
SU981359A1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ ЭШЕРИХИЙ | 1996 |
|
RU2117041C1 |
| Питательная среда для выращивания спор микроорганизмов из рода @ | 1981 |
|
SU1017729A1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ ЭШЕРИХИЙ | 1997 |
|
RU2142506C1 |
ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ ПОЧВЕННЫХ МИКРООРГАНИЗ.МОВ, включакицая азотнокислый калий, фосфорнокислый калий двузамещенный хлорное железо и дистиллированную воду, отличающаяся тем, что, с целью более полного выявления общего количества диссимилирукщих нитраты микроорганизмов в почве, а ; также обнаружения спорообразуннцих и восстанавливающих нитраты до нитритов микроорганизмов этой группы, среда дополнительно содержит мясопептонный бульон, уксуснокислый натрий, молочнокислый натрий, яблочнокислый натрий при следующем соотношении компонентов, г/л: Азотнокислый калий8,0-12,0 Фосфорнокисльш калий двузамещенный0,9-1,0 Хлорное железо 0,01-0,03 Мясопептонный бульон90-100 Уксуснокисльй 0,4-0,6 натрий О) Молочнокислый 1,3-1.7 натрий Яблочнокислый 0,4-0,6 натрий Вода дистиллироДо 1 л ванная
1,0.10 1,510 2,010 1,010Таблица2
4
3,2-10
1,2-10 5,2-10 1,0-10 3,2-Ю
г 2,0.10 4,5-10 3,2.10
Таблица 3
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Теппер Е.З | |||
| Шильникова В.К | |||
| и Переверзева Г.И | |||
| Практикум по микро биологии | |||
| М., Колос, 1979, с.144 (прототип). | |||
Авторы
Даты
1985-01-07—Публикация
1983-06-30—Подача