Изобретение относится к биотехнологии, в частности к микробиологии, и может быть использовано для выращивания культур эшерихий на простой и дешевой питательной среде без потери ее эффективности.
Выделение эшерихий, продуцирующих энтеротоксины, позволяет установить диагноз на колибактериоз при бактериологическом исследовании патматериала. Кроме того, при конструировании вакцин против колибактериоза необходимо учитывать наличие энтеротоксигенных штаммов и применять анатоксины.
Известна питательная среда для выращивания культуры эшерихий (см. а.с. СССР 1472495, кл. C 12 N 1/20, опубл. 15.04.89), содержащая гидролизат казеина, фильтрат культуральной жидкости пекарских дрожжей, глюкозу, фосфорнокислый однозамещенный калий, фосфорнокислый двузамещенный натрий, очищенный агар-агар и водопроводную воду.
Однако данная питательная среда пригодна только для накопления адгезивных антигенов K-99. Кроме этого, процесс приготовления первичных компонентов (гидролизат казеина, фильтрат культуральной жидкости пекарских дрожжей) для конструирования данной среды длителен и трудоемок.
Известна питательная среда Мартена для культивирования эшерихий и получения токсиносодержащего материала (см. А. С. Лабинская, Микробиология с техникой микробиологических исследований. М.: Медицина, 1978, с. 350-351), содержащая пептон и бульон Мартена. Для приготовления пептона требуются свиные желудки, которые необходимо измельчить и подвергнуть воздействию концентрированной соляной кислоты. Данная операция занимает 2 сут. Кроме этого, употреблять его можно не ранее чем через 5 сут после приготовления. Бульон Мартена готовят из мясного фарша "вырезки". Используют хлебные дрожжи. Проводят подщелачивание раствором едкого натра, добавляют ацетат натрия. Бульон Мартена стерилизуют дробно текучим паром 2 дня подряд по 40 мин.
Таким образом, среда Мартена содержит дорогостоящие компоненты. Приготовление ее трудоемко и длительно по времени.
Известна также питательная среда для культивирования эшерихий (см. а.с. СССР 1750690, кл. A 61 K 39/108, опубл. 30.07.92), содержащая перевар Хоттингера, сернокислый магний, однозамещенный фосфорнокислый натрий, однозамещенный фосфорнокислый калий, глюкозу и дистиллированную воду.
Однако для приготовления данной питательной среды необходимо использование животного сырья из мышечных тканей и поджелудочной железы. Способ предусматривает длительный этап приготовления первичного компонента среды - перевара Хоттингена (более 10 сут).
Таким образом, способ, также как и предыдущие аналоги, трудоемок и длителен по времени.
Наиболее близкой к заявляемой среде является питательная среда Альдерете (см. Методические рекомендации по получению, очистке энтеротоксинов эшерихий и изготовлению антитоксических сывороток. Харьков, 1988, с. 15 - 16), содержащая двузамещенный фосфорнокислый калий (K2HPO4), хлористый натрий (NaCl), хлористый аммоний (NH4Cl), сернокислый магний (MgSO4), хлористый марганец (MnCl2 • 4H2O), хлористое железо (FeCl3), трицин, дистиллированную воду и аминокислоты α -формы. Процесс приготовления питательной среды включает подготовку раствора двузамещенного фосфорнокислого калия с хлористым натрием, а затем второго раствора из микроэлементов. Оба раствора смешивают и стерилизуют в течение 30 мин. Затем в полученный стерильный раствор в строгой последовательности добавляют аминокислоты: α -пролин, α -аспарагин, α -аланин, α -серин, α -фенилаланин, α -гистидин, α -триптофан.
Основными недостатками данной среды являются сложность ее приготовления и необходимость строгого соблюдения последовательности внесения аминокислот. Кроме этого, аминокислоты являются дорогостоящими компонентами, что существенно повышает затраты на изготовление питательной среды.
Изобретение направлено на решение задачи создания дешевой и простой в изготовлении питательной среды для культивирования эшерихий, обеспечивающей как полноценное развитие кишечной палочки, так и продуцирование ею токсинов.
Поставленная задача решается с помощью состава, содержащего, мас.%:
Двузамещенный фосфорнокислый калий (K2HPO4) - 0,85 - 0,89
Хлористый натрий (NaCl) - 0,225 - 0,245
Хлористый аммоний (NH4Cl) - 0,09 - 0,11
Сернокислый магний (MgSO4) - 0,0047 - 0,0053
Хлористый марганец (MnCl2 • 4H2O) - 0,00047 - 0,00051
Хлористое железо (FeCl3) - 0,00047 - 0,00051
Аминокровин - 9 - 20
Дистиллированная вода - Остальное
В известных заявителю источниках патентной и научно-технической литературы не описано питательных сред для получения энтеротоксина E. coli на основе смеси солевых растворов микро- и макроэлементов с аминокровином, что позволяет сделать вывод о наличии в заявляемом изобретении критерия "Новизна". Кроме этого, неизвестно использование аминокровина в качестве компонента питательной среды для выращивания аэробных бактерий. Обычно аминокровин используют в качестве средства для парентерального питания больных людей при нарушениях процессов усвоения белков вследствие различных желудочно-кишечных и других заболеваний (см., например, Инструкцию по применению аминокровина, утвержденную Управлением по внедрению новых лекарственных средств и мед. техники 20.12.82). Сказанное позволяет сделать вывод о наличии в заявляемом изобретении критерия "Изобретательских уровень".
Двузамещенный фосфорнокислый калий - белые кристаллы солоноватого вкуса, хорошо растворимые в воде.
Хлористый натрий - белые кристаллы соленого вкуса, хорошо растворяются в воде.
Сернокислый магний - белые кристаллы кисловатого вкуса, хорошо растворимые в воде.
Хлористый марганец - розоватые кристаллы кисло-щиплющего вкуса, хорошо растворимые в воде.
Хлористое железо - темно-бурые кристаллы или порошок кислого вкуса, с запахом железа, хорошо растворимые в воде.
Хлористый аммоний - белые кристаллы щиплющего вкуса, без запаха, хорошо растворимые в воде.
Дистиллированная вода - pH 6,8 - 7,0.
Хлористый аммоний применяют как источник азотного питания микроорганизмов. Остальные соли служат как источник минерального питания, а также для обеспечения оптимальных окислительно-восстановительных реакций, необходимой величины pH, а также для осмотического давления и равновесия ионов.
Аминокровин - регистрационный номер 70/151/44, утвержден 28.10.81 Фармкомитетом М3 СССР, выпускается предприятием по производству бактерийных препаратов (ГНИИЭМ) г. Н.Новгород. Представляет собой неполный гидролизат крови (эритроцитарной массы и сгустков крови) человека. Содержит все свободные аминокислоты.
Питательную среду готовят следующим образом.
Готовят раствор N 1 из двузамещенного фосфорнокислого калия с хлористым натрием, затем раствор N 2 из хлористого аммония, сернокислого магния, хлористого марганца, хлористого железа. Растворы смешивают и стерилизуют в течение 30 мин при 121oC. Затем добавляют стерильный раствор аминокровина. Автоклавированию не подвергают.
Пример 1.
К 50 мл дистиллированной воды добавляют навески солей: K2HPO4 0,871 г, NaCl 0,235 г. В оставшиеся 50 мл дистиллированной воды вносят NH4Cl 0,1 мг, MgSO4 5 мг, MnCl2 0,495 мг, FeCl3 0,49 мг. Оба раствора объединяют и автоклавируют в течение 30 мин при 121oC. Полученный стерильный раствор остужают до 40 - 50oC и добавляют к нему 10 мл стерильного аминокровина. Полученную среду (pH 7,4 - 7,6) разливают в стерильные пробирки или колбы.
При бактериологическом изучении среды, приготовленной согласно предлагаемому способу, проводили сравнительные посевы на среду Мартена, среду Альдерете и среду с аминокровином и физраствором вместо растворов микро- и макроэлементов.
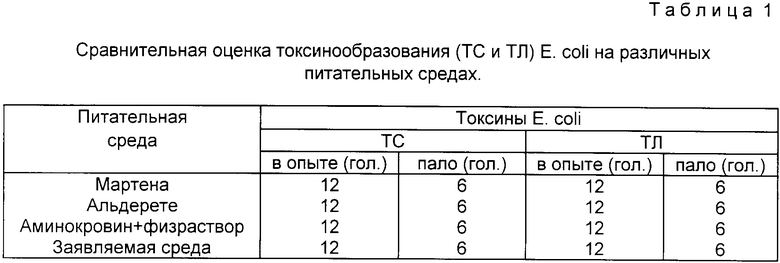
В качестве посевного материала использовали 2 штамма E. coli, продуцирующие термостабильный (ТС) и термолабильный (ТЛ) токсины. Посевы инкубировали в течение 7 сут при 37oC. Затем полученные суспензии подвергали центрифугированию при 4000 об/мин в течение 20 мин. Супернатант представлял собой ТЛ- или ТС-токсины E.coli, лишенные бактериальных клеток. Нативные токсины вводили внутрибрюшинно белым мышам весом 12 - 14 г в объеме 0,5 мл. Результаты представлены в таблице.
Нативные ТС- и ТЛ-токсины E.coli, полученные с заявляемой среды, обеспечивают LD50 на беспородных белых мышах в течение 48 ч после внутрибрюшинного введения в общепринятых дозах. ТЛ-токсин E.coli, полученный с аналогичной среды, но где вместо растворов макро- и микроэлементов использовали раствор хлористого натрия (физраствора), не вызвал гибели мышей в установленные сроки, так как минеральные соли необходимы для роста E.coli и продуцирования ТЛ-токсина.
Таким образом, заявляемая питательная среда обеспечивает полноценное развитие эшерихий, продуцирование термостабильных и термолабильных токсинов при своей относительной дешевизне и простоте приготовления. Кроме того, данная среда может готовиться как непосредственно перед употреблением, так и заранее, не изменяя свои эффективные свойства.
Изобретение относится к биотехнологии, в частности к микробиологии, и может быть использовано для выращивания культур эшерихий на простой питательной среде без потери ее эффективности. Питательная среда содержит, мас. %: двузамещенный фосфорнокислый калий 0,85 - 0,89, хлористый натрий 0,225 - 0,245, хлористый аммоний 0,09 - 0,11, сернокислый магний 0,0047 - 0,0053, хлористый марганец 0,00047 - 0,00051, хлористое железо 0,00047 - 0,00051, аминокровин 9 - 20, дистиллированная вода остальное. Простая в изготовлении питательная среда для культивирования эшерихий обеспечивает полноценное развитие кишечной палочки и продуцирование ею токсинов. 1 табл.
Питательная среда для культивирования эшерихий, содержащая двузамещенный фосфорнокислый калий, хлористый натрий, хлористый аммоний, сернокислый магний, хлористый марганец, хлористое железо и дистиллированную воду, отличающаяся тем, что она дополнительно содержит аминокровин при следующих соотношениях компонентов, мас.%:
Двузамещенный фосфорнокислый калий - 0,85 - 0,89
Хлористый натрий - 0,225 - 0,245
Хлористый аммоний - 0,09 - 0,11
Сернокислый магний - 0,0047 - 0,0053
Хлористый марганец - 0,00047 - 0,00051
Хлористое железо - 0,00047 - 0,00051
Аминокровин - 9 - 20
Дистиллированная вода - Остальноеи
| Методические рекомендации по получению, очистке энтеротоксинов эшерихий и изготовлению антитоксических сывороток | |||
| - Харьков, 1988, с.15 - 16. |
Авторы
Даты
1998-08-10—Публикация
1996-07-10—Подача