iiDipei, чем перхлоратов -i anariorojs по структуре,. Изобретен11е иллюстрируется примерам . IT р и м е р 1 . А. 4-Хлорфеииламид К-(2,-диметоксибензилиден)антраниловой кислоты (промежуточный продукт К раствору 2,47 г (0,01 моль) 4хлорфениламнда антраниловой кислоты в 10 мл этанола при пepeмelш вaнии в два приема приливают раствор 1,66 г (0,01 моль) 2,4-диметоксибензальдеги да в 7 мл этанола, соблюдая температ ру реакционной смеси 36. Оставляют при комнатной температуре на 30 мин затем выделившийся осадок отсасывают промывают на фильтре 10 мл охлажденного этанола, сушат при комнатной температуре. Получают данные иглы, окрашенные в желтый цвет с т.пл. 192 194С. Выход 98,2%. Найдено,%: С 67,02; Н 4,91; N 7,04. Cg H qClNzO, Вычислено,%: С 66,92; Н 4,85; N 7,09. ИК-спектр см (вазелиновое масло 1678, 1615, 1552, 1500; 1470; 1383; 1330; 1287; 1220. Б. 4-Хлорфениламид -(2,4-диметок сибензил)антраниловой кислоты. 1,95 г (0,005 моль) 4-хлорфенилам да N-(2,4-диметоксибензилиден)-антра ниловой кислоты и 0,2 г (0,0055 мол боргидрида натрия перемешивают до п лучения однородной маесы в сухом ви де, затем добавляют 25 мл этанола, охлажденного до 0°С. Реакционную смесь перемешивают при комнатной те пературе 2 ч, затем нагревают на вод ной бане 15 мин, фильтруют. Фильтра подкисляют 10%-ным раствором уксусн кислоты до слабокислой реакции по лакмусу. Выпавпшй осадок отфильтров вают, перекристаллизовьгоают из этанола. Получают бесцветные иглы с т.пл, 118-120°С. ч Выход,68,6%. Найдено,%: С 66,61; Н 5,30; N 7,11, С2гНд 1 , Вычислено,%: С 66,58; Н 5,33; N 7,06. ИК-спектр, см (вазелиновое масло) : 3425; 3313; 1642; 1515; 1478; 1305; 1218; 1162. Пример2.А. 4-Хлорфенилами Н-(3,4-диметоксибензилиден)антрани ловой кислоты (промежуточный продукт) . К раствору 2,47 г (0,01 моль) 4-хлорфениламида антраниловой кислоты в 10 мл этанола при. перемешивании в два приема прштивают раствор 1,66 г (0,01 моль) 3,4-диметоксибензальдегида в 7 мл этанола, соблюдая температуру реакционной смеси 38°С, оставляют при комнатной температуре на ЗОмин выпавший после охлаждения осадок отфильтровывают, промывают на фильтре 10 мл охлажденного этанола, сушат. Получают бесцветные кристаллы с т.пл. 132-134°С. Выход 74,5%. Найдено,%: С 67,03; Н 4,99; N 7,02. . Вычислено,%: С 66,92; Н 4,85; N 7,09. ИК-спектр, см (вазелиновое масло): 1675; 1638; 1605; 1522; 1470; 1383; 1322; 1280; 1165. Б. 4-Хлорфениламид Ы-(3,4-диметоксибензил)антраниловой кислоты. 1,95 г (0,005 моль) 4-Хлорфениламнда N-(3,4-диметоксибензилиден)-антраниловой кислоты и 0,2 г (0,0055 моль) боргидрира натрия хорошо перемешивают до получения однородной массы в сухом виде, затем добавляют 25 мл этанола, охлажденного до . Реакционную смесь перемешивают при комнатной температуре 2ч, затем нагревают на водяной бане 15 мин, фильтруют. Фильтрат подкисляют 10%-ным раствором уксусной кислоты до слабокислой реакции по лакмусу. Выпавший осадок отфильтровывают, перекристаллизовывают из этанола. Получают белый кристаллический порошок с т.пл. 170-173°С. I Выход 53,7%. Найдено,%: С 66,71; Н 5,20; N 7,18. Cg HziClNzO Вычислено,%: С 66,58; Н 5,33; N 7,06. ИК-спектр, см (вазелиновое масло) : 3263; 1632, 1580, 1520, 1471, 1423, 1270, 1165. Примеры 3-16. Промежуточные вещества для получения соединений общей формулы (I) - ариламиды N-диметоксибензипиденантраниловой кислоты получают тдк же, как в примере 1а и 2а (примеры 3-9). Характеристики и выходы промежуточных веществ приведены в табл.1 .
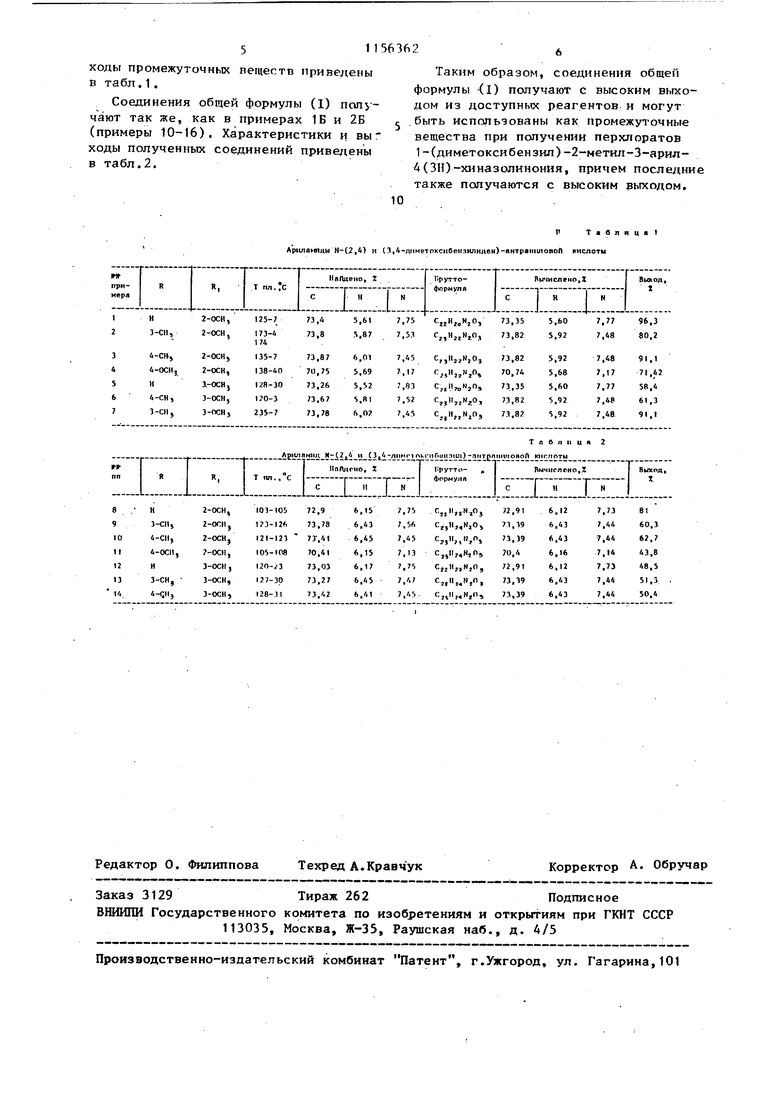
Соединения общей формулы (1) псшучают так же, как в примерах 1Б и 2Б (примеры 10-16). Характеристики и выходы полученных соединений приведены в табл.2.
Таким образом, соединения общей формулы (1) получают с высоким выходом из доступных реагентов и могут быть испсльзованы как промежуточные вещества при получении перхлоратов 1-(диметоксибензил)-2-метш1-3-арил4(ЗП)-хиназолинония, причем последние также получаются с высоким выходом.

Apилa э ды N-
АриламПды N-(2,4) и (,4-;м)метпксибеизнлнлен)-антра1)|тояоП кислоты
гТаблпцв1
| Перхлораты 1-бензил-2-метил-3-арил-4(3Н)-хиназолинония, обладающие анальгетической и противомикробной активностью | 1981 |
|
SU1014231A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1991-07-30—Публикация
1983-02-17—Подача