Целевые продукты представляют собой белые кристаллические вещества, трудно растворимые в спирте, толуоле, хлороформе, умеренно растворимые в диоксане, хорошо - в диметилсульфоксиде.
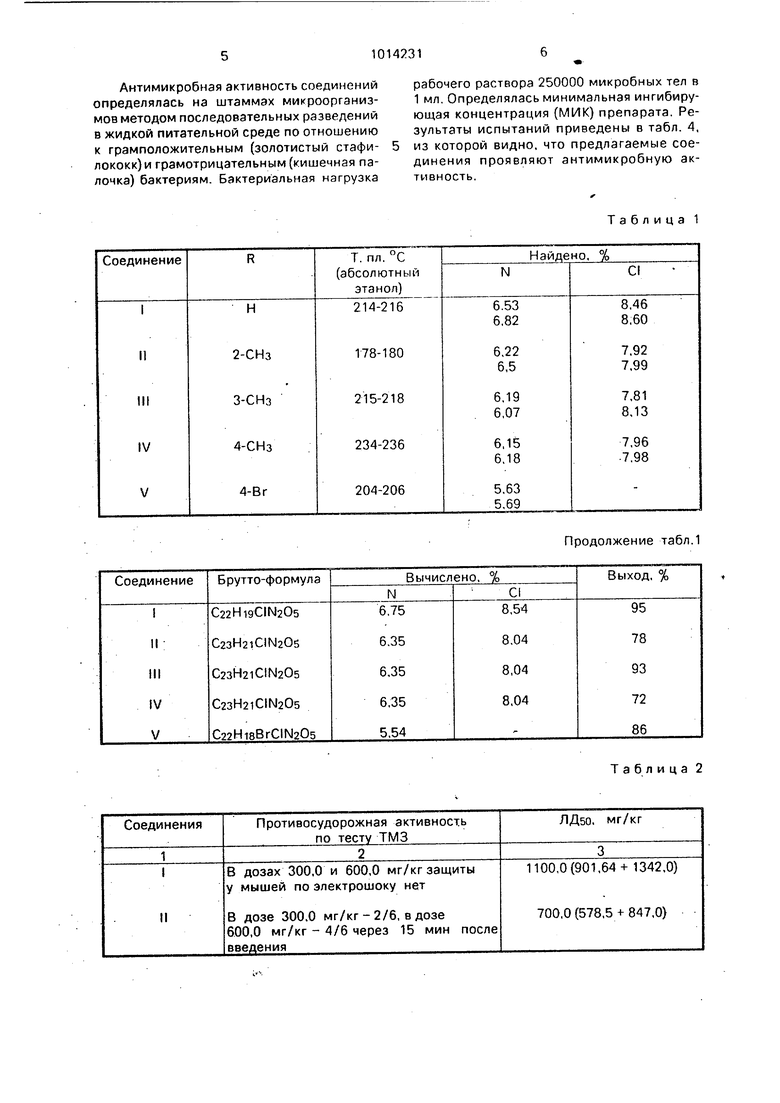
Физические свойства данных соединений приведены в табл. 1.
В ИК-спектрах обнаружены полосы поглощения при 1716-1725 см ( у ароматического цикла), 1300 см (-С N) ШОсм (СЮпО. Спектры ПМР синтезированных соединений также подтверждают их структуру. Триплет метильной группы в положении 2 соответствует области 2,3-2,4 м.д. Квадруплет метиленовой группы в положении 1 при 5,43-5,47 М.Д., а мультиплет ароматических протонов находится в области 7,41-7,7м.д.
Л р и м е р 1. Перхлорат 1-бензил-2-метил-3-фенил-4(ЗН)хиназолинония.
4,14 г (0,01 моль) анилида Ы-бензил-Мацетилантраниловой кислоты растворяют в 30мл метанола, приливают 1,76 г(0;01 моль) 57%-ной хлорной кислоты и выдерживают на водяной бане при 80°С с обратным холодильником в течение 45 мин. Затем отгоняют 15 мл метанола, выделившийся после охлаждения осадок отфильтровывают, промывают на фильтре 2 раза по 20 мл метанолом и кристаллизуют из абсолютного этанола в виде призм.
ИК-спектр (вазелиновое масло) см1: 1750, 1630, 1563, 1510, 1468, 1300, 1110.
ПМР-спектр(у(СРзСООН),2,3 ±0,05(СНз), 5,16 ± 0,05 ( СН2), 7,7±0,05 (СНз).
П р и м е р 2. Перхлорат 1-бензил-2-метил-3-(3-толил)-4(ЗН)хиназолинония.
4.29 г (0,01 моль)4-толуидида N-бенз.илN-ацетилантраниловой кислоты растворяют в 45 мл метанола, приливают 2 г (0,01 моль) 50%-ной хлорной кислоты и выдерживают на водяной бане при 80°С с обратным холодильником в течение 40 мин, затем отгоняют30 мл метанола, выделившийся после охлаждения осадок отфильтровывают, промывают дважды на фильтре по 20 мл метанола и кристаллизуют из абсолютного этанола.
ИК-спектр (вазелиновое масло), см1; 1730. 1630, 1560, 1500, 1460, 1290, 1110.
ПМР-спектр(, СРзСООН), м.д. 2,0±0,05 (СНз), 2,0±0,05(СНз). 5,43± 0,05 (СН2), 7,53±0.05(СНз).
Остальные соединения получены аналогично примерам 1 и 2.
Фармакологические исследования проводились на белых мышах обоего пола массой 16-22 г. Соединения вводились внутрибрюшинно в 2%-ной крахмальной слизи.
Изучалась острая токсичность, противосудорожная активность по тесту максимального электрошока (ТМЭ) и анальгетическая активность по методике Эдди и Леймбаха.
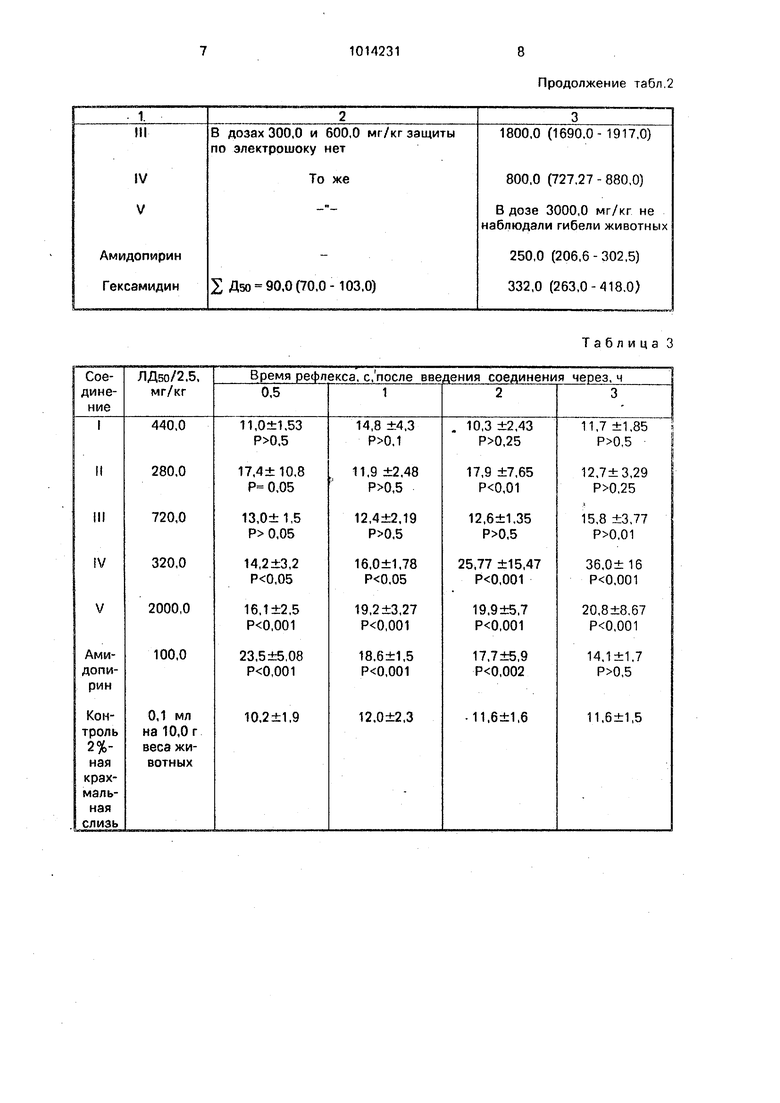
Результаты исследований по определению прртивосудорожной активности и токсичности приведены в табл. 2, из которой видно, что соединения не проявили противосудорожной активности в дозах 300 и 600
0 мг/кг при внутрибрюшинном введении их мышам, лишь соединение II проявило незначительную активность в дозах 300,0 мг/кг (защита у двух животных из шести) и 600,0 мг/кг (защита у четырех животных из
5 шести) через 15 мин после внутрибрюшинного введения.
Для определения анальгетической активности соединения вводились в зквитоксических дозах по отношению к
0 амидопирину, т.е. в дозах в 2,5 раза меньших, чем ЛДбо.
Результаты опытов по развитию анальгетического эффекта и наступлению его максимума (пика действия) в сравнении с
5 контролем и амидопирином представлены в табл.3. Как видно из табл.3, соединения II-V, обладают обезболивающим Действием, два из них - IV и V - на пике действия, 3 ч, активнее амидопирина (латентное время
0 оборонительного рефлекса у них статистически достоверно отличается от такового у амидопирина).
Все эти соединения менее токсичны, чем амидопирин.
5 Примерз. Перхлорат 1-бензил-2-метил-3-(4-толил)-4(ЗН)-хиназолинония.
Обладает выраженным анальгетическим действием. Латентное время рефлекса на пике действия равно 36,0±16,0 (разница
с контролем статистически достоверна при
Р 0,001). Соединение увеличивает время оборонительного рефлекса на пике своего действия - 3 ч - в 2,5 раза более, чем амидопирин.
45Малотоксичен. ЛДбо для белых мышей
при внутрибрюшинном введении 800.0 (727,3-880.0) мг/кг; в 3,2 раза менее токсичен амидопирина.
П р и м е р 4. Амидопирин (1-фенил-2.350 диметил-4-диметиламино-пиразолон-5).
В дозе 100,0 мг/кг. равной ЛД50/2,5. при внутрибрюшинном введении белым мышам обладает анальгетической активностью. Латентное время рефлекса на пике действия 30
55 мин равно 23,5±5.08 (разница с контролем статистически достоверна при Р 0,001).
Малотоксичен. ЛДво для белых мышей при внутрибрюшинном введении 250.0 (206,6-302.5) мг/кг.
Антимикробная активность соединений определялась на штаммах микроорганизмов методом последовательных разведений в жидкой питательной среде по отношению к грамположительным (золотистый стафилококк)и грамотрицательным (кишечная палочка) бактериям. Бактериальная нагрузка
рабочего раствора 250000 микробных тел в 1 мл. Определялась минимальная ингибирующая концентрация (МИК) препарата. Результаты испытаний приведены в табл. 4. из которой видно, что предлагаемые соединения проявляют антимикробную активность.
Таблица 1

Перхлораты 1-бензил-2-метил-3-арил4(ЗН)-хиназолинония общей формулы ClOi где R - водород или бром в положении 4 или метил, обладающие анальгетической и тивомикробной активностью. Изобретение относится к перхлоратам 1-бензил-2-метил-3-арил-4(ЗН)-хиназолинония общей формулы. ClOit где R - водород или бром в положении 4 или метил, обладающим анальгетической и противомикробной активностью. Указанные свойства позволяют предполагать возможность применения этих соединений в медицине. Известны перхлораты 1-зтил-2-метил-3арил-4(ЗН)-хиназолиния, обладающие противосудорожной активностью. В качестве вещества, проявляющего 4i. анальгетическую активность, находит приГО СО менение 1-фенил-2,3-диметил-4-диметиламинопиразолон-5(амидопирин), а в качестве вещества с противомикробной активностью - хлорамин Б. Способ получения предлагаемых соединений основан на известной реакции циклизации амидов 1М-бензил-Ы-ацетилантраниловой кислоты и заключается в том, что соответствующий ариламйд Ы-бензил-Мацетилантраниловой кислоты подверг1ают внутримолекулярной циклизации в среде метанола при температуре кипения реакционной смеси в присутствии хлорной кислоты.
Продолжение табл.1
Таблица 2
В дозах 300.0 и 600,0 мг/кг защиты по электрошоку нет
То же
2 Д50 90.0 (70.0-103.0)
Продолжение табл.2
В дозе 3000,0 мг/кг не наблюдали гибели животных
Таблица 3
10
1014231 Таблица А
| Авторское свидетельство СССР № 689164, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Чугунный экономайзер с вертикально-расположенными трубами с поперечными ребрами | 1911 |
|
SU1978A1 |
| Машковский М.Д | |||
| Лекарственные средства | |||
| --М.: Медицина, 1978, т | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Затвор для дверей холодильных камер | 1920 |
|
SU182A1 |
| Машковский М.Д, Лекарственные средства | |||
| -М.: Медицина, 1978, т | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| СПОСОБ ПОЛУЧЕНИЯ АЗОПИГМЕНТОВ | 1925 |
|
SU436A1 |
Авторы
Даты
1992-11-23—Публикация
1981-07-24—Подача