Изобретение относится к ветеринарной микробиологии и представляет собой живую вакцину против сальмонеллеза телят.
Цель изобретения - повышение иммуногенности вакцины и эффективности профилактики сальмонеллеза телят, получение бивалентной вакцины, одновременно защищающей телят от возбудителей Salmonella dublin и Salmonella typhi-murium.
Штаммы Salmonella dublin N 6 и Salmonella typhi-murium N 3, используемые для изготовления вакцины депонированы во Всесоюзном государственном научно-контрольном институте ветеринарных препаратов МСХ СССР и имеют регистрационные номера соответственно 9-16/2 и N 3.
П р и м е р 1. Изготовление бивалентной вакцины против сальмонеллеза телят серии N 1.
В реактор с питательной средой (бульон Хоттингера, 300 л) внесли посевной материал (матровую расплодку микробных клеток штамма S.dublin ВГНКИ N 9-16/2) из расчета 20 млн. клеток на 1 см3 бульона. Культивирование проводили при 37оС в течение 10 ч. Накопление микробных клеток составило 40 млрд/см3 бульона. После центрифугирования и разведения средой высушивания получили бакмассу в количестве 7 л с содержанием микробных клеток 50 млрд/см3.
В другой реактор с таким же объемом питательной среды внесли посевной материал (матровую расплодку микробных клеток штамма S.typhi-murium ВГНКИ N 3) в количестве, составившем 23 млн. клеток на 1 см3 бульона. Культивирование проводили при 37оС в течение 10 ч. Накопление микробных клеток составило 50 млрд/см3 бульона. После центрифугирования и разведения средой высушивания получили бакмассу в количестве 4 л с содержанием микробных клеток 150 млрд. в 1 см3.
Общее количество бактериальной массы, состоящее из равных объемов микробных клеток штаммов S.dublin ВГНКИ N 9-16/2 и S.typhi-murium ВГНКИ N 3 в соотношении 1: 3, составило 8 л. После расфасовки по 4 см3 и лиофилизации получили вакцину в количестве 38000 доз для подкожного и 3040 доз для перорального применения, содержащую, %:
Штамм S.dublin
ВГНКИ N 9-16/2
(живые клетки, 10 млрд/см3) 7,0
Штамм typhi-murium
ВГНКИ N 3 (живые клетки, 30 млрд/см3) 21,0 Среда высушивания 72,0
П р и м е р 2. Изготовление бивалентной вакцины против сальмонеддеза телят серии N 2.
В реактор с питательной средой (бульон Хоттингера 400 л) внесли посевной материал (матровую расплодку микробных клеток штамма S.dublin ВГНКИ N 9-16/2 из расчета 25 млн. клеток на 1 см3 бульона. Культивирование проводили при 37оС в течение 10 ч. Накопление микробных клеток составило 35 млрд/см3 бульона. После центрифугирования и разведения средой высушивания получили бакмассу в количестве 7,5 л с содержанием микробных клеток 55 млрд/см3.
В другой реактор с таким же объемом питательной среды внесли посевной материал (матровую расплодку микробных клеток штамма S.typhi-murium ВГНКИ N 3) в количестве, составившем 20 млн. клеток на 1 см3 бульона. Культивирование проводили при 37оС, в течение 12 ч. Накопление микробных клеток составило 40 млрд/см3 бульона. После центрифугирования и разведения средой высушивания получили бакмассу в количестве 5 л с содержанием микробных клеток 165 млрд. в 1 см3.
Общее количество бактериальной массы, состоящее из равных объемов микробных клеток штаммов S.dublin ВГНКИ N 9-16/2 и S. typhi-murium N 3 в соотношении 1:3, составило 10 л. После расфасовки по 4 см3 и лиофилизации получили вакцину в количестве 55200 доз для подкожного и 3340 доз для перорального применения, содержащую, %:
Штамм S.dublin
ВГНКИ N 9-16/2
(живые клетки, 15 млрд/см3) 9,0
Штамм S. typhi-murium
ВГНКИ N 3 (живые клетки, 45 млрд/см3) 27,0 Среда высушивания 64,0
П р и м е р 3. Изготовление бивалентной вакцины против сальмонеллеза телят серии N 3.
В реактор с питательной средой (бульон Хоттингера, 300 л) внесли посевной материал (матровую расплодку микробных клеток штамма S.dublin ВГНКИ N 9-16/2) из расчета 22 млн. клеток на 1 см3 бульона. Культивирование проводили при 37оС в течение 10 часов. Накопление микробных клеток составило 45 млрд/см3 бульона. После центрифугирования и разведения средой высушивания получили бакмассу 6,8 л с содержанием 60 млрд/см3 микробных клеток.
В другой реактор с таким же объемом питательной среды внесли посевной материал (матровую расплодку микробных клеток штамма S.typhi-murium ВГНКИ N 3) в количестве, составишем 25 млн. клеток на 1 см3 бульона. Культивирование проводили при 37оС в течение 11 ч. Накопление микробных клеток составило 50 млрд/см3 бульона. После центрифугирования и разведения средой высушивания получили бакмассу в количестве 4 л с содержанием микробных клеток 180 млрд. в 1 см3.
Общее количество бактериальной массы, состоящее из равных объемов микробных клеток штаммов S.dublin ВГНКИ N 9-16/2 и S.typhi-murium ВГНКИ N 3 в соотношении 1: 3 составило 8 л. После расфасовки по 4 см3 и лиофилизации получили вакцину в количестве 57900 доз для подкожного и 4632 дозы для перорального применения, содержащую, %:
Штамм S.dublin
ВГНКИ N 9-16/2
(живые клетки, 13 млрд/см3) 8,0
Штамм S.typhi-murium
ВГНКИ N 3 (живые клетки, 40 млрд/см3) 24,0 Среда высушивания 68,0
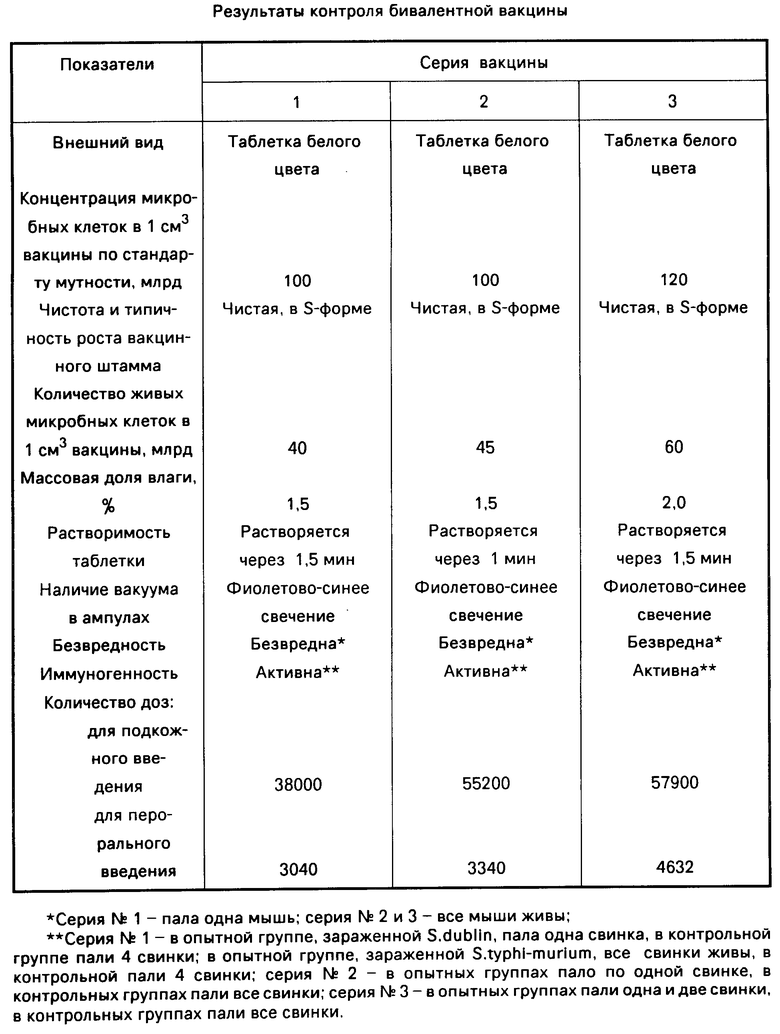
Полученные серии вакцины контролируют по следующим показателям: внешнему виду; концентрации микробных клеток в 1 см3 вакцины по стандарту мутности; чистоте и типичности роста вакцинных штаммов; количеству живых микробных клеток в 1 см3 вакцины; массовой доли влаги в %; растворимости таблетки; наличии вакуума в ампулах; безвредности; иммуногенности.
Результаты проверки представлены в таблице.
П р и м е р 4. Полученную вакцину применяют для профилактики сальмонеллеза телят в неблагополучных хозяйствах, где инфекцию вызывают сальмонеллы двух серотипов: S.dublin и S.typhi-murium.
Телят 3-5-дневного возраста иммунизируют перорально двукратно с интервалом 2-3 дня путем выпойки с молоком 50±5 млрд. микробных клеток при первом и втором выпаивании.
При подкожном способе вакцинации телят иммунизируют с 10-12-дневного возраста однократно в дозе 8±0,5 млрд. микробных клеток.
Проведено комиссионное производственное испытание с целью оценки эффективности бивалентной вакцины в сравнении с вакциной "Бовисальораль" и концентрированной формолквасцовой.
Испытания проводили в животноводческих хозяйствах с различными условиями содержания телят. Телят 3-30-дневного возраста иммунизировали в соответствии с наставлением по применению вакцин: бивалентной - подкожно однократно в дозе 8 млрд. микробных клеток и перорально двукратно с интервалом два дня суммарной дозой 100 млpд клеток; "Бовисальораль" - перорально однократно одной прививочной дозой; концентрированной формоквасцовой - подкожно двукратно с интервалом 5 дней в дозе 1,5 и 2 см3 (6 и 8 млрд. клеток); для сравнения испытывали также однократную пероральную иммунизацию бивалентной вакциной в дозе 50 млрд. клеток.
В опыте использовали 800 телят 3-20-дневного возраста. Три группы животных, сформированных по принципу аналогов, вакцинировали бивалентной вакциной подкожно 230 голов; вакциной "Бовисальораль" 260 голов и формолквасцовой 310 голов.
Реактогенные свойства. После введения вакцин у двух телят, иммунизированных бивалентной вакциной, одного - иммунизированного вакциной "Бовисальораль" и пяти - формолквасцовой вакциной отмечали отказ от корма, учащение дыхания и пульса, незначительную депрессию. Через 24 ч эти реакции проходили.
Иммуногенные свойства. В группе телят, иммунизированных бивалентной вакциной, остались живы все телята, иммунизированных вакциной "Бовисальораль" - от сальмонеллеза пало 5 телят и в группе, иммунизированной формолквасцовой вакциной, пало два теленка. Во всех случаях клинические и патологоанатомические признаки сальмонеллеза подтверждены бактериологическим диагнозом.
В откормочном комплексе, стационарно неблагополучном по сальмонеллезу, телят вакцинировали бивалентной вакциной подкожно - 100 голов; перорально двукратно 50 голов, перорально однократно 50 голов; вакциной "Бовисальораль" 102 головы; формолквасцовой 100 голов. В трех группах использовали телят 3-12-дневного возраста. Реактогенные свойства не отмечены.
Иммуногенные свойства. Через 1 месяц после вакцинации в группах телят, иммунизированных вакциной "Бовисальораль" и формолквасцовой, отмечено массовое заболевание телят с признаками сальмонеллеза: повышение температуры до 41-42оС, понос, отказ от корма, адинамия, слезотечение из глаз, истощение. В этих группах количество вынуждено убитых и сданных на санбойню мясокомбината телят составило соответственно 35,3 и 35%. Диагноз на сальмонеллез подтвержден бактериологически до 60%.
В группах, иммунизированных бивалентной вакциной подкожно, пало 9 телят (9%); иммунизированных перорально двукратно пало 12 телят.
В хозяйстве, где отмечена вспышка сальмонеллеза, применение вакцины "Бовисальораль" в рекомендованной дозе и формолквасцовой оказалось малоэффективным.
Бивалентная вакцина обеспечила достаточно высокую сохранность телят при подкожном и пероральном применении соответственно 91 и 84 %.
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ БАКТЕРИЙ SALMONELLA DUBLIN, ИСПОЛЬЗУЕМЫЙ ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИНЫ ПРОТИВ САЛЬМОНЕЛЛЕЗА ТЕЛЯТ | 1984 |
|
SU1197186A1 |
| ВАКЦИНА ПРОТИВ САЛЬМОНЕЛЛЕЗА СВИНЕЙ, СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ И СПОСОБ ПРОФИЛАКТИКИ САЛЬМОНЕЛЛЕЗА СВИНЕЙ | 1988 |
|
RU1577116C |
| АССОЦИИРОВАННАЯ ИНАКТИВИРОВАННАЯ ВАКЦИНА ПРОТИВ ХЛАМИДИОЗА, КАМПИЛОБАКТЕРИОЗА, САЛЬМОНЕЛЛЕЗА И ЛЕПТОСПИРОЗА МЕЛКОГО РОГАТОГО СКОТА | 1994 |
|
RU2086259C1 |
| ВАКЦИНА ПРОТИВ САЛЬМОНЕЛЛЕЗА СВИНЕЙ | 2003 |
|
RU2255763C2 |
| ВАКЦИНА ПРОТИВ САЛЬМОНЕЛЛЕЗА КУР И СПОСОБ ПРОФИЛАКТИКИ САЛЬМОНЕЛЛЕЗА КУР | 1992 |
|
RU2030916C1 |
| ПРЕПАРАТ ПРОТИВ САЛЬМОНЕЛЛЕЗА КУР И СПОСОБ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ САЛЬМОНЕЛЛЕЗА КУР | 1992 |
|
RU2026082C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИНАКТИВИРОВАННОЙ ВАКЦИНЫ ПРОТИВ ВИБРИОЗА РЫБ | 2005 |
|
RU2284830C1 |
| ШТАММ БАКТЕРИЙ Salmonella enteritidis № 22, ИСПОЛЬЗУЕМЫЙ ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИН И ДИАГНОСТИЧЕСКИХ ПРЕПАРАТОВ | 2002 |
|
RU2218177C2 |
| ШТАММ БАКТЕРИЙ SALMONELLA DUBLIN 160, ИСПОЛЬЗУЕМЫЙ ДЛЯ ИЗГОТОВЛЕНИЯ ВАКЦИНЫ ПРОТИВ САЛЬМОНЕЛЛЕЗА ТЕЛЯТ | 1986 |
|
SU1378389A1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ВАКЦИНЫ АССОЦИИРОВАННОЙ ПРОТИВ САЛЬМОНЕЛЛЕЗА И КОЛИБАКТЕРИОЗА НУТРИЙ | 2005 |
|
RU2292915C1 |
ВАКЦИНА ПРОТИВ САЛЬМОНЕЛЛЕЗА МОЛОДНЯКА, содержащая антиген из штамма Salmonella typhi-murium ВГНКИ N 3 и среду высушивания на основе сахарозы, желатина и воды, отличающаяся тем, что, с целью повышения эффективности профилактики сальмонеллеза телят, она дополнительно содержит антиген из штамма Salmonella dublin ВГНКИ N 9 - 16/2 при следующем содержании компонентов, об.%:
Штамм Salmonella typhi-murium ВГНКИ N 3 (30 - 45 млрд.микробных клеток в 1 см3) 21 - 27
Штамм Salmonella dublin ВГНКИ N 9 - 16/2 (10 - 15 млрд.микробных клеток 7 - 9
Среда высушивания 64 - 72
| Авторское свидетельство СССР N 959420, кл | |||
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
Авторы
Даты
1994-11-30—Публикация
1984-09-04—Подача