Изобретение касается новых циклических тиоэфиров фениларсонистой и н-амиларсонистой кислот, а именно 2-алкил(арил)-6,1,3,2-оксадитиаарсоканов, проявляющих фунгистатическую, фунгицидную и бактериостатическую активность.
Цель изобретения применение новых соединений в качестве противомикробного средства в ветеринарии и медицине.
П р и м е р 1. Получение 2-фенил-6,1,3,2-оксадитиаарсокана.
Реакцию проводят в атмосфере сухого инертного газа. К смеси 6,92 г (0,05 моль) димеркаптодиэтилового эфира и 7,9 г (0,1 моль) сухого пиридина в 200 мл абсолютного бензола прикапывают 11,14 г (0,05 моль) фенилдихлорарсина, растворенного в 60 мл абсолютного бензола, при перемешивании и охлаждении до 5оС. По окончании прикапывания реакционную смесь перемешивают 2 ч при комнатной температуре, затем отфильтровывают хлористоводородную соль пиридина. Из фильтрата отгоняют бензол с помощью водоструйного насоса и образовавшееся масло высушивают в вакуум-эксикаторе над парафином, при этом масло закристаллизовывается. Продукт очищают перекристаллизацией из сухого гексана. Выход 10,9 г (75,7%), т.пл. 64-66оС. Молекулярная масса (найденная методом криоскопии в бензоле) 295, рассчитанная молекулярная масса 288.
Найдено, Аs 25,93.
С10Н13АSO2.
Вычислено, Аs 26,04.
ИК-спектр, см-1: ν(С6Н5) 470, 485, 662, 695, 740, 3045, 3070, (Аs-С) 1080, (С-S) 635, (С-0) 1130, (С-Н) 2857/2870, 2958/2965.
П р и м е р 2. Получение 2-амил-6,1,3,2-оксадитиаарсокана.
Синтез проводят из 6,92 г (0,05 моль) димеркаптодиэтилового эфира и 10,84 г (0,05 моль) амилдихлорарсина в присутствии 7,9 г (0,1 моль) сухого пиридина по аналогичной методике в атмосфере сухого инертного газа. После удаления бензола из фильтрата остаток перегоняют в вакууме. Выход 9,99 г (70,8% ), т. кип. 163-165оС/4 мм рт.ст. nD20 1,5950, d420 1,3442. MRнайдено 71,36; МRрассчитано 70,86.
Найдено, As 26,33.
С9Н19АSO2
Вычислено, Аs 26,59.
ИК-спектр, ν, см-1; (Аs-C) 562, (С-S) 640, (С-Н) 2860/2872, 2920/2960, (С-О) 1112/1130.
Получение соединения хорошо растворимы в бензоле, хлороформе, четыреххлористом углероде, эфире, ацетоне.
Фунгистатическую и фунгицидную активность полученных препаратов изучают по отношению к грибам, возбудителям дерматофитии человека и животных: Trichophyton rubrum-695, Trichophyton mentagrophytes-1173, Microsporum canis-84 на жидкой питательной среде Сабуро методом серийных разведений по стандартной методике, принятой для изучения всех противогрибковых препаратов. Наблюдения проводят в течение 14 дней при 26-28оС. Чувствительность к препарату определяется его минимальной дозой, при которой не наблюдается рост грибов.
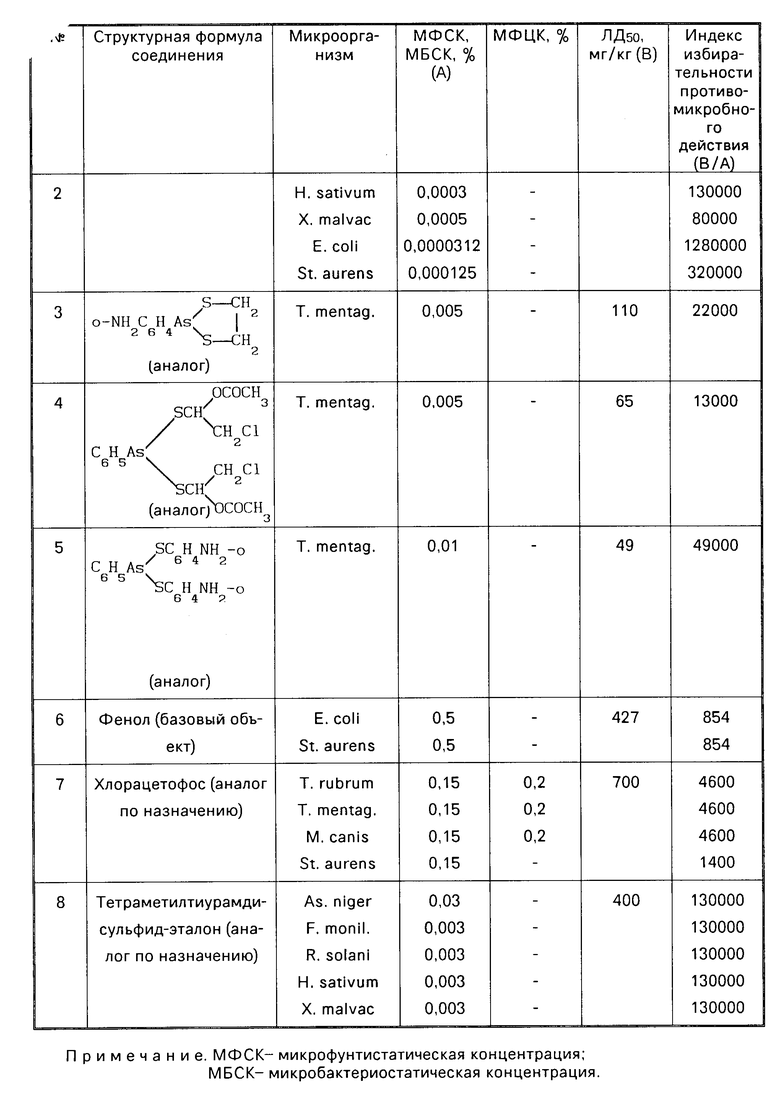
При определении фунгицидной активности культуры грибов-дерматофитов инокулируют на твердую среду Сабуро, содержащую возрастающие дозы соединения. Через 14 дней посевной материал из пробирок, в которых не отмечено роста, пересевают на чистую среду. Критерием фунгицидной активности считают отсутствие роста гриба в течение 30 дней при пышном росте в контроле. Результаты исследований приведены в таблице.
Противогрибковую активность соединений изучают на мицелии грибов, возбудителей заболеваний культурных растений: Aspergillus niger-1119, Fusarium monilihorme-136, Rhizoctonia solani-935, Helmintosporium sotivum-740. Испытания в отношении возбудителя бактериоза овощных и зерновых культур проводят на культуре бактерии Хanthomonas malvacearum-622. Активность определяют методом введения ацетоновых растворов в расплавленную агаризованную питательную среду, которую разливают в чашки Петри в стерильных условиях. После застывания среды ее инокулируют грибами и бактериями и выдерживают в термостате при 22-25оС в течение 3-5 дней. Затем проводят учет роста колоний микроорганизмов и по формуле Эббота подсчитывают процент подавления их роста.
Результаты исследований приведены в таблице.
Бактериостатическое действие циклических тиоарсенитов изучают по общепринятой в микробиологической практике методике серийных разведений по отношению к Escherichia coli-125 и Staphylococus aurens-209.
Бактериальная нагрузка в опыте составляет 300000 микробных тел в 1 мл. Результаты приведены в таблице.
Токсичность циклических тиоарсенитов для теплокровных животных определяют на белых мышах при пероральном введении ацетоновомасляных растворов с вычислением ЛД50 по методу Литчфилда и Уилкоксона. Результаты приведены в таблице.
Как видно из таблицы, предлагаемые соединения обладают выраженной фунгистатической, фунгицидной и бактериостатической активностью, превосходящей действие ближайших структурных аналогов, и отличаются от последних наличием широкого спектра противомикробного действия. Арсоканы высокоактивны против возбудителей плесневения, бактерий и возбудителей поверхностных микозов.
Предлагаемые соединения существенно отличаются от базовых объектов. По индексу избирательности противомикробного действия они превосходят фенол, который используется как наиболее доступное противомикробное средство в ветеринарии и медицине, в отношении кишечной палочки в 160-1500 раз, золистого стафилококка в 84-370 раз. Арсоканы превосходят фунгицид хлорацетофос в отношении дерматофитов в 70-140 раз, в отношении бактерий в 50-220 раз и активны в отношении возбудителей плесневения и бактериоза. Полученные соединения по токсичности уступают базовым объектам, однако по соотношению между ЛД50 для теплокровных животных и противомикробной концентрацией в отношении возбудителей дерматофитии и бактерий эти соединения обладают наибольшей избирательностью действия. Данные, приведенные в таблице, указывают и на высокую избиpательность полученных арсоканов в отношении возбудителей плесневения и бактериоза. Так, соединения 2 по этому показателю находится на одном уровне с эталоном-тетраметилтиурамдисульфидом (данные ВНИИХСЗР), а соединение 1 в отношении возбудителей плесневения уступает, а в отношении фузариоза превосходит эталон.
| название | год | авторы | номер документа |
|---|---|---|---|
| 0-АЛКИЛ-0-(ТРИАЛКИЛСТАННИЛ)-АЛКИЛТИО-(СЕЛЕНО)-ФОСФОНАТЫ, ОБЛАДАЮЩИЕ ФУНГИЦИДНОЙ, ФУНГИСТАТИЧЕСКОЙ, БАКТЕРИОСТАТИЧЕСКОЙ И ИНСЕКТИЦИДНОЙ АКТИВНОСТЬЮ | 1980 |
|
SU884271A1 |
| 4-Бромфенилгидразон ацетилхлорида | 1978 |
|
SU686310A1 |
| НОВЫЕ БЕНЗОФУРОКСАНЫ, ОБЛАДАЮЩИЕ ФУНГИЦИДНОЙ И БАКТЕРИЦИДНОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2428419C2 |
| Акриловый или @ -замещенные акриловые эфиры 4-оксиметилкарена-2, обладающие фунгистатической, бактериостатической и гербицидной активностью | 1980 |
|
SU926900A1 |
| СРЕДСТВО УХОДА ЗА КОЖЕЙ, ОБЛАДАЮЩЕЕ АНТИФУНГАЛЬНЫМИ СВОЙСТВАМИ | 2013 |
|
RU2536273C1 |
| Пербромиды 2,4-динитрофенилгидразо-HOB АлифАТичЕСКиХ и циКлОАлифАТичЕСКиХКЕТОНОВ,ОблАдАющиЕ фуНгицидНыМи ибАКТЕРиОСТАТичЕСКиМи СВОйСТВАМи | 1979 |
|
SU831767A1 |
| АНТИФУНГАЛЬНОЕ СРЕДСТВО НА ОСНОВЕ МЕТИЛОВОГО ЭФИРА 2-БЕНЗИМИДАЗОЛИЛКАРБАМИНОВОЙ КИСЛОТЫ ИЛИ ЕГО ПРОИЗВОДНЫХ | 2013 |
|
RU2546041C2 |
| СРЕДСТВО УХОДА ЗА КОЖЕЙ, ОБЛАДАЮЩЕЕ АНТИФУНГАЛЬНЫМИ СВОЙСТВАМИ (ВАРИАНТЫ) | 2014 |
|
RU2567036C1 |
| АРАЛКИЛБЕНЗИЛОВЫЕ ПРОСТЫЕ ЭФИРЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ, ПРИМЕНЕНИЕ ТАКИХ СОЕДИНЕНИЙ, СПОСОБЫ ЛЕЧЕНИЯ И/ИЛИ ПРОФИЛАКТИКИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ, СОДЕРЖАЩИЕ ЭТИ СОЕДИНЕНИЯ | 2010 |
|
RU2548009C2 |
| Эфиры на основе 1-оксиметил-1,2,4-триазола, обладающие фунгицидной и бактерицидной активностью | 1987 |
|
SU1512075A1 |

2-Алкил(арил)-6,1,3,2-оксадитиаарсораны общей формулы
где R C6H5, C5H11,
проявляющие фунгистатическую, фунгицидную и бактериостатическую активность.
| Z.anorg.alln.chem., 1974, v.407, s.35-39. |
Авторы
Даты
1995-07-20—Публикация
1984-07-03—Подача