Предлагаются новые биологически активные вещества ряда фосфорорганических соединений, т. е. О-алкил-О-(триалкилстаннил)-алкилтио-(селено)-фосфонаты общей формулы I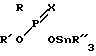 где R - метил, этил;
где R - метил, этил;
R′ - этил, пропил, бутил;
R″ - этил, пропил;
Х - атом серы, селена, которые обладают выраженной фунгицидной, фунгистатической, бактериостатической и инсектицидной активностью и могут быть использованы в медицине и сельском хозяйстве.
Известен О-(три-н-бутилстаннил)-н-дибутилтиофосфинат. Однако данные о биологической активности этого соединения отсутствуют.
Известны также О, О-диалкил-S-(триалкилстаннил)-дитиофосфаты и -фосфонаты общей формулы
RR′ P(S)SSnR″3 , где R - алкил С1-С2, алкокси группа С1-С3;
R′ - метил, алкокси группа С1-С3;
R″ - алкил С2-С4, фенил, обладающие фунгицидным и фунгистатическим действием в отношении гриба Stachybotrys alternaus при разведении 1: 2000 и 1: 5000. Они полностью предотвращают, а при дальнейшем разведении сильно задерживают рост гриба. Указанные соединения обладают инсектицидным действием на мух, вызывая их 100% -ную гибель через 24 ч при топикальном нанесении в концентрациях 1-8 мкг на особь. Однако эти соединения обладают невысокой фунгицидной активностью и незначительным спектром биологического действия.
Целью изобретения является выявление новых соединений фосфорорганического ряда, обладающих широким спектром действия: фунгицидной, фунгистатической, бактериостатической и инсектицидной активностью.
Поставленная цель достигается новым О-алкил-О-(триалкилстаннил)-алкилтио-(селено)-фосфонатами общей формулы I 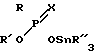 где R - метил, этил;
где R - метил, этил;
R′ - этил, пропил, бутил;
R″ - этил, пропил;
Х - атом серы, селена, обладающие фунгицидной, фунгистатической, бактериостатической и инсектицидной активностью.
О- Алкил- О- (триалкилстаннил)-алкил- тио-(селено)-фосфонаты получают взаимодействием триэтиламмониевых солей О-алкилалкилтио-(селено)-фосфоновых кислот с хлористым триалкилоловом в среде органического растворителя, например диэтилового эфира, при температуре 20-25оС.
О-Алкил-О-(триалкилстаннил)-алкил- тиофосфонаты представляют собой бесцветные вязкие жидкости, перегоняющиеся в вакууме без разложения. О-Алкил-О-(триалкилстаннил)-алкилселенофосфонаты представляют собой бесцветные или слегка желтоватые вязкие жидкости, очень чувствительные к воздуху, в вакууме перегоняются с разложением.
П р и м е р 1. Получение О-н-пропил-О-(триэтилстаннил)-метилтиофосфоната.
К раствору 6,46 г (0,025 моль) триэтиламмонийной соли О-н-пропилметилтиофосфоновой кислоты в 30 мл диэтилового эфира при перемешивании прибавляют по каплям при комнатной температуре 6,12 г (0,025 моль) хлористого триэтилолова в 15 мл диэтилового эфира. Реакционную смесь перемешивают 5 ч и оставляют на ночь. Выпавший осадок солянокислого триэтиламина отфильтровывают, вес его 3,4 г (теоретическое количество 3,48 г), растворитель отгоняют в вакууме и остаток перегоняют.
Получают 8,14 г (89,6% ) О-н-пропил-О-(триэтилстаннил)-метилтиофосфоната с т. кип. 99-100оС/0,045 мм рт. ст. , nD20 1,5240, d420 1,3076.
Найдено, % : С 33,60; Н 6,98; Р 8,34.
С10Н25О2РSSn
Вычислено, % : С 33,45; Н 6,97; Р 8,67.
ИК-спектр (ν , см-1): (Р-ОС) 1030-1090, 680 (Р= S), 525 (Sn-C).
В спектре ЯМР Р31 имеется один сигнал с химическим сдвигом (δ ) - 70,0 м. д. относительно 85% Н3РО4.
П р и м е р 2. Получение О-н-бутил-О-(триэтилстаннил)-метилтиофосфоната.
К раствору 5,6 г (0,02 моль) триэтиламмонийной соли О-н-бутилметилтиофосфоновой кислоты в 30 мл диэтилового эфира при перемешивании прибавляют по каплям при комнатной температуре 5,03 г (0,02 моль) хлористого триэтилолова в 15 мл диэтилового эфира. Реакционную смесь перемешивают 5 ч и оставляют на ночь. Выпавший осадок солянокислого триэтиламина отфильтровывают (теоретическое количество), фильтрат упаривают, а остаток перегоняют. Получают 4,85 г (62,5% ) О-н-бутил-О-(триэтилстаннил)-метилтиофосфона-та, т. кип. 102-103оС/0,042 мм рт. ст. , nD20 1,5080, d420 1,2711.
Найдено, % : С 35,80; Н 7,30; Р 8,28; S 8,63.
С11Н27О2РSSn
Вычислено, % : С 35,42; Н 7,24; Р 8,32; S 8,59.
В ИК-спектр (ν , см-1): 1030-1090 (Р-О-С), 675-680 (Р= S), 525 (Sn-C).
В спектре ЯМР Р31 имеется один сигнал с химическим сдвигом - 70,0 м. д. относительно 85% Н3РО4.
П р и м е р 3. Получение О-этил-О-(три-н-пропилстаннил)-этилтиофосфоната.
К раствору 3,48 г (0,014 моль) триэтиламмонийной соли О-этилэтилтиофосфоновой кислоты в 20 мл диэтилового эфира прибавляют по каплям при перемешивании при комнатной температуре 5,11г (0,014 моль) хлористого трипропилолова в 10 мл диэтилового эфира. Реакционную смесь перемешивают 5 ч и оставляют на ночь. Выделившийся осадок солянокислого триэтиламина отфильтровывают, фильтрат упаривают, а остаток перегоняют.
Получают 4,5 г (82,4% ) О-этил-О-(три-н-пропилстаннил)-этилтиофосфоната, т. кип. 117-118оС/0,07 мм рт. ст. , d420 1,2714, nD20 1,5192.
Найдено, % : С 38,26; Н 7,75; Р 7,81.
С13Н31О2РSSn
Вычислено, % : С 38,93; Н 7,74; Р 7,74.
ИК-спектр ( ν , см-1): 1030 (Р-О-С), 675 (Р= S), 525 (Sn-C).
В спектре ЯМР Р31 имеется один сигнал с химическим сдвигом -72,0 м. д. относительно 85% Н3РО4.
П р и м е р 4. Получение О-этил-О-(триэтилстаннил)-этилселенофосфоната.
К раствору 5,86 г (0,019 моль) О-этилэтилселенофосфоновой кислоты в 30 мл диэтилового эфира в токе аргона при перемешивании прибавляют по каплям 4,69 г (0,019 моль) хлористого триэтилолова в 15 мл диэтилового эфира. Реакционную смесь перемешивают в течение 1 ч и оставляют на ночь. Выпавший осадок солянокислого триэтиламина отфильтровывают (теоретическое количество), а фильтрат упаривают в вакууме ≈ 0,08 мм рт. ст. при 70-80оС до постоянного веса. Получают 7,1 г (90,1% ) О-этил-О-(триэтилстаннил)-этилселенофо-сфоната, nD20 1,5434, d420 1,4654, МRD найдено 87,38, МRD вычислено 86,42.
Найдено, % : С 29,99; Н 7,00; 6,19; Р 7,41.
С10Н25О2РSeSn
Вычислено, % : С 29,56; Н 6,16; Р 7,63.
ИК-спектр (ν , см-1): 1060 (Р-О-С), 525 (Sn-C).
В спектре ЯМР Р31 имеется один сигнал с химическим сдвигом -68,0 м. д. относительно 85% Н3РО4.
П р и м е р 5. Получение О-изопропил-О-(триэтилстаннил)-этилселенофосфоната.
К раствору 6,91 г (0,02 моль) триэтиламмонийной соли О-изо-пропилэтилселенофосфоновой кислоты в 30 мл диэтилового эфира в токе аргона при перемешивании добавляют 5,28 г (0,02 моль) хлористого триэтилолова в 20 мл диэтилового эфира. Реакционную смесь перемешивают в течение 1 ч и оставляют на ночь. Выпавший осадок солянокислого триэтиламина отфильтровывают, а фильтрат упаривают в вакууме 0,08 мм рт. ст. при 70-80оС до постоянного веса.
Получают 8,9 г (96,9% ) О-изопропил-О -(триэтилстаннил)-этилселенофосфоната, nD20 1,5364, d420 1,4304, МRDнайдено 91,61, MRD вычислено 91,03.
Найдено, % : С 31,80; Н 6,76; Р 7,03.
С11Н27О2РSeSn
Вычислено, % : С 31,43; Н 6,43; Р 7,38.
ИК-спектр ( ν, см-1): 1090 (Р-О-С), 525 (Sn-C).
В спектре ЯМР Р31 имеется один сигнал с химическим сдвигом -68,0 м. д. относительно 85% Н3РО4.
Фунгицидная активность О-алкил-О-триалкилстаннил-(тиоселено)-фосфонатов изучена по отношению к грибам - возбудителям дерматомикозов: Frichophyton rubrum, Frichophyton mentagraphytes, Microsporum canis, грибам-сапрофитам, возбудителям плесневения: Aspergillus niger, Fusarium avenaceum, Alternaria sp. , Helmintosporium sp. , и к представителю дрожжеподобных грибов - Candida albicans. Культуры грибов засевают на твердую среду Сабуро (дерматофиты) или Чапека (сапрофиты), содержащую возрастающие дозы соединения. Через 14 дней (в случае дерматофитов) и через 10 дней (в случае сапрофитов) посевной материал из пробирок, в которых не отмечено роста, пересевают на чистую твердую среду Сабуро или Чапека. Критерием фунгицидной активности считают отсутствие роста гриба в течение 30 дней при пышном росте в контроле. Критерием фунгистатической активности считают наименьшую концентрацию соединения, задерживающую рост грибов.
Бактериостатическое воздействие О-алкил-О-(триалкилстаннил)-алкилтио-(селе- но)-фосфонатов определяют по общепринятой в микробиологической практике методике серийных разведений. Бактериальная нагрузка в опыте составляет 300000 микробных тел в 1 мл.
Инсектицидное действие соединений определяют по отношению к комнатной мухе (Musca domestica L. ) и амбарному долгоносику (Calandra granaria L. ). В качестве эталона используют хлорофос. Мух обрабатывают топикально, с помощью микродозиметра. Ацетоновый раствор соединения наносят на среднеспинку насекомого. Гибель мух учитывают через 24 ч с момента обработки.
Контактное действие по отношению к жукам амбарного долгоносика определяют методом смачивания фильтровальной бумаги, помещенной на дно стакана (емкость 50 см3), ацетоновыми растворами соединения определенной концентрации из расчета 0,4 мл/см2. Насекомых подсаживают в стаканы после испарения растворителя. Повторность опыта - двукратная, количество насекомых на повторность 25. Гибель жуков учитывают на 5 сутки.
Экспериментальные данные обрабатывают статистически с помощью линии регрессии "доза пестицида-эффект" с вычислением ЛД50 (мкг/особь).
Токсичность соединений определяют на белых мышах при введении ацетоново-масляных растворов с вычислением ЛД50. Результаты исследования фунгицидного, фунгистатического, бактериостатического действия и токсичности для теплокровных животных О-алкил-О-(триалкилстаннил)-алкилтио-(селено)-фосфонатов, приведены в табл. 1. Результаты действия соединений формулы 1 приведены в табл. 2.
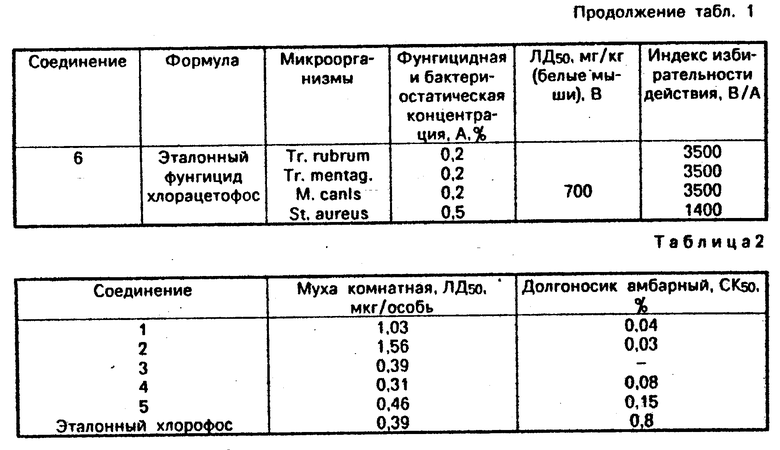
Из данных табл. 1 следует, что соединения формулы 1 обладают высокой фунгицидной и фунгистатической активностью по отношению к дерматофитам и сапрофитам, прекращая рост грибов в концентрации 0,001-0,05% и задерживая рост грибов в концентрации 0,001-0,01% . Соединения проявляют высокую бактериостатическую активность, задерживая рост бактерий в концентрации 0,001-0,025% . Индекс избирательности О-алкил-О-(триалкилстаннил)-алкилтио-(селено)-фосфонатов по отношению к патогенным грибам находится в пределах 3125-40000, к бактериям 2400-20000. По данному показателю описываемые соединения превосходят известный фунгицидный препарат хлорацетофос, который нашел применение в клинической практике.
Из данных табл. 2 следует, что соединения формулы 1 проявляют выраженную инсектицидную активность по отношению к домашней мухе (0,31-1,56 мкг/особь) и амбарному долгоносику (0,03-0,15% ). По данному показателю описываемые соединения приближаются (комнатная муха) и превосходят (амбарный долгоносик) эталонный препарат - хлорофос.
Сочетание в соединениях высокого противогрибкового действия как на возбудителей поверхностных, так и глубоких микозов и бактериостатического действия по отношению к представителю пиококков свидетельствует о том, что соединения могут найти применение в медицине в качестве противогрибкового средства.
Выраженная инсектицидная активность соединений свидетельствует о возможности применения в сельском хозяйстве и эпидемиологии в качестве средств борьбы с вредителями зерна и переносчиками инфекций. (56) Issbeil K. et al. Сильные, гермильные, станнильные эфиры фосфинистой кислоты типа [R2P(О)] nER4-n. J. Organometallic Chem. , 22, 375-386 (1970).
Пудовик П. Н. , Черкасов Р. А. , Быкова И. В. , Евстафьев Г. И. , Земская З. И. , Пазыпов М. Н. . Взаимодействие тетраалкил-(арил)-станнанов с дитиокислотами фосфора. ЖОХ, 42, 76-80 (1972).
Першин Г. Н. Методы экспериментальной химиотерапии. М. , 1971, с. 318-320.
Першин Г. Н. Методы экспериментальной химиотерапии. М. , 1971, с. 103-104.
Гар К. А. Методы испытания токсичности и эффективности инсектицидов. М. , 1963, с. 98.
Беленький М. Л. Элементы количественной оценки фармакологического эффекта. Л. , 1963, с. 152.
Авторское свидетельство СССР N 280768, кл. А 61 К 31/66, 1970.
Шрадер Г. Новые фосфорорганические инсектициды. М. : Мир, 1965, с. 36.

О-Алкил-О-(триалкилстаннил)-алкилтио-(селено)-фосфонаты общей формулы
где R - метил, этил;
R' - этил, пропил, бутил;
R'' - этил, пропил;
Х - атом серы, селена,
обладающие фунгицидной, фунгистатической, бактериостатической и инсектицидной активностью.
Авторы
Даты
1994-02-15—Публикация
1980-06-05—Подача