Изобретение относится к техноло- 1чт электрохимических производств, конкретно к получению хлора, например к процессам получения хлора и каустической соды по диaфpaгмeннo y или мембранному методам.
Целью изобретения является повышение коррозионной стойкости маталло окисных анодов, особенно при снижени содержания хлорида в анолите,
Пример 1. Окисный рутениево титановый анод (ОРТА) с активным покрытием на 30 молЛ RuOg и 70 кои.% TiO, нанесенных йа титан термическим разложением солей, облучают в ядерном jpeaKTOpe потоком нейтронов нейтронов/см, с в течение 200 ч. Такой электрод помещают в электрохимическую ячейку проточного типа, в которой катодное и анодное пространства дополнительно разделяются ионно-обменной мембраной для устранения всякой возможности попадания католита в анодное пространство ячейки и изменения в результате этого рН раствора, В ходе опыта в ячейку из вспомогательного сосуда непрерывно подают с постоянной ско- pocTblo (80 мл/ч) исследуемьтй раствор Вытекающий анолит собирает и периодически измеряют его радиоактиз кость Отдельно измеряют также радиоактивность раствора из спегщальяой с}:ллн- йи, Заполненной концентрированной соляной кислотой, в которой осуществлялось поглощенке рутения, уносимого иэ ячейки вместе с хлором з виде RuCif. Все величины приведенных скоростей коррозии ОРТА отражают суммарные потери рутения с электрода и выражены в .
Крона того, из ячейки периодически ютбирают. пробы газа я :: роматогра- фически определяют содержание в них
кислорода. Эти величины выражень: Е объемных процентах, -Периоди-чески контролир::/ют потентщал злектрода и рН раствора ( .м, таблицу опыт 5).
Харзк-.-ерной особенностью поведения ОРТА при анодной поляризации в хлоридньтх растворах является медленность установления стационарного состоянил (стацконарной скорости
коррозии). Не сразу устанавливается стационарная скорость коррозии и при замене исходного раствора NaCl на соответствующий раствор, содержащий добавку . Поэтому каждый
опыт проводят следующим образом. Первоначально электрод взодят в стационарное состояние путем поляризации его в исследуемом растворе KaCl при плотности тока 0,2 А/см и
температуре 87 в течение приблизительно 300 ч к измеряют стационарные скорость коррозии и содержание кислорода в хлоре. Затем без прерывания полярнзацт осуществлжот замену электролита в ячейке на раствор NaCl, содержащий соответствукядее количество фосфата, в котором электрод также выдержив,зют i менее 100 ч. После этого перехсдят к изнерениям
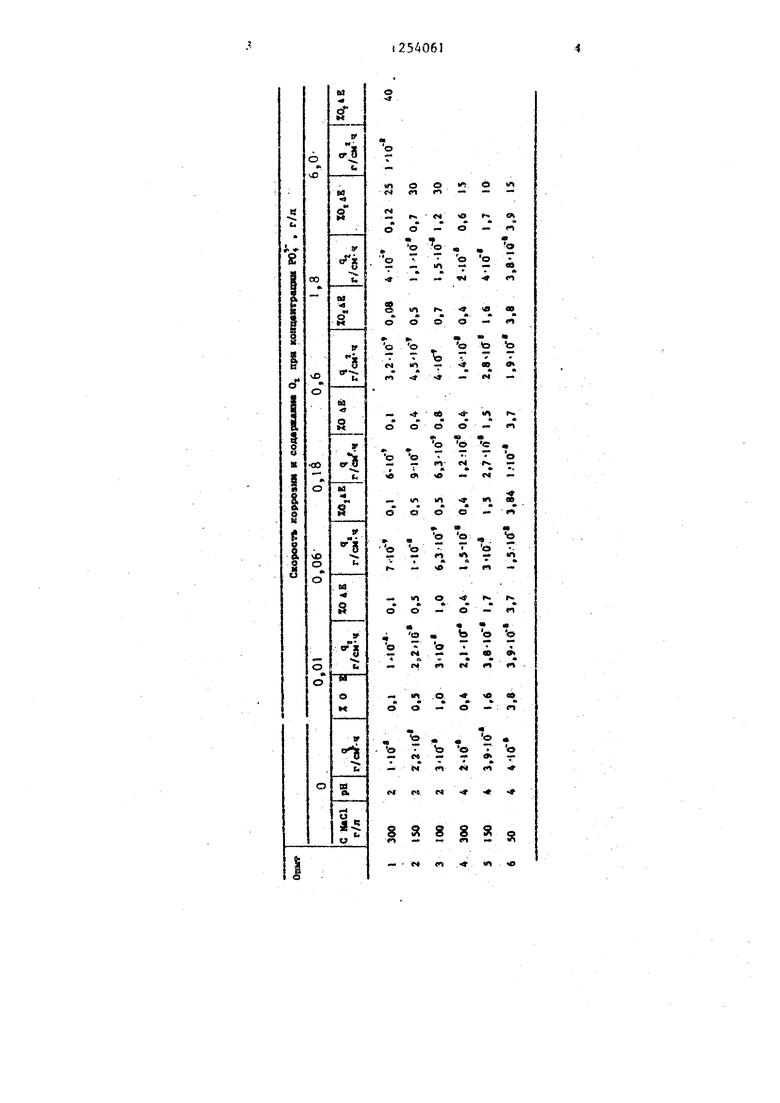
с более высокой концентрацией фосфа 1-ов. Т.-гкак г етодика проведения опытов гараип ует измерение ста1, дяоквр ных :на.личик скорссггйг коррозии, содержания кислорода 8 хлоре и потенЦ5 йла электрода. Результаты таких измерений предстгшлены в таблице. Веллчм- ы аЕ отражаит возрастание потенциала электрода при увеличении коннентрации Na-jPO в анолите по сравненкк с соо7ве гста5Ю цим раствором Had без фосфата. В тех случаях, когда велкч ша дЕ не превышала 15 мВ,, она в таблице не приводится .
Как видно из таблтда, при всех концентрациях NaCl и исследованных рН анолита введение в анолит фосфат- ионов (РО) в концентрации 0,06 - 2,0 приводит к снижению скорости коррозии ОРТА. Ингибирующее действие фосфата тем сильнее, чем ниже концентрация NaCl в анолита. В результате, если при уменьшении концентрации NaCl в исходном не содержащем фосфата растворе от 300 до 50 г/л, скорость коррозии ОРТА увеличивается примерно в 4 раза (см. таблицу, опыты i и 6 без фосфата) , то аналогичное изменение концентрации NaCl в присутствии 0,17 г/л РС не вызьюает возрастания скорости коррозии ОРТА (см. табли цу, опыты 1 и & без концентрации РО 0,18 г/л). В результате в раство ре NaCl 50 г/л + 0,18 г/л РО скорость коррозии ОРТА оказалась практически такой же, как в растворе NaCl 300 г/л, не содержащем фосфатов (см, таблицу, опыт 6 с концентрацией Р04 0,18 г/л и опыт 1 без фосфата). Оптимальной концентрацией РО в рассоле с точки зрения скорости коррози содержания кислорода в хлоре и потенциала электрода является концент- рация 0,6 г/л. При концентрации РО в растворе ниже 0,06 г/л фосфаты не оказьюают влияния на протекающие на электроде процессы. При увеличении концентрации фосфат-ионов выше 2,0 г/л происходит увеличение содержания кислорода в хлоре и потенциала электрода. Постепенно возрастает также скорость коррозии ОРТА (см. таблицу, опыт 1 и 2).
Пример 2. Измерения,аналогичные примеру 1, проводят также в растворах NaCl, в которые одно-временно вводят сульфат- и фосфат- ионы в концентрации 1-Ш и 0,18-- 2,0 г/л соответственно. При одновременном введении в хлоридные растворы фосфат- и сульфат-ионов наблюдается снижение скорости коррозии ОРТА и содержания кислорода в хлоре. Нап- ример, в растворе NaCl 150 г/л при
одиовременном введении 10 г/л S04 и только 0,18 г/л ионов POvj скорость коррозии снижается примерно в 2 раза (от 210 до 910 г/см . ч), а ,содержание кислорода в хлоре уменьшается от 1,4 до 1,0%. Таким образом если присутствие в хлоридных растворах сульфат-ионов в концентрации 10 г/л приводит к увел1-гчению содержания кислорода в хлоре и возрастани в определенных условиях скорости коррозии анодов (З), то при одновременном введении в хлоридные растворы фосфат- и сульфат-ионов происходит снижение скорости коррозии и содержания кислорода в хлоре.,
Полученные результаты показывают, что введение фосфат- к сульфат-ионов в хлоридные растворы оказьшается особенно полезным при проведении электролиза хлоридных растворов с низкой концентрацией NaCl.
Введение фосфатов в анолит при проведении хлорного электролиза мембранным и дйафрагменным методами может позволить значительно полнее вырабатьшать NaCl из поступающего на электролиз электролита, что дает в принципе возможность существенно уменьшить объем очистных сооруженш для приготовления рассола. Это особенно экономически целесообразно в случае мембранного электролиза, учитывая высокие требования, предъявляемые к очистке рассола. Снижение концентрахщи NaCl от 300 до 150 г/л приводит к снижению электропроводности электролита приблизительно в 2 раза. Однако в случае мембранного электролиза это не вызовет существенного увеличения напряжения на ванне, вследствие малого расстояния между мембраной и анодом, При этом сопротивление самой мембраны не увеличится и возрастет перенос воды из анодно1 о пространства в катодное, что снизит расход воды, необходимой для подпитки катодного пространства электролизера, и еще больше увеличит полноту использования поступающего на электролиз рассола„

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МОНОГИДРАТА ГИДРОКСИДА ЛИТИЯ ВЫСОКОЙ СТЕПЕНИ ЧИСТОТЫ ИЗ МАТЕРИАЛОВ, СОДЕРЖАЩИХ КАРБОНАТ ЛИТИЯ ИЛИ ХЛОРИД ЛИТИЯ | 2019 |
|
RU2751710C2 |
| Способ получения моногидрата гидроксида лития высокой степени чистоты из материалов, содержащих соли лития | 2021 |
|
RU2769609C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРА И ХЛОРСОДЕРЖАЩИХ ОКИСЛИТЕЛЕЙ И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2005 |
|
RU2315132C2 |
| Способ удаления нитрит-ионов из водных растворов | 2016 |
|
RU2625466C1 |
| СПОСОБЫ ОБРАБОТКИ ПРОМЫШЛЕННЫХ СТОЧНЫХ ВОД ЭЛЕКТРОЛИЗОМ | 2016 |
|
RU2730328C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИДА ЛИТИЯ ВЫСОКОЙ СТЕПЕНИ ЧИСТОТЫ ИЗ ПРИРОДНЫХ РАССОЛОВ | 1998 |
|
RU2157338C2 |
| Способ получения моногидрата гидроксида лития из рассолов | 2019 |
|
RU2713360C2 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОГИДРАТА ГИДРОКСИДА ЛИТИЯ ВЫСОКОЙ СТЕПЕНИ ЧИСТОТЫ ИЗ МАТЕРИАЛОВ, СОДЕРЖАЩИХ КАРБОНАТ ЛИТИЯ | 2001 |
|
RU2196735C1 |
| СПОСОБ ПРОИЗВОДСТВА ПЕРОКСИДА ВОДОРОДА И ХЛОРАТА | 2006 |
|
RU2375500C2 |
| УДАЛЕНИЕ ДИОКСИДА УГЛЕРОДА ИЗ ПОТОКОВ ОТХОДЯЩЕГО ГАЗА ПОСРЕДСТВОМ СОВМЕСТНОГО ОБРАЗОВАНИЯ КАРБОНАТНЫХ И/ИЛИ БИКАРБОНАТНЫХ МИНЕРАЛОВ | 2008 |
|
RU2477168C2 |


| 0 |
|
SU369923A1 | |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1986-08-30—Публикация
1984-04-25—Подача