Изобретение относится к способам регенерации серебряного катализатора для окисления этилена в окись этилена.
Известен способ регенерации катализатора для окисления этилена путем обработки отработанного серебряного катализатора водно-спиртовыми растворами солей цезия и рубидия. После .удаления растворителя регенерированный катализатор содержит 0,02 мас.% цезия (патент ФРГ № 2611856, кл. В 01 J 23/96, опублик. 1977).
Известен способ регенерации сереб25
30
ряного катализатора для окисления эти-15 ния этилена в окись этилена является лена путем его промывки водой с последующей обработкой солями щелочных металлов - цезия, калия и натрия - в органическом растворителе таким образом, чтобы количество щелочных металлических ионов Достигало величины А Ю -8 -10 з г-экв/кг катализатора (заявка ФРГ № 2746976, кл. В 01 J 23/50, опублик. 1978).
Известен способ регенерации катализатора для окисления этилена путем увлажнения катализатора водой и высу- пшванием его при 100-300 С (заявка ФРГ № 2709306, кл. В 01 J 23/96, опублик. 1977).
Известен способ регенерации катализатора для окисления этилена путем обработки его кислородом при 200-400 0 и давлении 0,1-100 бар в присутствии инертного газа (патент Англии № 1544081, кл. В 01 J 23/96, опуб-: лик. 1979).
Эти способы являются эффективными для некоторьк типов пассивации катализатора, главным образом для осуществления регенерации в лабораторном масштабе.
Однако присутствие в промышленных реакторах большого количества кислорода, главным образом при высоких не- адсорбированных количествах органических веществ, не только не повышает активность и селективность катализатора, но даже может вести к необратимой дезактивации или изменить обратимую пассивацию катализатора на необратимую. Увлажнение катализатора является практически неэффективным и может способствовать его более быстрому механическому износу.
Целью изобретения является повьш1е- ние эффективности способа.
высока эффективность, главным образом устранение отравления катал зато- ра углеводородами С и высшими соединениями серы, причем в значительной
20 степени предотвращаются необратимые изменения катализатора. Кроме того, существует возможность осуществления регенерации катализатора непосредственно в каталитических ложах промышленных реакторов, причем речь идет о коротком времени регенерации и безопасности такой регенерации. Причем способ позволяет снизить необратимое отравление катализатора, а также после осуществления регенерации произвести с более высоким эффектом активацию катализатора обработкой солями щелочных металлов и другими соединениями, которые в других случаях
35 могли быть практически неэффективными.
Регенерацию катализатора осуществляют в сравнительно широком диапазоне давлений, причем в большинстве случаев удобнее работать при давлениях ниже, чем те, которые используют при синтез е окиси этилена. Таким образом, необходимо сначала работать при низком общем давлении, а потом постепенно его повышать. Следователь40
45
но, общее давление может быть от О,1 кПа до 1,5 МПа.
Температура катализатора при реге- JQ нерации должна быть в пределах 200- .
Регенерацию можно осуществлять даже при высоком вакууме, но самьм подходящим с технико-экономической точки 55 зрения является диапазон легкодостижи мьпс давлений. Атмосферу может создавать синтез-газ, не содержащий кислород, но в этом случае необходимо как
Указанная цель достигается способом регенерации серебряного катализатора для окисления этилена в окись этилена, заключающимся в термообработке катализатора при 200-315 с и давлении от О,1 кПа до 1,5 МПа в атмосфере синтез-газа или атмосфере синтез-газа с добавлением корродирующего вещества - молекулярного хлора или окиси и двуокиси азота в количестве 1-10 - от массы катализатора.
Преимуществом способа регенерации серебряного катализатора для окисле
ния этилена в окись этилена является
высока эффективность, главным образом устранение отравления катал зато- ра углеводородами С и высшими соединениями серы, причем в значительной
степени предотвращаются необратимые изменения катализатора. Кроме того, существует возможность осуществления регенерации катализатора непосредственно в каталитических ложах промышленных реакторов, причем речь идет о коротком времени регенерации и безопасности такой регенерации. Причем способ позволяет снизить необратимое отравление катализатора, а также после осуществления регенерации произвести с более высоким эффектом активацию катализатора обработкой солями щелочных металлов и другими соединениями, которые в других случаях
могли быть практически неэффективными.
Регенерацию катализатора осуществляют в сравнительно широком диапазоне давлений, причем в большинстве случаев удобнее работать при давлениях ниже, чем те, которые используют при синтез е окиси этилена. Таким образом, необходимо сначала работать при низком общем давлении, а потом постепенно его повышать. Следователь
но, общее давление может быть от О,1 кПа до 1,5 МПа.
Температура катализатора при реге- нерации должна быть в пределах 200- .
Регенерацию можно осуществлять даже при высоком вакууме, но самьм подходящим с технико-экономической точки зрения является диапазон легкодостижи- мьпс давлений. Атмосферу может создавать синтез-газ, не содержащий кислород, но в этом случае необходимо как
можно более низкое давление для того, чтобы не произошло окисление кроме окисления этилена в окись этилена, также адсорбированных на катализаторе органических компонентов, а тем самым перегрев катализатора и агломерация частиц серебра. Поэтому необходимо работать с синтез-газом, практически освобожденным от кислорода, содержащим этилен, азот, аргон, углекислый газ, метан, этан и контролируемые ко.личества паров хлорорганических соединений или же других ингибиторов,. Такими хлорорганическими соединениями могут быть тетрахлоэтан, дихлорэтан, винилхлорид, трихлорэтилен. Под инертным газом из наиболее известных инертных газов подразумеваются также газы, которые в указанных условиях реакции ведут себя как инертные, следовательно, к ним относят также метан и этан. Корродирующим веществом является отдельный газ или смесь газов,
-возможно смесь газов и паров, которые при температуре регенерации или реактивации могут атаковать не только катализатор или его серебро и другие активные компоненты, но помогают удалению других металлов, которые являются нежелательным компонентом отравленного катализатора и которые попали на него уже с сырьем или в результате коррозии оборудования. Таким образом, корродирующее вещество позво
ляет избавить катализатор от каталитических ядов или как можно больше повысить поверхность частичек серебра.
Такими корродирующими веществами являются окислы азота - окись или двуокись.
Количество корродирующего вещества необходимо контролировать , так как избыточное количество может временно снизить активность катализатора. Кроме того, корродирующее вещество можно в контролируемых количества применять не только при реактивации или регенерации .катализатора, но в значительно меньших количествах в ка честве примеси в исходное сырье или другим способом непосредственно в реактор с катализатором при изготовлении окиси этилена.
Приме р 1. В реактор лабора- торной тест-аппаратуры вводят 0,5 г (0,4 см) серебряного катализатора с содержанием 9,2 мас.% серебра на аль;0
5 0
5 о
5
5
Q
о
5
фа-алюминии в качестве носителя. Зернистость катализатора О,5-0;63 мм, причем речь идет о катализаторе, приготовленном раздроблением отравленного катализатора, активность которого в течение двух лет использования понизилась приблизительно на одну пятую часть. На этот катализатор, нагретый на необходимую реакционную температуру, сначала на , подводят реакционный газ, содержащий, об.%: кислород 7, этилен 39, двуокись углерода 4, азот с аргоном 50, при объемной скорости 900 ч . Потом при давлении, практически близком к атмосферному (100 кПа), температуру постепенно по- вьшают, причем одновременно определяют конверсию и селективность этилена в окись этилена при одном проходе катализатором.
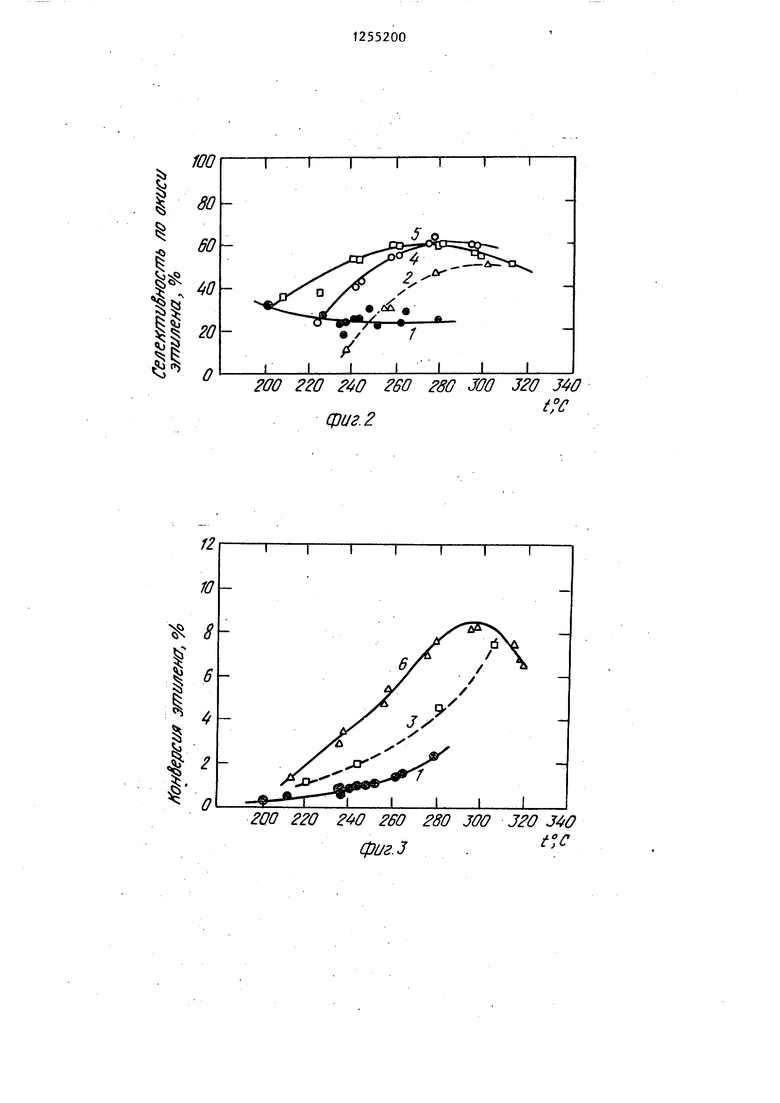
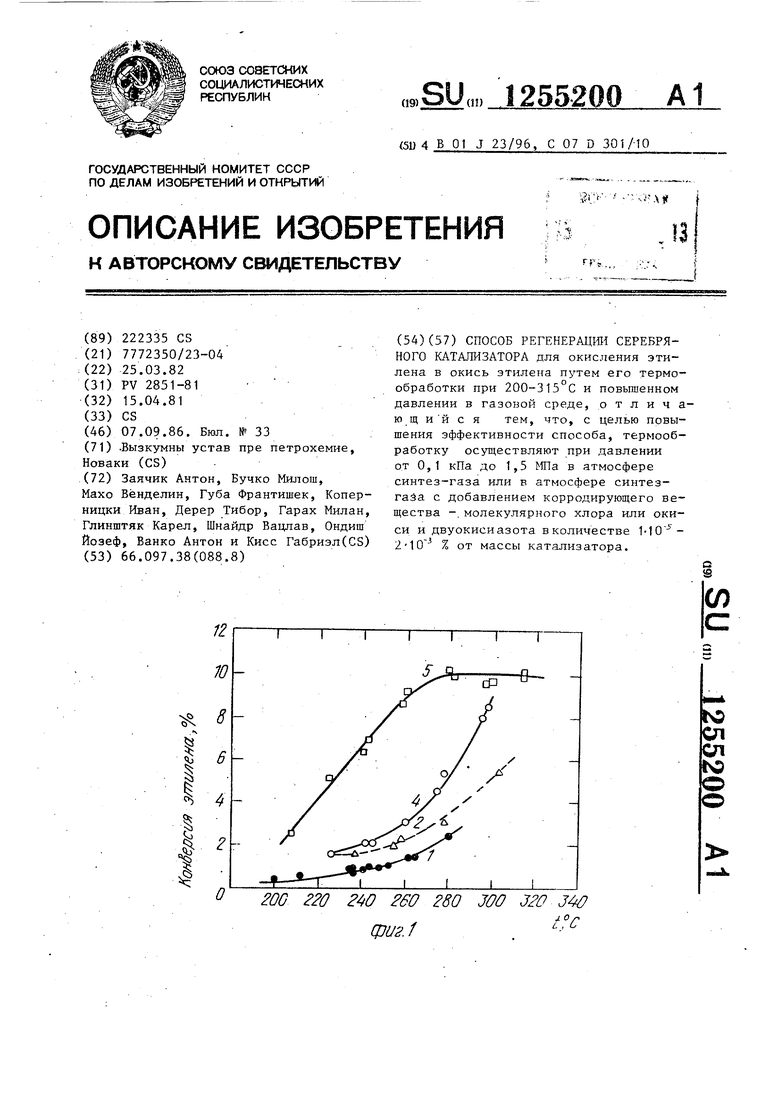
Результаты влияния нагревания на конверсию этилена и селективность в окись этилена в зависимости от температуры изображены на фиг,1 и 2 (кривая 1).
После окончания этих измерений на катализатор подводят реакционный газ, освобожденный от кислорода (ниже 1 об.%), при 220 С в течение 20 ч при объемной скорости 900 . Потом, после прополаскивания азотом, начинают добавлять реакционный газ указанного состава (7 об.% 0,, 39 об.% , 4 об.% COg, остаток составляет азот), при этом в два раза увеличивается конверсия этилена и селективность в окись этилена, как это видно из результатов влияния температуры на фиг.1 и 2 (кривая 4).
Приме р 2, Регенерацию катализатора, специфицированного в примере 1, производят в токе азота, содержащего 0,1 об.% двуокиси углерода и 0,15 об.% кислорода при 220 с и давлении 100 кПа в течение 20 ч при объемной скорости 1000 . По истечении этого времени приводят температурный . тест активности. Полученные резуль таты ( при использовании реакционного газа, специфицированного в примере 1) конверсии этилена при одном проходе через катализатор и селективность в окись этилена графически изображены на фиг.1 и 2 (кр1тая 2).
П р и м е р 3. Реге герацию серебряного катализатора на альфа-алюминии в качестве носителя, специфицированного в примере 1, производят в токе
.реакционного газа, также специфицированного в примере 1, при к давлении 100 кПа в течение 2 ч и объемной скорости 900 . Поток реактор с катализатором охлаждают до 220 С и при использовании реакционного газа, состоящего, об.%: кислород 7-, этилен 39, двуокись углерода 4, азот с примесью аргона 50, проводят температурный тест его активности.
Полученные результаты в зависимости о.т температуры графически изображены на фиг.1 и 2 (кривая 5). Очевидно существенно возрастание активности каташизатора, о чем свидетельству- ет значительное возрастание конверсии этилена и селективности перехода этилена в окись этилена.
Пример 4. Катализатор, специфицированный в примере 1, сначала на- 2о температуру постепенно понижают до
температуры производства окиси этиле-О,
гревают до в токе реакционного газа, специфицированного в примере 1. При этой температуре и объемной скорости 900 достигается конверсия этилена и селективность в окись эти- 25 лена, изображенные на фиг.1 и 2 (кривая 1). Затем в ток реакционного газа непосредственно перед реактором добавляют газообразный молекулярный хлор одноразовым введением в количе- зо стве 0,0020 мас.% (рассчитано на массу серебряного катализатора). После этого катализатор еще остается в токе реакционного газа, освобожденного от
На 215 G, причем во время понижения температуры давление в циркуляционном округе доводят до 1,7 МПа и концентрацию этилена регулируют на 30 мол.%. После достижения температуры 215 С и постепенном добавлении кислорода начинают синтез окиси этилена в зависимости от концентрации кислорода на выходе из реактора на 4,5 мол.%.
На регенерированном таким способом катализаторе достигают 97%-ного выхода окиси этилена, достигаемого на новом катализаторе, селективность по отношению к окиси этилена 75,6%.
кислорода, при объемной скорости 900 в течение 20 ч. По истечении этого времени осуществляют измерение активности катализатора. .
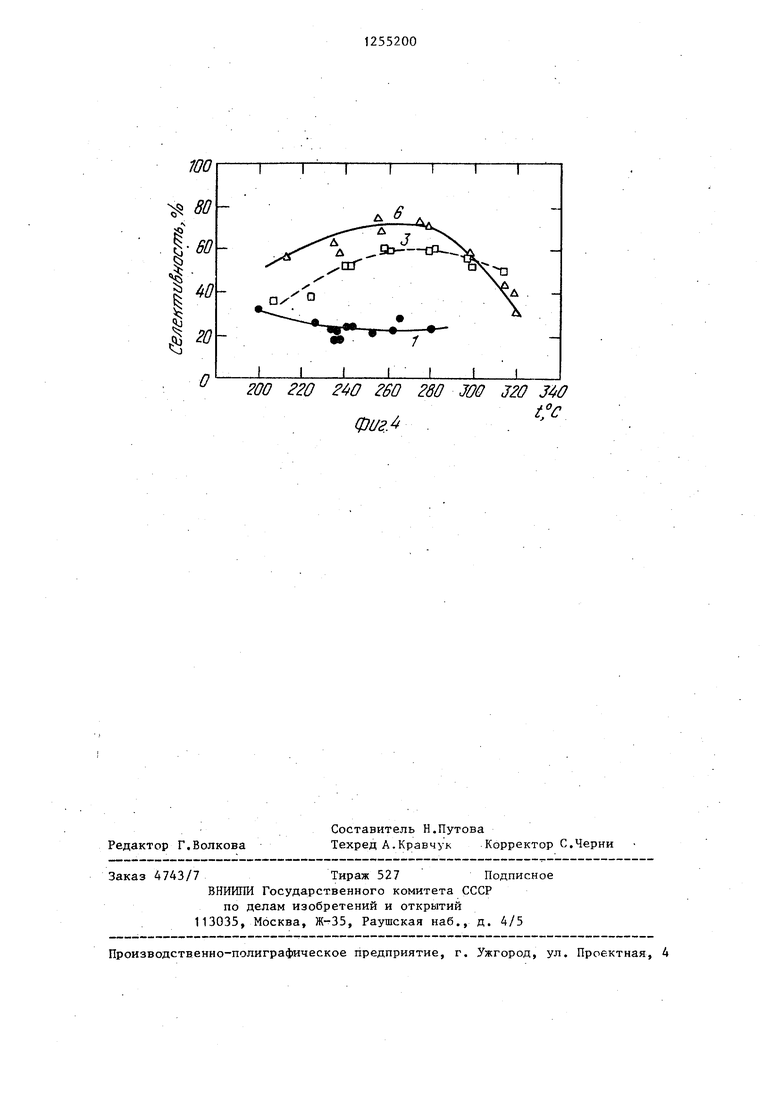
Полученные результаты графически изображены на фиг.З и 4 (кривые 3, 1 представляют референционные результаты на катализаторе без регенерации).
П р и-м е р 5. Регенерацию отравленного серебряного катализатора, , 45 специфицированного в примере 1, производят так же, как в примере 4, но Вместо хлора используют смесь окиси и двуокиси азота в количестве 0,002 мас.%. на массу катализатора. 50 Активность катализатора значительно повышается, как видно из графического
55200
, JQ
5изображения результатов на фиг.З и 4 (кривая 6) ,
Примерб. В полупроизводственном реакторе производства окиси этилена непосредственным окислением этилена и на катализаторе, специфицированном в примере 1, катализатор регенерируют таким образом, что давление трубковом реакторе с катализатором поддерживают на значении 0,7-1,5 МПа . синтез-газом, кислород которого проре- агировал. Состав газа, мол.%: этилен 30, углекислый газ 5, метан с этаном 44, аргон 4, азот остаток, причем этот газ содержит следы хлорорганиче- ских соединений в количестве общего т;одержания хлора 5-10 мас.%. Температуру реакции в течение 4 ч поддерживают на значении 240-260 С. Затем
-О,
На 215 G, причем во время понижения температуры давление в циркуляционном округе доводят до 1,7 МПа и концентрацию этилена регулируют на 30 мол.%. После достижения температуры 215 С и постепенном добавлении кислорода начинают синтез окиси этилена в зависимости от концентрации кислорода на выходе из реактора на 4,5 мол.%.
На регенерированном таким способом катализаторе достигают 97%-ного выхода окиси этилена, достигаемого на новом катализаторе, селективность по отношению к окиси этилена 75,6%.
П р и м е р 7. Катализатор, специфицированный в приме Ье 1, сначала нагревают до 200 С в токе реакционного газа, специфицированного в примере 1 при давлении 0,1 кПа.. Затем в ток реакционного газа непосредственно перед реактором добавляют газообразный молекулярный хлор полунепрерывно 110 мас.% (рассчитано на массу серебряного катализатора) в течение 16 ч. jjo истечении этого времени осуществляют измерение активности катализатора. При 280°С и объемной скорости 900 чГ достигается конверсия этилена-при одном проходе через катализатор 5,5%, а селективность по отношению к окиси этилена 60%.,
200 220 260 гвО JOO 320 340
tfc фиг.2


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения окиси этилена | 1979 |
|
SU1060110A3 |
| СПОСОБ ПОЛУЧЕНИЯ ОКИСИ ЭТИЛЕНА | 1972 |
|
SU340163A1 |
| СЕРЕБРЯННЫЙ КАТАЛИЗАТОР ДЛЯ ОКИСЛЕНИЯ ЭТИЛЕНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1987 |
|
RU2034648C1 |
| СПОСОБ ПЕРЕРАБОТКИ УГЛЕРОДОСОДЕРЖАЩЕГО СЫРЬЯ И КАТАЛИЗАТОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2011 |
|
RU2476583C1 |
| РЕГЕНЕРАЦИЯ СОДЕРЖАЩИХ МЕТАЛЛ КАТАЛИЗАТОРОВ | 2011 |
|
RU2579147C2 |
| ПРОКАЛИВАНИЕ В ИНЕРТНОМ ГАЗЕ В ПРИСУТСТВИИ ОКИСЛЯЮЩЕГО КОМПОНЕНТА В НЕБОЛЬШОЙ КОНЦЕНТРАЦИИ | 2006 |
|
RU2411997C2 |
| Способ получения циклогексанона | 1980 |
|
SU1255618A1 |
| НЕПРЕРЫВНЫЙ СПОСОБ БЕСКИСЛОРОДНОЙ КОНВЕРСИИ МЕТАНА | 2008 |
|
RU2467993C2 |
| СПОСОБ СЕЛЕКТИВНОГО ПОЛУЧЕНИЯ УКСУСНОЙ КИСЛОТЫ И КАТАЛИЗАТОР ДЛЯ СЕЛЕКТИВНОГО ОКИСЛЕНИЯ ЭТАНА И/ИЛИ ЭТИЛЕНА В УКСУСНУЮ КИСЛОТУ | 1997 |
|
RU2189969C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОКИСИ ЭТИЛЕНА ИЗ МЕТАНА | 1999 |
|
RU2156246C1 |
12
I I I I I
200 220 260 280 JOO J20 J4O фиг.З
L )(
J4O
L )(
200 220 гео т joo зго jw
t°c Фиг. ..
Редактор Г.Волкова
Составитель Н.Путова
Техред А.Кравчук Корректор С.Черни
Заказ 4743/7Тираж 527 Подписное
ВНИИПИ Государственного комитета СССР
по делам изобретений и открытий 113035, Москва, Ж-35, Раушская наб., д. 4/5
Производственно-полиграфическое предприятие, г. Ужгород, ул. Проектная, 4
Авторы
Даты
1986-09-07—Публикация
1982-03-25—Подача