Изобретение относится к микробиологической промышленности, молекулярной биологии и генетической инженерии и представляет собой вектор экспрессии чужеродных генов в клетках Escherichia coli.
Целью изобретения является упрощение процесса получения различных белковых продуктов и повышение уровня экспрессии чужеродных генов за счет создания нового вектора для экспрессии чужеродных генов в клетках E.coli.
Вектор для экспрессии чужеродных генов pGDP2 характеризуется следующими признаками: имеет длину около 4,6 тыс. п.о., состоит из:
линейной формы векторной плазмиды pBRH4,
фрагмента PF1 ДНК фага ⊘Х174 размером 230 п.о., содержащего регуляторную область гена D и присоединенного к EcoROI-сайту плазмиды pBRH4; содержит:
в качестве генетических маркеров гены Apr и Тсr,
уникальные сайты расщепления эндонуклеазами рестрикции, расположенные на следующих расстояниях от EcoRI-сайта: EcoRV 160 п.о. вправо, BamHI 350 п. о. вправо, Sal I 626 п.о. вправо, Bal I 1419 п.о., вправо Pvu 11 2041 п. о. вправо, Pst I 3584 п.о. вправо,
сайты расщепления другими эндонуклеазами рестрикции, расположенные на следующих расстояниях от EcoRI-сайта; Hind II 70 п.о. влево, 626 и 3882 п. о. вправо; чужеродные гены встраивают по уникальному EcoRI-сайту;
экспрессия чужеродных генов обеспечивается в любом штамме E.coli К 12 или его мутантах.
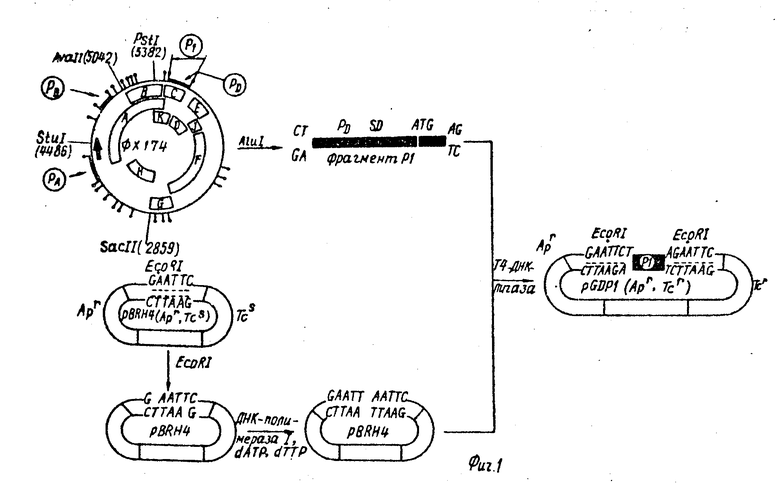
Конструирование вектора pGDP3 состоит в следующем. Фрагмент RF1 фага ⊘ Х174 соединяют с векторной плазмидой pBRH4, расщепленной по EcoRI-сайту, и получают рекомбинантную плазмиду pGDP1, малый Р1-фрагмент которой содержит в своем составе регуляторную область гена D фага ⊘Х174 (см.фиг.1).
Выделяют фрагмент Р1, подвергают его частичному гидролизу эндонуклеазой рестрикции Hinf I, встраивают полученный фрагмент Р2 в векторную плазмиду pBRH4, расщепленную по EcoRI-сайту, и получают плазмиду pGDP2, содержащую два EcoRI-сайта (см.фиг.2).
Инактивируют дистальный по отношению к N-концу гена D EcoRI-сайт и получают вектор pGDP3, имеющий уникальный сайт расщепления эндонуклеазой рестрикции EcoRI.
В состав вектора входит природная регуляторная область гена D фага ⊘Х174 обеспечивающая конститутивную (нерегулируемую) экспрессию чужеродных генов, встроенных в вектор.
Использование вектора позволяет значительно упростить технологию промышленного получения различных белковых продуктов (например, лейкоцитарных интерферонов человека, галактокиназы и др.) при сохранении высокого уровня биосинтеза. Упрощение технологии связано с тем, что при конститутивном биосинтезе белковых продуктов отсутствует необходимость индукции (путем разбавления культуры штамма-продуцента в 20-50 раз или в результате добавления индуктора).
Кроме того, вектор pGDP3 обеспечивает высокий уровень экспрессии чужеродных генов. Так, в случае гена Tcr EOP50 составляет 100 мкг/мл против 60 мкг/мл для вектора ptrpED5 1 (см.пункт 3 примера и таблицу).
П р и м е р. Конструирование вектора pGDP3.
1.Конструирование рекомбинантной плазмиды pGDP1.
150 мкг PF1 ДНК фага ⊘ Х174 расщепляют с помощью 200 ед. эндонуклеазы рестрикции Alu I в буфере, содержащем 50 mM NaCl, 10 mM трис-HCl (рН 7,6), 10 mM MgCl2 и 10 mM меркаптоэтанол, при 37оС в течение 2 ч. Общий объем реакционной смеси 800 мкл. Смесь субфрагментов обрабатывают фенолом, осаждают этанолом и растворяют в 150 мкл ТЕ-буфера, содержащего 10 mM трис-HCl (рН 8,0) и 1 mM ЭДТА, после чего наносят на 8%-ный полиакриламидный гель (ПААГ) и подвергают электрофоретическому разделению. Полоску геля, содержащую фрагмент ДНК A6, вырезают и ДНК элюируют по Максаму-Гилберту.
Полученный таким образом фрагмент Р1, содержащий промотор и рибосомсвязывающий участок (последовательность Шайн-Дальгарно) гена D фага ⊘ Х174, встраивают в плазмидный вектор pBRH4, который предварительно расщепляют эндонуклеазой рестрикции EcoRI, и обрабатывают Кленовским фрагментом ДНК-полимеразы E.coli в присутствии dATP и dTTP для достройки выступающих 5'-концов. 1 мкг подготовленного таким способом вектора pBRH4 и 0,1 мкг фрагмента Р1 соединяют с помощью 5 ед. Т4-ДНК-лигазы в буфере, содержащем 50 mM трис-HCl (рН 7,5), 10 mM MgCl2, 5 mM DTT и 0,2 mM ATP, при 15оС в течение 16 ч. Общий объем реакционной смеси 50 мкл. Полученной смесью рекомбинантных ДНК трансформируют клетки E.coli К 802 по известному методу. Отбирают клоны, устойчивые к тетрациклину (10 мкг на 1 мл), и проводят их рестрикционный анализ.
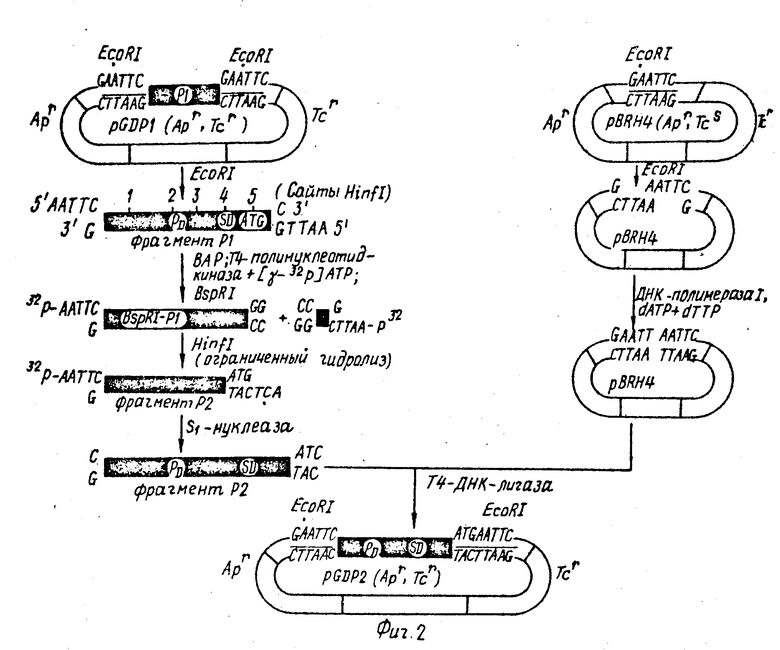
2.Конструирование рекомбинантной плазмиды pGDP2.
Схема получения плазмиды pGDP2 представлена на фиг.2.
200 мкг плазмиды pGDP1 расщепляют с помощью 400 ед. эндонуклеазы EcoRI в буфере, содержащем 100 mM NaCl, 50 mM трис-HCl (рН 7,5), 10 mM MgCl2, 1 mM DTT, при 37оС 90 мин. Общий объем реакционной смеси 800 мкл. Смесь субфрагментов обрабатывают фенолом, осаждают этанолом и растворяют в 150 мкл ТЕ-буфера. Отделение фрагмента Р1 от исходного вектора производят с помощью электрофореза в 8% -ном ПААГ. Фрагмент Р1 элюируют из геля, как описано ранее. Затем фрагмент Р1 дефосфорилируют, вводят 5'-концевую метку с помощью [α-32P] ATP и Т4-полинуклеотидкиназы по известной методике. Меченый фрагмент Р1 расщепляют эндонуклеазой рестрикции BspRI. 14 мкг полученной смеси фрагментов расщепляют с помощью 14 ед. эндонуклеазы Hinf I в буфере, содержащем 50 mM NaCl, 10 mM трис-HCl (рН 7,6), 10 mM MgCl2, 10 mM меркаптоэтанол, при 37оС и выделяют из реакционной смеси фрагмент Р2 с помощью электрофореза в 8% -ном ПААГ. 0,05 мкг фрагмента Р2 обрабатывают 5 ед. S1-нуклеазы в буфере, содержащем 0,2 М NaCl, 50 ml ацетат натрия (рН 4,5), 1 mM DTT и 5% глицерин, при 20оС в течение 20 мин. По окончании инкубации смесь обрабатывают фенолом, хлороформом, и ДНК осаждают этанолом. Затем подготовленный таким образом фрагмент встраивают в плазмиду pBRH4, предварительно расщепленную эндонуклеазой EcoRI и обработанную Кленовским фрагментом ДНК-полимеразы E. coli в присутствии dATP и dTTP. Ферментативное соединение фрагмента Р2 и вектора проводят, как описано ранее, с помощью Т4-ДНК-лигазы в 50 мкл реакционной смеси.
Полученной смесью рекомбинантных плазмид трансформируют клетки E.coli К 802 и отбирают клоны, устойчивые к 10-20 мкг тетрациклина на 1 мл среды.
3.Конструирование вектора pGDP3.
1,5 мкг ДНК плазмиды pGDP2 расщепляют 0,1 ед. эндонуклеазы рестрикции EcoRI в буфере, содержащем 10 мМ NaCl, 5,0 mM трис-HCl (рН 7,6), 10 mM MgCl2, 1 mM DTT, при 37оС в течение 1 ч. Общий объем рестрикционной смеси 15 мкл. Затем полученную ДНК обрабатывают Кленовским фрагментом ДНК-полимеразы 1 в присутствии dATP и dTTP для заполнения выступающих 5'-концов, а затем Т-4-ДНК-лигазой (10 ед) в буфере, содержащем 50 mM трис-HCl (рН 7,5), 10 mM MgCl2, 5 mM DTT и 0,2 mM ATP, при 12оС в течение 10 ч. Общий объем реакционной смеси 100 мкл. Продуктами плазмидной сшивки трансформируют клетки E. coli К 802. Отбирают клоны, устойчивые к тетрациклину, проводят рестрикционный анализ плазмидных ДНК, выделенных из этих клонов. С помощью эндонуклеаз рестрикции EcoRI и Hind II показано, что в 3-х из 32-х проанализированных клонов содержатся плазмиды, в которых инактивирован дистальный по отношению к N-концу гена D дистальный сайт EcoRI. Один из этих клонов используют в качестве источников вектора pGDP3.

ВЕКТОР PGDP3 ДЛЯ ЭКСПРЕССИИ ЧУЖЕРОДНЫХ ГЕНОВ В КЛЕТКАХEscherichia coli характеризуется следующими признаками: имеет длину около 4,6 тыс. п.о.; состоит из линейной формы векторной плазмиды pBRH4, фрагмента RFI ДНК фага размером 230 п.о., содержащего регуляторную область гена D и присоединенного к EcoRI-сайту плазмиды pBRH4;
содержит в качестве генетических маркеров гены Apr и Tcr; сайты расщепления эндонуклеазами рестрикции, расположенные на следующих расстояниях от EcoRI-сайта: EcoRV 160 п.о. вправо, BamHI 350 п.о. вправо, Sal I 626 п.о. вправо, Bal I 1419 п.о. вправо, Pvu II 2041 п.о. вправо, Pst I 3584 п.о. вправо, сайты узнавания другими эндонуклеазами рестрикции, расположенные на следующих расстояниях от EcoRI-сайта: Hind II 70 п.о. влево, 626 и 3882 п. о. вправо, чужеродные гены встраивают в EcoRI-сайт.
| Hallewell R.A | |||
| and Emtage S | |||
| Plasmid vestors containing the tryptophan operon promoter suitable For efficient regulated expression of foreign genes | |||
| Способ получения фтористых солей | 1914 |
|
SU1980A1 |
Авторы
Даты
1994-12-30—Публикация
1984-08-13—Подача