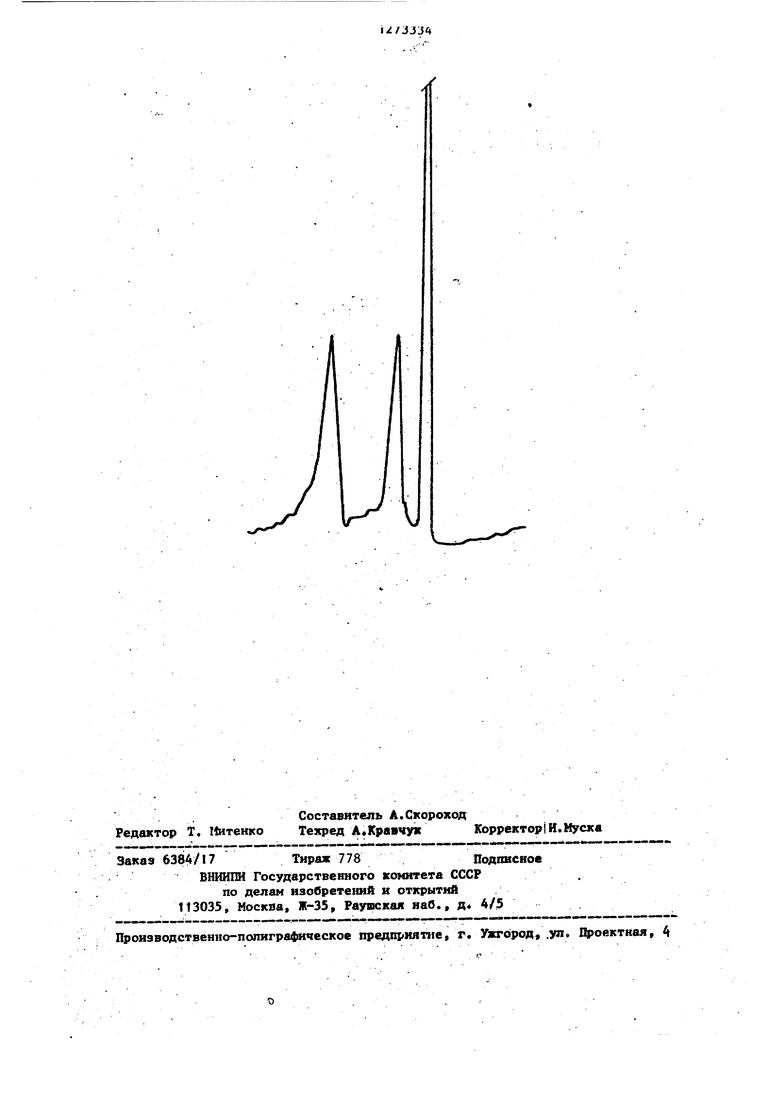
Изобретение относится к биохимии, в частности к способам определения стероидных горкомов. Цель изобретении повышение точности, чувствительности, специфичнос ти способа, а также возможность одновременного определения в пробе нескольких стимуляторов роста группы андрогенов , Способ осуществляют следзтощим образом, 3 - 10 г образца съедобных тканей сельскохозяйственных животных (мышц, печени или почек) гомогенизируют в смесителе с пятикратным объемом 0,14 М раствора Had. Гомогёнат переносят в плоскодоиную колбу, добавляют 2,5 Сбь:; ; смеси, растворителей эфир--нетн,пси/;.)1д (Itl) и встрнхи™ вают ч в а-;и-ЛГПге jinn встряхиааиип, Эк(::гра};;т ; и п-пггоряют рапным объемо 3K.:riin f;H а в те геиис 30 мин Ортаническую фазу (после отстаива ти смеси - Repxif-in фаза) отсасывают мороЕской пигг.еткой с групигй (или лю бьэ-i npиcпocoб.eнlш для отсасывания жидкостей)., переносят D колбу, фяпьт руют через б-viводный fki SO, н оыпар на рото1ио;- испар} теле при 40 С .(..,« гг7П поианпый эусстрпкт раст воряют в .киина.;1ьнон объеме xjiojjoфор1- а (З-З Hjt) и наносят ка колонку cmTiuairwiH (200 меш) , Используют ко .у 0,7:к7.,О см, Злюцию проводят с скоростью Of ь й/мкн. Фракция 1В Mil х.хо реформа -не содержит исследуекъе cTRpci.p.jJj фрак.|. 2 - .30 ;-ш О Зл-ного ;-1етанола w :щипк1форме .содержит малопопприме cTfipoi fc (метилтестостерон стероид К К, -нортестос.тероп стоиокд 1 ,1 „ 5 ,, трепбопон -- сг1р(пч д--агод . ростздч; 1/р -o.u-j-oi стероид I , S , 7, 17 .: о- -дигид.ротестостерсн, стероид i;.;), фракция 3 . 25 мл 15%-югс кста-но;.1а в х.лорофор™ ме - содершп поляр 1ые стероиды (I а ,8 ci-ерпид - i 1 -оксиметил. тестостеро5.;, ,1,1 стеронд -Д аидросгадие.1-1 7р -о.п.-З-он, J .1,10 стероид-6 fj оксиметандро(глч;:нолок) . Фракцило 2 (.после xpo aтoгpaфин на колонке силикаге м.л) вынарииагот в вакууме до минимального объема и наносят на гшастину ф.1Ю1)иэилас При ф.пориэи.г1 с флюоресцентным ин дикатором при А 254 нм (пластины 20х,0 см, толщина слоя 0,6 мм) Тон I A2 ослойную хроматографию проподят вукратно в системах растворителей: лороформ - этанол - бензол (85:5:15) гексан - дихлорэтанэтилацетат (50:20:20). Локализацию стероидов станавливают облучением пластины н Ф-свете и по Rf стандартов. Участки слоя силикагеля, соответствующие исследуемым стероидам, снймают с пластины, переносят в плоскодонные колбочки и элюиругот дважды (по 30 мин) 10 мл 96%-ного этанола на магнитной мешалке, Этанольные , рдстзоры после двукратной элюции объединяют, вьтаривают досуха и ис -. пользуют для количественного определения стероидов флюорометрическим или ПКХ методом. Фракцию 3, полученн то после хроыатографии.на колонке силикагеля и содержащую полярные стероиды, вы-, паривают до минимального объема и наносят на пластину окиси алюминия (прг меняют А1 0 с флюоресцентным индикатором при 254 нм, плас- тины 20x20 см, толщина слоя OjS мм), тех проводят двукратно в системах растворите.)ей: хлороформ - этилацетат (:) и бензол этанол (9,5: 0,5). Предлагаемые условия ТСХ на А1 О .позволяют эффективно разделить исследуемые гшлярные стероиды, Лока- . лиэацию стероидов на пластине определяют и их элюцию проводят как описано для алополярных стероидов, Да1Н1ььм методом определя.ют малополярные и полярные стероиды (кроме .д -андростадиен-1/Р -ол-З-он, который следует определять ПКХ-методом) , 11олуче П1ый на колечной стар.,ии очистки сухой остаток, соответстную ций одному из исследуегфгк стероидов, растворяют в 0,3 мл 9б%- , ного этанола и добавляют 1,5 мл реагента: 96%-ный этанол - концентрированная серная кислота (1:9). Смесь перемешивают , прогревают 8 мин при 80 5 охла кдают на ледяной бане и добав;шют 1 мл этанола. Смесь тщательно перемешивают и через 20 мин (выдерживают в темноте при комнатной температуре) измеряют флюоресценцию при А 520 «м,g., им. ПКХ (злектр9птый захват) метод количественного измерения. Метод может быть использован для количественного измерения малополяр.3 ных стероидов. Для получения фторпроизводных сухой остаток, соответствующий каждо из исследуемых стероидов, растворяют в 0,5 мл бензола и добавляют 2-3 капли гептафтормасляногсГ ангидрида. Смесь прогревают 50 мин при 70° и высушивают под струей азота. При фторировании от каждого из исследуемых стероийов ролучают 3- или I7-монофторпроизводные и 3,I7-дигептафторбути.раты. ГЖХ-анализ фторпроизводных стероидов проводят с использованием в качестве жидкой фазы 3% OV-t, нанесенной на хроматон N-AW DMCS; при меняют стеклянные колонки размером. ;1,5 н, температура колонки 200, испарителя 240, детектора 250С, газноситель - азот 40 мл/мин. Tims-iMHbie результаты ПКХ-аналиэа на примере фторпроизБодных и -андростадиен-Г/ -ол 3-он приведены на чертеже ПКХ (электронный захват)-анализ сте роидов позволяет выявить 0,00.02 вещества в пробе. Пример 1. Опыт проведен на откормочньк бычках черно-пестрой породы в возрасте одного года, вьфа щенных в условиях промьпаленного , ком17.лекса. Животные получали корм ВВОЛЮ. 67% питательности рациона составляли концентрированные корма .и 33% сенаж. Животным подкожно в область корня уха имплантировали 1 7oi -метил- Л андрост.адиен 1 7р -ол-З-он (метандростенолои) в дозах 130 и 70 мг за 1 и 2 мес до забоя. После убоя животных проводили rHrneHHjecKHft анализ мяса и субпродуктов с применением предлагаемого метода определения остаточных . честв биологически активных стероидов андростатювого ряда. Аналогичные исследования стероидов проводили в сьгаоротке кропи испытуемых животных полученной в разные сроки после имплантации препарата. В биопробах тканей (мясо, печень, жировая ткань) и сьшоротки крови выявлены следующие биологически а«: ивные стероиды:. I 7е -метил-Л -андроетен-1 7р-ол 3-он, 1 Ы-мeтил-5ei-aдpocтaн-l 7 -ол-З-он; I lfot-метил-дИ -андростадиен-6/J, 17 -диол-З-он, 1 7о(.метш1-Д -андростан- 7 -ол-3-он. Суммарное их содержание при-, в.едено ниже. 24 Образцы Суммарное содержатканей ние биологически бычков актив1{ьтх стероидов мкг/кг ткани Печень То же Печень То же -7 7 ,0 11р41веденные величины биологически активных стеровдов группы андрогенов в продуктах животноводства, полученных в условиях стимуляции бьпков 130 мг метандростенолона, превышают принятые в нашей стране н за- рубежом гигиенические регламенты содержания соединений данной группы. Вместе с тем, при имплантации бычкам метандростенолона в дозе 70 мг остаточные количества биологически активных стероидов в продуктах животноводства были существенно ниже. Пример 2. Баранчикам подкожно в область корня уха был имплантирован меченый препарат в дозе 50 мг. Бнопробы тканей и биологи™ ческих жидкостей были получены через 1,2 и 3 мес после имплантации. Кроме того, поставлен допопнительньй эксперимент на собаках по введению меченого метандростенолона. В биопробах от животных (печени, мьшц, слизистой кишечника биологических жидкостей) выявлены следующие биологически активные стероидные соединения группы андрогенов: 1 7о -метил-А -андростен-1 7р-ол-3-он; 1 7о1-метнл-5о1-андростан- 7)5-ол-3-он, 17о4.-метил- u-андростадиен-б, I 7 -диол-3-он, 17с -метил-й -андростен- Пр, 1 7;9-диол-3-он. Суммарное содержание названных тероидов в образцах от баранчиков, тимулированных в течение месяца, оставляли в среднем 13,4 мкг/кг (печень) 4,6 мкг/кг (мьшцы), ,8 мкг/кг (слизистая кишечника). риведенные величины содержания стеоидов в печени превышают допустимые ровни содержания биологически активых андрогенов в продуктах животноодства. Вместе с тем по сравнению с приведенными данными остаточные количества стероидов в печени живот ных, стимулированных в течение 2 и 3 мес были соответственно в 1,5и 2 раза ниже. В ткани мьппц через 2-3.мес после имплантации стероиды выявлены не были. Пример 3. Проведены опыты на 2 кроликах, которым был имплантирован А андростадиен-ол-1 7 -он-3 (по 10 мг препарата). Убой животных проводили через 20 и АО дней после имплантации. Исследование остаточных количеств пре парата проводился в тканях печени, почек, мьппц, жире, биологических жидкостях. В этих опытах исследовано также влияние препарата на горм нальный статус животных. В таблице приведены остаточные количества биологически активных стероидов в съедобных тканях живот ных . Как показано в таблице, остаточ ные количества биологически активн CTepoJWOB выявлены лишь через 20 дней после имплантации. Через 40 дней исследуемые соединения в съед ных тканях обнарулсены не были. Уро ни тестостерона, прогестерона, 11-оксшсортикостероидоп, альдостерона, тироксина, инсулина в сыворотке крови до имплантащ1и и через АО дней после имплантации существенно не отл1-гчались, Полученные да ные соответствуют гигиеническим тр бованиям и регламентам. . Ф о ф м у л а изобретени Способ определения стероидных гормонов в биологических объектах. 4 б клчающий экстракцию и биохимичесий анализ стимуляторов роста группы андрогенов, отличаюшийс я тем, что, с целью повышения точности , чувствительности и специфичности способа, а также одновременного анализа в них метилтестостерона, 19-нортестостерона, тренболона, -андррстадиен- 7р-ол-3-оиа, пр-оксиметилтйстостерона, 6р -оксиметандростенолона, д -андростадиен-Пр, 17 -диол-З-она, 17е --метш1-Зо -дигидротестостерона, водный гомогенат биоматериала экстрагируют смесью эфир, метилеихлорид в соотношении 11, экстракт наносят на колонку силикагеля, промывают хлоро-г формой, далее через колонку пропускают 0,5%-ный раствор метанола в хлороформе, и собирают фракцию малополярных стероидов, затем колонку элюируют 15%.-ньм раствором метанола в хлороформе н собирают фракцию полярных стероидов, далее фракцию малополярйых стероидов разделяют с помощью метода тонкослойной хроматографии на флоризеле, при этом идентифицирует 19-нортестостерои, тренболон, -андростадиен- 7 -ол-3-он метилтестостерон и 17о1-м9тйл-5о/-дигидротестостерон, а фракцию полярных стероидов разделяют метр- , дом тонкослойной хроматографии на окиси алюминия, при этом идентифицируют 1 1В-оксиметилтестостерои, 1 jt 6р-оксиметандростенолон,д - -яилпо-андррстадиен-11/J, 1 7 -диол 3-он, а количественное определение каждого из гормонов проводят флюориметрически или с помощью метода электроннозахьатной газожи,цкостной хроматографии .


Изобретение относится к биохимии, в частности к способам определения стероидных гормонов. Цель изобретения -. повьппение точности, чувствительности, специфичности способа, а также возможность одновременного определения в пробе нескольких стимуляторов роста группы андрогенов. Образцы тканей животных гомогенизируют в смесителе с пятикратным объемом 0,14 М раствора NaCl. Затем в гомогенат добавляют 2,5 объема смеси растворителей: эфир - метилеихлорид

| Ficat P., Arlet J | |||
| Coxopathles inchemiques | |||
| Rev.Chir.Orthop., 1972 | |||
| Способ окисления боковых цепей ароматических углеводородов и их производных в кислоты и альдегиды | 1921 |
|
SU58A1 |
Авторы
Даты
1986-11-30—Публикация
1984-07-31—Подача