Изобретение относится к химии фос- форорганических соединений с С-Р связью, а именно к усовертен ствоваино- му спйсобу получения р-нитроалкил- фосфорильных соединений общей лы .
P-CH-CH NO
i О R(I)
таток выдерживают 0,5 ч на открытом воздухе, затем перегоняют в вакууме. Выделяют 18,8 г (89,0%) 0,0-диметил- Ы-этил-р-нитроэтилфосфината с Т.кип. 5 (1,5 мм) n j 1-,4490, df 1,2250, Найдено, %: С 34,10, Н 6,70, N 6,72, Р 14,60, . Вычислено, %: С 34,12, Н 6,64, N 6,64, Р 14,69. ИКС (NaCl, см ): 1254 Ш (), 1032, 1060 (РО-С), 1380, 1562 (NOj). ПМР (CCl4,5 , м.д. J, Гц): &(ССН) 1,07/. J (Ш-0 6.6/, (CF) 1, (РН) 17.8/, & (Н„) 2,65/2 J (РИ;) 21,8, J (НССЫ) 6.2/, О (ОСН) честве полупродуктов фосфорорг.аничес- 15 3.74/ J (РН) 10,7/. ЯМР Р (м.д.):
5р 30.
РримерЗ. К раствору 1,38 г (0,01 моль) диэтилфосфита, 0,87 г (0,01 моль) 1-нитро-1-пропена и 1,09 г (0,01 моль) триметилхлорси- лана в 10 мл диэт1-шового эфира при перемешивании прикапывают 1,0 г (0,0 моль) тризтиламина и добавляют 5 мл воды, осадок отфильтровыгде R - алкил, алкоксил, фенил;
R -.алкоксил или фенил;
R - водород или алкил, которые могут найти применение в какого синтеза.
Цель изобретения - упроп ение процесса и повышение выхода целевых продуктов.
Пример 1.К раствору 11 ,0 г (0,1 моль) диметилфосфита, 8,7 г (0,1 моль) 1-нитро-1-пропена и
10.8г (0,1 моль) триметштхлорсила- на в 70, мл бензола при перемешивании и 0°С прикапывают 10,1 г (0,1 моль) триэтиламина. После добавления всего количества перемешивают еще полчаса, добавляют 15 мл воды до полного растворения хлоргидрата триэтиламина. Отделяют верхний бензольный раствор, сушат сульфатом натрия, бензол отгоняют. Перегонкой в вакууме остатка выделяют
16.9г (85,8%) 0,0-диметил-оС-метил- -р-нитроэтилфосфоната с т.кип. 80- 81° (0,05 мм), п р° 1,4476, 1,2640. Найдено, %: С 30,40,
Н 5,98, N 7,р5, Р 15,80. . Вычислено, %: С 30,46, Н 6,09, N 7,11, Р 15,74. ИКС (NaCl, см ): 1256 (), 1030, 1062 (РО-С), 1382, 1565 (N0).
ПМР (СС14 , S , м.д. J, Гц): 8 (Ы- -СН,) 1,29/ J (РН) 17,8/, S (Н) 2, (РН) 21,5, Ъ (НССНд,) 7,1/JnOCHj) 3,79/ J (РН) 10.6/. ЯМР Р (м.д.) Ь 30. Лит. данные Т.кип. 80-814. (0,05 мм) rf° 1,4473,
20
25
вают, эфир удаляют в вакууме, осj7.0
1,2635.
таток 0,5 ч выдерживают на открытом воздухе. Выделяют 2,04 г (90,5%) 0,0-диэтил-йС-метил-р-нитроэтилфос- фоната с т,кип. 82-83°С (0,5 мм) 30 Пд° 1,4412, df 1,1581. Найдено, %: С 37,38,.. Н 7,19, N 6,50, Р 13,70 C,H|tNOc.P. Вычислено, %: С 37,33, Н 7, lb N 6,22, Р 13,78. . I
Пример 4. К раствору 14,2 г
35 (0,1 моль) О- -хлорэтилметилфосфо- нита, 8,7 г (0,1 моль) 1-нитро-1- -пропена и 10,8 г (0,1 моль) триме- тилхлорсилана в 100 мл диэтилового эфира при перемешивании и 20 С прй40 капывают 10,1 г (0.1 моль) триэтиламина. Добавляют 15 мл воды, отделяют эфирньш раствор, промывают во- дои, сушат сульфатом натрия, эфир удаляют в вакууме 0,1 мм до посто
45 явного веса. Получают 23,0 г () О-р-хлорэтилметил-о -метил- -нитро- этилфосфината в В1зде вязкой, неперегоняющейся жидкости с Пр 1,4850. Найдено, %: С 31,00, Н 5,75, N 5,90,
50 Р 13,78. (;gK,,. Вычислено, %: С 31,37, Н 5,66, N 6,10, Р 13,51. Данные ЯМР Р: В.р 58 м.д.
Пример2. К раствору 11,0 г (0,1 моль) диметилфосфита, 10,1 г (0,1 моль) 1-нитро-1-бутена и 10,8 г (0,1 моль) трим етилхлорсилана в 60 мл диоксана при перемешивании и 20 С прикапывают 10,1 г (0,1 моль) триэтиламина и добавляют 15 мл воды. После завершения реакции осадок отфильтровывают, диоксан отгоняют, осРримерЗ. К раствору 1,38 (0,01 моль) диэтилфосфита, 0,87 г (0,01 моль) 1-нитро-1-пропена и 1,09 г (0,01 моль) триметилхлорси- лана в 10 мл диэт1-шового эфира при перемешивании прикапывают 1,0 г (0,0 моль) тризтиламина и добавля ют 5 мл воды, осадок отфильтровы5
вают, эфир удаляют в вакууме, остаток 0,5 ч выдерживают на открытом воздухе. Выделяют 2,04 г (90,5%) 0,0-диэтил-йС-метил-р-нитроэтилфос- фоната с т,кип. 82-83°С (0,5 мм) 0 Пд° 1,4412, df 1,1581. Найдено, %: С 37,38,.. Н 7,19, N 6,50, Р 13,70 C,H|tNOc.P. Вычислено, %: С 37,33, Н 7, lb N 6,22, Р 13,78. . I
Пример 4. К раствору 14,2 г
5 (0,1 моль) О- -хлорэтилметилфосфо- нита, 8,7 г (0,1 моль) 1-нитро-1- -пропена и 10,8 г (0,1 моль) триме- тилхлорсилана в 100 мл диэтилового эфира при перемешивании и 20 С прй0 капывают 10,1 г (0.1 моль) триэтиламина. Добавляют 15 мл воды, отделяют эфирньш раствор, промывают во- дои, сушат сульфатом натрия, эфир удаляют в вакууме 0,1 мм до посто
5 явного веса. Получают 23,0 г () О-р-хлорэтилметил-о -метил- -нитро- этилфосфината в В1зде вязкой, неперегоняющейся жидкости с Пр 1,4850. Найдено, %: С 31,00, Н 5,75, N 5,90,
0 Р 13,78. (;gK,,. Вычислено, %: С 31,37, Н 5,66, N 6,10, Р 13,51. Данные ЯМР Р: В.р 58 м.д.
Пример5. К раствору 1,25 г .(0,01 моль) 0-метилфенилфосфонита,
5 г (0,01 моль) 1-нитро-1-бутена и 1,09 г (0,01 моль) триметилхлорси- лана в 10 мл диэтилового эфира при перемешивании прикапывают 1,0 г (0,01 моль) триэтиламина. Добавляют
5 мл воды, после растворения осадка вводят дополнительно 20 мл эфира, эфирный раствор отделяют, его промывают водой, сушат сульфатом натрия, эфир удаляют в вакууме 0,1 мм до постоянного веса. Получают 2,2 г (98,5%) 0-метилфенил-с{-этил-р-нит- роэтилфосфината в виде вязкой, неперегоняющейся жидкости с ,5265. Найдено, %: С 51,39, Н 6,15, N5,20, Р 12,20. C,,H,5N04P.. Вычислено, %: С 51,36, .Н 6,23, N 5,45, Р 12,06. Р: 8р 43 м.д.
Примерб. К раствору 2,0 г (0,01 моль) дифенилфосфинита, 0,87 г (0,01 моль) 1-нитро-1-пропена и 1,09 г (0,01 моль)8 триметилхлорси- лана в 15 мл диэтилового эфира при перемешивании и 20°С прикапывают 1,0 г (0,01 моль) триэтиламина. Добавляют 5 мл воды, после растворения осадка вводят дополнительно 20 мл эфира, эфирньш раствор отделяют, промывают водой, сушат сульфатом натрия, эфир удаляют в вакууме 0,1 мм. Получают 2,7 г (93,4%) ди- фенил-о1-метил-| -нитроэтилфосфинокси- да с т.пл. 128-129 С (перекристаллизация из смеси бензола и гексана), Найдено, %: С 66,08, Н 5,68, N 4,97, Р 10,67. CijHt NOjP. Вычислено, %: С 62,29, Н 5,54, Ы 4,84, Р 10,76.
Составитель Л.Карунина Редактор И.Сегляник Техред В.Кадар Корректор А.Ильин
Заказ 344/26 . Тираж 348 . Подписное ВНИШШ Государственного комитета СССР
по делам изобретений и открытий 113035, Москва, Ж-35, Раушская наб., д. 4/5
Производственно-полиграфическое предприятие, г. Ужгород,ул. Проектная, 4
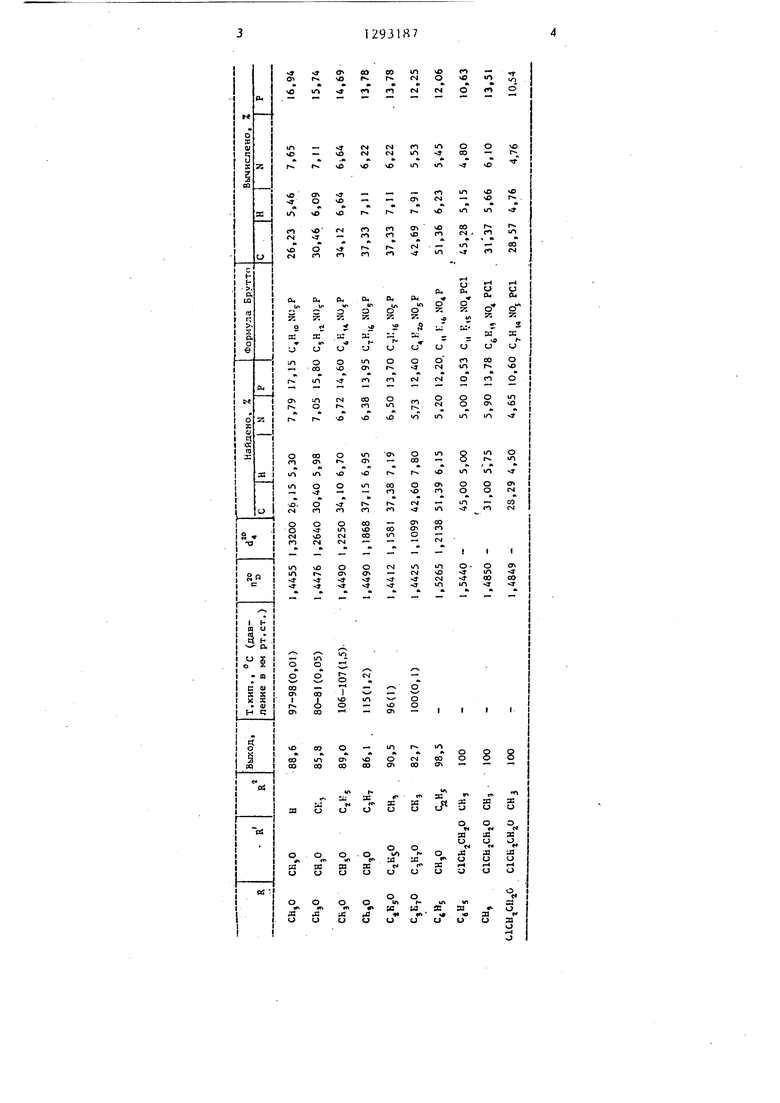
Аналогично получают другие -нит- роалкилфосфорильные соединения, представленные в таблице.
Формула изобретения
Способ получения /3-н 1троалкнлфос- форильных соединений общей формулы
R
Лр-сн-си ш
1/ п I
О Я
R
где R - алкил, алкоксил, фенил; R - алкоксил или фенил; К - водород или алкил, взаимодействием гидрофосфорильного
производного с 1-нитро-1-алкеном, отличающийся тем, что, с целью упрощения процесса и по- вьшгения выхода целевых продуктов, процесс ведут путем добавления триметилхлорсилана в раствор гидрофосфорильного сЬединения и 1-нитро-1- -алкена в апротонном растворителе, обработкой этой смеси триэтиламином при эквимольном соотношений всех
реагентов и температу11е 0-20 С, с последующим добавлением в образующуюся реакционную смесь воды.

Изобретение относится к химии фосфорорганических соединений с С-Р-связью, а именно к нолучению /З-нитроалкилфосфорильных соединений общей формулы RR P(0)CHR -CH2NO(I), где R - алкил, алкоксил, фенил, R - -алкоксил или фенил, R - водород или алкил, которые могут найти применение в качестве полупродуктов фосфорорганического синтеза. Соединения формулы I получают введением в раствор гидрофосфорильного соединения и 1-нитро-1-алкена в апротон- нЪм растворителе триметилхлорсилана, обработкой этой смеси триэтиламином при эквимольном соотношении реагентов и температуре 0-20 С с последующим добавлением в образующуюся реакционную смесь воды. Выход продуктов 82,7-100%. 1 табл. с (Л

| Гареев РоД | |||
| и др | |||
| О новом методе синтеза |Ь-нитроалкилфосфоно- вых кислот | |||
| - ЖОХ, 1975, 45, № 4, с | |||
| Реактивная катушка | 1924 |
|
SU944A1 |
| Баранов Г„М | |||
| и др | |||
| Синтез, свойства и строение нитро- и аминоал- кил (алкен)фосфонатов и их производ- нык | |||
| В сб | |||
| Химия и применение фрс- форорганических соединений | |||
| Труды IV конф | |||
| М.: Наука, 1972, с | |||
| Приспособление для нагрузки тендеров дровами | 1920 |
|
SU228A1 |
Авторы
Даты
1987-02-28—Публикация
1985-05-20—Подача