Изобретение относится к микробиологии, и касается получения биологически активных веществ.
Цель изобретения - разработка способа получения новых биологически активных соединений, обладающих высокой антибактериальной активностью in vivo в отношении грамположитель- ной и грамотрицательной микрофлоры.
Пример, Streptomyces rochei NRRL 3533 выращивают в среде,, содержащей, г/л: глюкоза 10, Difco пентон 4, Difco дрожжевой экстракт 4, MgSO
«7Н,0 0,5; 2; 4, в те- чение трех дней при 28 С-в круговой
качалке. Мицелий используют для ино- кулирования ферментационной среды указанного состава. Ферментацию проводят в течение 48 ч при в круговой качалке, В конце 48-го часа ин- тывают как описано выше, Метанольные кубирования добавляют U-57930 до ко- элюаты из колонки с Амберлитом ХАД-2 нечной концентрации 50 мг/л и ферментацию продолжают при 32 С, Спустя
Фракции 12-80 объединяют, концентрируют до водного раствора и сушат вымораживанием до получения препарата АДА-34,1 в количестве 12,22 г,
В другой серии опытов 6 л -ферментационного бульона, содержащего 2 г трансформированного U-57930, обрабасобирают, раствор, не концентрируя досуха, хроматографируют на Дауэкс-1 Для зтого приготавливают колонку с 300 мл Дауэкс-1 (Х-4) в ацетатной форме. Через колонку пропускают ме- танольньш раствор АДА-143В рН 8,2. Отработанный продукт собирают со скоростью 2,5 мл/мин - фракции 1-60 по 20 мл. Затем колонку промывают 1,5л воды (10 мл/мин; фракции 66- 108), После этого колонку злюируют 5%-ной уксусной кислотой (скорость 10 мл/мин, фракции 109-310).. Получа- 35 ют следующие группы фракций:
12 ч еще раз добавляют U-57930 до концентрации 150 мг/л. Соединение U 57930 имеет следующую структурную формулу:
X
Щ
Н-С-С1
I
CONH-CH НО/-0.
SCH.
он
Спустя еще 12 ч инкубирования концентрацию и-57930 повышают до 250 мг/л, Ферментацию продолжают при 32°С в течение 24 ч. Далее собирают фильтраты культур и определяют содержание сое- динения и-57930. Концентрация последнего не более 1 мг/л, 249 мг/л соединения транспортированы в бионеактивный материал.
Используемый штамм .Streptomyces rochei я вляется известньм и хранится в коллекции NRILL под номером 3533,
Берут 12 л ферментационного бульона, содержащего 3 г инактиварованного и-57930, фильтруют при рН 7,7, Содер- жащую мицелий лепешку промывают 1,2 л воды и удаляют. Прозрачный фильтрат и промьшки объединяют, устанавливают рН 6,0 и пропускают через колонку,
тывают как описано выше, Метанольные элюаты из колонки с Амберлитом ХАД-2
заполненную 600 мл Амберлита ХАД-2 со скоростью потока 40 мл/мин, Отра- ботанньм продукт тестируют на биоактивность до и после обработки щелочной фосфатазой и сливают. Колонку промьгеают 2 л воды. Водную промывку также проверяют на биоактивность перед и после обработки щелочной фосфатазой и сливают. Затем колонку элю- ируют смесью метанол - вода (70 : : 30 об./об.), Собирают фракции по 20 мл со скоростью 20 мл/мин.
Фракции 12-80 объединяют, концентрируют до водного раствора и сушат вымораживанием до получения препарата АДА-34,1 в количестве 12,22 г,
В другой серии опытов 6 л -ферментационного бульона, содержащего 2 г трансформированного U-57930, обрабатывают как описано выше, Метанольные элюаты из колонки с Амберлитом ХАД-2
собирают, раствор, не концентрируя досуха, хроматографируют на Дауэкс-1, Для зтого приготавливают колонку с 300 мл Дауэкс-1 (Х-4) в ацетатной форме. Через колонку пропускают ме- танольньш раствор АДА-143В рН 8,2. Отработанный продукт собирают со скоростью 2,5 мл/мин - фракции 1-60 по 20 мл. Затем колонку промывают 1,5л воды (10 мл/мин; фракции 66- 108), После этого колонку злюируют 5%-ной уксусной кислотой (скорость 10 мл/мин, фракции 109-310).. Получа- ют следующие группы фракций:
313
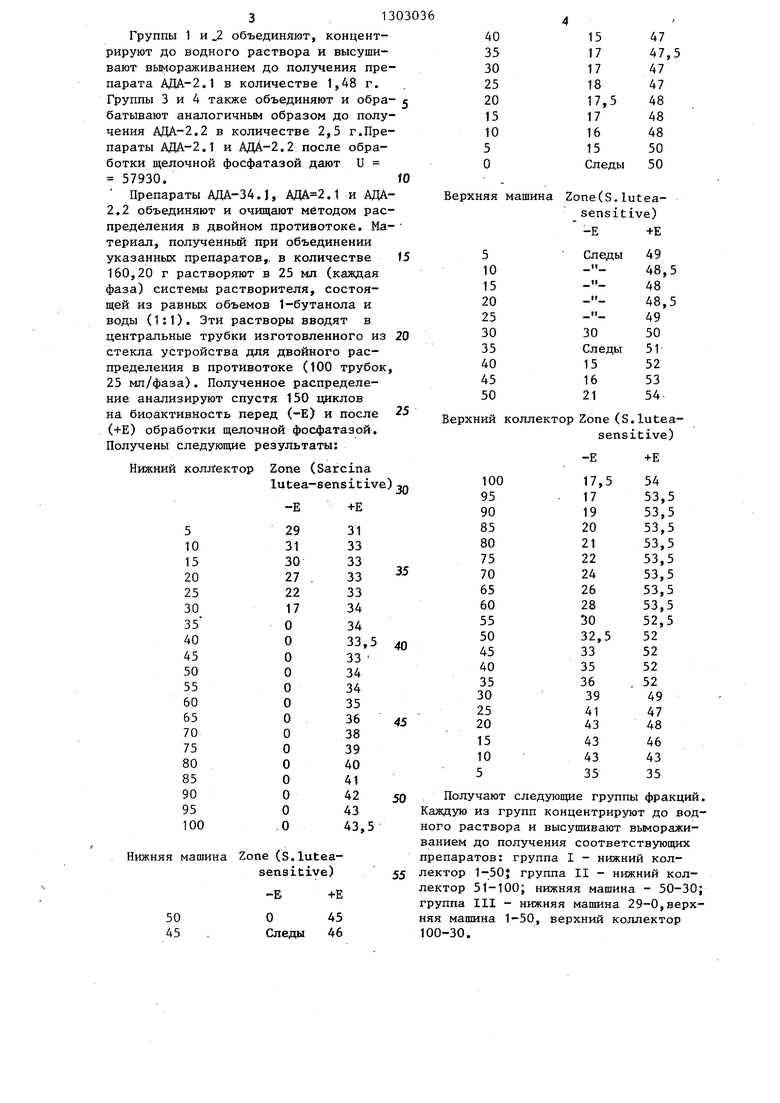
группы 1 и J. объединяют, концентрируют до водного раствора и высушивают вымораживанием до получения препарата АДА-2.1 в количестве 1,48 г. Группы 3 и 4 также объединяют и обра- батывают аналогичным образом до получения АДА-2,2 в количестве 2,5 г.Препараты АДА-2.1 и АДА-2.2 после обработки щелочной фосфатазой дают U 57930.
Препараты АДА-34.1, .1 и АДА- 2.2 объединяют и очищают методом распределения в двойном противотоке. Ма- териал, полученный при объединении указанных препаратов,, в количестве 160,20 г растворяют в 25 мл (каждая фаза) системы растворителя, состоящей из равных объемов 1-бутанола и воды (1:1). Эти растворы вводят в центральные трубки изготовленного из стекла устройства для двойного распределения в противотоке (100 трубок, 25 мл/фаза). Полученное распределение анализируют спустя 150 циклов на биоактивность перед (-Е) и после (+Е) обработки щелочной фосфатазой. Получены следующие результаты:
Нижний коллектор
Zone (Sarcina lutea-sensitive)
-Е
+Е
Нижняя машина Zone (S.lutea- sensitive)
-Е
О Следы
+Е
45 46
30
Получают следующие группы фракций. Каждую из групп концентрируют до водного раствора и высушивают вымораживанием до получения соответствующих препаратов: группа I - нижний коллектор 1-50} группа II - нижний коллектор 51-100; нижняя машина - 50-30; группа III - нижняя машина 29-0,верхняя машина 1-50, верхний коллектор 100-30.
5 1303036
Получают следующие группы препаратов: из первой группы - препарат АДА.-47.1. (9,78 г); из второй - пре парат АДА-47.2 (0,30 г) из третьей - препарт АДА-47.3 (5,29 г). Препараты 5 АДА-47,2 и АДА-47.3 объединяют и очищают с помощью хроматографии на ДЕАЕ-Сефадексе.
Перемешивают 300 г ДЕАЕ-Сефадекса А-25 в течение .1 ч с водой и в течение О 2 ч с 0,5 н, водной гидроокисью натрия. Ионообменник промывают водой до тех пор, пока рН не достигает значения -7,5. Затем материал перемешивают в течение 2 ч с 0,5 н.водной ук- 15 сусной кислотой, промьшают водой до нейтрального рН, выпивают в колонку и набивают под давлением 0,9 кг до постоянного веса. Затем колонку промывают 4 л воды, 8 л 0,1%-ного вод- 20 ного раствора трис-(оксиметил)ами- нометана (ТОАМ)и 3 л 0,03 М ТОАМ- ацетатного буфера рН 8,0 (получают при растворении 3,64 г ТОАМ в 800 мл воды, устанавливают рН 8,0 ледяной уксусной кислотой и затем доводят объем до 1 л). Исходные материалы - препараты АДА-47.,2 и АДА-47.3 в количестве приблизительно 5,50 г растворяют в 20 мл 0,03 М ТОАМ-ацетатного -30 буфера рН 8,О-и вводят в верхнюю часть колонны. Затем колонну элюиру- ют потоком вниз 0,3 М ТОАМ-ацетат- ным буфером рН 8,0. Собирают фракции 1-190 (20мл). В этот момент элюирова- 35 ние колонны начинают вести снизу вверх. Фракции A,B,C,D и Е (по 1 л каждая) собирают..
Тестирование на биоактивность, перед (Е) и после (+Е) обработки 40 щелочной фосфатазой дает следующие результаты:
Фракция
Zone (S.lutea- sensitive)
-Е
fE
3
6
9
12
15
18
21
24
27
30
33
36
лучают;
ппа
I
III
IV
I
VII
43,5
36
23,5
15
О
О
О
О
о о
15 17
21
23
23
23
22
21
21
22
21
22
23
22,5
22,5
22
22
20,5
20
44
36
23
16
О
О
О
О
о о 1620
26
27
30
29
24
23
24
26
35
44
51
54
52,5
52
54,5
56
56
Фракции
34-38
75-90 101-111 114-150 151-164 165-186
С, 1 лист
Объем, мл 280 (АДА-69В)
330 (АДА-69С) 180 (АДА-69В) 580 (АДА-69Е) 100 (АДА-69Г) 125 (АДА-69С) (АДА-69А)
Группа I (АДА-69В) содержит U- 57930 и ее сливают. Группа II (АДА- 69С) содержит неизвестный материал который дает U-57930 при обработке щелочной фосфатазой. УФ: нм.
Группа III (АДА-69Б) содержит U-57930- -цитидилат, и ее затем обрабатывают. УФ: 270 нм.. Группа IV (АДА-69Е) содержит U-57930-аденилат. УФ:Л,,ц 260 нм. Группа V (АДА-69Г) содержит смесь U-57930-аденилата, U-57930-ури- дилата и и 57930-г.уанилата. Группа VI (АДА-69С) содержит U-57930-гуани55
лат, и ее затем обрабатывают. УФ Дмакс 254, плечо на 275 нм. Группа VII
(АДА-69А) содержит смесь U-57930-rya- .нилата и U-57930-уридилата, затем этот раствор обрабатывают.
Группы III, IV и VI пропускают через колонки, содержащие Амберлит ХАД-2. Отработанный продукт сливают. Колонки промьшают водой,, а затем элю- ируют смесью метанол.- вода (70 : : 30 об./об.). Фракции анализируют (УФ) и тестируют на биоактивность перед и .после обработки щелочной фос- фатазой. Соответствзтощие фракции объеции .51-60 содержит и-57930-аденш1ат, фpaкци 62-73 (АДА-92.В) - U-57930- -уридилат, фракции 75-110 - U-57930- -гуанилат.
Подготавливают колонку из 50 мл Амберлита ХАД-2. Группу фракций АДА- 94В, содержащую U-57930-уридилат, про пускают через колонку со скоростью 2 мл/мин. Отработанный продукт слидиняют, концентрируют до водного рас- О вают. Колонку промьшают 200 мл воды.
20
твора и высушивают вымораживанием.
В табл. 1 приведены данные об использованном количестве Амберлита для каждой группы, количестве воды, которой осуществляют промывку, ме- танольного элюата и материала, кото- рьм получают.
Материал, полученный из группы III, носит название АДА-73.1, из группы 1У-АДА-74.1, из группы VI-AДA-75.1 Удаление ТОАМ-ацетатного буфера из группы V(AflA-69F) и группы VII (АДА-69А) с помощью хроматографии на Амберлите ХАД-2 осуществляют еле- 25 дующим образом.
Готовят колонку из 300 мл Амберлита ХАД-2. Группы V и VII, содержащие смесь и-57930-аденилата,и-57930- -уридилата д U-57930-гуанидилата, npo-jQ пускают через колонку. Отработанный продукт сливают. Колонку промывают 600 мл воды. Отработанный продукт сливают Колонку злюируют смесью метанол - вода (70:30). Фракции, содержащие биоактивный материал, после обработки щелочной фосфатазой объединяют, 300 мл смеси концентрируют до водного раствора и высушивают вымораживанием, в результате чего полу- .,. чают препарат АДА-71.1 (670 мг).
Берут 600 мл ДЕАЕ-Сефадекса в ацетатной форме, промьшают 0,ОЗМ ТОАМ- ацетатом рН 8,0, набивают в стеклянную колонку (внешний диаметр 4,5 см, высота 40 см) под гидростатическим давлением.
Препарат АДА-71.1. растворяют в Ю мл 0,03 М ТОАМ-ацетатного буфера рН 8,0 и вводят в верхнюю часть колонки. Колонку элюируют: 0,ОЗМ ТОАМ- ацетатом, рН 8,0 (фракции 1-79);0,12М ТОАМ-ацетатом, рН 8,0 (фракции 80- 395); 0,25М ТОАМ-ацетатом, рН §,0
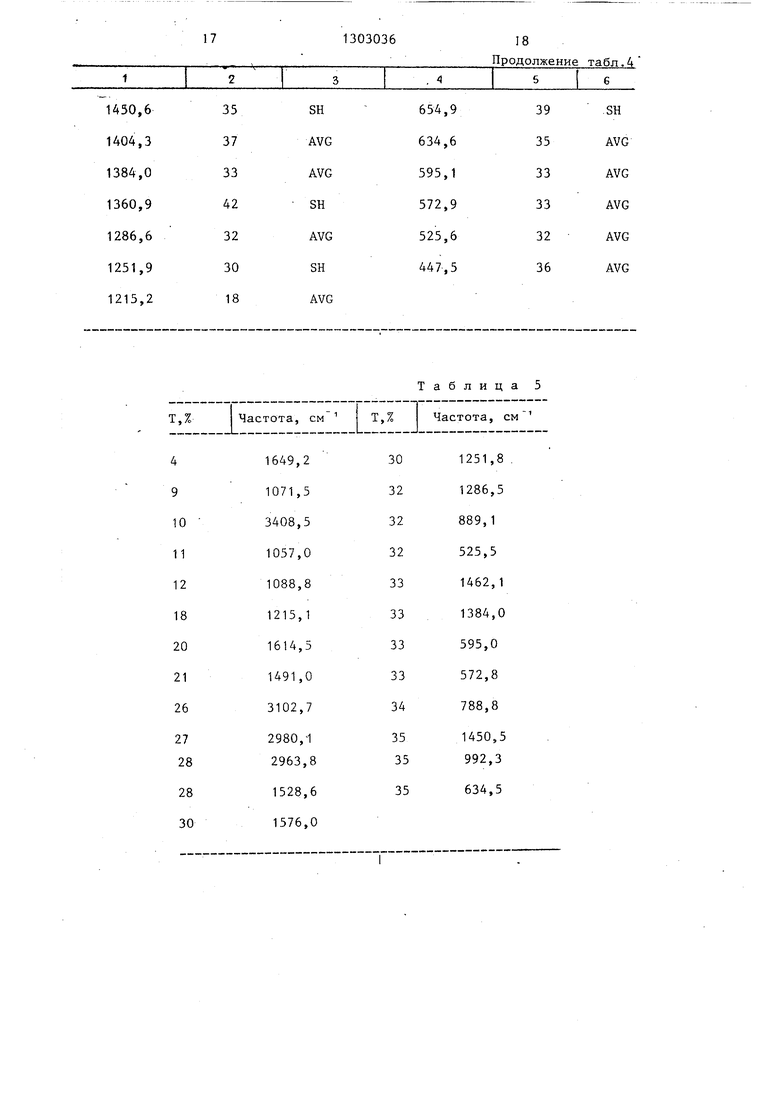
Промывки сливают. Колонку элюируют смесью метанол - вода (70:30 об./об.). Фракции,содержащие (по данным УФ-спек- троскопии) U-57930-уридилат, объеди- J5 няют (200 мл), концентрируют до вод- ного раствора и высушивают вымораживанием до получения АДА-95.1 (60 мг). Характеристики U-57930 3-(5 -цити- дилата) - ИК-спектры поглощения (в нуджоле и КВг) и наиболее сильные пики приведены в табл. 2-5.
Образец - эмульсия в минеральном масле. Т„дкс 87% (1848,0 ), при 3800 плотность 0,964 см /рт.
Образец - таблетка КВг.. Т,а 100%. (403.1); при 400 см Т 78%,- плотность 0,964 .
УФ спектр поглощения,мопс (а): в воде при. рН 2,0 279 нм (6,5); рН 7,0 270-нм (9,9); рН 11,0 271 нм (9,6).
.jNjO, S., (Мол.м.715). Рассчитано,%: С 43,64, Н 6,01; N 9,79; О 26,88; S 4,47, С1 4,89; Р 4,33
Cct. М07°(С, 0,854, вода). Хорошо растворяется в воде, метаноле и этаноле. Мало растворим в ацетоне и других кетонах, этилацетате и других сложных: эфидах, хлороформе, метиленхлориде. Нерастворим в насыщенных углеводородах. Антибактериальная активность U-57930 3-(5 -ци- тидилат) неактивен in vitro. Однако обработка щелочной фосфатазой или . фосфодиэстеразой I приводит к получению и-57930, которьш высокоактивен против различных грамположительных микроорганизмов как in vitro, так и in vivoo Т.пл. 205-207 С(с разложением) о
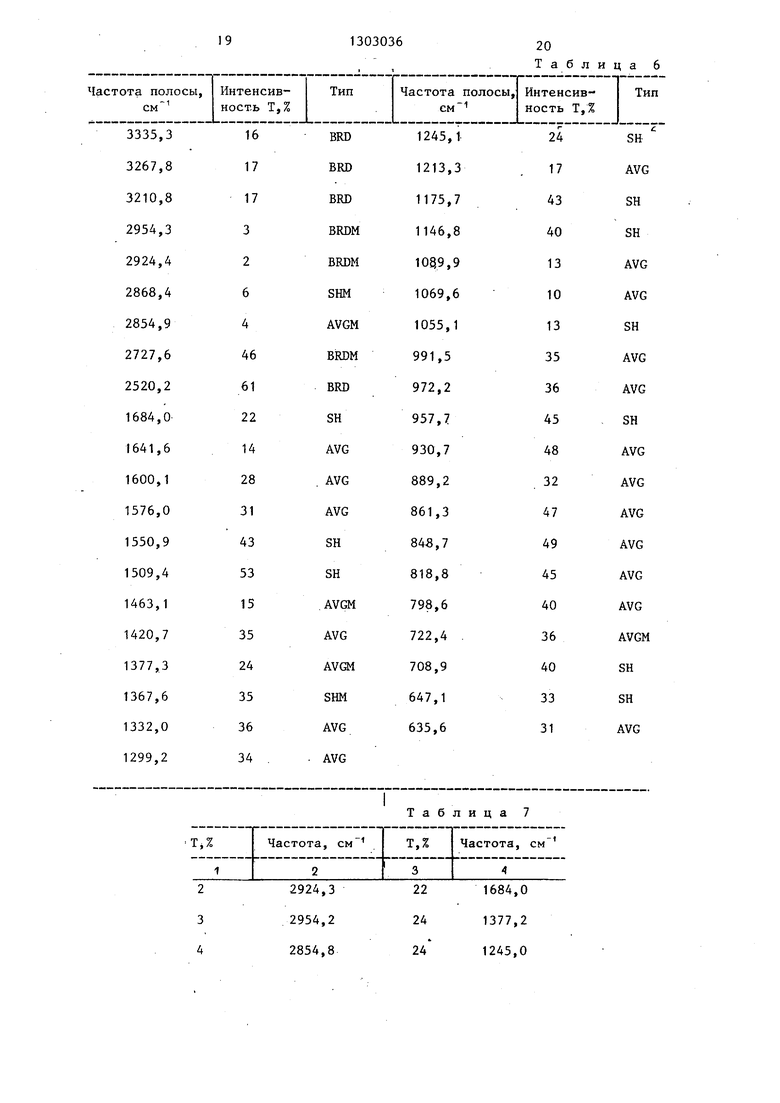
Характеристики U-57930 3-(5-адени- лата) - ИК-спектр поглощения(в нуджоле и КВг) и наиболее сильные пики
35
50
(фракции 396-750).55
Фракции по 20 мл собирают, анали- приведены в табл. 6-9. зируют с помощью УФ-спектроскопии и Образец - эмульсия в минеральном тестируют на биоактивность до и после масле. 85% (1864,4); при обработки щелочной фосфатазой. Фрак- 3800 плотность О, 964 см Урт.
ции .51-60 содержит и-57930-аденш1ат, фpaкци 62-73 (АДА-92.В) - U-57930- -уридилат, фракции 75-110 - U-57930- -гуанилат.
Подготавливают колонку из 50 мл Амберлита ХАД-2. Группу фракций АДА- 94В, содержащую U-57930-уридилат, пропускают через колонку со скоростью 2 мл/мин. Отработанный продукт сли0
5
jQ .,.
Промывки сливают. Колонку элюируют смесью метанол - вода (70:30 об./об.). Фракции,содержащие (по данным УФ-спек- троскопии) U-57930-уридилат, объеди- 5 няют (200 мл), концентрируют до вод- ного раствора и высушивают вымораживанием до получения АДА-95.1 (60 мг). Характеристики U-57930 3-(5 -цити- дилата) - ИК-спектры поглощения (в нуджоле и КВг) и наиболее сильные пики приведены в табл. 2-5.
Образец - эмульсия в минеральном масле. Т„дкс 87% (1848,0 ), при 3800 плотность 0,964 см /рт.
Образец - таблетка КВг.. Т,а 100%. (403.1); при 400 см Т 78%,- плотность 0,964 .
УФ спектр поглощения,мопс (а): в воде при. рН 2,0 279 нм (6,5); рН 7,0 270-нм (9,9); рН 11,0 271 нм (9,6).
.jNjO, S., (Мол.м.715). Рассчитано,%: С 43,64, Н 6,01; N 9,79; О 26,88; S 4,47, С1 4,89; Р 4,33
Cct. М07°(С, 0,854, вода). Хорошо растворяется в воде, метаноле и этаноле. Мало растворим в ацетоне и других кетонах, этилацетате и других сложных: эфидах, хлороформе, метиленхлориде. Нерастворим в насыщенных углеводородах. Антибактериальная активность U-57930 3-(5 -ци- тидилат) неактивен in vitro. Однако обработка щелочной фосфатазой или . фосфодиэстеразой I приводит к получению и-57930, которьш высокоактивен против различных грамположительных микроорганизмов как in vitro, так и in vivoo Т.пл. 205-207 С(с разложением) о
Характеристики U-57930 3-(5-адени- лата) - ИК-спектр поглощения(в нуджоле и КВг) и наиболее сильные пики
35
50
55
Образец таблетка КВч. (405,0); при 4000 см т 77%, плот- ность 0,964 см /рт.
УФ-спектр поглощения, Я 1, в воде при рН 2,0 258 нм (16,0), рН 7,0 261 нм (16,5); рН 11,0 261 нм (16,0)
N,0,0 SC1P Мол.м. 723).
Рассчитано,%: С 44,81 Н 5,94; N 13,55; О 22,13; S 4,41; Ct 4,84; Р 4,28.
Найдено,%: .N 12,87; S 5,39; CI 4,76; Р 3,83.
Ld.1 +94 (С, 0,887, вода).
Хорошо растворим в воде, метаноле и этаноле. Слабо растворим в ацетоне и других кетонах, этилацетате и других сложных эфирах, хлороформе и метиленхлориде. Нерастворим в насыщенных углеводородах.
.Антибактериальная активность. U- 57930 3-(5 -аденилат) неактивен in vitro. Однако после обработки щелочной фосфатазой или фосфодиэстеразой I получают и-57930, который обладает высокой активностью против различных грамположительных микроорганизмов как in vitro, так и in vivo. U-57930
20
25
Образец - эмульсия в минеральном масле. Т макс 97% (8762,6); при 3800 см Т 97% , плотность 0,964 см Урт. Образец - таблетка КВч. Т 97% (405,0); при 4000 см- Т 77%; плотность 0,964 .
УФ-спектр поглощения, (а): в воде при рН 2,0 256 нм (13,4); 280 нм (8,4), рН 7,0 254 нм (14,5); 273 нм (9,7);-рН 11,0 259 нм (12,6), 266 нм (12,4).
Найдено,%: N 13, 32; S 4,86, С1 4,49; Р 3,25.
.О,,
SC1P (мол.м.739). Рассчитано , %: С 43,84; Н 5,8Г
, ,,. , г О 23,27; S 4,33; С1 4,73; 3-(5 -аденилат) активен з.п vivo (.под-30 Р 4 19.
кожно, мышам) с CD порядка 0,62 (0,48-0,79) мг/кг против S.pyogenes. Т.пл. 203,5-205°С (с разложением). Характеристика U-57930 3-(5 -уриСыЗ
2 л
Р +97 0(0, вода, 0,855). Хорошо растворяется в воде, метаноле и этаноле. Плохо растворяется
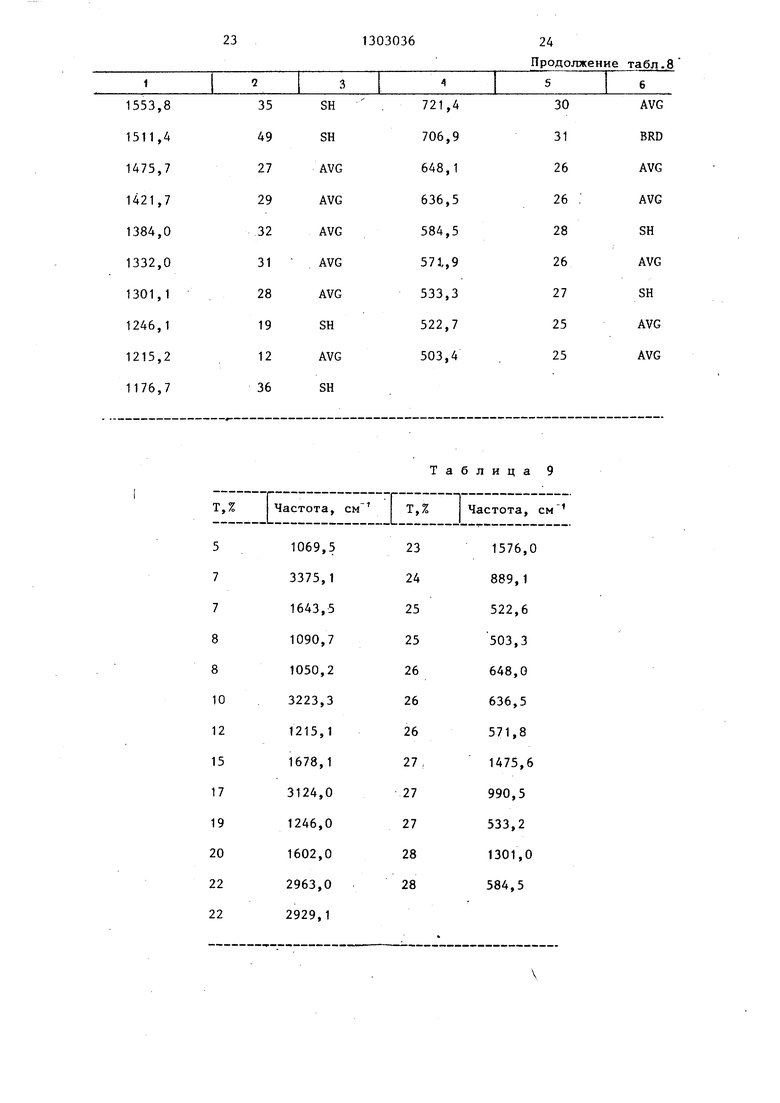
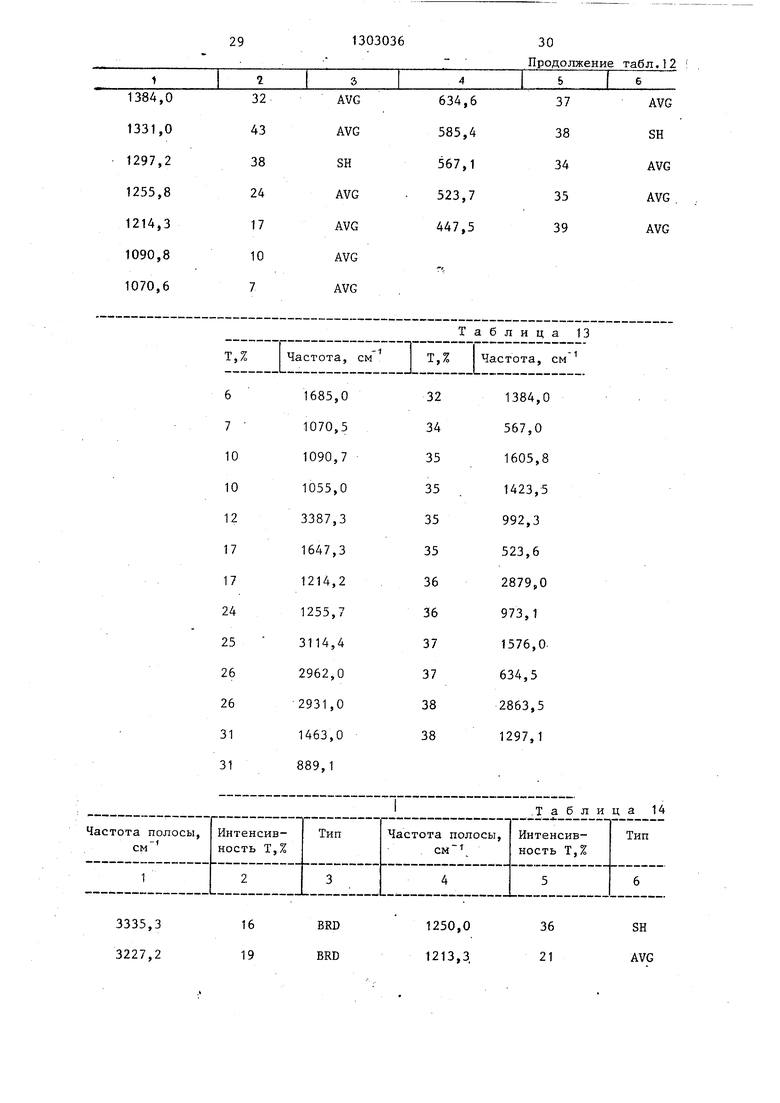
в ацетоне и других кетонах, этил- дилат) - полосы поглощения в ИК-спек- ацетате и других сложных эфирах, хло- тре (в нуджоле и КВг) и наиболее сильные пики приведены в табл. 10-13.
роформе и метиленхлориде. Нераствбрим в насьш1;енных углеводородах, Антибактериальная активность. U-57930 3-(5- -гуанилат) неактивен in vitro. ОднаОбразец - эмульсии в минеральном масле. Т.,., 86% (3764,5); при 3800 см
плотность 0,964 CM VpT.
Образец - таблетка КВг. Т 101% (405,0) ; при 4000 см , , плотность 0,964 см /рт.
УФ-спектр поглощения, X„акс (а): в воде при рН 2,0 261 нм (11,5); рН 7,0 262 нм (10,7); рН 11,0 262 нм (11,5).
(Мол.м.716).
Рассчитано,%: С 43,57; Н 5,86; N 7,82; О 29,05; S 4,46; С1 4,89; Р 4,33.
Cccjj° +105° (С, 0,94, вода).
Хорошо растворяется в воде, метаноле, этаноле. Плохо растворяется в ацетоне и. других кетонах, этил- ацетате и других сложных эфирах, хлороформе и метиленхлориде. Нераствори в насыщенных углеводородах.
5
0
5
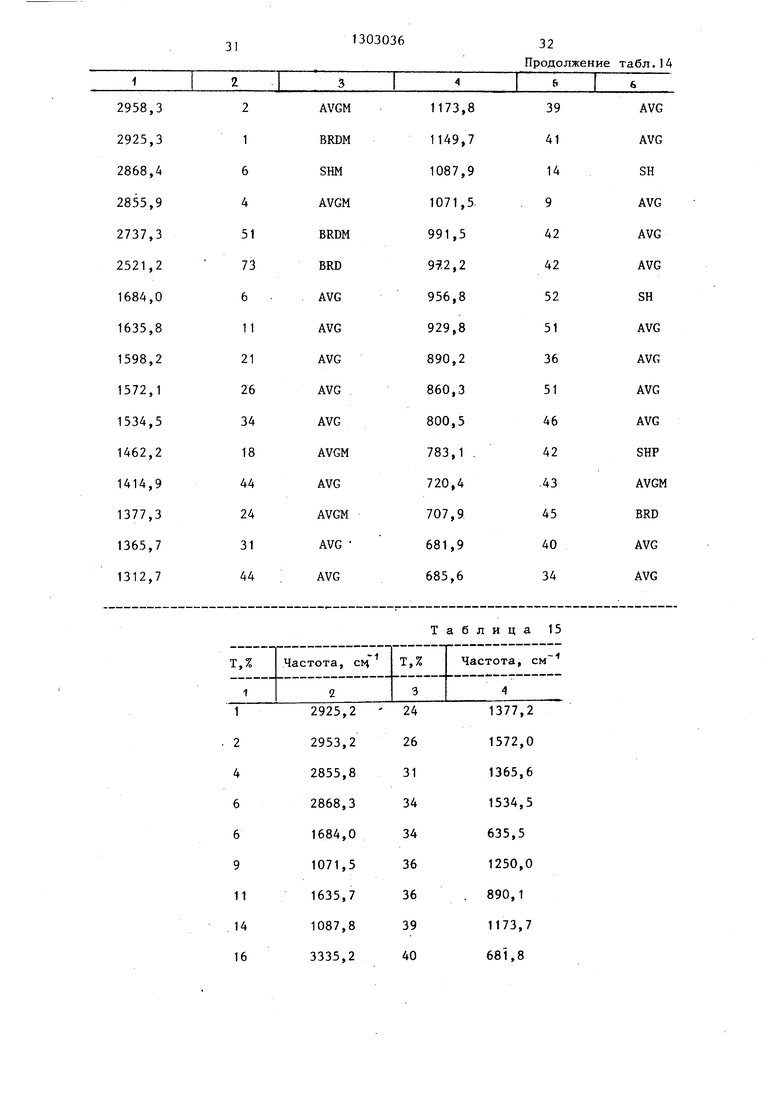
Антибактериальная активность. и-5793р 3-(5 -уридилат) неактивен in vitro. Однако после обработки щелочной фосфатазой или фосфодизсте- разой I получают U-57930, обладающий высокой активностью против различных грамположительных организмов как in vitro, так и in vivo. Т.пл. 202-203 0 (с разложением). Характеристики U-57930 3-(5 -гу- анилата) - полосы ИК-поглощения (нуд- жоль КВг); и наиболее сильные пики приведены в табл. 14-17.
Образец - эмульсия в минеральном масле. Т макс 97% (8762,6); при 3800 см Т 97% , плотность 0,964 см Урт. Образец - таблетка КВч. Т 97% (405,0); при 4000 см- Т 77%; плотность 0,964 .
УФ-спектр поглощения, (а): в воде при рН 2,0 256 нм (13,4); 280 нм (8,4), рН 7,0 254 нм (14,5); 273 нм (9,7);-рН 11,0 259 нм (12,6), 266 нм (12,4).
Найдено,%: N 13, 32; S 4,86, С1 4,49; Р 3,25.
.О,,
Рассчитано ,
СыЗ
2 л
Р +97 0(0, вода, 0,855). Хорошо растворяется в воде, метаноле и этаноле. Плохо растворяется
в ацетоне и других кетонах, этил- ацетате и других сложных эфирах, хло- роформе и метиленхлориде. Нераствбрим в насьш1;енных углеводородах, Антибактериальная активность. U-57930 3-(5- -гуанилат) неактивен in vitro. Одна40 ко после обработки щелочной фосфата- .зой или фосфодиэстеразой I получают и-57930, который обладает высокой активностью против различных грампо- ложительньк организмов как in vitro,
45 так и in vivo. Т.пл. 219-220 С (с .разложением).
Полученные вещества проявляют активность против различных грамположительных и грамотрицательных микроорганизмов, в связи с чем они могут использоваться в качестве дезинфеци- .рующих и лечебных средств. В частности, они активны в отношении Staphy- lococcus aureus, микоплазм, Pseudo- monas mirabilis. Streptococcus hemo- lyticus. В качестве антибактериальных агентов их используют в виде различных композиций.
Возможные формы и композиции антибактериальных средств.
Капсулы (1).
Готовят твердые желатиновые капсулы для орального приема, содержа- щие,г: и-57930 Е 250,- кукурузный крахмал 100} тальк 75; стеарат магния 25. Компоненты тщательно перемешивают и заполняют капсулы. Используют для систематического лечения взрослых больных путем орального приема через каждые 6 ч. Можно готовить капсулы с содержанием активного компонента 10; 25;50;100;500 мг вместо 250 г.
Капсулы (2).
Готовят желатиновые капсулы для орального применения, содержащие,г: соединение U-57930E 200; тетрациклина гидрохлорид 250; тальк 75, стеарат магния 25. Тетрациклин может быть заменен хлорамфениколом, окситетрациклином, хлортетрациклином, фумагил- лином, стрептомицином, дигидроново- биоцином или новобиоцином. Если вместо тетрациклина используют пенициллин G, то доза его составляет 250000 ёд. на капсулу.
Таблетки (3).
Берут 500 г соединения U-57930E, 125 г лактозы, 65 г кукурузного крах мала, 25 г стеарата магния, и 3 г легкого жидкого вазелина, тщательно смешивают до получения комков. Их размельчают, продаливая сквозь сито № 16.
3
Полученные гранулы прессуют в таблетки, в которых содержится 500 мг активного соединения.
Приведенные примеры использования рибонуклеотидов являются иллюстративными и не ограничивают возможности использования иных лекарственньк форм
Формула изобретения
Способ получения 3-(5 -рибонуклеотидов) общей формулы (I)
ОН,
с
Н-С-С1 CO JH-CH
HoJ-o
20
.
SCHj
он
где R - 5-рибонуклеотид, заключающийся в том, что штамм Strep- tomyces rochei NRRL 3533 культивируют в жидкой питательной среде, со- .держащей источники.углерода, азота и минеральные соли, с дробньм добавлением в процессе культивирования в культуральную жидкость соединения общей формулы (I), где R - водород, с последующим выделением целевого продукта.
Таблица 1
30
13
1303036
Примечание, Тип дан в локальной области пика: BRD - широкий;
AVG - средний; SHP - резкий; SH - плечо; М - возможно перекрывание с минеральным маслом.
Таблица 3
14
Продолжение табл.2
Табгица 4
35 37 33 42 32 30 18
SH
AVG
AVG
SH
AVG
SH
AVG
Т 7
1 ,/0
I
Частота, см
1649,2 1071,5 3408,5 1057,0 1088,8 1215,1 1614,5 1491,0 3102,7
2980,1 2963,8
1528,6 1576,0
39 35 33 33 32 36
SH
AVG AVG AVG AVG AVG
Таблица 5 T,%Частота, см
1251,8
1286,5
889,1
525,5
1462,1
1384,0
595,0
572,8
788,8
1450„5 992,3
634,5
Таблица
23
1303036
24 Продолжение табл.8
Таблица 9
25
1303036
26
Таблица 10
Таблица 12
Т,% Частота, см Т,% Частота,
1685,0 1070,5 1090,7 1055,0 3387,3 1647,3 1214,2 1255,7 3114,4 2962,0 2931,0 1463,0 889,1
16 19
BRD BRD
Частота,
Таблица 13
-1
см
1384,0
567,0
1605,8
1423,5
992,3
523,6
2879,0
973,1
1576,0
634,5
2863,5
1297,1
.Таблица 14
36
21
SH AVG
2
1
6
4
51
73
6
11
21
26
34
18
44
24
31
44
AVGM
BRDM
SHM
AVGM
BRDM
BED
AVG
AVG
AVG
AVG
AVG
AVGM
AVG
AVGM
AVG
AVG
1303036
32 Продолжение табл.14
39 41 14 9
42 42 52 51 36 51 46 42 .43 45 40 34
AVG
AVG
SH
AVG
AVG
AVG
SH
AVG
AVG
AVG
AVG
SHP
AVGM
BRD
AVG
AVG
Таблица 15
33
130303634
Продолжение табл.15
Редактор В. Петраш
Составитель Г. Смирнова
Техред Л.блейник Корректор Т. Колб
Заказ 1228/58 Тираж 500Подписное
ВНИИПИ Государственного комитета СССР
по делам изобретений и открытий 113035, Москва, Ж-33, Раушская наб, д. 4/5
Производственно-полиграфическое предприятие, г. Ужгород, ул. Проектная, 4











Изобретение относится к микробиологии и касается получения биологически активных веществ. Цель изобретения - разработка способа получения новых биологически активных соединений, обладающих высокой антибактериальной активностью. Штамм Streptomyces rochei NRRL 3533 вьфа- щивают в жидкой питательной среде.. Проводят ферментацию и инкубирование. Далее собирают фильтраты культур, выделяют целевые продукты. Полу- ченные вещества проявляют активность против грамположительных и грамотри- цательных микроорганизмов. Они могут использоваться в качестве дезинфеци- рующих и лечебных средств. 17 табл. а S (У) с со о со о со О5. о

| Патент США № 3671647, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1987-04-07—Публикация
1982-04-19—Подача