Изобретение отн.осится к органической химии, а именно к способу получения 1,7-диаз а-4,10,13-триоксацикло- пентадекана (диаза-15-краун-5) формулы
,
HR RH - Q
.А-л TsO
0 m,co3.cH,cN J«
y
Пример 1. В 3-горлую колбу, снабженную обратным холодильником, капельной воронкой и мешалкой помета щают 11,4 г (0,11 М) 1,5-диамино-З- оксапентана и 60 г (0,55 М) карбоната натрия в 200 мл абсолютного ацето- нитрила, К кипящей смеси в течение 3 ч прибавляют раствор 50,4 г (0,11 М) дитозилата триэтиленгликоля в 100 мл абсолютного ацетонитрила. После прибавления кипячение продолжают еще 3 ч. Смесь охлаждают, фильтру- ют,осадок отбрасывают, а ацетонитрил упаривают на ротационном испарителе. Кипячением с гексаном образующегося масла выделяют 7,0 г (29%) диаза-15- краун-5. Т.пл. 89°С. По литературным данным 89 - 90°С. Контроль чистоты получаемого продукта осуществляли JCX на готовых пластинах Silufoluv- 254,. элюент спирт-аммиак-ацетонитрил (5:1:1) с обнаружением нингидридом, R 0,38.
Вычислено, %: N 12,84. Найдено, %: N 12,91. Спектр ПМР,ч. на млн.: 7,15 (2Н, с, N Н); 3,60 (12 Н, т. ОСН); 2,75 (8 Н,- т. NCH).
Примеры 2-10 выполнялись аналогично примеру 1.
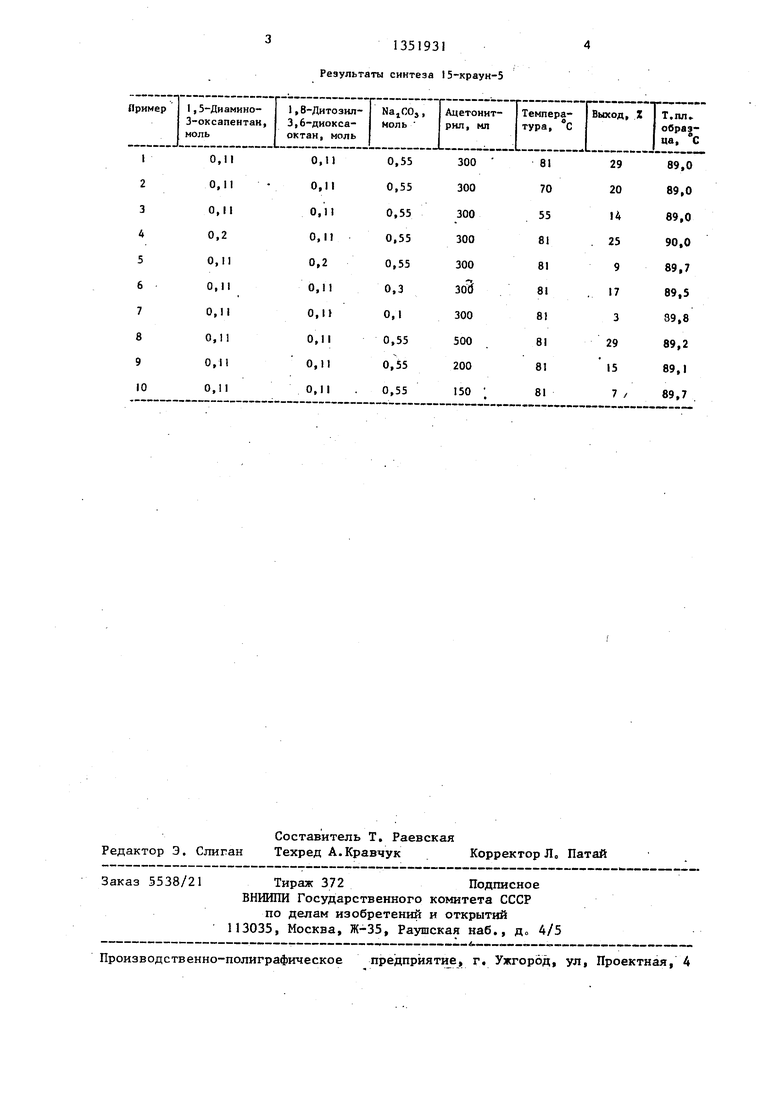
Сведения о режимах выполнения и результаты эксперимента приведены в таблице,
Пример 1 иллюстрнрует осуществление предлагаемого способа при оптимальных режимах температуры и мольных отношениях реагентов.
Примеры 2 и 3 иллюстрируют осу- ществление способа при температуре
который используется в органической . химии в качестве промежуточного соединения в синтезе различных криптан- дов и других.макроциклических систем 5 Целью изобретения являются упрощение технологии и ускорение процесса получения целевого продукта.
Синтез осуществляется по следующей схеме:
J«
y
ниже точки кипения ацетонитрила.
Примеры 5 - 7 иллюстрируют проведение способа при выходе за эквимо- лярное отношение 1,5-диамино-З-окса- пентана , 1,8-дитозил-3,6-диоксаокт а- на и малом количестве карбоната натрия .
Примеры 8-10 иллюстрируют осуществление предлагаемого способа при выходе за оптимальный объем растворителя (ацетонитрил).
Предлагаемый способ позволяет повысить выход целевого продукта в 1,7 раза (с 17 в прототипе до 29% в предлагаемом способе), сократить время проведения процесса в 8 раз (6ч в настоящем способе и 47 в известном) . Выделяемый продукт соответствует литературным константам и не требует дополнительной очистки методом
жидкостной колоночной-хроматограбзии.
.
Формула изобретения
Способ получения 1,7-диаза-4,10, 1 3-т риоксациклопентадекана взаимодействием 1,5-диамино-З-оксапентана с алкилирующим агентом при эквимоляр- ном соотношении реагентов в среде абсолютного ацетонитрила в присутствии карбоната натрия при температуре кипения растворителя, отличающийся тем, что, с целью упрощения технологии и ускорения процесса, в качестве алкилирующёго агента используют 3,6-диокса-1,8-дитозилоктан.
Результаты синтеза 15-краун-5
Редактор Э. Слиган
Составитель Т, Раевская
Техред А.Кравчук Корректор Л Патай
5538/21
Тираж 372Подписное
ВНИИПИ Государственного комитета СССР
по делам изобретений и открытий 113035, Москва, Ж-35, Раушская наб., д 4/5
Производственно-полиграфическое предприятие, г. Ужгород, ул. Проектная, 4
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ БИС(2-ГИДРОКСИФЕНИЛ)ОВОГО ЭФИРА ОЛИГОЭТИЛЕНГЛИКОЛЯ В ВИДЕ МОНОГИДРАТА | 2014 |
|
RU2564257C1 |
| 1,12-Диаза-2,5,8,11,15-пентаоксациклогептадекан и способ его получения | 1990 |
|
SU1726475A1 |
| Способ получения N-(I-пиперазинил)бутилглутаримидов | 1991 |
|
SU1836365A3 |
| СПОСОБ ПОЛУЧЕНИЯ СИММЕТРИЧНОГО И НЕСИММЕТРИЧНОГО ДИБЕНЗО-КРАУН-ЭФИРОВ | 2014 |
|
RU2564258C1 |
| Способ получения 20,24-динитро-2, 3, 11, 12-дибенз-1,4,7,10,13,16-гексаоксациклооктадека-2,11-диена и 20,25-динитро-2,3,11,12-дибенз-1,4,7,10,13,16-гексаоксациклооктадека-2,11-диена | 1987 |
|
SU1567583A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,5-БИС(2-ГИДРОКСИФЕНОКСИ)-3-ОКСАПЕНТАНА МОНОГИДРАТА | 2001 |
|
RU2203882C1 |
| Способ получения производных цис- или транс-диаминодибензоилдибензо-18-краун-6 | 1985 |
|
SU1313856A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,5-БИС(2-ГИДРОКСИФЕНОКСИ)-3-ОКСАПЕНТАНА МОНОГИДРАТА | 2012 |
|
RU2483055C1 |
| Способ получения двубромистого диаллилолова | 1985 |
|
SU1310399A1 |
| Способ получения 1,4,7-триметил-4,5,7,8-тетрагидро-6Н-имидазо-(4,5- @ )-1,4-диазепин-5,8-диона | 1989 |
|
SU1684283A1 |
Изобретение относится к гетероциклическим соединениям, в частности к получению 1,7-диаза-4,10,13-триок- сациклопентадекана (I), которьш используется в качестве промежуточного соединения в синтезе различных макро- циклических систем. Цель - упрощение технологии и ускорение процесса. Получение соединения 1 ведут из 1,5- диамина 3-оксапентана и 3,6-диокса- Г, 8-дитозилоктана в качестве алкили- рующего агента. Процесс проводят при эквимолярном соотношении реагентов в среде абсолютного ацетонитрила в присутствии карбоната натрия при температуре кипения растворителя. Способ позволяет сократить время проведения npoalecca с 47 до 6 ч, повысить выход соединения 1 с 17 до 29%. 1 табл. S (Л с со ел со со

| S | |||
| Kulstad, L.А.Malms ten | |||
| Diaza- czovm ethers syntheses and metal ion complexes | |||
| Parts I, p | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
Авторы
Даты
1987-11-15—Публикация
1986-02-25—Подача