Изобретение относится к биохимии, а именно к технике производства очищенных ферментных препаратов из растений, в частности к получению карбоангидразы, и может быть исполь зовано в научных исследованиях различных направлений биохимии, биотехнологии, генетики, а также в медиди- для физиологических исследований.
Карбоангидраза (КФ 4.2.1.1, кар- бонатгидролиаза - КА) представляет собой фермент, катализирующий обратимую реакцию гидратации двуокиси ут лерода. Этот фермент широко распространен в растительном мире и
имеет значение для самых разнообразных нроцессов жизнедеятельности клетки. Карбоангидраза - высокочувствительный фермент, остро реагирующий на дефицит цинка при минеральном питании растений, животных и человека и используется как диагностический тест болезней, связанных с цинковой недостаточностью.
Цель изобретения - повышение выхода, активности и стабильности при хранении целевых продуктов, упрощение и ускорение процесса.
Способ осуществляют следующим образом.
В качестве источника сырья используют литья бобов сорта Черные русские, обладающие повышенным содержанием КА v бобов) .
После осуществления, гомогенизации листьев бобов производят подкисление Г омогената путем прибавления 0,1 н. по каплям рн 6,0-6,5 с последующим его центрифугированием для получения супернатанта-экстракта, обладающего КА-активностью, и отдел(.- ния от осажденных балластных белков . Это позволяет полнее извлечь целевые продукты, лучще отделить их от примесных белков. Подкисление гомогена- та до рИ меньше 6 приводит к уменьшению количества-балластного белка в супернатанте, однако при этом наблюдается значительная инактивация обеих форм КА, особенно формы 1. При увеличении рН более 6,5 увеличивается количество примесного белка, пе рещедшего в экстракт (при рН 8,0 белка в экстракте в 2 раза больше, чей при рН 6,0), что снижает качество последующего отл,елвния форм 1 и 2 от этого белка.
Белки экстракта, обладающие КА-активностью, высаливают сернокислым аммонием в узком интервале концентра- 5 ций (40-55%). Осадок белков, получен- ньй при 40%-ном Насыщении, не имеющий КА-активности, отбрасывают. Собирают осадок .белков, полученный при 55%-ном насыщении сульфатом аммония.
10 При -расширении интервала фракционирования до 30-60% происходит сильное загрязнение КА-фракции примесным белком.
Осадок белков, полученный высали15 ванием сернокислым аммонием и содержащий карбоангидразу, перед проведением гель-фильтрации растворяют в минимальном объеме цитратно-фосфатного буфера с рН 4,5-5,5. Карбоангидраза
20 переходит в супернатант при последующем центрифугировании (20000д, 20 мин), а нерастворивщийся белок, не обладающий КА-активностью, отбрасывают. При увеличении значения рН
25 из осадка в раствор переходит большее количество примесного белка, что существенно ухудшает эффективность выделения и очистки КА на этой стадии. При уменьшении значе30 ния рП происходит резкое снижение выхода КА в растворимую фракцию.
Гель-фильтрацию проводят на колонке размером 2,5-70 см, заполненную сефарозой 6В; белки элюируют
от общего белка листьев 35 фосфатным буфером с рН 6,5-7,0.
Такое проведение гель-фильтрации увеличивает скорость элюации и ускоряет процесс выделения форм 1 и 2 на этой стадии по сравнению с прото40 типом в 2 раза. Указанные значения рН буфера являются оптимальными, поскольку обеспечивают стабильное состояние обоих форм КА при проведении гель-фильтрации. Уменьшение
4-5 или увеличение значения рН приводит к соответствующему снижению стабильности формы 1 либо формы 2 в растворе, вплоть до полного исчезновения активности за время осущест50 вления гель-фильтрации (5 ч), и к потере этих ферментов в ходе последующего выделения и очистки другими методами.
55 Полученную после гель-фильтрации карбоангидразпую фракцию подвергают ионообменной хроматографии на ДЕАЕ- целлюлозе, которую проводят на ко- лонке размером 3-16 см, обеспечиваюБелки экстракта, обладающие КА-активностью, высаливают сернокислым аммонием в узком интервале концентра- ций (40-55%). Осадок белков, получен- ньй при 40%-ном Насыщении, не имеющий КА-активности, отбрасывают. Собирают осадок .белков, полученный при 55%-ном насыщении сульфатом аммония.
При -расширении интервала фракционирования до 30-60% происходит сильное загрязнение КА-фракции примесным белком.
Осадок белков, полученный высаливанием сернокислым аммонием и содержащий карбоангидразу, перед проведением гель-фильтрации растворяют в минимальном объеме цитратно-фосфатного буфера с рН 4,5-5,5. Карбоангидраза
переходит в супернатант при последующем центрифугировании (20000д, 20 мин), а нерастворивщийся белок, не обладающий КА-активностью, отбрасывают. При увеличении значения рН
из осадка в раствор переходит большее количество примесного белка, что существенно ухудшает эффективность выделения и очистки КА на этой стадии. При уменьшении значения рП происходит резкое снижение выхода КА в растворимую фракцию.
Гель-фильтрацию проводят на колонке размером 2,5-70 см, заполненщей хорошую скорость элюации и позволяющей весь процесс разделения форм КА провести за 4-5 ч вместо 72 ч, необходимых для проведения изоэлектрического фокусирования, т.е. уменьшающей временные затраты на осуществление этой стадии. Использование 0,01 М триссульфатного буфера рН 8,0-8,5, содержащего 20 мм сульфата натрия в качестве уравновешивающего буфера, обеспечивает опти- машьную сорбцию исходной КА и полное связывание с ДЕАЕ-целлюлозой. При последующем промывании ДЕАЕ-целлюло- зы указанным буфером КА-активность в элюате не обнаруживается. Использование рН уравновешивающего буфера ниже значений 8,0 ведет к неполной адсорбции форм 1 и 2 КА на ДЕАЕ-цел- люлозе, к частичной десорбции КА и обнаружению ее активности в элюате. При значениях рН выше 8,5 К/ -активность в элюате не обнаруживается, формы 1 и 2 связываются ДЕАЕ-целлюлозой полностью, однако промывание этими растворами инактивирует форму 2.
Картину элюировання форм 1 и 2 КА, помимо рН, определяет также ионная сила буфера, которая создается добавлением сульфата натрия в буферный раствор. При значениях рН буфера 8,0 - 8,5 и концентрациях сульфата натрия 60-70 мМ с ДЕАЕ-целлюлозы элюируется только форма 1. При концентрациях сульфата натрия в буфере с рН 8,0-8,5, меньших 60-70 мМ, К.А.активность в элюате не обнаруживается, а при больших концентрациях наблюдается частичная инактивация форм 1 и 2. Получение формы 2 в этих условиях нежелательно вследствие ее сильной инактиации в растворе с рН 8,0-8,5. Оптимальную десорбцию фор- 4ы 2 с ДЕАЕ-целлюлозы осуществляют 0,01 М нитратно-фосфатным буфером, -фН 5,5-6,5, содержащим 40-50 мМ сульфата натрия. Перед снятием формы 2 этим раствором колонку с ДЕАЕ-целлюлозой тщательно освобождают от формы 1 и постороннего белка вначале вышеуказанным промыванием 0,01 М триссульфатным буфером, рН 8,0-8,5, содержащим 60-70 мМ сульфата натрия (500 мл), затем раствором 0,01 М цитратно-фосфатного буфера, рН 4,5-5,5 (500 мл), содержащим 40-50 мМ сульфата натрия. Во
всех случаях промывание колонки продолжают до полного исчезновения белка в элюате, что контролирует по измерению поглощения при 280 нм.
Пример 1. Объектом служат листья бобов сорта Черные русские. Растения выращивают в деревянных ящиках с почвой.
Стадия 1. 300 г свежеотобранных листьев (28--дневных) фиксируют жидким азотом и растирают в фарфоровой ступке с 300 мл О,1 М триссульфатного буфера, рН 7,8, содержащего
0,1 М МЭ и 0,002 ЭДТА. Растертую массу медленно размораживают путем настаивания при 4 С в течение 5 ч при периодическом перемешивании. Полученный гомогенат при непрерывном перемешивании-подкисляют до рН 6,3 прибавлением по каплям 0,1 н H2S04 и тотчас фильтруют через двойной слой капрона. Фильтрат центрифугируют при 22000 g в течение 20 мин. Недостаточная жидкость содержащая 1380 мг белка, - экстракт листьев.
Стадия 2. В экстракт добавляют твердый сульфат аммония до 40%-ного насьш ;ениЯо Осадок белков, полученный
при этом насыщении, отделяют центри- фурированием при 10000 g, 20 мин и отбрасывают. К супернатанту добавляют сульфат аммония до 55%-ного насыщения. Осадок, обладающий КА-активностью, собирают центрифугированием (lOOOOg, 20 мин) и растворяют в минимальном объеме (5-10 мл) 0,01 М цитратно-фосфатного буфера, рН 5,0, .содержащего 0,05 М МЭ, при перемешивании. Нерастворившийся белок, не обладающий КА-активностью, отделяют центрифугированием при 20000д, 20 мин.
Стадия 3. Полученный супернатант
наносят на стеклянную хроматографи- ческую колонку (размером 2,5-70 см), заполненную сефарозой 6В, уравнове- щенную фосфатным буфером, рН 6,8, содержашим 0,05 М МЭ. После выхода
100 мл пустого объема сбор фракций по 5 мл осуществляют на коллекторе фракций со скоростью 2 мл/мин.
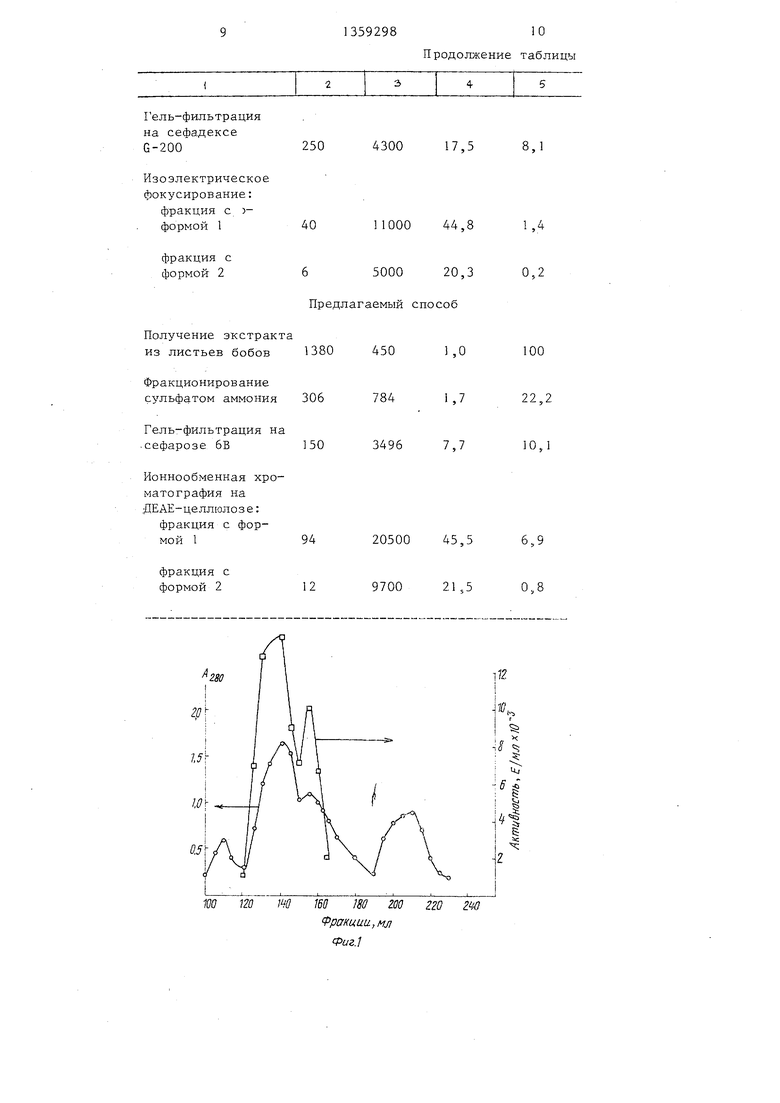
Типичная картина гель-фильтрации на сефарозе 6В показана на фиг.1 .
Во фракциях промеряют белок по поглощению при 280 нм и активность КА колориметрическим методом. Наиболее активные фракции с объемами выхода 1 20210 мл объединяют; полученный объем составляет 90 мл.
Стадия 4. Ферментньш раствор наслаивают на колонку (размером 3-16 см) с ДЕАЕ-целлюлозой (номинальная емкость 0,60-0,80 мэкв/г, фактор набухаемости 9,0 мл/г сухого анионита, фирма Реанал, Венгрия), уравновешенную 0,01 М триссульфатным буфером, рН 8,2, содержащим 0,05 М МЭ и 20 мМ сульфата натрия (200 мл). Неадсорбированньй белок вымывают тем же раствором, получая элюат, не обладающий КА-активностью, которьй отбрасывают. Фракционирование белков с ДЕАЕ-целлюлозы проводят в 2 этапа. Первоначально колонку промывают растворами 40 мМ для промывки (200 мл, фракция О и 60 мМ (фракция 11, 200 мл) сульфата натрия в 0,01 М триссульфатном буфере, рН 8,2. Затем белки с ДЕАЕ-целлюлозы элюируют растворами 20 мМ для промывки (200 мл, фракция 111) и 40 мМ 200 мл, фрак- ция 1У) сульфата натрия в 0,01 М ци- тратно-фосфатном буфере, рН 5,8. Промывание растворами во всех случая продолжают до полного исчезновения поглощения белка в элюате при 280 нм Фракции 1 и 111, не обладающие КА- активностью, отбрасывают. Активность КА обнаруживается во фракциях 11 и 1 Сбор фракций 10 мл осуществляют на коллекторе фракций со скоростью 10 мл/мин.
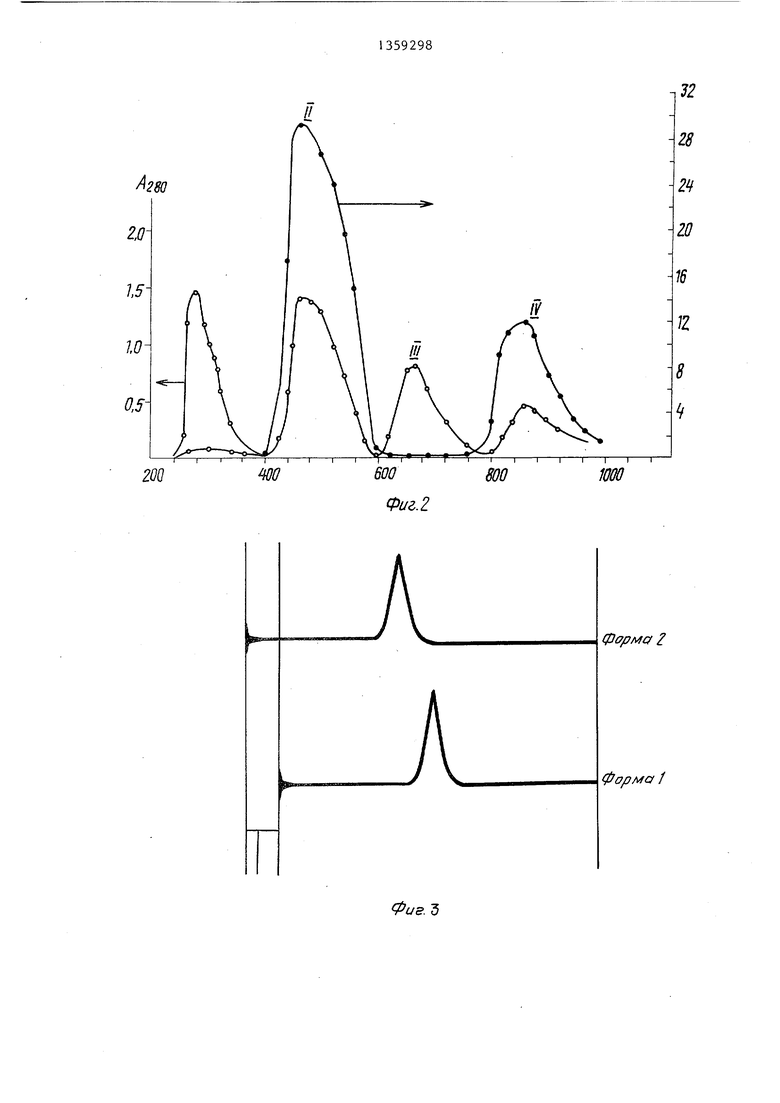
Фиг.2 отражает типичную картину элюации.
Во фракциях промеряют белок по поглощению при 280 пм и активность КА. Наиболее активные фракции с объемами выхода 50-150 мл объединяют,. Первая активная фракция 11 соответствует форме 1, содержит 94 мг белка, и имеет удельную активность 20500 Е/мг белка. Вторая активная- фракция 1 является формой 2, Содержит 12 мг белка и имеет удельную активность 9700 Е/мг белка.
Стадия 5. Полученные ферментные растворы форм 1 и 2 КА раздельно концентрируют сульфатом аммония при 70%-ном насыщении, центрифугируют при 22000д, 20 мин и хранят в виде осадков под сульфатом аммония- при - 20 С. Активность формы 1 сохраняется в течение 6 мес без изме5 0 5 О g
0 5
0
5
нения, а формы 2 - 1 мес в этих условиях.
Полученные препараты форм 1 и 2 гомогенны: при исследовании в аналитической центрифуге Spinco, модель Е (США), каждый фермент показывает единственный пик (Фиг.З) с коэффициентами седиментации 15,8 S и 16,0 S Соответственно для форм 1 и 2 (скорость вращения ротора 48660 об/мин, съемка сделана после 16 мин достижения равновесия при концентрации белка 3,5 мг/мл). При аналитическом диск-электрофорезе в 7,5% полиакри- ламидном геле каждая форма мигрирует в виде одной белковой полосы (фиг.4).
Результаты очистки и выделения форм 1 и 2 КА из листьев бобов приведены в таблице, где для сравнения даны также результаты очистки по из в е стному спо со бу.
Результаты, приведенные в таблице, показывают, что предлагаемый способ по сравнению с известным позволяет повысить активность гомогенных форм 1 и 2 КА в 2 раза и выход в 4 раза (в % от общего белка листьев).
Пример 2. Способ осуществляют как в примере 1. После гомогенизации листьев бобов гомогенат подкисляют до рН 6,5, центрифугируют. Экстракт, содержащий 1600 мг белка с удельной активностью 585 Е/мг белка, высаливают сульфатом аммония в интервале 40-55% и садок растворяют в 5 мл 0,01 М цитратно-фосфатного буфера, рН 5,5. Полученньм супернатант с удельной активностью КА 800 Е/мг белка, содержапщй 350 мг белка, подвергают гель-фильтрации на сефарозе 6В 0,01 М фосфатным буфером, рН 7,0. КА-фракцию, имеющую удельную активность 4000 Е/мг белка (180 мг белка), хроматографируют на ДЕАЕ-целлюлозе, элюируя вначале форму 1 растворами 30 мМ (для промывки) и 70 мМ сульфата натрия в 0,01 М триссульфатном
буфере, рН 8,5, затем форму 2 - растворами 30 мМ и 50 мМ сульфата натрия в 0,01 М цитратно-фосфатном буфере, рН 6,5. Формы 1 и 2 получают гомогенными с выходом 7 и 0,6%, степенью очистки 22 и Д р , удельной активностью 22000 и 9500 Е/мг белка соответственно. Показатели также значительно вьше, чем по известному способу..
7
Пример 3. Способ осуществляют как в примере 1. Однако гомо- генат подкисляют до рН 6,0, осадок белков, высаливаемых сульфатом аммония, растворяют в 0,01 М цитрат- но-фосфатном буфере с рН 4,5, гель- фильтрацию на сефарозе 6В проводят при рН 6,5, Последующее разделение форм 1 и 2 КА методом ионообменной хроматографии на ДЕАЕ-целлюлозе ведут растворами 20 мМ (для промывки) и 60 мМ сульфата натрия в 0,01 М триссульфатном буфере, рН 8,0 и раствором 40 мМ сульфата натрия в 0,01 М цитратно-фосфатном буфере рН 5,5. Формы 1 и 2 КА вьще- ляются по этому способу с показателями (удельной активностью, выходу, гомогенности, степени очистки, стабильности), аналогичными примеру 1.
Таким образом, использование прелагаемого способа получения форм 1 и 2 карбоангидразы из растений упрощает технологию получения целевых продуктов и ускоряет процесс выделения ферментов в 15 раз за счет применения ионообменхюй хроматографии на ДЕАЕ-целлюлозе вместо изоэлектри ческого фоку-сирования, позволяет получить высокоочищенные ферменты за счет подбора оптимальных условий вьщеления и очистки карбоангидразы на стадиях гомогенизации, гель- фильтрации, ионообменной хроматографии, повысить их активность в 2 раИзвестный способ
Получение экстракта из листьев бобов
Фр ак циониров ание сульфатом аммония
8
за, выход в 4 раза и стабильность при хранении.
g Формула изобретенияСпособ получения двух молекулярных форм карбоангидразы, предусматривающий гомогенизацию наземной
0 части растений в буферном растворе, отделение твердой фазы из гомогената, осаждение белков из полученного экстракта сульфатом аммония при насыщении 40-55%, раст5 ворение осадка и его гель-фильтрацию с последующим разделением двух форм фарбоангидразы, отличаю- щ и и с я тем, что, с целью повьппе- ния выхода, активности и стабильнос0 ти при хранении целевых продуктов, упрощения и ускорения процесса, го- могенат подкисляют до рН 6,0-6,5, растворение осадка осуществляют цитратно-фосфатным буфером с рН
5 4,5-5,5, гель-фильтрацию проводят на сефарозе 6В фосфатным буфером с рН 6,5-7,0 с последующим разделением и очисткой целевых продуктов ионообменной хроматографией на колонке с 0 ДЕАЕ-целлюлозой, при этом колонку промывают триссульфатньш буфером с рН 8,0-8,5, содержащим 20-40 мМ сульфата натрия, затем элюируют карбоангидразу 1 и карбоангидразу П 5 триссульфатным буфером, содержащим сначала 60 - 70 мМ, затем 40-50 мМ сульфата натрия с рН 8,0-8,5 и 5,5- 6,5 соответственно.
1,0
100
981
3,0
33
135929810
Продолжение таблицы
е
250
4300
17,5
40
11000 44,8
6 5000 20,3 Предлагаемый способ
Получение экстракт
из листьев бобов
Фракционирование сульфатом аммония
Гель-фильтрация на .сефарозе 6В
Ионнообменная хроматография на ДЕАЕ-целлюлоз е: фракция с формой 1
фракция с формой 2
12
4300
17,5
11000 44,8
5000 20,3 емый способ
1,0 1,7 7,7
100
22 ,
10,
20500 45,56,9
9700
21 ,5



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения карбоангидразы | 1981 |
|
SU955930A1 |
| Способ очистки нуклеазы из проростков ячменя | 1989 |
|
SU1703688A1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСА ИНГИБИТОРОВ ЛЕЙКОЦИТАРНЫХ ПРОТЕИНАЗ | 1995 |
|
RU2086650C1 |
| СПОСОБ ВЫДЕЛЕНИЯ И ОЧИСТКИ ТРОФОБЛАСТИЧЕСКОГО БЕТА-1-ГЛИКОПРОТЕИНА | 2008 |
|
RU2367449C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЛАЦЕНТАРНО-СПЕРМАЛЬНОГО ГАММА-ГЛОБУЛИНА | 1991 |
|
RU2031653C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЛАЦЕНТАРНО-СПЕРМАЛЬНОГО β-ГЛОБУЛИНА | 1991 |
|
RU2008908C1 |
| Способ получения гликопротеина | 1979 |
|
SU1431691A3 |
| СПОСОБ ПОЛУЧЕНИЯ α -ГЛОБУЛИНА ПУЗЫРНОЙ ЖИДКОСТИ, АССОЦИИРОВАННОГО С ИСТИННОЙ ПУЗЫРЧАТКОЙ | 1993 |
|
RU2043117C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭСТРОГЕНСВЯЗЫВАЮЩЕГО БЕЛКА, АССОЦИИРОВАННОГО СО ЗЛОКАЧЕСТВЕННЫМИ НОВООБРАЗОВАНИЯМИ | 2012 |
|
RU2489440C1 |
| СПОСОБ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО ФАКТОРА НЕКРОЗА ОПУХОЛЕЙ АЛЬФА ЧЕЛОВЕКА | 1997 |
|
RU2144958C1 |

Изобретение относится к технике производства очищенных ферментных препаратов. Цель изобретения - повышение выхода, а также упрощение и ускорение процесса. Способ заключается в том, что для получения экстракта, обладающего карбоангидраз- ной активностью, из гомогенизированных листьев бобов гомогенат подкисляют до рН 6,0-6,5 с последующим растворением белков, осажденных сульфатом аммония, в цитратно-фос- фатном буфере с рН 4,5-5,5, проведением гель-фильтрации на сефарозе 6Б при рН 6,5-7,0, разделением и очисткой форм 1 и 2 карбоангидразы методом ионо-обменной хроматографии на ДЕАЕ-целлюлозе, при этом колонку промывают триссульфатным буфером с рН 8,0-8,5, содержащим 20-40 мМ сульфата натрия, затем элюируют последовательно карбоангидразу 1 и карбоангидразу 2 триссульфатным буфером, содержащим сначала 60-70 мМ, затем 40-50 мМ сульфата натрия с рН 8,0-8,5 и 5,5-6,5 соответственно. Способ позволяет получить две высокоочищенные формы карбоангидразы, повысить в 2 раза их активность, увеличить в 4 раза выход целевых продуктов и обеспечить высокую стабильность ферментов при хранении. 1 табл. 4 ил. ( сл w сд ;о ю со оо
V«7
15/W
WS Ш zoo 220 Фракции., мл Фиг.
1/2
форма 2
форма /
Фие.Ъ
ipopf a 2Форма 1
Фиг Л
| Kachry R.B., Anderson Z.E.Plan- ta, 1974, V | |||
| Прибор для массовой выработки лекал | 1921 |
|
SU118A1 |
| Комарова Ю.М., Доман Н.Г., Шапошников Г.Л | |||
| Биохимия, 1982, т.47, № 6, с„1027-1034. | |||
Авторы
Даты
1987-12-15—Публикация
1986-07-14—Подача