Изобретение относится к новым химическим соединениям формулы I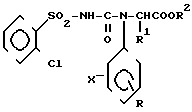 где Х 3-Сl;
где Х 3-Сl;
R 4-Me- или ОМе;
R1 H, Me;
R2 Мe, Et, Pr; X-4-Cl; R-H;
R' Me;
R2-Et; X-H; R-2 или 4-ОМе, или 2-ОМе;
R'-Me, R2-Et или изо-Pr;
Х-2-Ме, R-6-Et, R'-Me, R2-Et, которые обладают рострегулирующей активностью.
Целью изобретения является изыскание в ряду производных α-аминокислот новых регуляторов роста растений, обладающих повышенной рострегулирующей активностью.
П р и м е р. Этиловый эфир N-(2-хлорфенилсульфониламинокарбонил)-N-4-метоксифенилаланина (соединение 5: Х Н; R 4-ОМе; R1 Me; R2 Et).
В четырехгорлую колбу, снабженную мешалкой, термометром, обратным холодильником с хлоркальциевой трубкой и капельной воронкой, помещают 5,2 г (0,027 г-моль) этилового эфира N-4-метоксифенилаланина и 20 мл тетрагидрофурана. Реакционную массу перемешивают и затем прикапывают 5,8 г (0,027 г-моль) о-хлорфенилизоцианата. При этом происходит разогрев реакционной массы до 40-50оС. К концу реакции часть растворителя удаляют и реакционная масса становится вязкой. Далее реакционную массу растирают в серном эфире, в результате происходит кристаллизация конечного продукта. Продукт отфильтровывают, промывают эфиром и сушат.
Получают 9,4 г этилового эфира N-(2-хлорфенилсульфониламинокарбонил)-N-(4-метоксифенил)-аланина; т. пл. 167-169оС. Выход 80,3% По данным тонкослойной хроматографии и масс-спектрального анализа продукт не содержит исходные вещества и другие примеси.
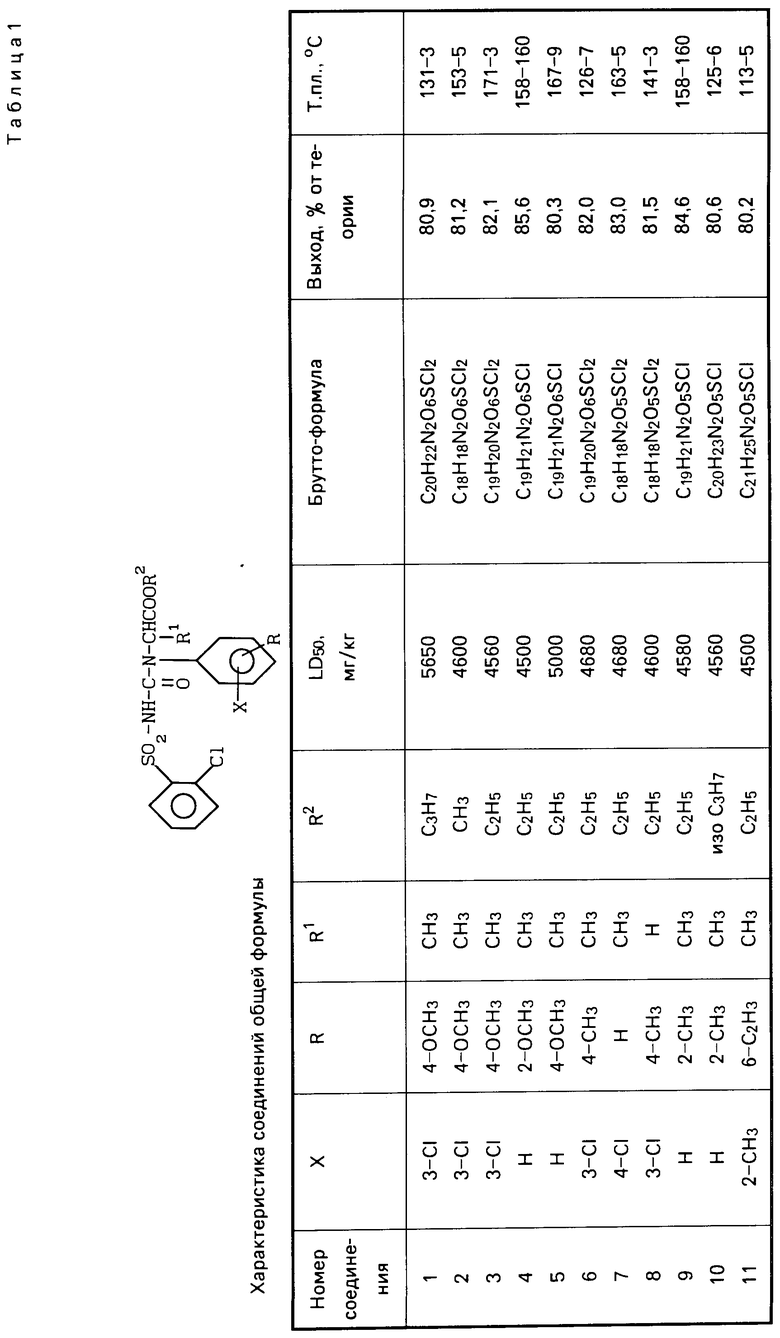
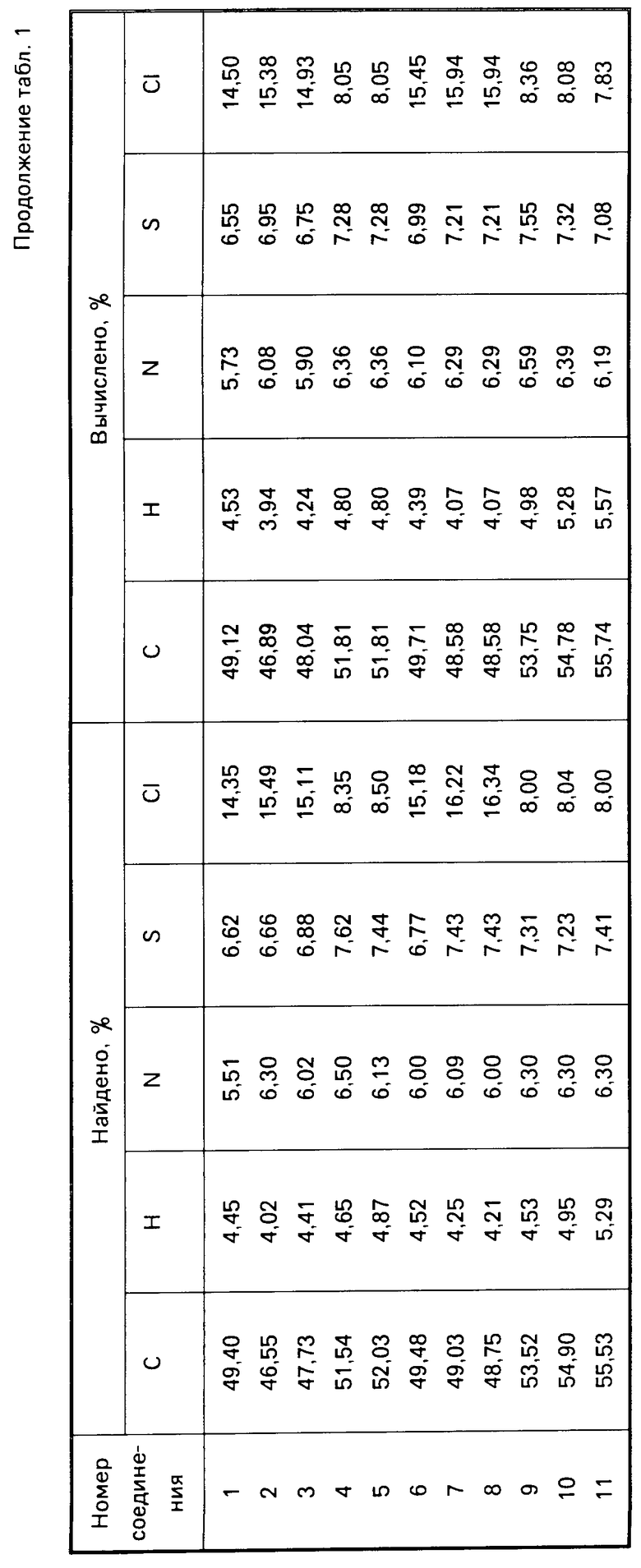
Аналогично получены и другие соединения 1-11, характеристика которых приведена в табл. 1.
В ИК-спектрах полученных соединений I имеются полосы при 1710 см-1 (СООR2); 1655-1665 см-1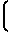 NH-CO-N
NH-CO-N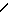
 1360 и 1178 см-1 (SО2).
1360 и 1178 см-1 (SО2).
Изучение физиологической активности.
Рострегулирующая активность производных α-аминокислот I сравнивалась с таковой для описанного соединения N-бензоил-3,4-дихлорфенилаланина (соединение 12), аналога соединений 1. Эталон применяли в той же концентрации, что и испытуемые соединения.
А. Опыты на семенах огурцов, пшеницы, фасоли.
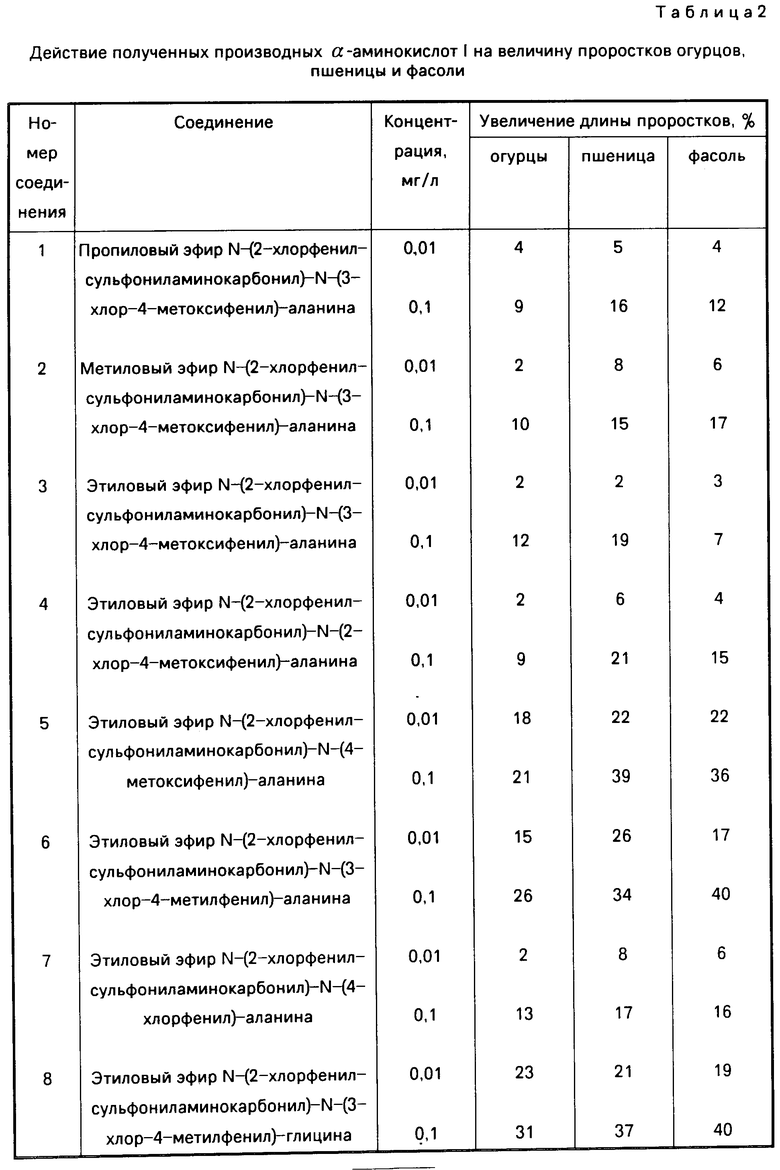
В чашке Петри раскладывают сухие семена и заливают 4 мл испытуемого раствора и помещали в термостат на 48 ч при температуре 28оС. Препараты испытывают в концентрации 0,01-0,1 мг/л. Эффективность определяют в сравнении с контролем по линейным замерам. Результаты приведены в табл. 2.
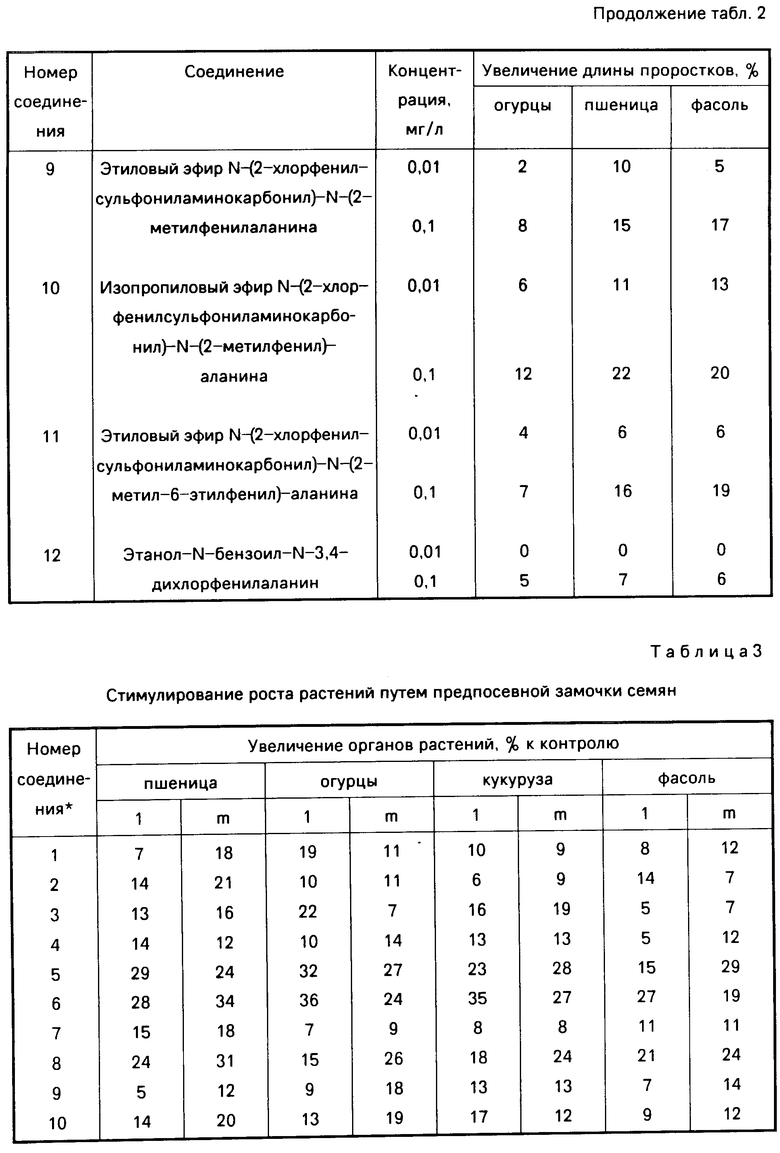
Б. Предпосевная замочка семян огурцов, фасоли, пшеницы, кукурузы. Предпосевную замочку семян огурцов, пшеницы, фасоли, кукурузы проводят в растворах препаратов в концентрации 1000 мг/л в течение 0,5 ч при 25оС. Семена высевают в сосудах емкостью 2 л. Эффективность учитывали через 30 дней после посева. Результаты приведены в табл. 3.
В. Послевсходовая обработка растений фасоли.
Растения фасоли, выращенные в сосудах, обрабатывают препаратами в концентрации 50 и 250 мг/л. Эффективность определяют через 3 недели после обработки. Результаты испытаний приведены в табл. 4.
Приведенные результаты испытаний (см. табл. 2-4) свидетельствуют о том, что обработка семян, вегетирующих растений пшеницы, кукурузы, огурцов, фасоли новыми соединениями I в меньшей концентрации стимулирует их рост и развитие в большей степени, чем обработка аналогом по структуре и назначению N-бензоил-N-3-4-дихлорфенилаланином. Максимальный эффект достигается при обработке этиловыми эфирами N-(2-хлорфенилсульфониламинокарбонил)-N-(4-метоксифенил)-аланина (соединение 5), N-(3-хлор-4-метилфенил)-глицина (соединение 8) и N-(3-хлор-4-метилфенил)-аланина (соединение 6).
Полученные соединения могут найти применение в качестве регуляторов роста растений в посевах, сельскохозяйственных культур в дозах от 0,01 до 5 кг/га; по активности они существенно превосходят известный аналог N-бензоил-N-3,4-дихлорфени- лаланин.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ N-(БЕНЗОТИАЗОЛИЛ-2)- α -АМИНОКИСЛОТ, ОБЛАДАЮЩИЕ РОСТРЕГУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 1990 |
|
SU1669153A1 |
| АМИДНОЕ СОЕДИНЕНИЕ ИЛИ ЕГО СОЛЬ, СЕЛЬСКОХОЗЯЙСТВЕННЫЙ И САДОВЫЙ ИНСЕКТИЦИД И БАКТЕРИЦИД, СОДЕРЖАЩИЕ ДАННОЕ СОЕДИНЕНИЕ, И СПОСОБ ПРИМЕНЕНИЯ ДАННОГО ИНСЕКТИЦИДА И БАКТЕРИЦИДА | 2014 |
|
RU2664574C1 |
| СОЕДИНЕНИЯ БЕНЗОИЛПИРАЗОЛА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ГЕРБИЦИДЫ, СОДЕРЖАЩИЕ ИХ | 2007 |
|
RU2462457C2 |
| СОЕДИНЕНИЕ N-(4-ПИРИДИЛ)НИКОТИНАМИД ИЛИ ЕГО СОЛЬ | 2018 |
|
RU2785399C2 |
| НЕМАТОЦИДНЫЕ СУЛЬФОНАМИДЫ | 2010 |
|
RU2531317C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ПИРИМИДИНИЛОКСИ-ПИРИДИНА В КАЧЕСТВЕ ГЕРБИЦИДОВ | 2016 |
|
RU2735278C2 |
| НОВЫЕ ПИРИДАЗИНОНОВЫЕ ГЕРБИЦИДЫ | 2016 |
|
RU2764746C2 |
| СОЕДИНЕНИЕ АНТРАНИЛАТА КИСЛОТЫ, ЕГО СОЛЬ, ФУНГИЦИД, ВКЛЮЧАЮЩИЙ ЭТО СОЕДИНЕНИЕ, И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2016 |
|
RU2720996C2 |
| ГЕРБИЦИДНЫЕ ЗАМЕЩЕННЫЕ ПИРИМИДИНИЛОКСИБЕНЗОЛЬНЫЕ СОЕДИНЕНИЯ | 2014 |
|
RU2703460C1 |
| ГЕРБИЦИДНЫЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ СОЕДИНЕНИЯ БЕНЗОИЛПИРАЗОЛА, И СПОСОБ УНИЧТОЖЕНИЯ НЕЖЕЛАТЕЛЬНЫХ РАСТЕНИЙ | 2009 |
|
RU2514184C2 |
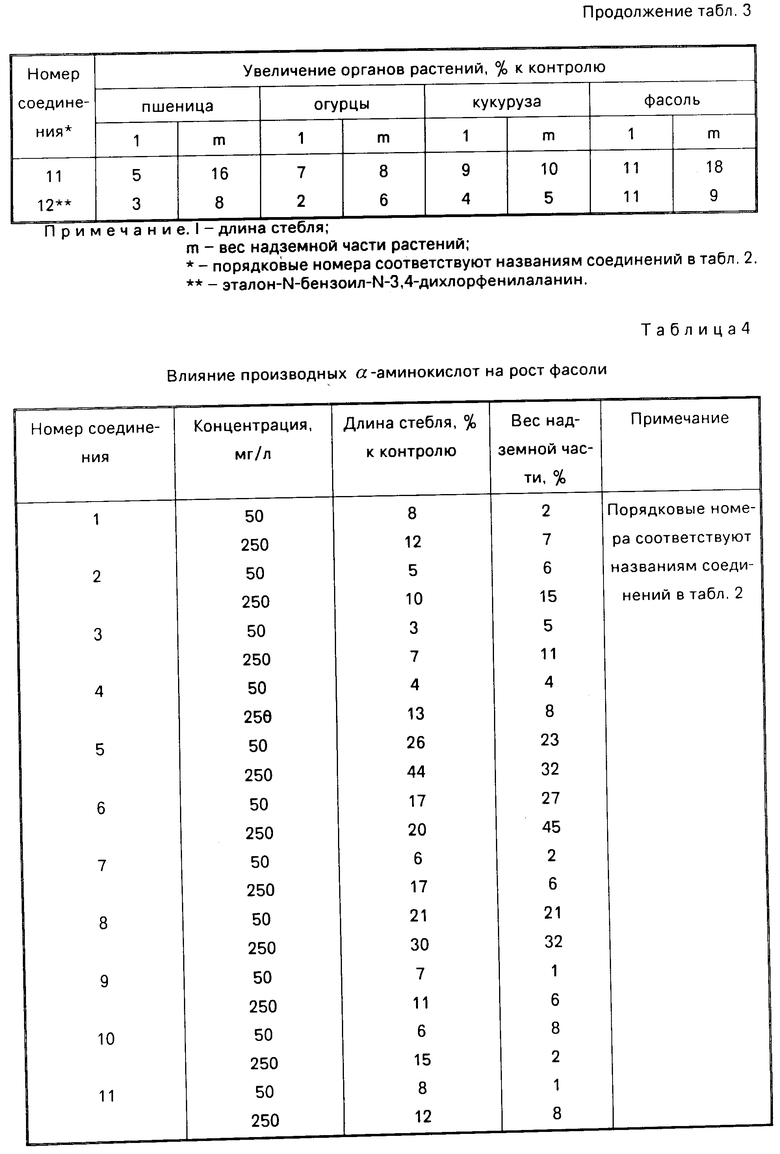

Изобретение относится к области сульфокислот, в частности к производным a - аминокислот (ПАК) формулы 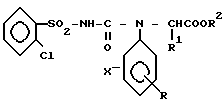 где X=3-Cl; R= 4-OMe или -Me; R1= Me или H; R2= Me, Et или Pr; X=4-Cl, R=H, R1= Me, R2= Et; X=H, R=3- или - 4-OMe, или 2-Me; R1= Me, R2= Et или изо-Pr; X=2-Me, R1= 6-Et, R1= Me, R2= Et, которые обладают рострегулирующей активностью. Цель - создание более активных веществ указанного класса. Получение ПАК ведут из N-фенилзамещенного эфира α - аминокислоты с ароматическим изоцианатом (при молярном соотношении 1:1-1,1) в тетрагидрофуране при 20-30°С. Выход ПАК 80-85%. Полученные ПАК могут найти применение как регулятор роста растений. В дозах от 0,01 до 5 кг/га, по активности они превосходят известный N-бензоил-N-3,4-дихлорфенилаланин. 4 табл.
где X=3-Cl; R= 4-OMe или -Me; R1= Me или H; R2= Me, Et или Pr; X=4-Cl, R=H, R1= Me, R2= Et; X=H, R=3- или - 4-OMe, или 2-Me; R1= Me, R2= Et или изо-Pr; X=2-Me, R1= 6-Et, R1= Me, R2= Et, которые обладают рострегулирующей активностью. Цель - создание более активных веществ указанного класса. Получение ПАК ведут из N-фенилзамещенного эфира α - аминокислоты с ароматическим изоцианатом (при молярном соотношении 1:1-1,1) в тетрагидрофуране при 20-30°С. Выход ПАК 80-85%. Полученные ПАК могут найти применение как регулятор роста растений. В дозах от 0,01 до 5 кг/га, по активности они превосходят известный N-бензоил-N-3,4-дихлорфенилаланин. 4 табл.
Производные a -аминокислот формулы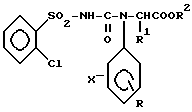
где X=3-Cl, R=4-OMe или -Me;
R1=Me или H, R2=Me, Et или Pr;
X=4-Cl, R=H, R1=Me, R2=Et;
X=H, R=2- или 4-OMe, или 2-Me;
R1=Me, R2=Et или изо-Pr;
X=2-Me.
R=6-Et, R1=Me, R2=Et,
обладающие рострегулирующей активностью.
| Патент США N 3598859, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-04-10—Публикация
1986-01-07—Подача