см
Изобретение касается способа получения новых хлорсодержащнх производных гексадецена, имеюпщх обпше формулы (la) и (16) /


Изобретение касается галоидуг- левбдородов, в частности получения спорсодержащих производных гексаде- цена формул I или II (CH)-СХ-(СН2)з СХр(СНз) -(СН2)-СС1(СНэ) (ОН г)з-С(СНз)СН.. .CH-jCE (I); (СЕ )- СХ-(СН2)з-СХ,(СНз)-(СН2)з-ССЕ(СН з) - (ОН 2)з-ССе(СНз) (II) или их смесей, где X и X , - равные или разные Н или СР, полупродуктов в синтезе витамина . Процесс ведут реакцией НС S с полиеном общей формулы III (СНз)2СУ -СНУ2-(СН2)2-С1з(СН з) . (СН,),-С(СНз) CH...(CH)2 - С(СН,)- , где Y, - Н или CJ; У,- Н илиСу 1 + У J - связь; УЗ и Y4 - Н или вместе связь. Процесс ведут в присутствии катализатора, образованного хлоридом меди с хлоргидратом триэтиламина, в инертном растор ителе при (-10)-0°С при условии, когда а) , то используют 2 моля НС на 1 моль полиена; б) или Cf; и УЗ + У - связь, то берут 3моля НС6 на 1 моль полиена; BJ СУ,+ + у, (Yj + y)- связь, то берут 4моля НС на 1 моль полиена. Целевые вещества могут быть сконденсированы с триметилгидрохиноном с образованием соединения формулы IV (СНз)СХ-(СН2)э-СХ(СНз)-(СН)з - СС1 (СНэ)-(СН)з-Z, где X указано; СНз О 1-НзС СНз он , которое с о сн. может быть гидрогенизировано в токоферол, или последний после ацетили- рования превращен в ацетат токоферола. со с 00 00 Oi о ро
;
сн
- Х 2
ш.
СНп
СНп
НЗ
/с
/сн,
ч
где X и
1
одинаковые или различ- .
ные, водород и ее хлор, или их смесей, которые могут найти применение, в частности, как полупродукты при синтезе витамина Е.
сщ сн
l-CHj CH(bcH:
х
I
где X и Х| имеют значения, указанные выте,
которое может быть гидрогенизировано в токоферол или в ацетат токоферола после ацетилирования,
Ацетилирование соединения, имеющего общую формулу (ill) осзпцествляет ся с помощью уксусного ангидрида в присутствии хлорида цинка или в присутствии смеси триэтиламина и диметил аминопиридина при температуре, при- . близительно равной .
Гидрирование соединения, имеющего об1чую формулу (III), или его ацетата в токоферол или ацетат токоферола может быть осуществлено с помощью водорода 6 присутствии такого катализатора, как палладий на угле в органическом растворителе, например в уксусной кислоте или этаноле, при 50- 100°С, возможно при давлении.
Пример 1. В трехгорлую колбу емкостью 500 см, снабженную магнитным перемешивателем, термометром и погрз женной трубкой, вводят в атмосфе ре аргона 3,4 г хлоргидрата триэтиламина, 2,5 г хлора меди и 270 см метиленхлорида. Содержимое колбы охлаждают до и к таким образом полученному гомогенному желтому pacTвору прибавляют 136 г мирцена . (1 моль), чистота которого вьше 95%, а затем в течение 6 ч вводят 80 г безводной соляной кислоты. Полученный
н.
СНг
/СН2
снГ
сн,
-ч.
сн, сн
С1 .СН2
(1а)
СНз
/Cv
Н, I СНл
С1 )
/СНз
ев
снз
U1
СН
5
0
cH:
Соединение, имеющее общую формулу (la) и (1б), может быть сконденсировано с триметилгидрохиноном для образования соединения, отвечающего общей
формуле (III).
Lm
Шк х/Т «
2
CHi
Шь
/гч
30
5
.О 5
д j
водного раствора 10%-ного аммония и 300 см пентана.
.. ,
таким образом раствор выдерживают
при -25°С в течение 18 ч.
Реакционную смесь выливают в смесь 400 см хлорида
После декантирования органическую фазу промывают трижды 200 см воды, а затем высутчивают на карбонате калия. После фильтрования и выпаривания растворителя получают 237,8 г светло- желтого масла, содержащего в основном 1,7-дихл6р-3,7-диметил-2-октена в виде смеси изомеров Е и Z.
В реактор емкостью 250 см вводят 12,15 г магния, 30 см тетрагидрофу- рана и один кристалл иода. Содержимое охлаждают до -20°С, после чего в течение 5 ч 30 мин прибавляют раствор 20,9 г 1,7-дихлор-3,7-диметил-2- октена, полученного ранее, в 85 см тетрагидрофурана. Перемешивание осуществляют 18 ч, температура смеси -20°С. Избыток магния удаляют путем фильтрования, после этого полученный раствор, защищенный от воздуха и влаги, вводят в подводящую трубку,
В реактор емкостью 250 см вводят 0,5 г иодида меди и 5 см тетрагидрофурана, после чего прибавляют 1,5 см магнийсодержащего раствора. Затем быстро прибавляют 19,5 г 3-хлормирце- на, чистота которого превышает 87%, взятого в 10 см тетрагидрофурана. Содержимое реактора охлаждают до
, после чего прибавляют в течение 3 ч оставрпшся магниевьй раствор Раствор оставляют с тем, чтобы его температура поднялась в течение 1 ч до значения, примерно равного 20°С. Затем к реакционной смеси прибавляют воду (5 см ) и пентан (100 см), Органическую фазу отдаляют путем декантации, сугаат на сульфате магния. После фильтрования и выпаривания рас творителя получают 29,7 г масла. После количественного анализа, осуществ ляемого путем хроматографии паровой фазы с внутренним этанолом, определяют, что процент превращения 3-хлор- мирцена составляет 69%. Полученное масло нагревают до 100-105°С при пониженном давлении (0,5 - 1 мм рт.ст. 0,067-0,13 кПа) для удаления соединеНИИ , которые не прореагировали. Полученньй остаток (20 г) содержит 85% 15-хлор-3-метилен-7,11,15-триме - тил-1,6,10-гексадетриена. Выход составляет 82% по отношению к использованному 3-хлормирцену.
Структура полученного соединения подтверждается масс-спектром и спектром ядерно-магнитного резонанса протона.
В реактор емкостью 250 см вводят в атмосфере аргона 0,48 г хлоргидра- та триэтиламина, 15 см метиленхлори- да, 10 см уксусной кислоты и 90 мг хлористой меди. Реакционную смесь перемешивают до получения гомогенного раствора. Этот раствор охлаждают до -10°С, после чего прибавляют 10 г (0,032 моль) 15-хлор-3-метилен-7,11, 15-триметил-1,6,10-гексадекатриена и в течение Гч 3,9 г (0,109 моль.) соляной кислоты в виде сухого газа. Реакционнзпо смесь выливают в 100 см водного раствора хлорида аммония, имеющего концентрацию 100 г/л. Органическую фазу отделяют путем декантирования, после чего водную фазу экстрагируют дважды 100 см метиленхлори- да Собранные органические фазы промывают в 100 см воды, после чего сушат на карбонате калия. После филь трования и выпаривания растворителя ползпают 13,1 г 1,7,11 ,15-тет,рахлор- 3,7,11,15-тетраметил-2-гексадецена при выходе 96,5%. Структура полученного соединения подтверждается масс- спектром.
Пример 2. В реактор емкостью 250 см вводят в атмосфере аргона
10
г15 20
.
3860Ш
0,48
г хлоргидрата триэтиламина, 15 см метиленхлорида, 10 см уксусной кислоты и 90 мг хлористой меди. Реакционную смесь перемешивают до получения гомогенного раствора. Этот раствор охлаждают до , после чего прибавляют 10 г (0,036 моль) р-спрингеиа ив течение 1 ч 5,2 г (0,152 моль) соляной кислоты в виде сухого газа. После обработки реакционной смеси в условиях, аналогичных указанным выше, получают 14,2 г 1,7, 11,15д;-тетрахлор-3,7,1 1,15 тетраметил- 2-гекс адецена при выходе 94%. Структура полученного соединения подтвер-, ждается после его гидрирования в
фитан.
Пример З.В реактор емкостью 250 см вводят 8,4г трйметилгидрохинона,, 22 г 1,7,11,15-тетрахлор-3,7 ,11,1 5-тет- раметил-2-гексадецена и 30 см уксусной кислоты. Затем в течение 10 мин вводят раствор 1,5 г хлорида цинка 25 в 15 см безводной уксусной кислоты. Температура смеси поднимается с 25 до 30®С. Реакционную смесь перемешивают в течение 2 ч при 30°С, после чего ее выливают в смесь 100 см гек- сана и 100 см воды. Органическую фазу, отделенную путем декантирования, промывают 100 см смеси метанол- вода (50-50 по объему). В гексановой /фазе образуется белый осадок, который отделяют путем фильтрования и промывают 50 см смеси метанол-вода (50-50 по объему). После высушивания, осуществляемого при пониженном давлении, получают 14,3 г 2,5,7,8-тетраметш1- 2-(4 ,8,12 -трихлор-4 , 8 ,12 -три- метилтридецил)-б-хроманола в виде белых кристаллов, плавящихся при 102-104 С. Выход составляет 62%. Структура полученного соединения подтверждается масс-спектром и спектрами ядерно-магнитного резонанса протона и С.
Пример 4, В реактор вводят в атмосфере аргона 186 мг хлорида цинка и 3 см уксусной кислоты. Затем при-, бавляют 1,85 г
.3
30
35
40
45
50
триметилгидрохинона,
1,5 см уксусной кислоты и 4,5 см
5
Затем в течение С вводят 5,1 г соеди- примере 3, взято-
метиленхлорида 15 мин и при 23 нения, полученного в го в растворе 4 см уксусной кислоты и 4 см метиленхлорида. После двухчасового перемешивания при 22 - 25°С прибавляют 3,5 см уксусного ангидрида. Температура поднимается до . После 15 ч при температуре, равной приблизительно 25°С, прибавляют 100 см воды, затем - бикарбонат натрия до нейтральной реакции. Экстрагируют 2 раза 50 см зтилацетата. Органические фазы cjraiaT на карбонате калия. После фильтрования и выпаривания растворителя получают 5,82 г масла, содержащего 64% ацетата 2,5, 7,8-тетраметил-2-(4,8,12 -трихлор- ,12 -триметилтридецил)-6-хрома- нола. Выход составляет 53%.
Пример 5.В трехгорлую кол- бу, снабженную магнитным перемешива-. телем, термометром и холодильником, возвьппающимся над верхней частью, где осурдествляется гидрирование, вводят 1 г соединения, полученного в примере 4, 20 см уксусной кислоты и 0,1 г палладия на угле, содержащего 10% палладия.
Реакционную смесь нагревают до при атмосферном-давлении водо- рода. Теоретическое количество водорода абсорбировано на 2 ч. После охлаждения катализатор отделяют путем фильтрования. После выпаривания растворителя получают 0,9 г очень свет- ло-желтого масла, содержащего 89,5 мас.% ацетата токоферола.
Пример 6.В трехгорлую колбу емкостью 250 см в атмосфере аргона вводят 360,5 мг хлоргидрата триэтил- амина (о, 26-.10 моль), 126 мг хлористой меди (0,13-10 моль), 9 см уксусной кислоты и 9 см метиленхло- рида. Осуществляют перемешивание содержимого до получения гомогенного раствора желтого цвета. Охлаждают этот раствор до 0°С, после чего быстро прибавляют 13,96 г (0,05 моль) З-метилен- 7,11,15-триметил-1 ,б-гекса- декадиена, чистота которого состав- ляет 95%. Охлаждают раствор до -5 С, после чего пропускают через раствор поток безводной газообразной соляной кислоты в течение 1 ч 20 мин с тем, чтобы ввести в этот раствор 5 г (0,137 моль) соляной кислоты. После тридцатиминутного :ререме11швания, осуществляемого при -5°С, реакционную смесь выливают в 20 см пентана и 20 см водного 10%-ного раствора хлористого аммония при 20 С. Органичес- кую фазу отделяют, путем декантации, после чего осуществляют высушивание на сульфате натрия. После фильтрова
ния и выпаривания растворителя полу чают 17,31 г неочищенного соединения, анализ которого методом масс-спектро- графии и ядерно-магнитного резонанса протона показывает присутствие в нем 90% смеси 1,7-дихлор-3,7,11,15-тетра- метил-2-гексадецена (95 мас,%) и 3,7- дихлор-3,7,11,15-тетраметш1-1-гекса- децена (5 мас.%). Для подтверждения линейности скелета полученного соединения обрабатывают 1,7 г полученного вьше соединения, взятого в растворе в 20 см этанола, при 80°С, при давлении водородного столба, составляющего 20 ат. в присутствии 170 мг палладия на угле в количестве 10%. |После фильтрования катализатора и выпаривания растворителя анализ, проведенный путем хроматографии паровой фазы с инертным этанолом, показывает, .что выход фитан а составляет 83,7% по отношению к использованному триену Селективность образования фитана по отношению к другим изомерам составляет 98%.
Пример 7. Действуют аналогично указанному в примере 6, однако используют следующие соединения; 14 г (0,05 моль)-2-метилен-7,I1,15- триметил-1,6,14-гексадекатриена; 37.0 мг хлоргидрата триэтиламина, 130 130 мг хлористой меди, 9 см уксусной кислоты и 9 см метиленхлорида.
Через смесь этих соединений пропускают поток безводной газообразной соляной кислоты в течение I ч с тем, , чтобы ввести 7,3 г соляной кислоты (0,2 моль). После обработки реакционной смеси получают 19,31 г масла, анализ которого методом масс-спектрометрии и ядерно-магнитного резонанса протона показывает, что оно состоит из 1,7,15-трихлор-З,7,11,15-тетраме- тил-2-гексадецена (95 мас.%) и 3,7, 15-трихлор-З,7,11,15-тeтpaмeтил-l-гeк caдeцeнa (5 мас.%) и, что оно не содержит сопряженных диенов.
i
Гидрирование соединения, полученного в условиях, описанных в примере 1, показывает, что после количественного анализа, осуществленного методом хроматографии в паровой фазе с инертным этанолом, выход фитана составляет 63% по отнощению к использованному 2-метилен-7,11,15-триметил-1,6,14- гексадекатриену.
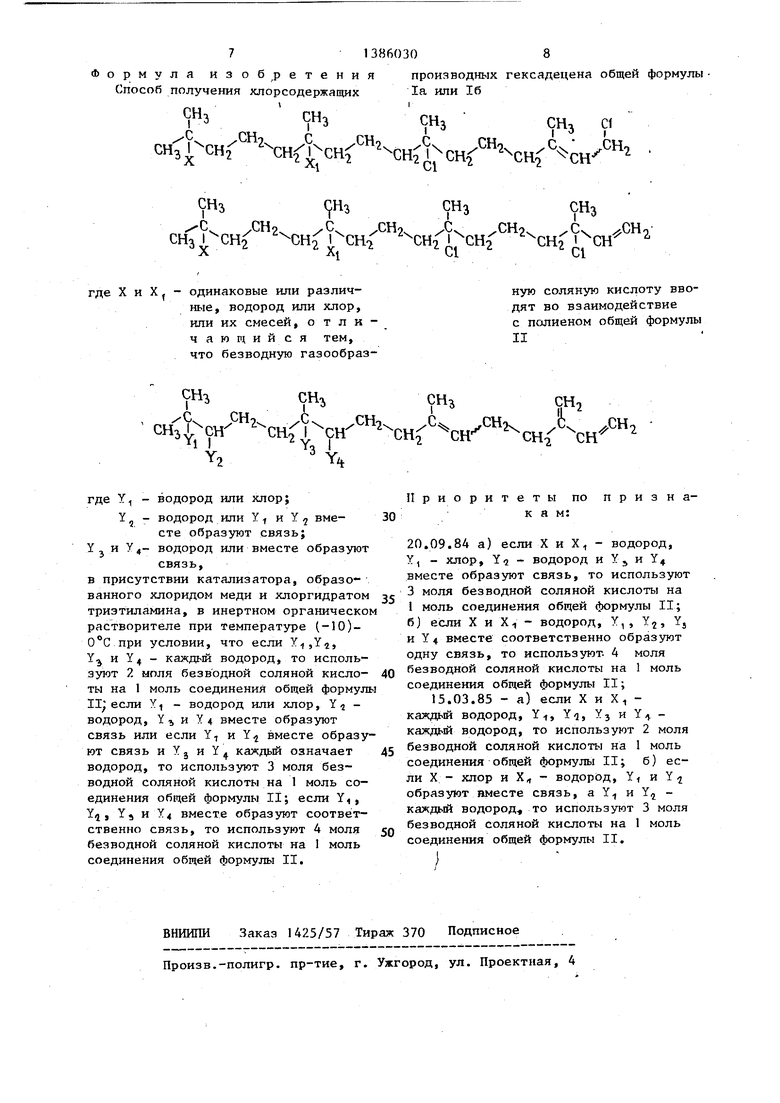
ормула изобретения Способ получения хлорсодержащих
СНз сн,
- - ЧнГ снГ™
Xi
X и X, одинаковые или различные, водород или хлор, или их смесей, отличающийся тем, что безводную газообразсн
/а
СНа
с
, VJ -C T--CHi. f I
10 I
Y
где
Yi - . водород или хлор;
водород или Y и Y 5 вме-
сте образуют связь; YJ и У4- водород или вместе образуют
связь,
в присутствии катализатора, образованного хлоридом меди и хлоргидратом тризтиламина, в инертном органическо растворителе при температуре (-10)- при условии, что если , Y и У4 - каждьй водород, то используют 2 ыпля безводной соляной кисло- ты на 1 моль соединения общей формул II если YI - водород или хлор, Y - водород, У и У4 вместе образуют связь или если У, и Y вместе образуют связь и Yj и У каждый означает водород, то используют 3 моля безводной соляной кислоты на 1 моль соединения об1чей формулы II; если У, , y,j, У, и У4 вместе образздот соответственно связь, то используют 4 моля безводной соляной кислоты на 1 моль соединения общей формулы II,
производных гексадецена общей формулы 1а или 16
СН,
I
Ci CH2i; CHf 4Hf CH
,xCs
снз .с.
-снгЬсн
С1
СН2,
ную соляную кислоту вводят во взаимодействие с полиеном общей формулы
II
CH
CH.
I
/Ч
.
CH. CH
,2
Приоритеты по к а м:
п р и 3 н а20.09.84 а) если X и Х - водород, У, - хлор, У -2 - водород и У 5 и У 4 вместе образуют связь, то используют 3 моля безводной соляной кислоты на 1 моль соединения общей формулы II; б) если X и Х - водород. У,, У, Уа и У4 вместе соответственно образуют одну связь, то использздот- 4 моля безводной соляной кислоты на 1 моль соединения общей формулы II;

| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Прибор для периодического прерывания электрической цепи в случае ее перегрузки | 1921 |
|
SU260A1 |
| Водоотводчик | 1925 |
|
SU1962A1 |
Авторы
Даты
1988-03-30—Публикация
1985-09-19—Подача