(21)4010535/23-04
(22)22.01.86
(31)8501908
(32)31.01.85
(33)FR
(46) 15.04.88. Бюл. № 14
(71).Санофи (FR)
(72)Ален Бадорк, Даниель Фреэль, Жан-Пьер Маффран и Эрик Балле (FR)
(53)547.82.07(088.8)
(56)Патент Франции № 2495156, кл. С 07 D 495/04, опублик. 1984.
Гетероциклические соединения,/ Под ред. Р.Эльдерфильда. М.: Издательство иностранной литературы, 1953, т. 1, с. 32.1.
Вейданд-Хильгетаг. Методы эксперимента в органической химии. М.: 1968, с. 413-419.
(54)СПОСОБ ПОЛУЧЕНИЯ ПРОИЯВПДНЫХ е/- Г2-ОКСО-2,4,5,,7а-ГЕКСАГИЛРО-5- ТИЕНО-(3,2-е)ПИРЙДИЛ -ФЕНИЛУКСУСНОЙ КИСЛОТЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ
(57)Изобретение касается получения производных пиридина, в частности соединений общей ф-л
где a)Y-OH или OR; R или изо-алкил, (СН 2)11 ,;; п - целое число 1-4; R, и R каждый С t-С -ал- кил, б) Y-NRjR ; RэИ R4 - независимо Н, или изоалкил, -гетеро- аралкил или NRзR -пиppoлидин или мор- фолин Х-Н, С,-С -алкил, галоген, 4 алкоксигруппа, которые ингиби- руют агрегацию тромбоцитов и могут быть использованы в медицине. Цель - создание новых активных веществ указанного класса. Их синтез включает: конденсацию 4,5,6,7-тетрагидротиено (3,2-с) пиридина с (.)3C-Cl в присутствии основания; обработку производным лития BuLi; конденсацию с ал-it килборатом (три-н-бутилборатом); окисление группы ()2B до (R O),B-O-; гидролиз (отщепление (R o)B-гpyппы) сначала водой и экстракцию , а затем гидролиз в кислой среде (98%- ная НСООН) отщепление группы С()эЗ, конденсацию с галоидфенил- уксусным производным в присутствии основания в инертном растворителе при 60 С и выделение целевого продукта, которьш при необходимости гидролизуют в кислой среде (перевод группы OR - ОН) при комнатной температуре или переводят в фармацевтически приемлемые соли. Новые вещества малотоксичны и имеют степень ингибирования агрегации тромбоцитов 46-96%. 3 табл.
I
СО
00
с со а
со
Ы
1
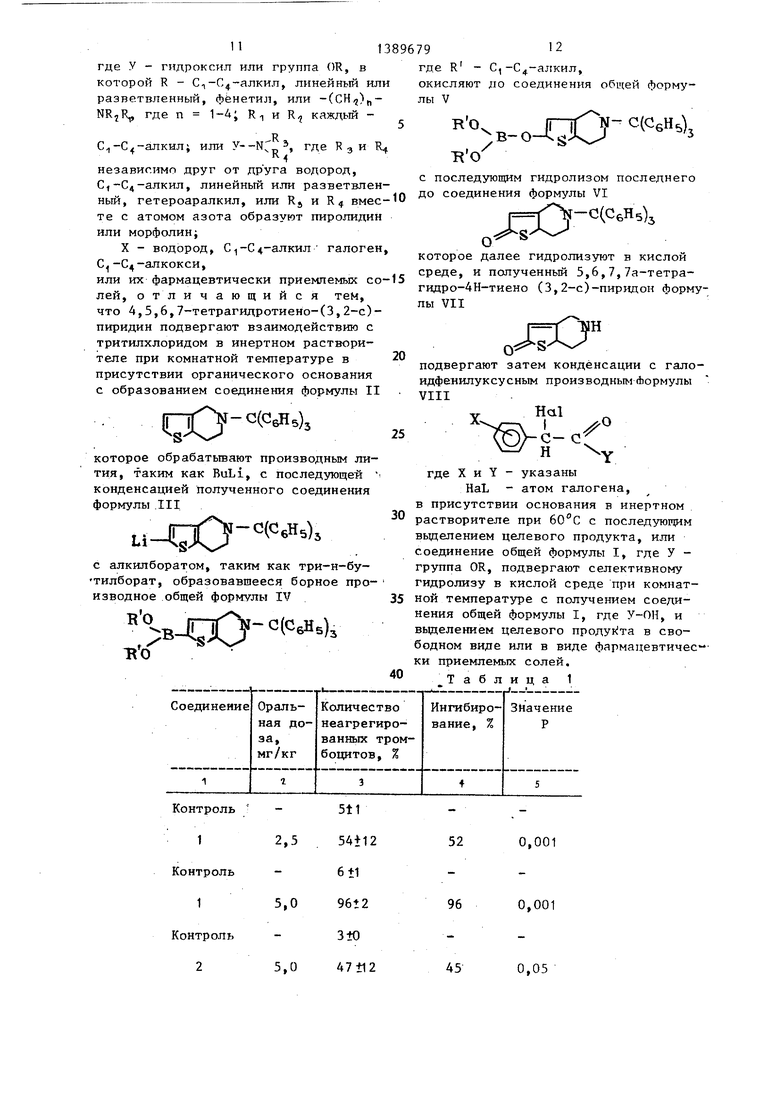
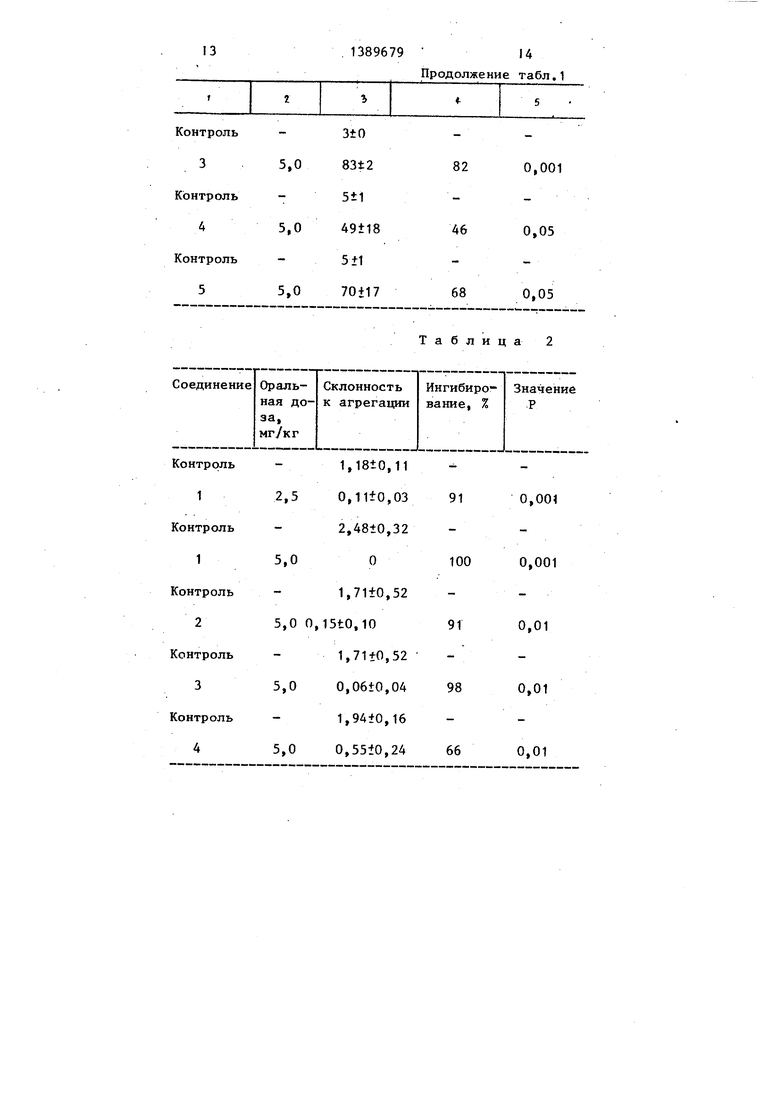
Изобретение относится к химии получения новых производных 5,6,7,7а- тетрагидро-4Н-тиено(3,2-с)пиридона общей формулы
где У - гидроксил или группа OR, в которой R-C,-С4-алкил, линейный или разветвленньш, фенетил, или -(СН)- NRjRi, где п 1-4, каждый
R -С,-С4-алкил; или y--N де Rg и R,
независимо друг от друга - водород, . С,-С4-алкил, линейный или разветвленный, гетероаралкил, или Rg и R4
вместе с атомом азота образуют пир- ролидин или морфолин;
X - водород, С -С4-алкил, галоген, С -С4-алкоксил или их фармацевтически приемлемых солей, обладающих свойствами ингибиторов агрегации тромбоцитов.
Целью изобретения является поиск в ряду производных тиено-(3,2-с)-пи- ридона соединений, обладающий анти- тромботической и антиагрегационной активностью.
Пример 1. 5-Трифенилметил-4, 5,6, 7-тетрагидротиено-.(3, 2-е)пиридин,
К раствору 100 г (0,718 моль) 4, 5,6,7-тетрагидротиено-(3,2-е)пиридина в 200 мл дихлорметана добавляют 80,мл (0,789 моль) триэтиламина, затем по каплям 200,2 г (0,718 моль) трифенилметилхлорида при комнатной температуре. Оставляют реакционную смесь стоять в течение ночи при комнатной температуре. Реакционную смесь выливают в 2000 мл воды, Органичес20 добавляют воду и экстрагируют дихлор- метаном. Органическую фазу экстракции промывают водой и сушат над сульфатом натрия, Вьшаривание растворителя досуха дает остаток, который кристал25 лизуется из диизопропилового эфира. Кристаллы бежевого цвета, т,пл, 210 С (с разложением). Выход 64%,
30
ИК-спектр (КВг): .,675 CM , (СБС1з), м,д,: 7,48-6,96 (мультиплет, 15Н); 6,02 (синглет, 1Н); 4,08 (мультиплет, 1Н)-,3, 78-1,43 (мультиплет, 6Н) ,
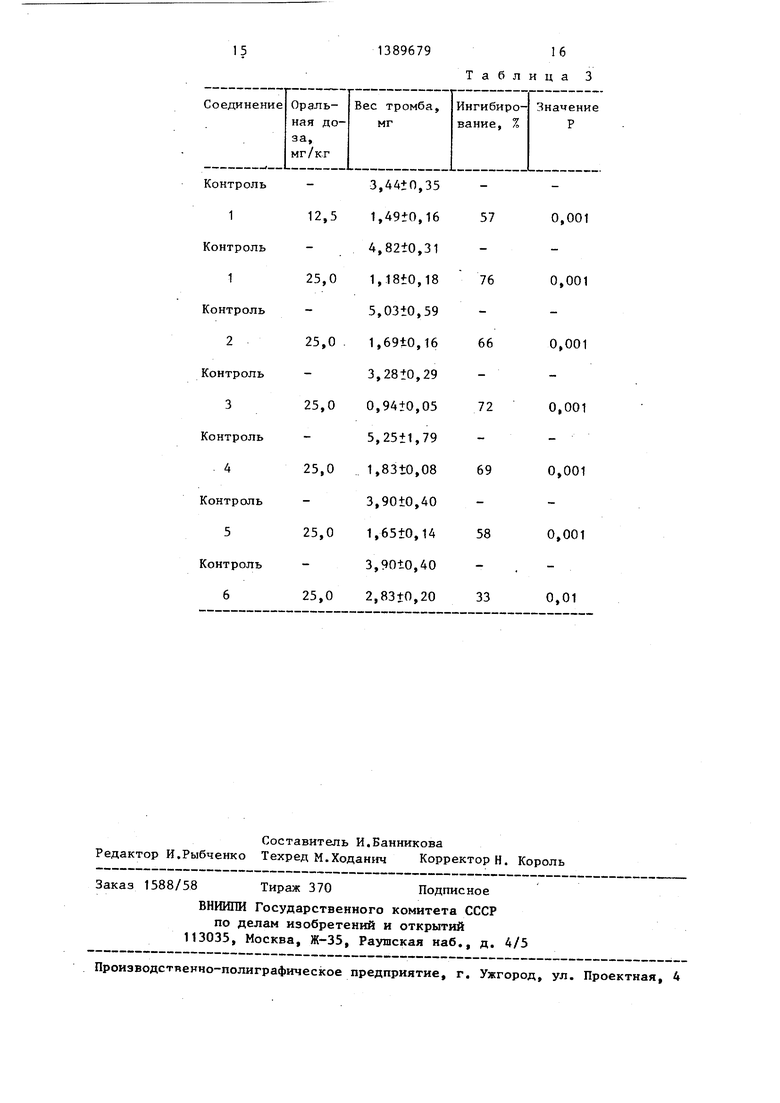
П р.и м е р 3, 5,6,7,7а-Тетра- 2g гидротиено-(3,2-с)пиридон-2 (II),
В течение 1 ч нагревают при 90°С 56,9 г (О,.143 моль) 5-трифенилметил- 5,6,7,7а-тетрагидро-4Н-тиено-(3,2-с) 40 пиридона-2 (VIII) в 350 мл 98%-ной муравьиной кислоты. После охлаждения добавляют избыток насыщенного раствора газообразного хлорводорода в ди- этиловом эфире и реакционную смесь кую фазу декантируют, сушат над суль- .45 концентрируют до 100 мл. Затем добав- фатом натрия и выпаривают досуха. Ос- ляют 1000 мл диэтилового эфира и от
, и
3896792
К раствору 27 г (0,0707 моль) 5- трифенилметил-4,5,6,7-тетрагидротие- но-(3,2-е)пиридина (IV) в 300 мл тетс рагидрофурана прикапывают при 5,31 мл бутшшития (1,6 М раствор в гексане 0,085 моль), перемешивают в течение 15 мин при комнатной температуре, затем охлаждают до и при
10 этой температуре прикапывают 23 мл (0,085 моль) три-н-бутилбората, растворенного в 50 мл тетрагидрофурана. Перемешивают в течение 1 ч при 10°С, После охлаждения реакционной среды до
15 -40 С прикапывают 20,1 мл (Q, 1 77 моль) . 30 об.% перекиси водорода. Оставляют температуру повышаться до комнатной и при этой температуре перемешивают в течение 1 ч, В реакционную среду
20 добавляют воду и экстрагируют дихлор- метаном. Органическую фазу экстракции промывают водой и сушат над сульфатом натрия, Вьшаривание растворителя досуха дает остаток, который кристал25 лизуется из диизопропилового эфира. Кристаллы бежевого цвета, т,пл, 210 С (с разложением). Выход 64%,
30
ИК-спектр (КВг): .,675 CM , (СБС1з), м,д,: 7,48-6,96 (мультиплет, 15Н); 6,02 (синглет, 1Н); 4,08 (мультиплет, 1Н)-,3, 78-1,43 (мультиплет, 6Н) ,
П р.и м е р 3, 5,6,7,7а-Тетра- 2g гидротиено-(3,2-с)пиридон-2 (II),





таток очищают фильтрацией через слой двуокиси кремния (элюирование с помощью дихлорметана), Кристаллы белого цвета, т,пл, 95 с (пастообразно), выход 96%,
(CDC1 з) м,д,: 7,57-6,90, (мультиплет, 15Н); 6,80 (дублет, J :6,5 Гц, 1Н); 6,43 (дублет,,5 Гц, IH); 3,35 (синглет, 14); 3,00-2,33 (мультиплет, 4Н),
Пример 2,5-Трифенилметил- 5,6,7,7а-тетрагидро-4Н-тиено-(3,2-с)- пиридон.
фильтровывают образовавшиеся кристаллы, которые промывают диэтиловым эфиром. Полученные кристаллы снова растворяют в воде и водный раствор после обработки животным углем и фильтрации через слой цеолита, лиофилизи- руют. Таким образом, полученные кристаллы промывают последовательно ацетоном, затем диэтиловым эфиром и высушивают. Кристаллы кремового цвета, т,пл, (с разложением), выход 81%,
ИК-спектр (КВг): (.о 1650 см .
ЯМР- Н (DMCO-dp f м.Д.;6,47 (син- глет, 1Н)- 4,97-4,58 (мультиплет, 1Н)-, 4,46-3,83 (2 дублета, 2Н) .
Пример 4. Метил-у- 2-оксо- , 2,4,6,7,7а-гексагидро-5-тиено-(3,2-с)- пиридилЗ-(2-хлорфенил)-ацетат (I:Y OCHj; ) соедине.ние 1.
К раствору 10 г (0,052 моль) хлор- гидрата 5,6, 7, 7.1-тетрагидро-4Н-тиено- Q (3,2-с)пиридона-2 (II) в 100 мл ди- метилформамида добавляют 10,43 г (0,104 моль) бикарбоната калия и
ОСН,; X 2-Cl i ). Реакционную среду нагревают при 60°С в течение 90 мин. После охлаждения реакционную среду выливают в 600 мл воды. Экстра- 20 гируют этилацетатом, органический экстракт промьшают водой. Органическую фазу сушат над сульфатом натрия, Выпаривание растворителя дает остаток, который очищают фильтрацией че- 25 рез слой диоксида кремния (элюнрова- ние этилацетатом). Полученный маслянистый продукт превращают в хлоргйд- ат для его последней очистки. Хлор- гидрат, кристаллы белого цвета, т.пл. зо 130 С (с разложением), выход 58%.
ИК-спектр (КВг) : Vc-o (сложный : эфир) 1745 см Vc о (тиолактон) 1680 см-
ЯМР- H (DMCO-dj) ,м.д; . 7,43 (мультиплет, 4H)J 6,27 (синглет, 1Н)-, 5,33 и 5,25 (синглет, IH-, 2 диасте- еоизомера); 4,77-4,38 (мультиплет, 1Н)-, 3,67 (синглет, ЗН),
Пример 5, Метил-с/- 2-оксо- ,Q 2,4,5,6,7,7а-гексагидро-5-тиено-(3, 2-с)-пиридил -фенилацетат (I:Y OCHji X Н), соединение 2,
Это соединение получают согласно примеру 4 путем ацилирования 5,6,7, ,с 7а-тетрагидро-4Н-тиено(3,2-с)пиридо- на-2(11) с помощью метил-« -хлорфенил- ацетата (111:У . ОСНз; X Н; Гал. С1), Бромгидрат, кристаллы белого цвета, т,пл. 205°С (с разложением), „ выход 86 %.
ИК-спектр (КВг): Vj.p (сложный эфир) 1745 см , сго тиолактон) 1695 см- ,
ЯМР- Н (DMCO-d) М.Д.: 7,60 (мультиплет, 5H) j 8,57 (синглет, 1Н);
Пример 6. Метил-(/- 2-оксо- 2,4.,5,6, 7, 7а-гексагидро-5-тиено-(3,.
2-е)пиридил -(2-фторфенил)-ацетат (1ГУ OCHj; X 2F), соединение 3,
Это соединение получают согласно примеру 4 путем алкилирования 5,6,7, 7а-тетрагидро-4-Н-тиено-(3,2-е)-пи- ридона-2 (II) с помощью метил-а -хлор- (2-фторфенил)-ацетата (III:Y ОСИ 3; X 2F; Гал. С1).
Бромгидрат, кристаллы белого цвета, т.пл. , выход 70%,
ИК-спектр (КВг): V ( ложный эфир) 1745 , v, (тиолактон) 1690 см- .
ЯМР- H (DMCO-d), м.д; 7,48 (мультиплет, 4Н); 6,43 (синглет, 1Н);5,60 (синглет, 1Н); 4,83-3,37(мультиплет, 3H)i 3,72 (синглет, ЗН).
Пример 7, Этил-о - 2-оксо- 2,4,5,6,7,7а-гексагидро-5-тиено- (3,2-е)-пиридил -(2-хлорфенил)-ацетат (I:Y X 2-Cl), соединение 4,
Это соединение получают согласно примеру 4 путем алкилирования 4,6,7, 7а-тетрагидро-4Н-тиено- (3,2-с)пиридот на-2 (II) с помощью.этил-oi-xлop-(2- хлорфенил)-ацетата (III :Y iOC5H5; X 2-Cl : Гал. Cl),
Бромгидрат, кристаллы белого цвета, т.пл. 200 С, выход 64%.
ИК-спектр {КВг): Vj...g (сложный эфир) 1755 , .д( гколак тон) 1680 см- .
ЯМР- Н (DMCO-d), М.Д.: 7,52 (мультиплет, 4Н); 6,53 (синглет, 1Н); 5,78 (синглет, 1Н)-, 4,30 (мультиплет, 2Н), 1,18 (триплет,-j 7 Гц,
ЗН)..
Пример 8. Этил-о - С2-оксо- 2,4,5,6,7,7а-гексагидро-5-тиено-(3, 2-е)-пиридил -(2-метилфенил)-ацетат (I:Y X 2-СНз), соединение 5,
Это соединение получают согласно примеру 4 путем алкилирования 5,6,7, 7а-тетрагидро-4Н-тиено-(3,2-с)пири- дона-2 (II) с помощью этил-с -хлор- (2-метилфенил)-ацетата (III:Y X 2-СНз, Гал. С1) ,
Бромгидрат, кристаллы белого цве- та, т,.Ш1. 222°С (с разложением), выход 79%,
ИК-спектр (КВг) : Oj..,p(сложный эфир) 1745 см -Jj-.Q (тиолактон)
-1
1685 см
ЯМР- Н (DMCO-d) м.д,: 7,38 (мультиплет, 4Н)-, 6,60 (синглет, 1Н), 5,60 (синглет, 1H)i 4,23 (мультиплет.
2Н), 2,53 (сингл ет, ЗН) ; 1,13 (три- плет, J 7 Гц, ЗН).
Пример 9. Изопропнл-о/- 2- оксо-2,4,5,6,7,7а-гексагидро-5-тиено (3,2-е)пиридилJ-(2-хлорфенил)-ацетат (I:Y ОСН(СНз); X 2-С1), соединение 6.
Это соединение получают согласно примеру 4 путем алкилирования 5,6,7, 7а-тетрагидро-4Н-тиено-(3,2-е)пири- дона-2 (II) с помощью изопропил-с/- хлор-(2-хлорфенил)-ацетата (III:Y OCHCCHj); X 2-Cl, Гал. Cl).
Неполный сульфат, кристаллы беже- вого цвета, т.пл. 110°С, выход 69%.
ИК-спектр (КБг): (сложный эфир) 1750 см , (.о тиолактон) 1690 см- .
ЯМР- и (DMCO-d), М.Д.: 7,50 (муль типлет, 4Н); 6,36 и 6,28 (синглет, 1Н, 2 диастереоизомера); 5,36и5,28 (синглет, 1Н, 2 диастереоизомера)-j 1,33-0,87 (мультиплет, 6Н).
Пример 10. Трет-бутил-(/- С 2-оксо-2,4,5,6,7,7а-гексагидро-5- тиено-(3,2-е)пиридилJ-(2-хлорфенил)- ацетат (I:Y ОС(СНз)з; X 2-С1), соединение 7.
Это соединение получают согласно примеру 4 путем алкилирования 5,6,7, 7а-тетрагидро-4Н-тиено-(3,2-с)пири- дона-2(11) с помощью трет-бутил-с/-. хлор(2-хлорфенил)-ацетата (III:Y ОС(СНз)з; X 2-С1; Гал, С1).
Маслянистое основание, выход 69%. .
, ИК-спектр (пленка): J.Q(сложный эфир) 1740 см ,(,(т11олактон ) 1690 см-Ч
ЯМР
и (DMCO-d), М.Д.: 7,36 (мультиплет, 4Н); 6,02 (синглет, 1Н); 4,63 (синглет, 1Н) 4,76-4,13 (мультиплет, 1Н)-, 1,40 (мультиплет, 9Н) .
Пример 11. М- о/ 2-Окео-2,4, 5,6,7,7а-гексагидро-5-тиено-(3,2-е)- пиридилЗ-(2-хлорфенил)} ацетилпирролиОдин (I:Y ,), соединение 8.
К раетвору 4,5 г (0,023 моль) хлоргидрата 5,6,7,7а-тетрагидро-4Н- тиено-(3,2-е)пиридона-2 (II) в 45 мл диметилформамида добавляют 4,7 г (0,047 моль) бикарбоната калия, затем -3,5 г (0,023 моль) иодида натри К этой реакционной среде добавляют 6,1 г (0,023 моль) 0 -хлор-(2-хлорфенил)-ацетилпирролидина (III:Y
t
Х 2-С1, Гал, С1), и все
0
реагенты выдерживают при в течение 2 ч. После охлаждения добавляют этилацетат . Органический раствор промывают водойJ затем сушат над сульфатом натрия. Выпаривают досуха и остаток очищают над сульфатом натрия. Выпаривают досуха и остаток очищают путем фильтрации через слой диоксида кремния (элюент - этилацетат) , Последняя очистка осуществляется путем превращения в хлоргидрат в диэтиловом эфире.
Хлоргидрат, кристаллы белого цвета, т.пл. , выход 69%. .
ИК-спектр (КВг) : v c o (тиолактон) 1690 ей- , % с,о(амид) 1650 см .
ЯМР- H (СВС15),м.д.: 7,31 (мультиплет, 4Н); 5,90 (синглет, 1Н); 4,90 (синглет, 1Н).
Пример 12. Ы,М-Диметил- /- С2-оксо-2,4,5,6,7,7а-гексагидро-5- 5 тиено-(3,2-е)пиридил -(2-хлорфенил)- ацетамид (I:Y ,N(.CK )j ; X 2-Cl), соединение 9,
Это соединение получают согласно примеру 11 путем алкилирования 5,6, 7,7а-тетрагидро-4Н-тиено-(3,2-е)пи- ридона-2(11) с помощью of -xлop-N,N диметил-(2-хлорфенил)-ацетамида. (III: :Y N(CH)jL ;;Х 2-Cl; Гал. С1).
0
35
Хлоргидрат, кристаллы белого цвета, т.пл. 145°С. Выход 73%.
ИК-спектр (KBr) (тиолактон) 1690 . (амид 1655 ем-
ЯМР- H (DMCO-dj)., м.д. : 7,70 (муль- типлет, 4Н)-, 6,08 и 6,00 (еинглет, 1Н, 2 диастереоизомера), 2,93 (еинглет, 6Н) .
Пр.им ер 13. (2-Фенилэтил) Г2-окео-2,4,5,6,7,7а-гекеагидро-5- тиено(3,2-с)пиридил -(2-хлорфеНил)- ацетат (15 OCHjCH C Hj; X 2-Cl),
Это соединение получают еоглаено примеру 4 путем алкилирования 5,6,7, 7а-тетрагидро-4Н-тиено-(3,2-е) пири- дона-2 (II) е помощью (2-фенштэтил)- 0/-хлор-(2-хлорфенил)-ацетата :(Т11:У ; OCHsCHiC Hs; X 2-Ci; Гал. С1).
Хлоргидрат, криеталлы бежевого цвета, т.пл. 175°С (ацетон), выход 71%.ИК-епектр (КВг): V сложный эфир) 1755 см , -Oj.-о (тиолактон) 1690 см
ЯМР- Н (DMCO-dj) М.Д.: 7,80-6,83 (мультиплет, 9Н, ароматические); 6,28 (синглет, 1Н), 5,46 и 5,28 (син- глет, 1Н, 2 диастересизомера).
Пример 14. Ы-(/-Г2-Оксо- 2,4,6,7,7а-гексагидро-5-тиено-(3,2-с)- пиридил -(2-хлорфенил)} ацетилморфолин (I;Y М Otx 2-С1).
Это соединение получают согласно примеру 11 путем алкилирования 5,6, 7,7а-тетрагидро-4Н-тиено-(3,2-с)пи- ридина-2 (II) с помощью с/-хлор-(2- хлорфенил)-ацетилморфолина (III:Y
2-Cl Гал.. Cl).
Хлоргидрат, гидрат, кристаллы белого цвета, т.пл. 150°С, выход 60%
ИК-спектр (КВг) : (тиолактон) 1690 см- , ) 1660 см-
ЯМР- (DMCO-dt), М.Д.: 7,51 (мультиплет, 4Н)-, 6,45 и 6,26 (синглет, 1Н, 2 диастереоизомера)j 4,86 и 4,73 (синглет, 1Н, 2 диастер еоизоме- ра). ,
Пример 15. К-(3-Пиридш1ме- тил)-о/- 2-оксо-2,4,5,6,7,7а-гексагид- ро-5-тиено (3,2-с)пиридил -(2-хлор-
фенил) -ацетамид (I:Y .TJHCH о- V; X 2-С1). - -VNV
Это соединение получают согласно примеру 11 путем алкилирования 5,6,7, 7а-тетрагидро-4Н-тиено(3,2-е)пиридо- на-2 (II) с помощью (/-хлор-К-(3-пири- дилметил)-(2-хлорфенил)-ацетамкда I . , . (III:Y NHCH2- 2-С1; Галр С1). : . N
Хлоргидрат, гидрат, кристаллы бежевого цвета, т.тш, 165 С выход 55%.
ИК-спектр (КВг): (тиолактон) 1690 1660 см- .
ЯМР- Н (DMCO-d)g М.Д.: 8,95-7,38 (мультиплет, 8Н); 6,38 и 6,32 (синглет, 1Н, 2 диастереоизомера) , 5,52 и 5,43 (синглет, 1Н, 2 диастереоизо- мера).
Пример 16. Этил-о( -С2-оксо- .2,4,5,6,7,7а-гексагидро-5-тиено-(3, 2-е)пиридил -(4-метоксифеНИЛ)-ацетат (I,:Y X 4-ОСНз).
Это соединение получают согласно примеру 4 путем алкилирования 5,6,7, 7а-тетрагилро-4-Н-тиено-(3,2-с)пи- ридона-2(11) с помощью этил-с/-хлор
10
15
20
30
0
5
O
5
(4-метоксифенил)-ацетата (llliY OCjEsl Х 4-ОСНз; Гал, С1).
Хлоргидрат, кристаллы белого цвета, т.пл. 140°С, выход 91%.
ИК-спектр (КВг): J(..o( эфир) 1715 см ; V(- д(тиолактон) 1690 см .
ЛИР- Н (DMCO-d), М.Д.: 7,65 (мультиплет, 4Н)j 6,53 и 6,61 (сии- глет, 1Н, 2 диастереоизомера); 5,73 и 5,63 (синглет, 1Н, 2 диастереоизо- мера); 3,80 (синглет, ЗН).
Пример 17. 2-(К,Н-Диэтилами- но)-этил- /- 2-ОКСО-2,4,5,6,7,7а-тек- caгидpo-5-тиeнo-(3,2-c)пиpидилJ-(2- хлорфенил)-ацетат (I:Y . N()J ;. X 2-С1).
Это соединение получают согласно примеру 4 путем алкилирования 5,6,7, 7а-тетрагидро-4Н-тиено-(3,2-е)пиридо- на-2 (II) с помощью 2-(N,N-диэтил- амино)-этил-а;-хлор-(2-хлорфенил)- а.цетата (III:Y ( g ); X 2-Cl, Гал, Cl). Оксалат, кристаллы бежевого цвета, т.пл. , выход 61%.
ИК-спектр: (КВг): (сложный эфир) 1745 см , Vc-o (тиолактрн) 1685 см- .
(DMCO-dg), М.Д.: 7,64- 7,25 (мультиплет, 4Н); 6,23 (синглет, 1Н); 4,94 (синглет, 1Н).
Прим е р 18. (/- 2-Оксо-2,4, 5,6,7,7а-гексагидро-5-тиено-(3,2-е) пиридил}-(2-хлорфенил) -ацетамид (I:Y Шз; X 2-С1).
Это соединение получают согласно примеру 11 путем алкилирования 5,6,7, 7а-тетрагидро-4Н-тиено-(3,2-с)пиридо- на-2 (II) с помощью о(-хлор-(2-хлорфенил )-ацетамида (III:Y X 2-Cl, Гал Cl).
Хлоргидрат, кристаллы бежевого цвета, т.пл. 185°С, выход 53%.
ИК-спектр (КВг): (тиолактон) 1685 см- ; ,..д(амид) 1640 см .
Фармакологические и токсикологические результаты. Которые приведены ниже, демонстрируют свойства соединений общей формулы I как в плане токсичности и толерантности, так и в плане их активности (ингибирование агрегации тромбоцитов и антитромбо- тические свойства).
Токсикологические исследования.
Соединения по предлагаемому способу обладают малой токсичностью. Опыты осуществленные на острую, хроническую, субхрон ческую и пролонгированную токсичности на различных видах животных, не позволяют, выявить какую-либо локальную или общую реакцию, расстройство или аномалию в биохимических, макроскопических или микроскопических испытаниях.
Активность соединений как ингибиторов агрегации тромбоцитов.,
Эксперимент осуществляют на крысе, которая получала перорально соеЭтот метод состоит в адаптации метода Friedman и др, (Ам,J.Physiol 1980, 199, 770-774), Разрезанная ме таллическая спираль (bourre - паста дантиста) помещается в нижнюю полую
динение.I, Берут на анализ 4 мл крови по способу Renaud из яремной вены анестезированного животного. Эту цит-|5 вену крысы, которая получает за 2 ч ратированную кровь используют при из-. До этого перорально испытуемое соемерениях агрегации.
Измерение агрега11;ии тромбоцитов с аденозиндифосфатом (АДФ),
2 мл цитратированной крови быстро вьшивают в маленький стаканчик, помещенный на магнитную мешалку и снабженный магнитным стержнем. После перемешивания в течение нескольких
секунд в стаканчик вводят 0,4 мп ра- 25 затем освобождают от тромба, высуши35
40
створа, содержащего 0,66 г АДФ на 1 мл. После перемешивания в течение 90 с осуществляют два отбора по 0,5 мл крови: первый смешивают с 0,5 мл раствора ЭДТК-формол, второй смешивают с 0,5 мл раствора только
эдтк,
Целью добавления ЭДТК-формола явля-- ется стабилизация крови и, следовательно, фиксация агрегации, в то время как ЭДТК, напротив, вызьшает дезагрегацию всех тромбоцитных скоплений.
После стояния в течение 10 мин, центрифугирования 2 смесей с медленной скоростью в течение 5 мин и отделения красных глобул надосадочнук плазму, обогащенную тромбоцитами (пот), отбирают, разбавляют и подсчитывают количество тромбоцитов, д5
вают и снова взвешивают. Таким образом получают разницу, т,е, средний вес тромба,
Антиагрегирующая активность соеди- 30 нений по отношению к АДФ и коллагену приведена в табл, 1 и 2 соответственно, антитромботическая активность в 1одели витка - в табл, 3,
Соединения по патенту Франции № 2495156 при дозе 5 мг/кг достигают активности ингибирования лишь 47-48%,
Соединения по патенту Франции № 2495156 при дозе 5 мг/кг достигают лишь 17,4% ингибирования.
Как видно из представленных в таблицах данных, предлагаемый способ позволяет получить соединения, обладающие комплексом ценных фармакологических свойств.
Интенсивность агрегации определяется отношением числа тромбохщтов в ЭДТК-формоле к числу тромбоцитов в ЭДТК и выражается в процентах неагрегированных тромбоцитов,
Измерение агрегации тромбоцитов с коллагеном,
К 1,5 мл цитратированной крови добавляют О,10 мл раствора, содержащего 10 мкг коллагена на 1 мл. Среду выдерживают при перемешивании, подсчет числа тромбоцитов осуществляют без перерыва.
o
9679 ,0
Уменьшение числа свободных тромбоцитов в зависимости от времени непрерывное и позволяет изрисовать кривую, наклон которой дает начальную скорость агрегации,
Антитромботическая активность изучается согласно методу венозного тромбоза с витком.
Этот метод состоит в адаптации метода Friedman и др, (Ам,J.Physiol, 1980, 199, 770-774), Разрезанная металлическая спираль (bourre - паста дантиста) помещается в нижнюю полую
5 вену крысы, которая получает за 2 ч До этого перорально испытуемое соединение в виде суспензии в 10 мг/кг водного 5%-ного раствора гуммиарабика.
Спустя 5 ч эту спираль извлекают вместе с тромбом, которьй она удерживает, осторожно высушивают последовательными тампонациями на фильтровальной бумаге и взвешивают, Спираль
вают и снова взвешивают. Таким образом получают разницу, т,е, средний вес тромба,
Антиагрегирующая активность соеди- нений по отношению к АДФ и коллагену приведена в табл, 1 и 2 соответственно, антитромботическая активность в 1одели витка - в табл, 3,
Соединения по патенту Франции № 2495156 при дозе 5 мг/кг достигают активности ингибирования лишь 47-48%,
Соединения по патенту Франции № 2495156 при дозе 5 мг/кг достигают лишь 17,4% ингибирования.
Как видно из представленных в таблицах данных, предлагаемый способ позволяет получить соединения, обладающие комплексом ценных фармакологических свойств.
Формула изобретения
Способ получения производных о/ - 2-оксо-2,4,5,6,7,7а-гексагидро-5- тиено-(3,2-е)пиридил J-фенилуксусной кислоты общей формулы I
55
./Л-§
(TnQf- С(СбН5),
30
которое обрабатывают производным лития, таким как BuLi, с последующе-й конденсацией полученного соединения формулы .III
алкилборатом, таким как три-н-бу- тилборат, образовавшееся борное про- изводное общей формулы IV35
В Б О
V-JQO
2,5
5,0
511
54112
611
9612
ЗЮ
5,0
47±12
Hal
25
где X и Y - указаны
HaL - атом галогена, в присутствии основания в инертном растворителе при 60°С с последуюпсим выделением целевого продукта, или соединение общей формулы I, где У - группа OR, подвергают селективному гидролизу в кислой среде при комнатной температуре с получением соединения общей формулы I, где У-ОН, и вьщелением целевого продукта в свободном виде или в виде фармацевтичес ки приемлемых солей. Таблица 1
52
0,001
96
0,001
45
0,05
-1,1810,11
2,50,11tO,03910,001
-2,4810,32-5,0 О1000,001 -1,71+0,52-5,0 0,15tO,10910,01 -1,7110,52
5,00,06tO,04980,01 -1,9410,16
5,00,5510,24660,01
Таблица 2
5
138967916
Таблица 3
Авторы
Даты
1988-04-15—Публикация
1986-01-22—Подача