1
Изобретение относится к биохимии и медицине, касается количественного определения гликозилированных белков крови и может быть использовано при проведении биохимических анализов в лабораторной медицинской практике.
Цель изобретения - повышение чувствительности и упрощение способа.
На чертеже изображен предлагаемый способ.
Способ определения гликозилированных белков крови осуществляют следующим образом.
Готовят анализируемую белковую пробу, в которой необходимо определить концентрацию гликозилированных белков. Производят отделение белков ОТ избытков сахара и других низкомолекулярных соединений методом гельфильтрации на колонке с сефадексом G-25. Собранную белковую фракцию разбавляют 0,05 М Na-фосфатным буфером, рН 6,8, до конечной концентрации. - 10 М. Концентрацию белка определяют спектрофотометрически. К белковой пробе добавляют 100-кратный избыток перйодата калия (KJO) для окисления углеводных остатков и выдерживают 20 - 30 мин. При окислении глюкозы, связанной с белком, образуется остаток глюкозы, содержащий альдегидную группу. Затем добавляют 100-кратный молярный избыток пиридок- самина НС1, который формирует с альдегидной группой остатка глюкозы, основание Шиффа. Через 13-17 мин после формирования основания Шиффа добавляют 1000-кратный избыток бор4
а СП
о о
31465766
1гидрида натрия (NaBH4.), в результате: чего происходит восстановление нестабильного аддукта (основания Шиф- фа), приводящее к ковалентному связыванию пиридоксамина с белком через остаток глюкозы.
Через 1 - 2 ч производят отделе- ние .избытка пиридоксамина НС1 и друПример 1. Сывороточный альбумин человека фирмы Reanal .(ВИР), концентрацией. 10 М инкубируют в течение 5 сут при 37°С в водном растворе Д-глюкозы концентрацией 10 М. После инкубации отбирают аликвоты в количестве 1 мл и на колонке с сефа- дексом G - 25 производят отделение
НИе ИЗОЬПКа llИpиM - - - - ,-.1гих низкомолекулярных соединений од- ю свободной и лабильносвязаннои глюконим из известных методов отделения сахароз от белков (гельфильтрация, диализ, осаждение ТХУ и т.д). Собирают белковую пробу и измеряют интен- сивности флуоресценции не. длине волны 390 - 410 нм при длине волны возбуждающего света 325 - 335 нм.
Концентрация пиридоксамина, кова- лентно свя-занного с белком, соответствует концентрации глюкозы в составе макромолекулы при условии полного окисления перйодатом калия углеводных остатков и достаточно высоких концентрациях пиридоксамина.
зы. Собранную белковую фракцию разбавляют 0,05 Na-фосфатным буфером, рН 6,8, до конечной концентрации , 10 и 10 М. Концентрацию белка оп- 5 ределяют спектрофотометрически, учитывая,, что 0,1%-ньш раствор сьюоро- точного альбумина человека имеет оптическую плотность 0,54 при 278 нм. К белковой пробе последовательно добавляют 100-кратньш избыток перйодата калия, вьщерживают 25 мин, затем добавляют 100-кратный избыток пиридоксамина НС1 и через 15 мин (после фор мирования основания Шиффа) добавляют
20
25 избыток (2 мг) боргидрида натрия. Так как флуоресценция пиридоксами- Через 1,5 ч производят отделение изна, свободного и связанного с белком, существенно не различается, то для определения концентрации глюкозы,. связанной с белком, строят калибро- зО вочньй график зависимости интенсивности флуоресценции свободного пиридоксамина от его концентрации.
По оси абсцисс откпадьшают коли- .чественные значения свободного пири- g доксамина НС1 в молях, а по оси ординат - знач-ения интенсивности флуоресценции свободного пиридсксамина НС1, измеренные на спектрофлюориметре Aminco - Bonmiari (США) в относитель- д ных едишцах. При этом используют длину возбуядйющего света 330 нм, а регистрацию ведут на маьгсимуме флу- .оресценции - 400 нм« Учитывая, что квантовый выход флуоресценции свобод- ног-о Шридоксамина практически соот- - :Ветствует квантовому выходу флуорес- ценции пиридоксамина, кб:валентно связанного с белком через остаток сахара, измеряют интенсивность флуорес- g ценции белковой пробы и по калибровочному графику через интенсивность флуоресценции определяют по оси абсцисс концентрацию пиридоксамина, ковалентно связанного с белком черкез . gg ;ООтаток сахара. Определенная таким образом концентрация пиридоксамина соответствует искомой концентрации гликозшгарованного белка.
бытка пиридоксамина НС1 и .других низкомолекулярных соединений на ко лонке с сефадексом G - 25. Собирают белковую пробу в концентрации 1 - 2 М„ Измеряют интенсивность флуоресценции на максимуме - 400 нм при длине волны возбуждающего света 330 н Искомую концентрацию гликозилирован- .ного белка в пробе определяют по калибровочному графику через интенсивность флуоресценции.
Пример 2. Плазму больных сахарным диабетом получают из цельной крови центрифугированием при 3000 об/мин. Для отделеш я избытка сахара и- других низкомолекулярных соединений плазму в количестве 0,4 мл наносят на колонку с сефадексомС-25 Собранную белковую фра.кцию разбавляю 0,03 Na-фосфатным буфером, рН 6,8, до конечной концентрации 1-2 , Концентрацию плазмы определяют спект рофотометрически, считая, что М мг плазмы человека в 1 i-ш Na-фосфатного буфера, рН 6,8, имеет оптическую плотность О,.69 при 278 н:м. К плазме добавляют 100-кратньй избыток перйодата калия, вьщерживагат 25 мин, затем добавляют 100-кратный молярньш избыток пиридоксашна НС1 и через 15 ми .(после формирования основания Шиффа добавляют 2 мг (100-кратный избыток боргидрида натрия. Через 1,5 ч прои
66
Пример 1. Сывороточный альбумин человека фирмы Reanal .(ВИР), концентрацией. 10 М инкубируют в течение 5 сут при 37°С в водном растворе Д-глюкозы концентрацией 10 М. После инкубации отбирают аликвоты в количестве 1 мл и на колонке с сефа- дексом G - 25 производят отделение
свободной и лабильносвязаннои глюкозы. Собранную белковую фракцию разбавляют 0,05 Na-фосфатным буфером, рН 6,8, до конечной концентрации , 10 и 10 М. Концентрацию белка оп- ределяют спектрофотометрически, учитывая,, что 0,1%-ньш раствор сьюоро- точного альбумина человека имеет оптическую плотность 0,54 при 278 нм. К белковой пробе последовательно добавляют 100-кратньш избыток перйодата калия, вьщерживают 25 мин, затем добавляют 100-кратный избыток пиридоксамина НС1 и через 15 мин (после фор мирования основания Шиффа) добавляют
избыток (2 мг) боргидрида натрия. Через 1,5 ч производят отделение избытка пиридоксамина НС1 и .других низкомолекулярных соединений на ко лонке с сефадексом G - 25. Собирают белковую пробу в концентрации 1 - 2 М„ Измеряют интенсивность флуоресценции на максимуме - 400 нм при длине волны возбуждающего света 330 нм Искомую концентрацию гликозилирован- .ного белка в пробе определяют по калибровочному графику через интенсивность флуоресценции.
Пример 2. Плазму больных сахарным диабетом получают из цельной крови центрифугированием при 3000 об/мин. Для отделеш я избытка сахара и- других низкомолекулярных соединений плазму в количестве 0,4 мл наносят на колонку с сефадексомС-25. Собранную белковую фра.кцию разбавляют 0,03 Na-фосфатным буфером, рН 6,8, до конечной концентрации 1-2 , Концентрацию плазмы определяют спектрофотометрически, считая, что М мг плазмы человека в 1 i-ш Na-фосфатного буфера, рН 6,8, имеет оптическую плотность О,.69 при 278 н:м. К плазме добавляют 100-кратньй избыток перйодата калия, вьщерживагат 25 мин, затем добавляют 100-кратный молярньш избыток пиридоксашна НС1 и через 15 мин .(после формирования основания Шиффа) добавляют 2 мг (100-кратный избыток) боргидрида натрия. Через 1,5 ч производят отделение избытка пиридоксами- на НС1 и других низкомолекулярных соединений на колонке с сефадексом . G - 25. Собирают белковую фракцию в концентрации I-Z-IO M и измеряют ий-- тенсивность флуоресценции ( Лре - : 400 нм, Лв„5 330 нм). Искомую концентрацию гликознлированных белков
дата, пиридоксамина и боргидрида натрия с последующим графическим определением количества гликозилировал- ных белков в пробе по интенсивности флуоресценции на длине волны 390- 4 to нм при длине возбуждающего света 325 - 335 нм. .
Упрощение определения при осуществ пробе определяют по калибровочному ю влении предлагаемого способа обеспе- графику через интенсивность флуорес- чивается тем, что известный способ ценции.
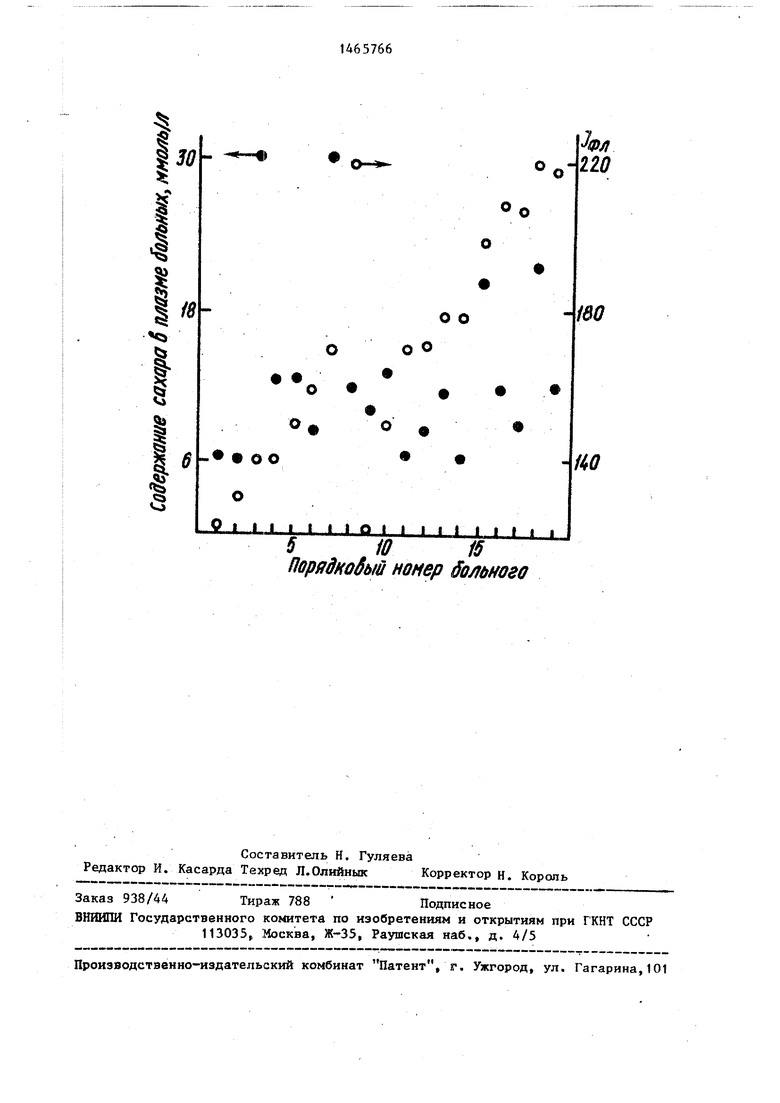
При постановке опыта (пример 2) одновременно сравнивают количество глипредусматривает приготовление анализируемой пробы, отделение белков от Сахаров, обработку их щавелевой кискозилированных белков плазмы, рпреде- 5 лотой, кипячение в течение 24 ч, охляемых с помощью пиридоксамина у больных сахарным диабетом, с уровнем свободного сахара в плазме крови больных (см. чертеж).
Для этого строят график, где по левой оси ординат откладьюают концентрацию свободного сахара в плазме больных в ммоль/л, по правой оси ординат - интенсивность флуоресценции ; пиридоксамина, связанного с белками плазмы, в относительных единицах при
20
boat
330 нм и
А per нм
лаждеяие белков трихлоруксусной кислотой, добавление к надосадочной.жидкости тиобарбитуровой кислоты и спек- трофотометрирование, в то время как предлагаемый способ облегчает определение за счет устранения ряда операций - кипячения, охлаждения белков что позволяет уменьшить время определения до 2-3 ч при исследовании каж- 25 дой пробы по сравнению с 26 - 30 ч при использовании способа-прототипа определении гликозилированных белков
оси абсцисс обозначены порядковые номера больных, взятых для обследования (всего 19 больных).
Точками показаны значения концентрации свободного сахара в .плазме, знаком о - интенсивность флуоресценции. Уровень сахара в плазме fSpnb- ных определяют 0-толуидиновым мето- ,дом. С увеличением количества кова- леитно связанной с белками плазмы глюкозы и, соответственно, количест-; вом связавшегося с ней пиридоксамина, возрастает интенсивность флуоресценции :
Предлагаемьй способ по сравнеш1Ю с известным повьшиет чувствительность определения более, чем на 2 за счет использования в качестве реагентов для обработки белков в приготовленной анализируемой пробе перйог
30
35
Формула изобретения
Способ определения гликозилирован ных белков крови,включающий приготовле ние анализируемой пробы и отделение бел ков от Сахаров с последующей обработ кой их химическими реагентами и коли чественной оценкой, отличающийся тем, что, с целью повышени чувствительности и упрощения способа пробу белка берут в концёнтрахйш 10 10 М, обрабатывают последовательно перйодатом, пиридоксамином и боргид- ридом натрия при мсхпярном соотношени белок пробы химические реагенты соответственно 1:100:100:1000, а количество гликозилированных белков определяют флуоримётрически на длине f волны флуоресценции 390 - 410 нм, пр длине возбудцающего света 325 - 335 нм
40
5766
дата, пиридоксамина и боргидрида натрия с последующим графическим определением количества гликозилировал- ных белков в пробе по интенсивности флуоресценции на длине волны 390- 4 to нм при длине возбуждающего света 325 - 335 нм. .
Упрощение определения при осуществлении предлагаемого способа обеспе- чивается тем, что известный способ
предусматривает приготовление анализируемой пробы, отделение белков от Сахаров, обработку их щавелевой кислотой, кипячение в течение 24 ч, ох
лаждеяие белков трихлоруксусной кислотой, добавление к надосадочной.жидкости тиобарбитуровой кислоты и спек- трофотометрирование, в то время как предлагаемый способ облегчает определение за счет устранения ряда операций - кипячения, охлаждения белков, что позволяет уменьшить время определения до 2-3 ч при исследовании каж- дой пробы по сравнению с 26 - 30 ч при использовании способа-прототипа определении гликозилированных белков.
Формула изобретения
Способ определения гликозилированных белков крови,включающий приготовление анализируемой пробы и отделение белков от Сахаров с последующей обработкой их химическими реагентами и количественной оценкой, отличающийся тем, что, с целью повышения чувствительности и упрощения способа, пробу белка берут в концёнтрахйш 10 М, обрабатывают последовательно перйодатом, пиридоксамином и боргид- ридом натрия при мсхпярном соотношении белок пробы химические реагенты соответственно 1:100:100:1000, а количество гликозилированных белков определяют флуоримётрически на длине волны флуоресценции 390 - 410 нм, при длине возбудцающего света 325 - 335 нм.
п .
порйокооый номер больного


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОРОФОРМИРОВАНИЯ В МЕМБРАНАХ КЛЕТОК ПЕЧЕНИ С ПОМОЩЬЮ ОБРАБОТКИ ИХ ГЕМОЛИЗИНОМ II Bacillus cereus | 2012 |
|
RU2504389C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЛИПОПОЛИСАХАРИДОВ | 1993 |
|
RU2077723C1 |
| Способ определения эффективности гемосорбции | 1989 |
|
SU1818586A1 |
| СПОСОБ ВЫЯВЛЕНИЯ ВЛИЯНИЯ НИЗКОМОЛЕКУЛЯРНЫХ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ НА КОНФОРМАЦИЮ БЕЛКА | 2019 |
|
RU2698628C1 |
| Азопроизводные 5-аминосалициловой кислоты, обладающие способностью ингибировать образование конечных продуктов гликирования | 2024 |
|
RU2837878C1 |
| Способ получения водосодержащей суспензии частиц, состоящих из антиоксидантного фермента супероксиддисмутазы, поликатиона и полианиона | 2019 |
|
RU2709536C1 |
| Композиция, снижающая окислительный стресс в глазу | 2019 |
|
RU2733928C2 |
| НОВЫЙ КЛАСС ФИЗИОЛОГИЧЕСКИ АКТИВНЫХ ГЛИКОПРОТЕИНОВ | 2000 |
|
RU2223781C2 |
| СОРБЕНТ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1996 |
|
RU2094117C1 |
| N-КОНЦЕВОЕ ПОЛИСИАЛИЛИРОВАНИЕ | 2007 |
|
RU2432175C2 |
-Изобретение относится к медицине и может быть использовано для проведения биохимических анализов в клинике и эксперименте. Цель изобретения - повышение чувствительности и упрощение способа. Способ состоит в том, что в анализируемой пробе проводят отделение белков от избытка низко- молекулярных соединений, белковую фракцию разводят в 0,05 М Na-фосфат- ном буфере, рН 6,8, до конечной концентрации 10 - 10 М. Пробу последовательно обрабатьшают перйодатом калия, пиридоксамином и боргидридом натрия при молярном соотношении белка и химических реагентов соответст- венно 1:100:100:1000. Содержание гликозилированных белков определяют флу- ориметрически при длине волны флуоресценции 390-410 нм и длине волны возбузкдающего света 325-335 нм. Предлагаемый способ прост (время определения 2-3 ч) обладает высокой чувствительностью. 1 ил. (Л

| Способ определения в крови гликозилированных соединений,содержащих кетоаминовую связь | 1986 |
|
SU1363072A1 |
Авторы
Даты
1989-03-15—Публикация
1986-11-14—Подача