Изобретение относится к усовершенствованному способу получения (i)За,6,6,9а-тетраметилпергидронаф-. то 2,1-в фурана ((+) амброксида), который обладает душистыми свойствами и находит применение в парфюмерной промьшшенности.
Цель изобретения - упрощение процесса и повьпиение выхода целевого продукта за счет восстановления б, - -гомофарнезиловой кислоты алюмогидридом лития и последующей циклизацией 5, -гомофарнезола в присутст- ВИИ фторсульфоновой кислоты при молярном соотношении, равном 1:10-15 соответственно в среде 2-ниТропропа- на при (-80)-(-90) С.
Пример 1. Получение исходного Е,- -гомофарнезола.
К раствору 800 мг (3,2 ммоль) б,-гомофарнезиловой кислоты в 10 мп абсолютного эфира добавляют 240 мг (6,31 ммоль) алюмогидрида лития. Реакционную смесь кипятят с обратным холодильником в течение 3 ч. Избыток алюмогидрида лития разлагают 5 мл этилацетата. Затем к смеси добавляют 15 МП 10%-ного раствора серной кислоты и экстрагируют эфиром (3x10 мп) Эфирный экстракт промывают водой (2x10 мл), насьш енным раствором бикарбоната натрия (10 мп), снова водой (10 мп), сушат над безводным сульфатом натрия и растворитель отгоняют. Получают 702 мг (выход 93%) ,-гомофарнезола. i К раствору 33 мг (0,14 ммоль) ,Б-гомофарнезола в 0,3 мп 2-нитро4
:о эо
Old
314987
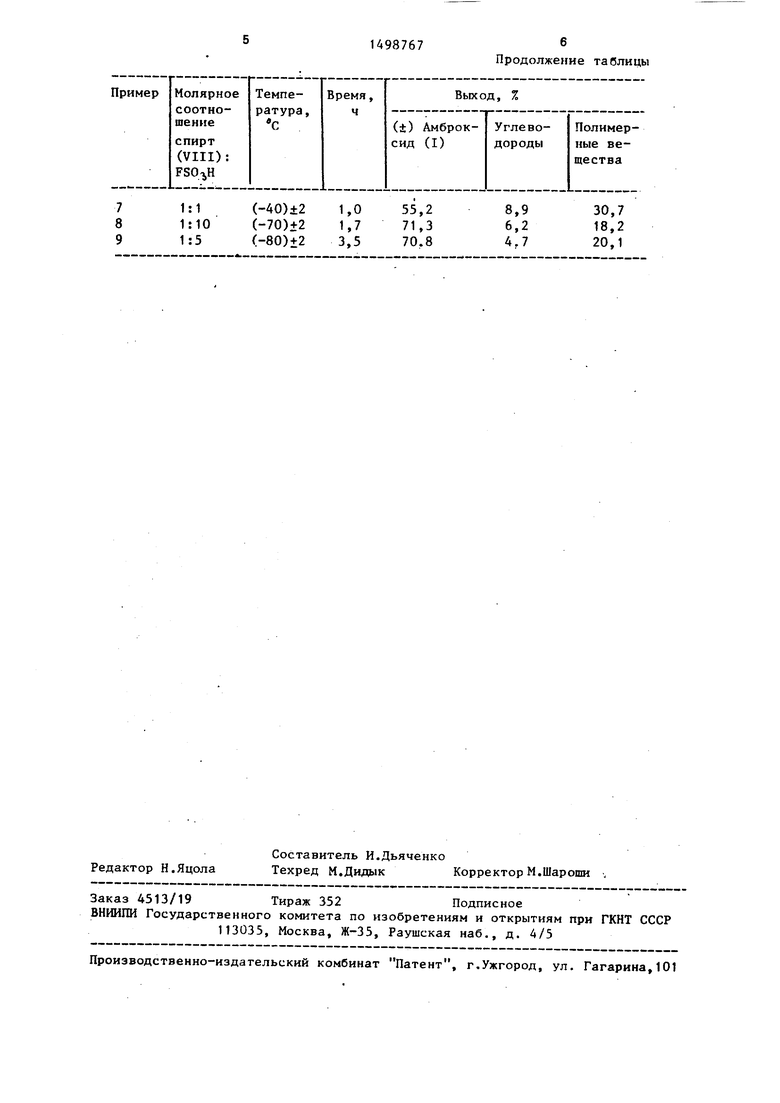
пропана добавляют при перемешивании при (-80)±2°С охлажденный раствор 140 мг (1,40 ммоль) фторсульфоновой кислоты в 0,2 мл 2-нитропропана. Пе- ремешивают раствор при этой температуре 2,5 ч, после чего добавляют в реакционную смесь 0,28 мл.триэтнл- амина. Разбавляют смесь водой (10 мл) и экстрагируют петролейным эфиром (3x5 мп). Эфирный слой промывают водой до нейтральной реакции, сушат над безводным сульфатом натрия, от- фштьтровывают, растворитель отгоняют. Остаток (31,4 мг) хроматрграфируют на колонке с 0,7 г силикагеля (L 100/ /160ju). Петролейным эфиром вымывают 1 ,8 мг углеводородной фракции. Смесью петролейного эфира и этилаце- тата (19:1) элюируют 24 мг (вькод ) (+)За,6,6,9а-тетраметилпергид- ронафтр| 2,1-в фурана(1), идентифицированного хроматографическим и спектральным сравнением с образцом оптически активного амброксида. Опи- санный примердемонстрирует оптимальные условия циклизации, подобранные варьированием условий реакции. Данные примеров 2-9 приведены в таблице.
Целевой продукт может быть вьщелен не только хроматографически, но и кристаллизацией. Константы целевого продукта: т.пл. 70-73°С (из МеОН)J. ИК-спектр (CCl, см-О: 1040, 1053 (тетрагидрофурановое кольцо), 1376 и 1373 (С(СН,)), идентичен спектру образца оптически активной формы амброксида.
Реакция структурно- и стереонап- равлена. Циклизация алифатического спирта в полициклическую окись (I) осуществляется в одну стадию. Супер
кислотная циклизация в -гомофар- незола лучше проходит при (-80)±2 С с использованием десятикратного молярного избытка циклизирующего аген- fai Увеличение или дальнейшее уменьшение температуры сказывается отрицательно на выходе целевого продукта (IX
Общий выход (+)амброксида (I) в расчете на исходную 8, 5 -гомофарне- зиловую кислоту составляет , что на 14% вьшге, чем в известном способе.
Преимущество предпоженого способа перед известным состоит и том, что он позволяет упростить процесс получения (+)амброксида (I) за счет циклизации алифатического в.Е -гомофар- незола, сокращая число стадии за счет |исключения стадии ш41сЛизации , 6 -гомофарнезиловой кислоты в (+)нор- амбреинолид, и увеличить выход целевого, продукта в расчете на кислоту на 14%.
Формула изобретения
Способ получений (±)Зa,6,6,9a-тeт- paмeтилпepгидpoнaфтoP, 1 в фурана на основе / -гомофарнезиловой кислоты с использованием алюмогидрида лития, органического растворителя и охлаждением, о тли чаю щи А с я тем, что, с целью упрощения процесса и повышения выхода целевого продукта, 5,Е-гомофарнезиловую кислоту восстанавливают алюмогидридом лития в ере- де диэтилового эфира и полученкь 6 6 гомофарнезол циклизуют в присутствии фторсульфоновой кислоты .рри молярном соотношении 1:10-: 15 срртвет- ственно в среде 2-нитропропана при (-80)-(-90)°С.
1:1
1:10
1:5
(-А0)±2 (-70)±2 -80)+2
1,0 1,7 3,5
8,9 6,2 4.7
30,7 18,2 20,1

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения тетрагидрофуранов | 1980 |
|
SU988817A1 |
| Способ выделения и очистки амброксида | 2016 |
|
RU2720094C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 7-АЛКИЛ-2,3-ДИГИДРО-1Н-ПИРРОЛО[1,2-d][1,4]ДИАЗЕПИН-4(5Н)-ОНА | 2017 |
|
RU2659390C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛИЧЕСКИХ ТЕРПЕНОИДОВ | 1972 |
|
SU335926A1 |
| 3А ,3 - 3а,6,69а-тетраметилпергидронафто(2,1-в)фуран,обладающий амбровым запахом | 1975 |
|
SU529166A1 |
| СПОСОБ ПОЛУЧЕНИЯ СМЕСЕЙ ИЗОМЕРНЫХ БИЦИКЛОГОМОФАРНЕЗАЛЕЙ | 1972 |
|
SU421684A1 |
| 2-ФЕНИЛБЕНЗО(В)ФУРАНЫ И -ТИОФЕНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2120443C1 |
| ПРОИЗВОДНЫЕ КСАНТИНА В ВИДЕ СМЕСИ ИЗОМЕРОВ ИЛИ ИНДИВИДУАЛЬНЫХ ИЗОМЕРОВ, ОБЛАДАЮЩИЕ СВОЙСТВАМИ АНТАГОНИСТОВ АДЕНОЗИНА | 1992 |
|
RU2057752C1 |
| Способ получения производных фурокумарина | 1978 |
|
SU876058A3 |
| Способ получения этилового эфира @ -ацетиламино- @ -карбэтокси- @ -(5-бензилокси-3-индолил) пропионовой кислоты | 1980 |
|
SU1018939A1 |
Изобретение касается гетероциклических соединений ,в частности, способа получения (±)3A, 6,6,9A-тетраметилпергидронафто(2,1-B)фурана, обладающего душистыми свойствами, что находит применение в парфюмерии. Цель - упрощение процесса и повышение выхода целевого продукта. Процесс ведут восстановлением ε,ε - гомофарнезиловой кислоты алюмогидридом лития в среде диэтилового эфира при кипячении в течение 3 ч. Затем полученный ε,ε-гомофарнезол циклизуют в присутствии фторсульфоновой кислоты при их молярном соотношении 1:(10-15) в среде 2-нитропропана при (-80)-(-90)°С. Способ позволяет увеличить выход целевого продукта в расчете на кислоту на 14%, сократить число стадий за счет исключения стадии циклизации ε, ε - гомофарнезиловой кислоты в (±)норамбреинолид. 1 табл.

| Патент США № 4503240, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Пневматический водоподъемный аппарат-двигатель | 1917 |
|
SU1986A1 |
Авторы
Даты
1989-08-07—Публикация
1987-06-04—Подача