1
(21)4317146/28-14
(22)19.10.87
(46) 15.09.89. Бюп. № 34
(71)Алтайский государственньв1 медицинский институт им. Ленинского комсомола
(72)В.А.Карташов и В.А.Кнауб (53) 612.015(088.8)
(56) Титова А.В. Изучение процесса экстракции лекарственных соединений из биологического материала - Авто- реф. на соиск, учен, степени канд. фарм. наук, М., 1984.
(54) СПОСОБ ОПРЕДЕЛЕНИЯ АЗОТСОДЕРЖАЩИХ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ ОСНОВНОГО ХАРАКТЕРА В ТКАНИ ПЕЧЕНИ (57) Изобретение относится к фармации, а именно к химико-токсикологическому анализу для определения азотсодержащих лекарственных веществ основного характера в печени. Целью изобретения является упрощение способа. Сущность изобрете.ния состоит в том, что выявляют оптимальные условия экстракции и очистки введенного в ткань нейтрального красного и используют их для определения азотсодержащих лекарственных веществ основного характера. 5 табл.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения азотосодержащих лекарственных веществ | 1986 |
|
SU1461463A1 |
| Способ спектрофотометрического количественного определения но-шпы, выделенной из биологического материала | 1987 |
|
SU1594427A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ 4-НИТРОФЕНОЛОВ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 1994 |
|
RU2121681C1 |
| Способ определения алкил-динитрофенолов в биологическом материале | 1990 |
|
SU1786426A1 |
| Способ получения убихинона | 1980 |
|
SU950394A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ГЕТЕРОЦИКЛИЧЕСКИХ НИТРОСОЕДИНЕНИЙ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 1996 |
|
RU2100808C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СЛОЖНОГО НИТРОФЕНОЛЬНОГО ПРЕПАРАТА "НИТРАФЕН" В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 1999 |
|
RU2153169C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ Н-БУТИЛОВОГО ЭФИРА 2-[4-(5-ТРИФТОРМЕТИЛПИРИДИЛ-2-ОКСИ)ФЕНОКСИ]ПРОПИОНОВОЙ КИСЛОТЫ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2005 |
|
RU2287812C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ СУММЫ КАРОТИНОИДОВ В ПЛОДАХ ДЕРЕЗЫ КИТАЙСКОЙ | 2021 |
|
RU2763265C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ 2,4,6-ТРИНИТРОМЕТИЛБЕНЗОЛА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2006 |
|
RU2319142C1 |
Изобретение относится к фармации, а именно к химико-токсикологическому анализу для определения азотсодержащих лекарственных веществ основного характера в печени. Целью изобретения является упрощение способа. Сущность изобретения состоит в том, что выявляют оптимальные условия экстракции и очистки введенного в ткань нейтрального красного и используют их для определения азотсодержащих лекарственных веществ основного характера.
Изобретение относится к фармации, точнее к химико-токсикологическому анализу для определения азотсодержащих лекарственных веществ основного характера в ткани печени.
Цель изобретения - упрощение способа при сохранении точности.
Сущность изобретения заключается в том, что в отличие от известного способа определения лекарственных веществ в биологическом материале, согласно изобретению перед экстракцией вводят в ткань печени нейтральный красный (НК), выявляют оптимальные условия его экстракции и очистки и используют их для определения азотсодержащих лекарственных веществ основного характера.
Пример 1, В качестве экстра- гейтов используют водные растворы
кислот: соляной, серной, уксусной, щавелевой, и органические растворители - этанол, ацетонитрил, ацетон.
Экстракцию и последующее количественное определение проводят по следующей методике.
К 5,0 г ткани печени, измельченной на мясорубке, добавляют 0,5 мп 0,1%-ного водного раствора нейтрального красного, тщательно перемешивают и оставляют на 2 ч (при большей экспозиции наблкдалось разложение нейтрального красного, что доказывалось методом тонкослойной хроматографии) . Затем к печени добавляют 5,0 мл соответствуииего экстрагента и экстрагируют на аппарате для встряхивания в течение 10 мин, центрифугируют 5 мин при 2,5 тыс. об/мин. Экстракты спивают во флаконы, операцию
СП
х ел
1508156
экстракции и центрифугирования повторяют еще 3 раза, сливая экстракты в новые флаконы. Параллельно получают экстракты из печени, не содержащей НК, к которым после экстракции добавляют 0,1 мл 0,1%-ного раствора нейтрального красного (стандартные пробы). Кроме того, анализируют холостые пробы. Все экстракты подщелачивают 50%-ным раствором едкого натра до рН 10-11, добавляют 5,0 мл воды, 10,0 мп хлороформа, встряхивают и центрифугируют как описано выше. Органические фазы отделяют, фильтруют через небольшие бумажные фильтры, отбрасывая первые порции фильтрата. Оптические плотно™ сти измеряют с помощью спектрофотометра СФ-26 в кюветах 1 см при длине волны 523 нм относительно хлороформа, Затем к раствору в кювете добавляют 1 каплю насыщенного раствора трихлор- уксусной кислоты в хлороформе, перемешивают и вновь измеряют оптическую плотность при той же длине волны, Разность (ЛД) между оптическими плотностями пржмо пропорциональна концентрации НК, закон Бугера соблюдается в интервале концентрации 1,5-15 мкг/мл Примеси из ткани печени (в холостых пробах) влияния на количественное определение не оказывали, т,.е, не дают изменения оптической плотности в описанных условиях. Расчет количественного содержания НК в процентах прово-35 и печени различной степени измельченности добавляют по 5,0 мл ацетона и получают экстракты по описанной
дят по формуле X
4flii CA lOAiliOO
Л Дет-0,5
(%)
методике,
Результаты эксперимента представлены в табл, 2,
где йДиссл я ЛДст разность между оптическими плотностями растворов исследуемых и стандартмзпс проб соответственно.
Результаты экспериментов приведены в табл, 1,
Из табл, 1 видно, что перспективными экстрагентами являются этанол, ацетонитрил, ацетон. Из них как наиболее доступный и дешевый выбран ацетон. При использовании в качестве экстрагента ацетона извлечения, полученные на 1-й ступени экстракции, содержали меньше соэкстрактивных веществ, чем на последукщих трех (по ультрафнолетовым спектрам абсорбции нулевых проб, по образованию эмульсии при экстрагировании хлороформом). Содержание воды в ткани печени людей
колеблется в пределах 60-75%, т.е, в 5,0 г печени содерзкится около 3- 3,7 мл воды. В процессе экстракции ацетон смешивается с водой (в соотношении приблизительно 5:3), Использование на 2, 3, 4-й ступенях экстракции вместо ацетона смеси ацетона с водой в соотношении 5:3 не влияло на выход НК и в то же время уменьшило количество примесей, поэтому в качестве оптимального экстрагента на 1-й ступени экстракции используют ацетон, на 2, 3, 4-й. смесь ацетона и воды в соотношении 5:3.
Пример 2. Выбор степени измельчения ткани печени. Для проверки влияния измельчения ткани печени на выход НК бьши поставлены опыты на экспериментальных животных (собаках) по следующей методике. Собаке весом 10 кг через зонд вводят 0,5 г нейтрального красного в виде водного раствора. Через 1,5 ч животное, умертвляют с помощью электрического тока. Часть печени измельчают с помощью гомогенизатора (РТ-1-У4-2 8000 об/мин), часть - с помощью мясорубки, именщей решетки с различным диаметром отверстия: 4,5 (P/z) 7,5 мм (Pj); 10,5 мм (Р); 13 мм (PS), а также берут для анализа цельные кусочки печени размером I ll к 4,5 см (Рб). Затем к 5,0 г тка0
5
0
5
методике,
Результаты эксперимента представлены в табл, 2,
Дисперсионный анализ результатов, представленных в табл. 2 показал, что различия между оптическими плотностями при различной степени измельчения значимы (по критерию Фишера), а в случае исследования цельных кусочков (Pg) результаты существенно ниже остальных. При сравнении оптических плотностей растворов, полученных при исследовании печени со степенью изг- мельчения Pi -Per, значимых различий нет (по критерию Дункана), За оптимальную степень измельчения ткани печени принимают измельчение с помощью мясорубки с диаметром отверстий . решетки 4,5 мм,
Пример 3« Выбор продолжительности экстракции.. Собаке весом
10 кг через зонд вводят в желудок 0,5 г НК в виде водного раствора, Через 1,5 ч собаку умертвляют. Печень измельчают с помощью мясорубки и экстрагируют в течение разного времени (10, 35 и 60 мнн) по описанной методике.
Результаты эксперимента представлены в табл. Зо
Данные табл, 3 показывают, что увеличение продолжительности экстракции от 10 до 60 мин влияния на выход НК из ткани печени не имеет. Продолжительность экстракции 0 мин опти- мал ьн а,
Пример 4. Выбор оптимапьных условий очистки. Отделение ацетона от воды с одновременной экстракцией НК в ацетон., Для этой цели применяю безводный карбонат калия, при добавлении которого в избытке к ацетоно- водному экстракту и встряхивании происходит разделение ацетона и воды (высаливание ацетона) и гомофазная экстракция НК в ацетоновый слой. Выход НК в процентах, определенный по описанной методике, составил 97%,
Пример 5, Выбор условий ре- экстрак1-гии нейтрального красного в соляную кислоту.
К ацетону добавляют смесь эфира и гексана. Для выбора оптимальных условий на этой стадии применяют планирование эксперимента методом крутого восхождения. В качестве факторов рассматривают: Хц - объем снеси эфир - гексан, мл; Х - процентное содержание эфира в смеси эфир - гексан; Х объем 0,5 н,раствора соляной кислоты Критерием оптимизации (У) является выход нейтрального красного в процентах, который определяют по следующей методике. К высаленному ацетону добавляют определенные количества смес эфир - гексан и 0,5 н,раствора соляной кислоты. Встряхивают и центрифугируют в течение 5 мин при 2,5 тыс. об/мин о Водную фазу отделяют и измеряют оптическую плотность при длине волны 525 им. Расчет процентного выхода НК проводят по стандарту, добавляют Ojl мл 0,1%-ного раствора НК к соляно-кислом:, реэкстракту. После реализации полного факторного экспе- риметра (сМо табл, 4) оптимальными
508156 5
оказались следующие условия: объем смеси эфир - гексан (в расчете на 10,0 мл ацетона) 15,0 мл| соотношение эфир - гексан в смеси 1:1; объем 0,5 н, раствора соляной кислоты 1,5 мл, Дчя более полной реэкстракцин НК операцию повторяют дважды.
Пример 6. Выбор условий эк--: 0 стракции НК в органический растворитель. Подщелачивание соляно-кислого реэкстракта до рН 10-11 50%-ным раствором гидроксида натрия, насьпдение кристаллическим хлоридом натрия и 15 последукхцая экстракция 10,0 мл эфира обеспечивают выход НК, равный 95-97%. Таким образом, выход НК на этапах экстракции из ткани печени и последующей очистки составил в среднем 80%. 20 Пример 7. Использование вы-- явленных оптимальных условий экстракции и очистки для определения азотсодержащих лекарственных веществ основного характера в ткани печени.
25
0
5
0
Лекарственные вещества основного характера (имизин, но-шпа, верапамил) экстрагируют и очищают в условиях, выявленных для НК по описанной методике. Количественное определение проводят после испарения эфира и растворения остатков в спирте. Оптические плотности растворов определя- ют с помощью спектрофотометра СФ-26 в кювете 1 см при длинах волн соответственно для имизи- на, но-шпы, верапамила при 254, 360 и 228 нм. При количественном определении учитывают фоновое поглощение примесей. Выход имизина, но-шпы и верапамила (см. табл, 5) коррелирует с выходом НК.
45
50
55
Формула изобретения
Способ определения азотсодержащих лекарственных веществ основного характера в ткани печени, включающий их экстракцию и последующую очистку, о т- л и чающий ся тем, что, с це- лью упрощения способа при сохранении точности, экстракцию и очистку проводят в условиях, аналогичных экстракции и очистке введенного в ткань нейтрального красного.
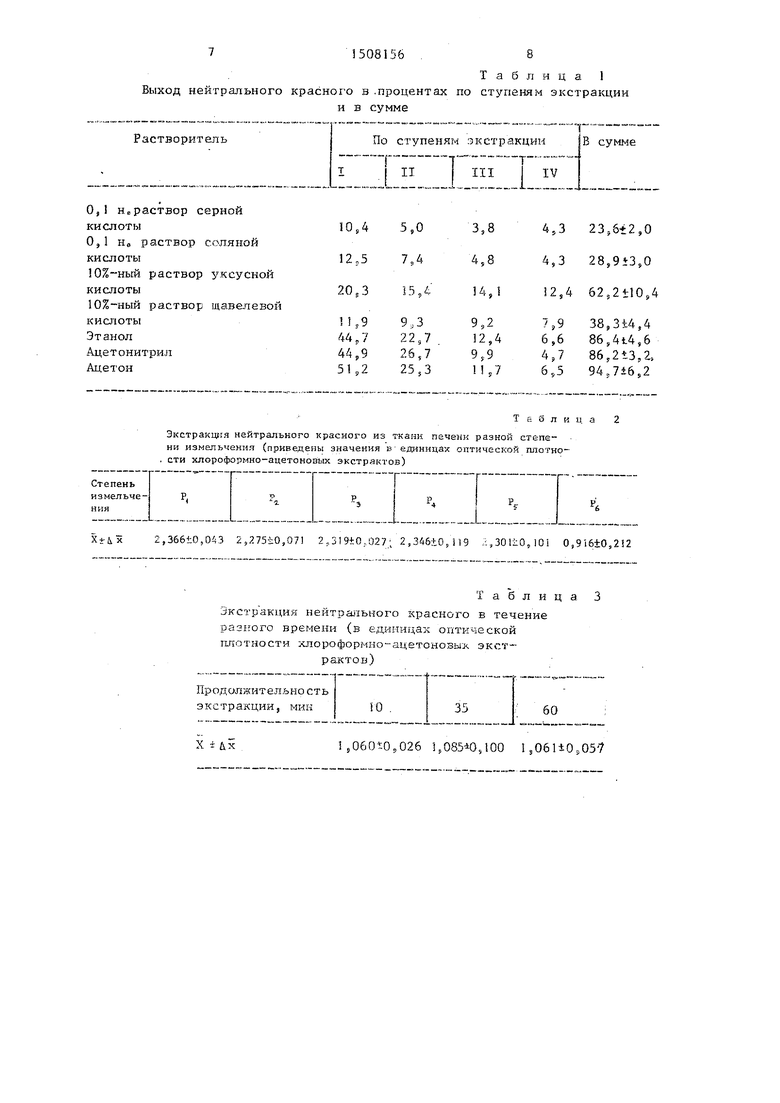
Т а б л и ц а 1 Выход нейтрального красного в .процентах по ступеням экстракции
и в сумме
, „™..„. „,.-.....,. -...„..„,. ..„.„ .„„„.
Растворитель
рной
оляной
уксусной
щавелевой
10,4 12,5 20,3
11,9 44,7 44,9 51,2
Таблица 2
Экстракция нейтрального красного из тканк печени разной степени измельчения (приведены значения в единицах оптической плотно- . сти хлороформно-ацетоновых экстрактов)
Степень
измельче-Р, р Р|р
L
Xi-ix2,36610,043 2,275-1:0,07 2,31940,027; 2,346ЬО,П9 ;i:,301tOJOi 0,9i6±0,
Таблица 3
Экстр акция нейтрао шного красного в течение разного времени (в единицах оптической П.ПОТНОСТИ хлороформно-ацетоноБых экстрактов)
Продолжительность
экстракции, мик10 .35/ 60
X ±йх
I5060t0.,026 1,,100 s061t0505 7
По ступеням экстракции .„.-. , ., . . ...
иIIIIV
В сумме
3,8
4,8 14,1
9,2 12,4 9,9 1 /7
4,323,,0
4,328,9i3,0
2,462,2tlO,4
7,938,3i4,4
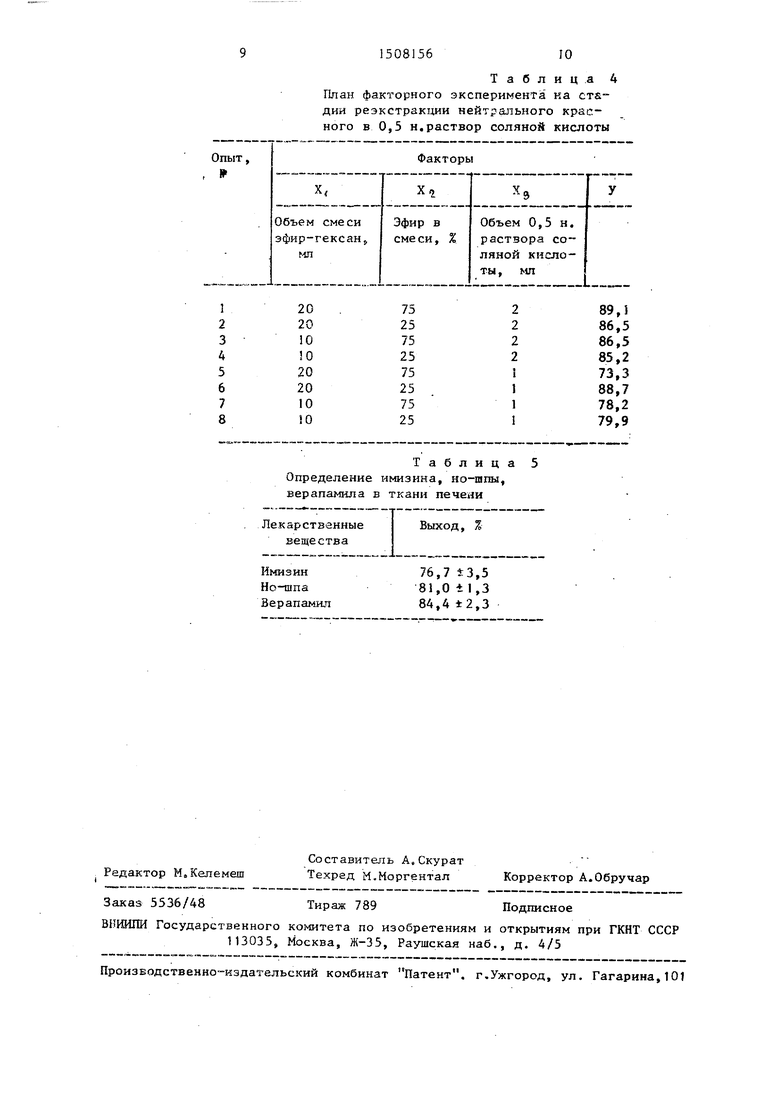
Таблица 4
План факторного эксперимента ка CTS дни реэкстракгдии нейтрального красного в 0,5 н.раствор соляной кислоты
Таблица
Определение имизина, но-шпы, верапамила в ткани печени
Авторы
Даты
1989-09-15—Публикация
1987-10-19—Подача