Изобретение относится к медицине и ветер1 иарии, преиьгущсственно к лабораторной иммунодиагностике, и может быть использовано для определения
недостаточности клеточного иммуниге- та при врожденной и приобретенной иммунодефицитности, при инфекционных процессах, напримрр при (ли1вир ю-щей герпесвирусной, стафилококковой или туберкулезной инфекции.
Цель изобретения - повьшение точности определения нарушения специфического Т-клеточного иммунитета за счет дифференцированной оценки уровня антигенраспознающей и акцепторной функции Т-лимфоцитов по отношению к эндогенному и экзогенному трансфер- фактору.
Способ осуществляют следующим образом.
Способ основан на реакции конгломерации лейкоцитов свежевзятой крови пациента в присутствии исследуемого антигена. Для каждого антигена готовят по два одинаковых ряда разведений и устанавливают разницу между концентрацией , антигена, которая вызывает конгломерацию лейкоцитов в отсутствии и присутствии содержащего экзогенный трансфер-фактор лимфоцитарного ультрафильтрата, И при увеличении этой разницы более чем в 2 раза судят о недостаточности распознавательной и акцепторной функции Т-лимфоцитов, лежащей в основе дефицита специфического клеточного иммунитета. При этом используют ультрафильтраты, приготовленные из смеси лимфоцитов от 50 или более случайно выбранных здоровых доноров.
Способ включает следующие этапы.
А. Выбор тест-антигенов.
При конкретном осуществлении способа поставлена задача диагностировать нарушение клеточного иммунитета, специфичного в отношении антигенов трех произвольно выбранных патогенных возбудителей: вируса простого герпеса (типы I и II), микобактерий туберкулеза и золотистого стафилококка. В качестве тест-антигенов используют коммерческие реагенты: жидкая герпетическая (тканевая, убитая) вакцина, содержащая обезвреженные формальдегидом вирусы простого герпеса I и II типов, очищенный туберкулин - ПГЩ (10 мкг/мл в 1%-йом цитрате натрия на 0,85%-ном хлориде натрия , о -шщенный стафилококковый белок А (10 мкг/мл в 1%-ном цитрате натрия на 0,85%-ном хлориде натрия).
Б. Приготовление препарата трансфер-фактора.
Препаратом, содержащим трансфер- факторы, специфичные в отношении пе- речисленинх антигенов, служит лиофи0
5
0
5
0
5
0
5
0
5
лизированный ультрафильтрат, для приготовления которого используют человеческие миндалины, удаленные при хроническом тонзиллите. Взвесь лимфоцитов миндалин, содержащую не менее 95% живых клеток, готовят не позднее 3 ч после тонзиллэктомии, очищают от адгезивных клеток фильтра11 1ей через синтетическую (полиамидную) вату, осаждают центрифугированием (400g, 20 мин), ресуспендируют дистиллированной водой до концентрации 2-10 клеток в 1 мл и замораживают при температуре ниже -20°С. Отдельные порции лимфоцитарного экстракта раз- мораживают при , объеди 1яют так, чтобы смесь содержала экстракт из лимфоцитов не менее 50 доноров, разрушают клеточный детрит, пропуская взвесь через инъекционную иглу при помопщ шприца, центрифугируют при 6000g в течение 1 ч при 4 С и декап- тируют надосадочную жидкость. Полученный экстракт подвергают ультрафильтрации при 0,15 МПа на мембране с ретенцией 15 КДа. Ультрафильтрат разливают по ампулам и лиофилизиру- ют„ Трансфер-факторную активность ультрафильтрата контролируют в опытах индукции ГЗТ к трем указанным тест- антигенам на мышах и золотистых хо-, г-1ячках.
В. Постановка реакции.
Методом оценки специфического клеточного иммунитета, а также акцепторной функции Т-лимфоцитов в отношении экзогенного трансфер-фактора служит реакция конгломерации переживающих лейкоцитов (РКЛ) периферической крови, которую ставят следующим образом.
Из кубитальной вены исследуемого индивида берут 4 мл крови в 1 мл 5%-ного цитрата натрия и охлаждают на льду. В и-образные лунки 96-луноч- ной панели для микротитрования помещают по 100 мкл 1%-ного цитрата натрия в 0,85%-ном хлориде натрия и готовят в этом растворе серию последовательных разведений с шагом 1:2 для каждого из тест-антигенов. В ряду из 8 лунок 7 содержат последовательно убываюг ие разведения антигена, а 8-я - только 1%-ный нитрат на 0,85%-ном растворе натрия. Каждый ряд разведений всех трех тест-антигенов повторяют еще раз, пользуясь в качестве
515
разводящей жидкости 1%-ным раствором щтрата натрия с 0,85%-ным хлоридом натрия, содержащим препарат трансфер- фактора (., лимфоцитарный ультрафильтрат) в концентрации, эквивалентной 2-10 лимфоцитов в 1 мл. Таким образом, для каждого обследуемого индивидуума на панели готовят по две серии разведений каждого из трех тест-антигенов - одну серию без трансфер-фактора, другую с ним. Затем в каждую лунку вносят по 100 мкл стабилизированной цитратом крови иссле- дуемого индивидуума. После этого па- нель герметизируют адгезивной пленкой, закручивают крышкой и помещают на качалку (120 качаний в 1 мин)при 37°С на 2 ч. ,
После инкубации из содержимого каждой лунки готовят по две толстые капли об7земом 50 мкл и диаметром 20 мл на предметных стеклах и оставляют для высушивания при комнатной температуре на горизонтальной поверх- ности. Во время приготовления препаратов толстой капли панель находится на термостатируемом подогреваемом столике при 37°С. Высушенные пре:па- раты без фиксации окрашивают 0,01%- ным раствором метиленового синего, осторожно погружая предметные стекла в раствор красителя вертикально на 10 мин.
После окрашивания препараты извлекают из,красителя и высушивают на воздухе. Перед микроскопом всю поверх
ность окрашенных толстых капель . покрывают иммерсионным маслом для- просветления и просматривают вдоль продольного диаметра с объективом X 20, отмечая численность лейкоцитов .в конгломератах. Определяют число лейкоцитов в трех самых крупных из встретившихся конгломератов. Именно это число служит показателем конгломерации лейкоцитов в данной лунке, отражающим количество адгезивных лейкоцитов в:исследуемой пробе крови и степень их взаимной адгезив- ности. Показатели конгломерации лей- кодатов в лунках, содержап5их последовательные разведения тест-антигена, сравнивают с показателями 8-й лунки, которая служит контролем. Пре вьшение показателя на 2 и более единицы (клетки) расценивается как достоверное. Лунка, в которой наблюдается это отличие, содержит пороговую
Q 5
0 5 0
5
5
Q п
5
76
концентрацию тест-антигена. Сравнивая пороговые концет1трации тест-антигенов, П1)1зывающие увеличение показателей конгломерации лейко1р1тов без трансфер-фактора и л присутствии трансфер-фактора, судят об его эффекте.
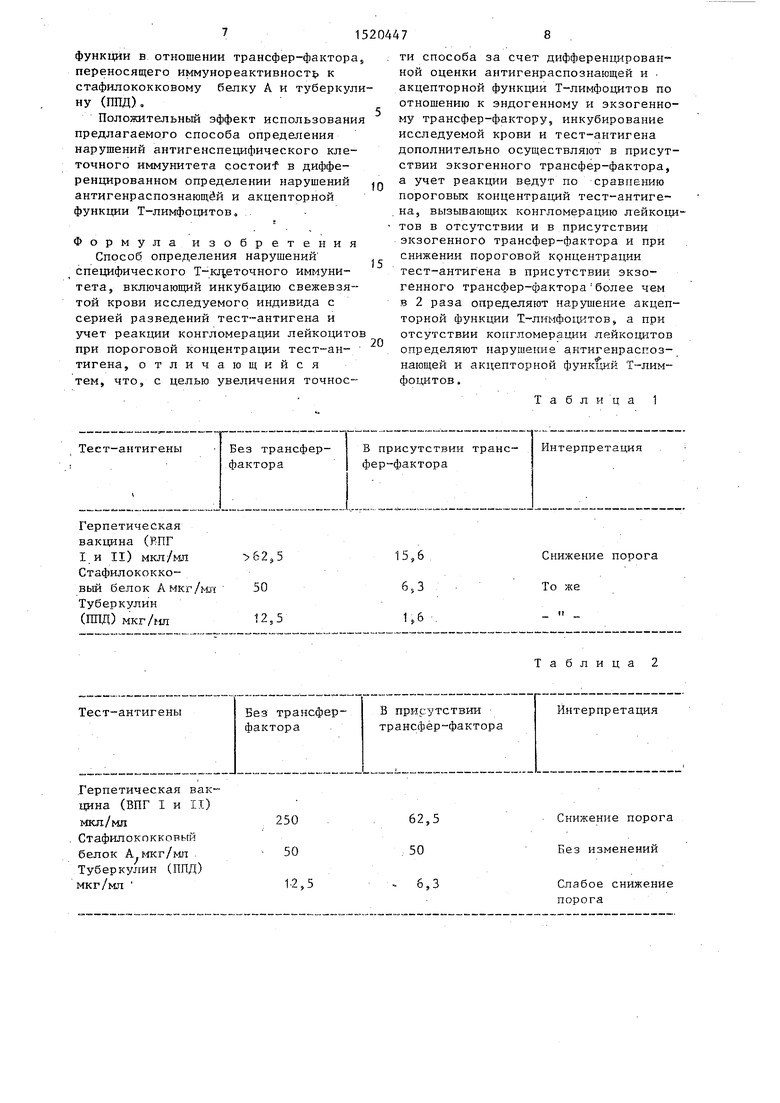
Пример 1. Представленные п табл. 1 результаты РКЛ с кровью больного Д.1П.А„, 1918 г рождения, диагноз: рецидивирующий древовидный кератит с поражением стромы правого глаза, свидетельствуют о высоком пороге положительной реакции для всех трех тест-антигенов, что указывает на недостаточность клеточного иммунитета у данного больного в отношении соответствующих возбудителей. Однако способность Т-лимфоцитов пассивно воспринимать специфическую им- мунореактивность (т.е., акцептировать экзогенный трансфер-фактор) сохранена, так как в присутствии лимфо- цитарного ультрафильтрата наблюдается существенное снижение пороговой концентрации тест-антигенов, вызыва- юш:их положительную РКЛ.
Пороговые концентрации тест-антигенов, вызывающие достоверное увеличение показателя конгломерации лейкоцитов крови больного Д.10.А., приведены в табл. 1.
Пример 2. Больной Е.Б.П., 1945 г. рождения, диагноз: кератоуве- ит левого глава.
Пороговые концентрации тес-антигенов, вызываюпще достоверное увеличение показателя конгломерации лейкоцитов крови больного Е.Б.П., представлены в табл. 2.
Как и в примере 1, у больного Е.Б.П. также обнаружены высокие пороги концентраций герпетической вакцины и туберкулина (ШТД)., вызывающ1-1е конгломерацию РКЛ и ареактивность в отношении стафилококкового белка А. Прибавление препарата трансфер-фактор .вызывало достоверное снижение пороговой концентрагщи герпетической вакцины, т.е. индуцировало иммунореактив- ность на антигены ВПГ 1 и II, однако существенно не повлияло на результаты РКЛ со стафилококковым белком А и туберкулином (ШЩ) . Такой результат интерпретирован как утрата Т-лимфо- цитами больного Е.Б.П. акцепторной
функции в отношении трансфер-фактора, переносящего иммунореактивност к стафилококковому белку А и туберкулину (ПОД),
Положительный эффект использования предлагаемого способа определения нарушений антигенспецифического клеточного иммунитета cocтoиf в дифференцированном определении нарушений антигенраспознающёй и акцепторной функции Т-лимфоцитов,
Формула изобретения
Способ определения нарушений специфического Т-кц,еточного иммунитета, включающий инкубацию свежевзятой крови исследуемого индивида с серией разведений тест-антигена и учет реакции конгломерации лейкоцито при пороговой концентрации тест-антигена, отличающийся тем, что, с целью увеличения точнос0
5
0
ти способа за счет дифференцированной оценки антигенраспознающёй и акцепторной функции Т-лимфоцитов по отношению к эндогенному и экзогенному трансфер-фактору, инкубирование исследуемой крови и тест-антигена дополнительно осуществляют в присутствии экзогенного трансфер-фактора, а учет реакции ведут по сравнению пороговых концентраций тест-антигена, вызывaющIix конгломерацию лейкоцитов в отсутствии и в присутствии экзогенного трансфер-фактора и при снижении пороговой крнцентрации тест-антигена в присутствии экзогенного трансфер-фактора более чем в 2 раза определяют нарушение акцепторной функции Т-ЛНМФО1ЩТОВ, а при отсутствии конгломерации лейкоцитов определяют нарушение антигенраспознающёй и акцепторной функций Т-лимфоцитов .
Таблица 1


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА "АФФИНОЛЕЙКИН" ДЛЯ ПРОТИВОИНФЕКЦИОННОЙ ИММУНОТЕРАПИИ | 1991 |
|
RU2076715C1 |
| СПОСОБ ПРОФИЛАКТИКИ ПОВЫШЕННОГО ОНКОЛОГИЧЕСКОГО РИСКА | 1993 |
|
RU2088245C1 |
| Способ определения состояния клеточного иммунитета | 1978 |
|
SU789104A1 |
| СПОСОБ МУЛЬТИПЛЕКСНОГО АНАЛИЗА В-КЛЕТОК ДЛЯ ОЦЕНКИ КЛЕТОЧНОГО ЗВЕНА ИММУННОЙ СИСТЕМЫ РОГАТОГО СКОТА | 2020 |
|
RU2761468C1 |
| Способ определения иммунологической реактивности организма | 1988 |
|
SU1629848A1 |
| СПОСОБ ПРИЖИЗНЕННОЙ ДИАГНОСТИКИ ТУБЕРКУЛЕЗА | 2004 |
|
RU2296334C2 |
| Группа антигенов и тест-система для диагностики инфекции М.tuberculosis complex | 2022 |
|
RU2802789C1 |
| СПОСОБ ОТБОРА КРУПНОГО РОГАТОГО СКОТА НА УСТОЙЧИВОСТЬ К ТУБЕРКУЛЕЗУ | 1995 |
|
RU2080061C1 |
| Способ определения и количественной оценки специфического клеточного иммунитета к антигенам N-белка вируса SARS-COV-2 | 2023 |
|
RU2818080C1 |
| СПОСОБ ПОЛУЧЕНИЯ АУТОЛОГИЧНОЙ ВАКЦИНЫ ДЛЯ ЛЕЧЕНИЯ ТУБЕРКУЛЕЗА | 2008 |
|
RU2372936C1 |
Изобретение относится к лабораторной иммунодиагностике в медицине и ветеринарии и позволяет дать четырехстепенную классификацию выраженности нарушений клеточного иммунитета на основе дифференцированной оценки уровня антигенраспознающей функции Т-лимфоцитов и сохранности акцепторной функции Т-лимфоцитов в отношении эндогенного и экзогенного трансфер-фактора. Целью изобретения является повышение точности определения нарушения специфического Т-клеточного иммунитета за счет дифференцированной оценки уровня антигенраспознающей и акцепторной функции Т-лимфоцитов. Возможность такой оценки достигается тем, что для каждого антигена готовят по два одинаковых ряда разведений и устанавливают разницу между концентрациями антигена, которые вызывают конгломерацию лейкоцитов в отсутствии и присутствии содержащего трансферфактор лимфоцитарного ультрафильтрата, и при выявлении снижения концентрации антигена в присутствии экзогенного трансфер-фактора более чем в 2 раза определяют недостаточность эндогенного трансфер-фактора, а при выявлении отрицательной реакции конгломерации лейкоцитов определяют более глубокое нарушение - нарушение акцепции трансфер-фактора. При этом в качестве источника эндогенного трансфер-фактора используют ультрафильтраты, приготовленные из смеси лимфоцитов от 50 или более случайно выбранных здоровых доноров. Положительный эффект предлагаемого способа определения нарушений антигенспецифического клеточного иммунитета состоит в дифференцированном определении нарушений антигенраспознающей и акцепторной (по отношению к эндогенному и энезогенному трансфер-фактору) функций Т-лимфоцитов.
Таблица 2
| Юсипова И.П., Мац А.Н., Тугано- ва В.Е | |||
| - Клиническая медицина, 1972, К 4, с | |||
| Счетный сектор | 1919 |
|
SU107A1 |
Авторы
Даты
1989-11-07—Публикация
1987-06-23—Подача