Изобретение относится к сельскому хозяйству.
Цель изобретения - повышение стабильности состава при рН выше или равном 5 (Р рубце) и выделении биоло- гически-актитзного вещества при рН меньшем или равном 3,5.
При скармливании животным лечебных препаратов или биологически-активных веществ (витаминов, аминокислот) в рубце происходит эн шматпческое разрушение этих веществ и к-аписимости от времени их нахождения в рубце (от нескольких часов до нескольких дней)
См
и рН среды (от 5 до 6), Для капсули- рования биологически-активных веществ предложен состав, включающий связующую систему из пленкообразующих компонентов и чувствительное к изменению рН вещество,
Составы, согласно изобретению, могут быть получены путем диспергирования или растворения очень чувстви- тельного к изменениям рН вещества, в известных случаях соединенного с добавкой, в растворе или дисперсии свя- ,зующего в органическом растворителе или в смеси соответствующим образом выбранных органических растворителей в зависимости от вида связующего. В основном состав оболочки получают после выпаривания растворителя или растворителей.
Составы оболочек, согласно настоящему изобретению, особенно полезны при вводе жвачным животным оральным путем. Покрытые оболочкой вещества обычно смешиваются с кормом для жи- вотных, Терапевтические или питательные вещества могут быть в таердом или жидком виде.
Покрытые оболочкой вещества являются гранулами в форме микрокапсул, состоящие из центрального сердечника, окруженного непрерывной пленкой из состава оболочки. Однако активные вещества могут быть также диспергированы в составе оболочки, В основном состав оболочки составляет 5-60 вес.% гванулы или дисперсии.
Гранулы могут быть получены посредством применения известных техно- логий. В зависимости от вида состава оболочки и, осрбенно от вида неводорастворимого связующего используют либо технологию экструзии или распыления раствором, или эмульсий в ки- пящем слое, либо технологию изготовления капсул в расплавленной или полурасплавленной среде, либо технологию покрытия оболочкой в жидкой среде типа концентрации.
Гранулы, полученные согласно настоящему изобретению, являются стабильными при хранении и при транспортных операциях, не разрушаются при изготовлении корма для животных и не разрушаются при приеме корма животными.
Размер гранул зависит от назначения определенному виду животных.
5
0 5 0
Можно покрывать оболочкой актив ные вещества для получения гранул размером 0,1-5 мм. В качестве активных веществ гранулы содержат метио- нин, лизин или витамины (витамин А), роль которых очень важна при откорме животных, особенно жвачных.
Для выявления чувствительности составов оболочек к изменениям рН использованы тесты, которые позволяют измерять высаливание активного вещества в зависимости от времени при разных значениях рН, в частности при рН 6 до рН 2, или при рН 5 до рИ 1,5,
Тест заключается в выполнении из ПЛРНКИ состава оболочки диска, на верхнюю сторону которого помещается известное количество активного вещества, а другая сторона диска вступает в контакт с поверхностью водного раствора, перемешиваемого магнитным путем. Количество высаленного активного вещества в водном растворе определяется путем отбора проб, причем одна и та же проба проверяется сначала при рН 6 и затем при рН 2,
Другой тест заключается в помещении между двумя одинаковыми дисками состава оболочек известного количества активного вещества.
Этот комплект, герметичность которого обеспечивается загибанием краев, погружается в определенное количество водного раствора, перемешиваемого магнитным способом. Количество высаленного активного вещества проверяется при отборе пробы при рН 6, затем при рН 2.
Высаливание активного вещества в виде гранул или микрокапсуль исследуется при перемешивании в определенных условиях, а именно известное количество гранул или микрокапсул в среде выдерживается при постоянном рН и при 40°С. Сравнивают скорости высаливания образца при различных значениях рН, в частности при рН 6 и 2.
Пример 1. Согласно технологии псевдоожиженного,слоя покрывают 200 г- метионина, предварительно гранулированного в форме сферических частиц с. титром 98%, диаметр которых составляет 0,5-0,6 мм, раствором в тетрагидрофуране 60 г состава для капсулирования, состоящего из 55% этилцеллюлозы, 30% дипропиленгликоля
и 25% сополимера 2-винилпиридина со стиролом (70-30).
Пример 2. Согласно технологии псевдоожиженного слоя 200 г мети онина, предварительно гранулированного в форме сферических частиц с титром 98%, диаметр которых составляет 0,5-0,6 мм, покрывают растзором тет- рагидрофурана 60 г состава для капсу лирования, состоящего из 37,5% этил- целлюлозы, 37,5% дипропиленгликоля и 25% сополимера 2-винилпиридина со . стиролом
Пример 3. Согласно технологии псевдоожиженчого слоя 200 г ме- тионина, предварительно гранулированного в виде сферических частиц, с тиром 98%, диаметр которых составляет ,6 мм, покрывают раствором в тетрагидрофуране 60 г состава для капсулирования, состоящего из 40% этилцеллюлозы, 40% пропиленгликоля и 20% сополимера 2-винилпиридина со стиролом (70-30).
Пример 4. Согласно технологии псевдоожиженного слоя, 200 г ме- тионина, предварительно гранулированного в виде сферических частиц с титром 93%, диаметр которых составляет 0,5-0,6 мм, покрывают раствором в тетрагидрофуране, 60 г состава для капсулирования, состоящего из 45% этилцеллюлозы, 30% пропиленгликоля и 25% сополимера 2-винилпиридина со стиролом (70-30).
Пример 5. Согласно технологии псевдоожиженного слоя, 200 г метионина, предварительно гранулированного в виде сферических частиц с титром 98%, средний диаметр которых составляет 0,5-0,6 мм, покрывают раствором в тетрагидрофуране 60 г состава для капсулирования, состоящего из 41,25% этилцеллюлозы, 33,75% пропиленгликоля и 25% сополимера 2-ме- тил-5-винилпиридина со стиролом (80-20),
Пример 6. Согласно технологи псевдоожиженного слоя 200 г метио- нина, предварительно гранулированного в виде сферических частиц с титром ; 98%, средний диаметр которых составляет 095-0,6 мм, покрывают раствором в тетрагидрофуране 60 г состава для капсулирования состоящего из 40% этиленцеллюлозы, 50% пропиленгликоля и 20% сополимера 2-метил-5-винилпири- дина со стиролом (80-20).
0
5
0
5
0
5
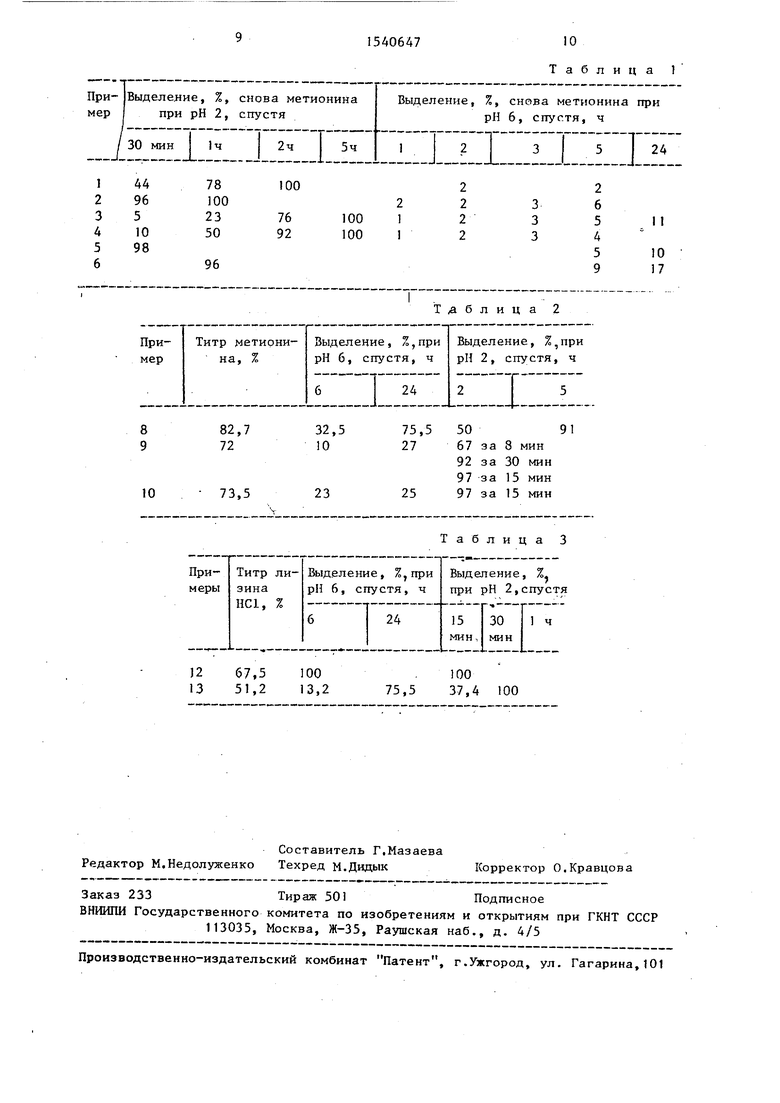
Результат по примерам 1-6 представлены в табл. 1,
Пример 7. Согласно технологи псевдоожиженного слоя 200 г монохлор гидрат а лизина, предварительно гранулированного в .виде сферических частиц, с титром 85%, диаметр которых составляет 1-1,25 мм покрывают раствором и в тетрагидрофуране 200 г состава для капсулирования, состоящего из 37,5% этилцеллюлозы, 37,5% пропиленгликоля и 25% сополимера 2-винилпиридина со стиролом.
При рН 2 процент выделившегося мо- нохлоргидрата лизина составляет .96%, спустя 30 мин, и 100%, спустя 1 ч.
При рН 6, процент выделившегося монохлоргидрата лизина составляет 1%, спустя Зч, 6% спустя б ч и 65 спустя 24 ч.
Пример 8. Согласно технологии псевдоожиженного слоя с ванной, снабженной системой Wurster, 350 г метионина, предварительно гранулированного в виде сферических частиц с титром 98%, средний диаметр которых составляет 0,5-0,63мм, покрывают ра-- створом (дисперсией в 1000 см смеси 1,2-дихлорэтана с этанолом, 1:1 по объему), 20 г состава для капсулирования, образованного 85% этилцеллюлозы, 8,3% триацетина и 16,6% сополимера стирола с 2-винилпиридином (29,6-69,5 по весу) с удельной вязкостью 0S592, измеренной по концентрации 5 г/л в диметилформамиде при 20 С.
П р и м е р 9. Согласно технологии псевдоожиженного слоя с ванной, снабженной системой Wurster, 250 г метионина, предварительно гранулированного в виде сферических частид. с титром 98%, средний диаметр которых составляет 0,5-0,63 мм, покрывают раствором (дисперсией в 1000 см9 смеси 1,2-дихлорэтана с этанолом, 1:1 по объему), 150 г состава для капсулирования, образованного 60% зеина, 20% этилцеллюлозы, 6,6% триацетина и 13,3 сополимера стирола с 2-винилпиридином (29,5-69,5 по весу) с удельной вязкостью 0,592, измеренной при концентрации 5 г/л в диметилформами- де при .
Пример 10. Согласно технологии псевдоожиженного слоя с ванной, снабженной системой Wurster, 350 г метионина, предварительно гранулированного в виде сферических частиц, с титром 98%, средний диаметр которых составляет 0,5-0,63 мм, покрывают раствором (дисперсией в 1000 см смеси 1,2-дихлорэтана с этанолом, 1:1 по объему), 140 г состава для капсулирО- вания, образованного 57,1% зеина, 14,3% этилцеллюлозы, 7,1% поливинил- ацетата, 7,1% триацетина и 20% сополимера стирола с 2-винилпиридином (29,5-69,5 по весу) с удельной вязкостью 0,592, измеренной при концентрации 5 г/л в диметилформамйде при 20°С,
Результаты по примерам 3-Ю представлены в табл. 2.
Пример 11. Согласно технологии псевдоожиженного слоя с ванной, снабженной системой Wurster, 350 г метионина, предварительно гранулированного в виде сферических частиц с титром 98%, средний диаметр которых составляет 0,5-0,63 мм, покрывают раствором (дисперсией в.000 см смеси 1,2-дихлорэтана с этанолом, 1:1 по объему), J20 г состава для капсу- лирования, образованного 50% зеина, 25% этилцеллюлозы, 8,3% триацетона и 16,6% сополимера 2-винвдгаиридина со стиролом (70-30), удельная вязкость которого составляет 0,560, измеренная при концентрации 5 г/п в диметилформамйде при 20°С.
По истечении 3 ч, получают равномерно покрытые оболочки гранулы с титром-72,1% метионина,
При рН б, выделение метионина составляет 10%, спустя 6ч, 25%, спустя 24 ч.
При рН 2.выделение метионина составляет 100%, спустя 15 мин.
Пример 12. Согласно технологии псевдоожиженного слоя в ванной, снабженной системой Wurster, 350 г хлоргидрата лизина, предварительно гранулированного в виде сферических частиц с титром 85%, средний диаметр которых составляет 0,63-0,8 мм, покрывают раствором (дисперсией в 1000 см смеси 1,2-диэхлорэтана с этанолом, 1:1 по объему), 120 г состава для капсулирования, образован0
5
0
5
0
5
0
5
0
ного 50% зеина, 25% этилцеллюлозы, 8,3% триацетина и 16,6% сополимера 2-винилпиридина со стиролом (70-30), удельная вязкость которого составляет 0,560, измеренная при концентрации 5 г/л, в диметилформамйде при 20°С.
Получают гранулы, титр которых по хлоргидрату лизина составляет 67,5%.
П р и м е. р 13, Работают, как в примере 12, используя тот же состав для капсулирования, для получения г гранул титр по хлоргидрату лизина которых составляет 51,2%.
Результаты по примерам 12 и 13 представлены в табл. 3. Формула изобретения
Состав для капсулирования биологически-активного вещества, зключаю- щий связующую систему из пленкообразующих компонентов и чувствительное к изменениям рН вещество, о т л и ,- чающийся тем, что, с целью повышения стабильности состава, при рН выше или равном 5 (в рубце) и выделении биологически-активного вещества при рН меньшем или равном 3,5 в качестве пленкообразующих веществ связующей системы состав содержит ацетобутират целлюлозы и/или этил- целлюлозу, и/или пеливинилацетат, и/или зеин и дополнительно компоненты, регулирующие гидрофильно гидро- фобный баланс, выбранные из группы: пропиленгликоль, дипропиленгликоль и триацетин, а в качестве чувствительного к изменениям рН вещества состав содержит сополимеры стирола с 2-винилпиридином или с 2-метил-5- винилпиридином или хитозан при следующем соотношении компонентов, %: Пленкообразующие компоненты
связующей системы 37,5-80,0 Компоненты, регулирующие
гидрофил ьно-гидр о- фобный баланс 6,6-40,0 Чувствительное к изменениям рН вещество 9,0-25,0
Таблица 1



| название | год | авторы | номер документа |
|---|---|---|---|
| СОСТАВ ДЛЯ КАПСУЛИРОВАНИЯ БИОЛОГИЧЕСКИ-АКТИВНОГО ВЕЩЕСТВА | 1992 |
|
RU2038025C1 |
| Способ нанесения покрытия на действующее начало | 1991 |
|
SU1816212A3 |
| Состав для капсулирования биологически активного вещества | 1988 |
|
SU1797470A3 |
| Способ получения кормовых гранул для жвачных животных | 1987 |
|
SU1651775A3 |
| СПОСОБ НАНЕСЕНИЯ ПОКРЫТИЙ ЛЕКАРСТВЕННЫЙ И/ИЛИ КОРМОВЫХ ВЕЩЕСТВ | 1991 |
|
RU2076701C1 |
| Состав для капсулирования биологически активного вещества | 1987 |
|
SU1748630A3 |
| КОРМОВАЯ ИЛИ МЕДИКАМЕНТОЗНАЯ КОМПОЗИЦИЯ ДЛЯ ЖВАЧНЫХ ЖИВОТНЫХ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1993 |
|
RU2106096C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГРАНУЛ КОРМОВОЙ ДОБАВКИ ДЛЯ ЖВАЧНЫХ ЖИВОТНЫХ | 1991 |
|
RU2035164C1 |
| МНОГОКОМПОНЕНТНАЯ ДОЗИРОВАННАЯ ФОРМА С КОНТРОЛИРУЕМЫМ ВЫДЕЛЕНИЕМ АКТИВНОГО ИНГРЕДИЕНТА | 1991 |
|
RU2111743C1 |
| Композиция защитной оболочки для биологически активных веществ | 1982 |
|
SU1428178A3 |
Изобретение относится к сельскому хозяйству. Целью изобретения является повышение стабильности состава при PH, большем или равном 5, и выделении биологически-активного вещества при PH, меньшем или равном 3,5. Состав для капсулирования биологически-активного вещества, например метионина или лизина, содержит связующую систему из пленкообразующих компонентов и чувствительное к изменениям PH вещество. В качестве пленкообразующих веществ используют ацетобутират целлюлозы, и/или этилцеллюлозу, и/или поливинилацетат, и/или зеин. Состав дополнительно содержит компоненты, регулирующие гидрофильно-гидрофобный баланс, выбранные из группы: пропиленгликоль, дипропиленгликоль и триацетин. В качестве чувствительного к изменениям PH вещества состав содержит сополимеры стирола с 2-винилпиридином или с 2-метил-5-винилпиридином или хитозан. Компоненты взяты в следующем соотношении, %: пленкообразующие компоненты связующей системы 37,5-80, компоненты, регулирующие гидрофильно-гидрофобный баланс 6,6-40, чувствительное к изменениям PH вещество 9 - 25. Для выявления чувствительности составов к изменению PH были использованы тесты, которые позволяют измерять высаливание активного вещества в зависимости от времени при разных значениях PH, вч при PH = 6 до PH = 2 или при PH = 5 до PH = 1,5. Результаты показывают, что в рубце (при PH, большем или равном 5) предложенный состав стабилен, а биологически-активное вещество активно выделяется и освобождается при PH, меньшем или равном 3,5. 3 табл.

| СПОСОБ ПРОИЗВОДСТВА ТАБАЧНОГО СЫРЬЯ | 2009 |
|
RU2401621C1 |
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
| БУРОИНЪЕКЦИОННАЯ СВАЯ С ЛОКАЛЬНЫМИ УШИРЕНИЯМИ | 2012 |
|
RU2514261C1 |
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
Авторы
Даты
1990-01-30—Публикация
1985-12-19—Подача