Изобретение относится к усовершенствованному способу получения 1,4-бис- полифторалкил-7-оксабицикло 2,2. fj- гептанов, которые обладают высокой стабильностью в интервале температур 300-330°С и могут быть использованы в технике в качестве высокотемпературных рабочих тел в замкнутом объеме.
Целью изобретения является повышение выхода и расширение ассортимента целевых продуктов за счет того, что в качестве исходного соединения используют соответствующие 2,5-бис- полифторалкил-1,3,4-оксадиазолы и проведения процесса при молярном соотношении производного оксадиазола и этилена, равном 1:6 в течение 20- 25 ч.
Пример 1. Получение 1,4- -бис(трифторметил)-7-оксабицикло- L2.2. Qгептана.
В сухую металлическую пробирку, содержащую 9,6 г (0,046 моль) 2,5- -бис(трифторметил)-1,3,4-оксадиазола и продутую сухим азотом конденсируют при -120°С 6 л (0,275 моль) отиле- на. Смесь нагревают при 220-230°С в течение 24 ч, охлаждают до -120°С, вскрывают, доводят до комнатной температуры и отгоняют избыток этилена. Остаток перегоняют. Выход 8,9 г (81%), т.кип. 143°С, т.пл. 24°С,
„25 „„,„ ,45
1Ј
1 ,3915, d4 1,4230.
СД
СД
со ел
Найдено, %: С 41,32; Н 3,20.
CgHsF60.
Вычислено, %: С 41,03; Н 3,42.
Пример 2. Получение 1,4-бис- (пентафторэтил)-7-оксабицнкло 2.2. f - гептана.
Аналогично примеру 1 из 2 г (0,006 моль) 2,5-бис(пентафторэтил)-1, 3,4-оксадиазола и 0,8 л (0,036 моль) этилена выделяют 1,7 г (78%), т.пл. . При выделении в отличие от припроцесса на выход целевых продуктов представлены в табл. 1 и 2.
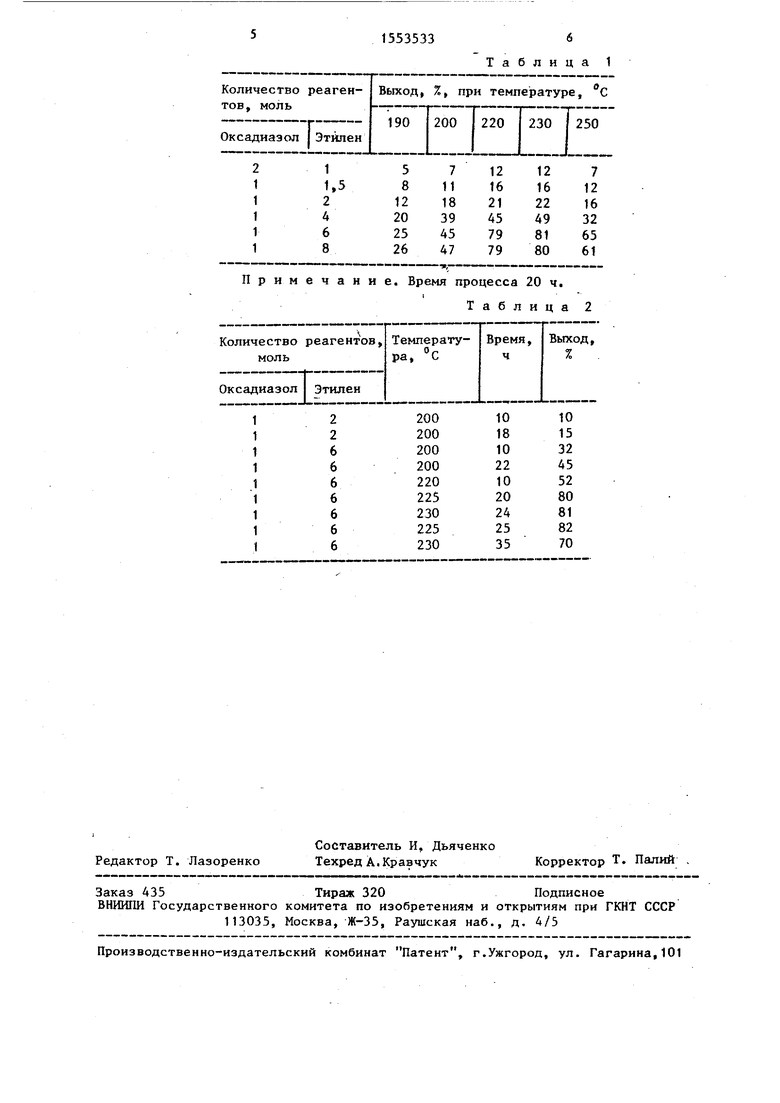
Как видно из табл. 1 и 2, выход целевых 1,4-бисполифторалкил-7-ок- сабицикло р. 2.1J гептанов максимален при молярном соотношении производное оксадиазола:этилен, равном 1:6, температуре 220-230 С и длительности

| название | год | авторы | номер документа |
|---|---|---|---|
| ДИФЕНИЛЬНЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ | 1997 |
|
RU2175319C2 |
| Способ получения производных 2-оксиметил-1,3,4-оксадиазола | 1974 |
|
SU511004A3 |
| Способ получения производных 1,2,5-оксадиазол-3,4-бис-карбоновой кислоты или их фармакологически приемлемых кислотно-аддитивных солей | 1982 |
|
SU1138026A3 |
| ПРОИЗВОДНЫЕ НИТРОКАТЕХОЛА В КАЧЕСТВЕ ИНГИБИТОРОВ СОМТ | 2006 |
|
RU2441001C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1,3-БИС-О-(ПОЛИФТОРАЛКИЛ)ГЛИЦЕРИНА | 2014 |
|
RU2559319C1 |
| Способ получения полифторалкиловых эфиров хлоругольной кислоты | 1985 |
|
SU1315451A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,1-ДИХЛОР-2,2-БИС-(4-ХЛОРФЕНИЛ)ЭТИЛЕНА | 2003 |
|
RU2257371C1 |
| Способ получения замещенных 1,4-дигидропиридинов | 1983 |
|
SU1360585A3 |
| Способ получения 2-ациламино-1,3,4-оксадиазолов | 1982 |
|
SU1074872A1 |
| Способ борьбы с нежелательной растительностью | 1989 |
|
SU1836015A3 |
Изобретение касается химии гетероциклических соединений, в частности получения 1,4-бисполифторалкил-7-оксабицикло-[2,2.1]-гептанов (где полифторалкил-трифторметильная, пентафторэтильная или гептафторпропильная группа), которые обладают высокой термостабильностью и может быть использовано в качестве высокотемпературных рабочих тел в замкнутом объеме. Цель - расширение ассортимента целевых продуктов и повышение выхода. Получение целевых продуктов ведут реакцией 2,5-бисполифторалкил-1, 3, 4-оксадиазолов (где полифторалкил указан выше) с этиленом в замкнутом объеме при нагревании до 220 - 230°С в течение 20 - 25ч и молярном соотношении реагентов 1:6. Эти условия позволяют повысить выход целевых веществ до 81% (в 2 раза). 2 табл.
мера 1 используют возгонку при атмос- JQ процесса 20-25 ч. Выход за указанные
25
;ферном давлении.
Найдено, %: С 35,71; Н 2,51.
,eO.
Вычислено, %: С 35,93; Н 2,39.
Пример 3. Получение 1,4- |5 -бис(гептафторпропил)-7-оксабицик- ло 2.2. гептана.
Аналогично примеру 2 из 2 г (0,005 моль) 2,5-бис(гептафторпропил)- -1,3,4-оксадиазола и 0,7 л (0,030 моль) JQ этилена выделяют 1,6 г (75%), т.пл. 58°С.
Найдено, %: С 33,51; Н 1,56.
с «г HgF,o.
Вычислено, %: С 33,18; Н 1,84.
Пример 4. Получение 1,4-бис- (трифторметил) -7-оксабицикло 2.2. Г гептана.
В сухую металлическую пробирку помещают 4,8 г (0,023 моль) 2,5-бис- (трифторметил)1,3,4-оксадиазола и конденсируют при -120°С 1 л (0,046 моль) этилена. Смесь нагревают при 205°С в течение 8ч, охлаждают, вскрывают, перегоняют. Выделено
2г (37%) целевого продукта с т.кип. 140 С, т.пл. 24°С, также зафиксировано выделение побочного продукта присоединения этилена 1,2 г и олигомер- ные вещества. Исходный 2,(три- фторметил)-1,3,4-оксадиазол был идентифицирован в легкокипящей фракции при помощи газожидкостной хроматографии, его содержание в смеси не более 20 (конверсия 98%).
Данные о влиянии температуры, соотношения реагентов и длительности
30
35
40
45
значения параметров приводит к сниже- нию выхода целевых продуктов.
Данный способ позволяет расширить ассортимент целевых продуктов (за счет получения соединений, где по- лифторалкил - пентафторэтил или геп- тафторпропил) и в 2 раза увеличить выход целевых продуктов по сравнению с прототипом.
Формула изобретения
Способ получения 1,4-бисполифтор- алкил-7-оксабицикло 2.2.Лгептанов формулы
i-O-
i -
где К, - трифторметильная, пентафторэтильная или гептафтор- пропильная группа,
взаимодействием 2,5-бисполифторалкил- -1,3,4-оксадиаэола с этиленом в замкнутом объеме при 220-230°С, отличающийся тем, что, с целью увеличения выхода и расширения ассортимента целевых продуктов, в качестве полифторсодержащего оксадиазо- ла используют соединения формулы
U-N
к
о
где 1Ц имеет указанные выше значения и процесс проводят при молярном соотношении 2,5-бисполифторалкил-1,3,4- -оксадиазол:5тилен, равном 1:6 в течение 20-25 ч.
5
5
Q
0
5
0
5
значения параметров приводит к сниже- нию выхода целевых продуктов.
Данный способ позволяет расширить ассортимент целевых продуктов (за счет получения соединений, где по- лифторалкил - пентафторэтил или геп- тафторпропил) и в 2 раза увеличить выход целевых продуктов по сравнению с прототипом.
Формула изобретения
Способ получения 1,4-бисполифтор- алкил-7-оксабицикло 2.2.Лгептанов формулы
i-O-
i -
где К, - трифторметильная, пентафторэтильная или гептафтор- пропильная группа,
взаимодействием 2,5-бисполифторалкил- -1,3,4-оксадиаэола с этиленом в замкнутом объеме при 220-230°С, отличающийся тем, что, с целью увеличения выхода и расширения ассортимента целевых продуктов, в качестве полифторсодержащего оксадиазо- ла используют соединения формулы
U-N
к
о
где 1Ц имеет указанные выше значения и процесс проводят при молярном соотношении 2,5-бисполифторалкил-1,3,4- -оксадиазол:5тилен, равном 1:6 в течение 20-25 ч.
Примечание. Время процесса 20 ч.
t
Таблица 2
Таблица 1
| Васильев Н.В., Ляшенко Ю.Е., Коломиец А.Ф., Сокольский Г.А | |||
| ХГС, 1987, № 4, с, 562. |
Авторы
Даты
1990-03-30—Публикация
1988-01-28—Подача