Изобретение относится к химии фос- форорганических соединений, а именно к усовершенствованному способу получения известных о -аминоалкилфосфо- нистых кислот общей формулы О
Н-СН-Р-Н
NH2 ОН
где R - -СН3, ,сНз
,
(СН5
C6H5CH2.CH5SCH2CH2
аналогов об-аминокарбоновых кислот, и может найти применение в качестве ингибиторов ферментов антибактериальных средств и гербицидов.
Целью изобретения является упрощение процесса и повышение выхода целевых продуктов
фос- енно олуо-
а
2CH2
т, тве иальрощецелеПоставленная цель достигается тем, что оксим альдегида добавляют к раст- 5 вору фосфорноватистой кислоты в низшем спирте и процесс проводят при тем-| пературе кипения растворителя
Известно, что оксимы под действием концентрированных сильных кислот и при повышенных температурах способны перегруппироваться в амиды (перегруппировка Бекмана), превращаться в нитрилы (для альдоксимов) и гидролизо- ваться до карбонильных соединений„
Фосфорноватистая кислота является сильной кислотой и следует ожидать, что при повышенных температурах окси- мы под ее воздействием будут претерпевать описанные превращения. Кроме Того, H3PO-z. является термически неустойчивым соединением,,
Согласно предлагаемому способу взаимодействие оксимов с Н3РО при повышенных температурах в среде полярного органического растворителя протекает иным образом и приводит к аминоалкилфосфонистым кислотам.
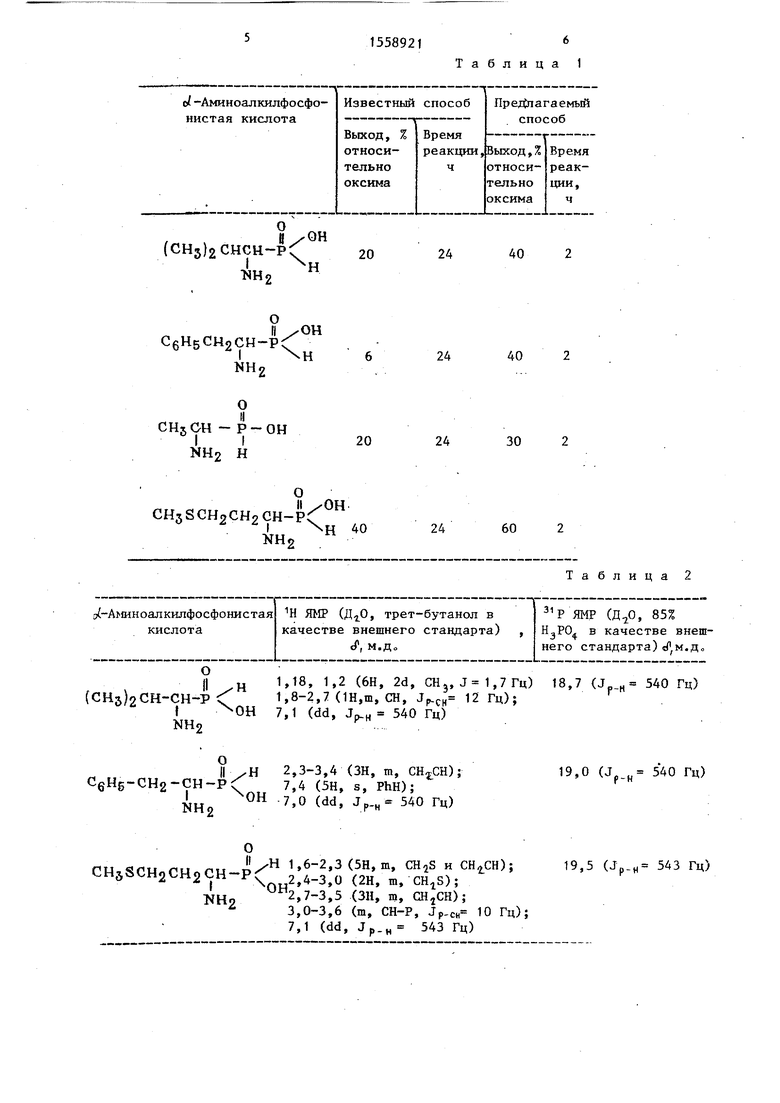
Выходы о/-аминоалкилфосфонистых кислот приведены в табл 1„
Пример К Получение о(амино- этилфосфонистой кислоты в метанолео
К раствору 10,6 г NaHjPO -H.p
(0,1 моль) в 6 мл воды добавляют порциями 10 мл конц I1C1, а затем б мл изопрапилового спирта, Выпавлзий осадок фильтруют, фильтрат упаривают в вакууме при температуре не выше 40°С, остаток растворяют в 10 мл абСоСН3ОН, нагревают до кипения и при перемешивании добавляют в атмосфере инертного газа в течение 30 мин раствор ацетСНЭОН„ После кипячения в ч охлазвдают до 20 С, удаляальдоксима (3,65 г, 0,05 моль) в 10 мл абс течение 2 ют растворитель в вакууме -Амино- этилфосфонистую кислоту выделяют известным способом Выход 3,4 г (32%). ТсПЛо 208-2100С„
Найдено,, Р 28,27
%: С 22,23; Н 7,43;
C,jH802PN
Вычислено, %: С 22,00; Н 7,35; Р 28,41 о
Rf 0,35 (восходящая хроматогра- атя на пластинах Silufol UVlS4 система изопропиловый спирт-концо аммиак- вода 7:1:2, проявление нингидрином и реактивом на фосфорК
U отн Ala 0,90 (электрофорез на бумаге FN 18, буфер 0,05 М (СНЭСООШ4)«
При окислении бромом в солянокислом растворе единственным продуктом является ot-аминоэтилфосфоновая кислота с,
Н ЯМР ( трет-бутанол как внешний стандарт) сГ, 7,l(dd, J р-Н 538 Гц); 2,9-3,6 (га, ЛрсИ10,5 Гц); 1,5 (ЗН, dd)0
3fP ЯМР (ЦгО, 85% НЭРО« как внешний стандарт) Р ; 22,2 м„д, Jp..i538rq,
Пример 2„ Получение о -амино- этилфосфонистой кислоты в этаноле.
О
5
0
5
0
5
45
К раствору 10,6 г Na H1P04
Н20
0
( моль) в 6 мл воды прибавляют пор- цИ, ми 10 мл конц,, НС1, а затем 6 мл изопропилового спирта Выпавший осадг-к фильтруют, упаривают в вакууме при емпературе не выше 40°С, остаток разоряют в 10 мл абс„ С2Н5ОН, нагрева ji до кипения и при перемешивании доб -вляют в атмосфере инертного газа в течение 30 мин раствор ацетальдог- сима (3,65 г, 0,05 моль) в 10 мл абс. С2Н50Н„ После кипячения в течение 2 ч Йроводят обработку реакционной смеси как в примере 10 Получают 3,2 г (Зр%) вещества
Аналогичным образом получают о(-ами- ноизобутилфосфонистую кислоту, о/-ами- но- у-бензилметилфосфонистую кислоту, о{-амино- v-метилтиопропилфосфонястую кислоту
Данные элементного анализа и физико-химические характеристики полученных соединений приведены в табЛо2„ i
Таким образом, предлагаемый способ получения сб-аминоалкилфосфонистых кислот позволяет упростить процесс и повысить выход целевых продуктов.,
Формула изобретения
Способ получения о -аминоалкь.чфос- фонистых кислот взаимодействием ок- сима альдегида с фосфорноватистой кислотой в атмосфере инертного газа, отличающийся тем, что, с целью упрощения процесса и повышения выхода целевого продукта, процесс ведут в среде низшего алифатического спирта при кипячении реакционной смеси путем добавления оксима альдегида к раствору фосфорноватистой кислоты в спирте
Таблица 1

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения эфироамидов фосфорноватистой кислоты | 1984 |
|
SU1182046A1 |
| Способ получения @ , @ -диалкил(диалкоксиметил)-фосфонитов | 1984 |
|
SU1182045A1 |
| СИНТЕЗ КАРБАМОИЛПИРИДОНОВЫХ ИНГИБИТОРОВ ИНТЕГРАЗЫ ВИЧ И ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ | 2009 |
|
RU2527451C2 |
| Способ получения С-фосфор (Ш) замещенных азометинов | 1987 |
|
SU1444339A1 |
| ПРОИЗВОДНЫЕ ПИРАЗОЛОПИРИМИДИНА, КАК ИНГИБИТОРЫ ЦИКЛИН-ЗАВИСИМОЙ КИНАЗЫ | 2005 |
|
RU2414472C9 |
| ПРОМЕЖУТОЧНОЕ ПРОИЗВОДНОЕ ЦЕФАЛОСПОРИНА И СПОСОБ ПОЛУЧЕНИЯ ЦЕФАЛОСПОРИНА | 1995 |
|
RU2150471C1 |
| Синтез карбамоилпиридоновых ингибиторов интегразы ВИЧ и промежуточных соединений | 2013 |
|
RU2638923C2 |
| Способ получения амидов цианкарбоновых кислот (способ Станкявичюса) | 1989 |
|
SU1625872A1 |
| Способ получения N-( @ -замещенный алкил)-N @ -(имидазол-4-ил)-гуанидина или его кислых аддитивных солей | 1988 |
|
SU1802811A3 |
| Новые 3,4-гидроксиамины пинановой структуры | 2016 |
|
RU2631871C1 |
Изобретение относится к химии фосфорорганических соединений, в частности к получению α-аминоалкилфосфонистых кислот общей ф-лы R-CH(NH2)-P(O)(OH)-H, где R = -CH3, (CH3)2-CH-, C6H5CH2-, CH3SCH2CH2-, которые находят применение в качестве ингибиторов ферментов антибактериальных средств и гербицидов. Цель - упрощение процесса и повышение выхода целевого продукта. Получение ведут путем добавления оксима альдегида к раствору фосфорноватистой кислоты в спирте в среде низшего алифатического спирта в атмосфере инертного газа. 2 табл.
О
и/он
(СН5)2СНСЦ-Р -NH2
н
О
и /он
C6H5CH2CH-PCQ NH2
О
СН5СН -Р-ОН NH2 H
О
II /ОН
CH5SCH2CH2CH-PC
NH2
1Н ЯМР (ДгО, трет-бутанол в качестве внешнего стандарта)
М.До
О
(СНз)2СН-СН NH2
|| н 1,18, 1,2 (6Н, 2d, CH«tJ- 1,7Гц) 18,7 (J н -Р С1,8-2,7 (1H,m, CH, 12 Гц);Г
7,1 (dd, 540 Гц)
ОН
о
, /
Н2,3-3,4 ЗН, т, );
С6Нб-СН2--СН-Р 7,4 (5Н, s, PhH);
NHo °Н7 ° (dd JP-H 54° ru)
Ј
20
24
40
24
40
20
24
30
24
60
Таблица 2
31
Р ЯМР (Д70, 857
в качестве внешнего стандарта) .д„
нэро4
540 Гц)
19,0 (J 540 Гц)
Авторы
Даты
1990-04-23—Публикация
1988-06-14—Подача