Изобретение относится к медицинской вирусологии, а именно к производству вирусных препаратов.
Однако целевой продукт, получав-; мый этим способом, обладает низкой : инфекционной активностью.
Целью изобретения является снижение количества дефектных интерферирующих частиц в вирусной популяции, повышение ее инфекционной активности и улучшение тем самым качества вирусного препарата.
Пример 1. Получение биомассы вакционного штамма вируса гриппа ГА/Ленинград/0139/ 76/H3N2/,
I пассаж на развивающихся куриных эмбрионах (РКЭ)о Десятикратные разведения маточного вируса в объеме 2 мл делают на эабуференном физиологическом растворе рН 7,2, в который добавляют 0,01 М сернокислого магния и мономицин до концентрации 500 мкг/мл. Каждым разведением вируссодержащей жидкости в объеме 0,2 мл заражают по четыре 10-11-дневных РКЭ и инкубируют при в течение 18 ч О наличии размножившегося вируса судят по результатам реакции гемагглютинации СРГА) с 1% куриными эритроцитами. Инфекционную активность вируса (ЭИД5о
СЛ
о
4
00 СП
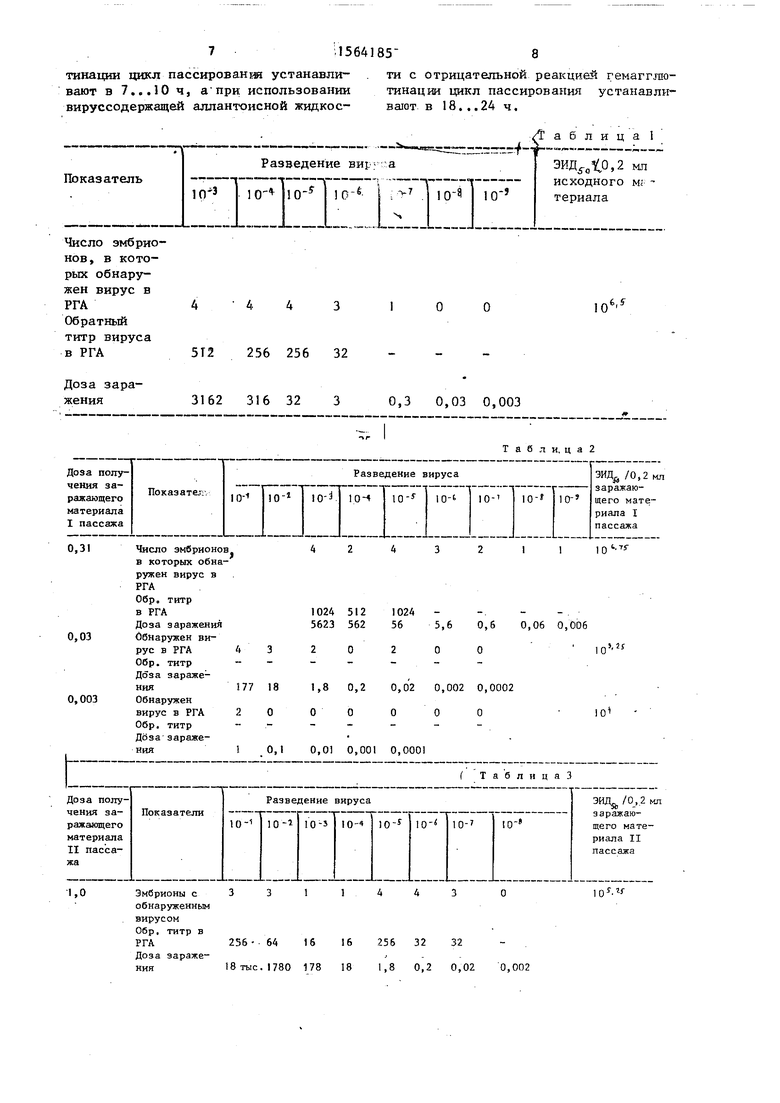
/0,2 мл) рассчитывают по результатам РГА методом Кербера в модификации t Ашмарина, после чего вычисляют дозы заражения, соответствующие использованным разведениям вируса. Результаты титрования приведены в табл.1.
Для последующего пассажа раздельно собирают вируссодержащую аллантоис- йую жидкость (ВАЖ) из РКЭ, заражен- йых последним разведением, обеспечивающим учитываемую репродукцию вируса (), а также ВАЖ с отрицатель- Ной РГА (разведения исходного материала Ю- и )
II пассаж на РКЭ. Отобранные 3 образца ВАЖ разводят с шагом 10 физиологическим раствором, содержащим указанные добавки 0,2 мл каждого разведения заражают 3 параллельные пар- тии РКЭ, которые инкубируют в течение 20 ч при 36 С. Далее определяют нали-i чие вируса в РГА. Результаты приведены в табл.2.
Для последующего пассажа раздель- но собирают ВАЖ из РКЭ, зараженных разведением, которая при наименьшем содержании вирусных частиц обеспечивает репродукцию вируса, определяемую в РГА. Таковым материалом является ВАЖ, полученная после заражения в I пассаже дозой 0,003. Для III пассажа отбирают ВАЖ из разведений ряда: и 10 (первое из этих разведений является минимальным с положительной РГА, а остальные характеризуются отрицательной РГА)
III пассаж на РКЭ. Отобранные 4 образца ВАЖ разводят с шагом 10 указанным раствором. 0,2 мл каждого разведения заражают 4 параллельные партии РКЭ, которые инкубируют в течение 22 ч при 36 С Затем определяют наличие вируса в РГА. Результаты представлены в табло3
В качестве посевного материала для накопления вируса используют вирус III пассажа,полученный в результат заражения наименьше дозой,еще обеспечивающей репродукцию вируса, определяемог в РГА.Таковым материалом является ВАЖ, полученная после заражения дозой 0,6 ЭЙД 5о/0,2 мл.
Накопление вируса. Посевной материал помещают в холодильник при +4°С на 18 ч о Этот срок необходим в используемом в данном примере варианте заражения РКЭ на стадии накоп- ления вируса наперед заданной дозой
5
5
(возможен вариант проведения стадии накопления без определения заражающей дозы ). В период хранения ВАЖ в холодильнике производят титрование ее пробы для установления инфекционной активности. В данном примете посевной вирус, используемый для накопле- чя имеет инфекционную активность 10 ЭИД в 0,2 мл.
Для накопления вируса партию 10- -дневных РКЭ заражают дозой 10 } ,2 мл и инкубируют в течение 24 ч при 36°С. Получают целевой продукт - ВАЖ с инфекционной активностью 10 3Hflg.0/0,2 мл и обратным титром в РГА 512. Индекс ИА/ГА 10 f0 5 :512 10r g
Контроль о Для контроля пассирование данного вируса проводят 3-кратно при той же температуре и экспозиции по 48 ч с использованием заражающей дозы 1-3 ЭИД50/0,2 мл с последующим .накоплением вируса в том же режиме при заражающей дозе 103 ЭЙД jo/0,2 мл. Получают ВАЖ с инфекционной активностью 09 °и обратным титром в РГА 2048. ИА/ГА 109 :2048 1057 что существенно ниже, чем в предлагаемом способе.
Для контроля проводят также седи- ментационный анализ целевых продуктов, полученных по прототипу и по данному примеру. Вирусная популяция, полученная по прототипу, гетерогенна. Вирусная популяция, полученная предлагаемым способом, гомогенна и состоит из стандартного (инфекционного) вируса, т.е. вируса, не содержащего ДИЧ,
П р и м е р 2. Полученные биомассы вакционного штамма вируса гриппа A/Texac/l/77a/H3N2/.
Маточный лиофилизированный вирус указанного штамма трехкратно пассируют на РКЭ при кратности разведений заражающего материала с шагом 10. Для последующих заражений при пассировании отбирают ВАЖ ближайших двух разведений с отрицательной РГА после разведения, использование которого давало положительную РГА (как описано в примере 1). Пассирование проводят при температуре 35°С и экспозициях 18, 20 и 24 ч (заявляемый режим экспозиции), а также 16 и 30 ч (запре-i дельные режимы).
Стадию накопления вируга проводят при 35°С в течение 20 ч с использованием заражающей дозы 100 ЗИД5о/0,2мл.
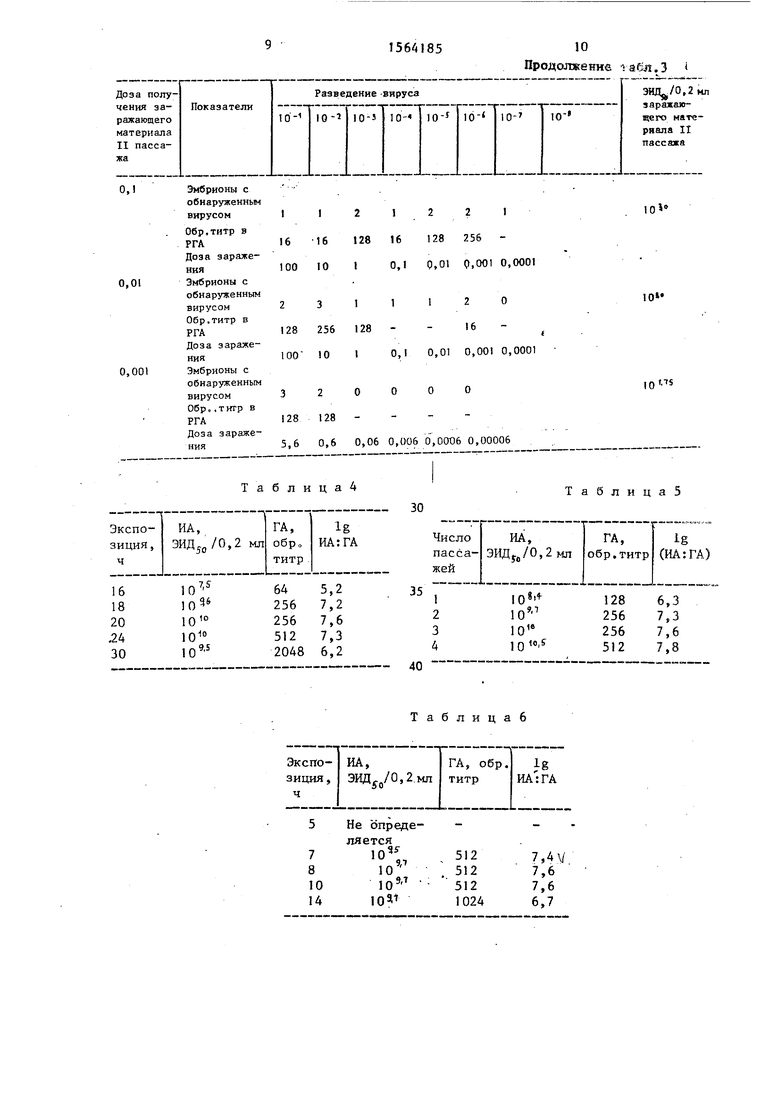
Получают целевые продукты (ВАЖ) с характеристиками, указанными в табл.4.
Как видно из табл.3,наибольшая степень обогащения ВАЖ инфекционным вирусом имеет место при экспозиции v 18-24 ч. В этом режиме наблюдается резкий максимум удельной активности (ИА:ГА,) , что свидетельствуете повышении качества целевого продукта.
П р и м е р 3. Получение биомассы вакционного штамма вируса гриппа А/Техас/1/77a/H3N2/ в зависимости от числа пассажей.
Маточный лиофилизированный вирус указанного штамма пассируют на РКЭ при 35°С,экспозиция 20 ч. Стадию накопления вируса проводят, как описано в примере 2, после 1,2,3 и 4 пас сажей. Результаты контроля полученной ВАЖ приведены в табл.5 (отбор материала для последующего пассирования производили, как в примере 2).
Из табло 5 видно, что одного пассажа недостаточно для обеспечения высокого качества целевого продукта.
. П р и м е р 4. Маточный лиофилизированный вирус гриппа штамма А/Техас/1/7 a/H3N2/ двухкратно пассируют при 35°С и экспозициях 7,8 и 10 ч (предлагаемый режим) и 5 и 14 ч (запредельные режимы). Во 2-ом цикле пассирования РКЭ заражают ВАЖ с положительной РГА при минимальной дозе заражения эмбрионов предыдущего цикла (10 ЭВД50/0,2 мл). После II пассажа собирают БАЯ из эмбрионов, еще содержащих вирус по данным РГА в последнем разведении. Эта ВАЖ является посевным материалом для стадии накопления вируса.
Стадию накопления вируса проводят как в примере 2.
ВАЖ отбирают. Получают целевой продукт с характеристиками,приведенными в табл.6.
Как видно из табл„6, только в предлагаемом режиме достигается высокое качество целевого продукта по показателю удельной активности.
П р и м е р 5. Маточный лиофилизированный вирус гриппа штамма А/Техас/ /l/77a/H3N2/ пассируют при 35 С в течение 8 ч. Для второго пассажа отбирают ВАЖ с отрицательной РГА при дозе заражения 0,1 и 0,01 ЭИД5о/0,2 мл Второй пассаж проводят инкубированием в течение 20 ч. После II пассажа со
1564185
0
5
5
0
0
5
0
5
0
5
бирают ВАЖ нз эмбрионов, еще содержащих вирус по данным РГА в последнем разведении Эту ВАЛ используют в качестве посевного материала на стадии накопления вируса. Ей соответствует доза заражения предшествующего разведения 0,01 ЭИД,/0,2 мл.
В данном примере для III пассажа используют в качестве заражающего материала ВАЖ II пассажа с положительной РГА при минимальной дозе заражения в указанном пассаже. Поэтому экспозицию III пассажа устанавливают равной 8 ч.
В качестве посевного материала для накопления вируса используют ВАЖ III пассажа, полученную в результате заражения дозой, еще обеспечивающей репродукцию вируса, учитываемую в РГА.
Стадию накопления вируса проводят как в примере 1. Получают целевой продукт с инфекционной активностью ИА - 10™ ,2 мл и ГА 512. Следовательно lg (ИА:ГА) 10,8 - -Ig512 8,1.
В табл.7 приведены сравнительные данные технических характеристик целевых продуктов, полученных по пред- ла-раемому способу и прототипу. Эти данные систематизированы по результатам 50 испытаний каждого из способов на указанных штаммах вируса гриппа. При этом для предлагаемого способа обобщены выходные данные различных режимов его осуществления.
Формула изобретения
Способ культивирования вируса гриппа путем многоциклового пассирования, вычисления инфекционной активности вируса и .последующего накопления вируса в развивающихся куриных эмбрионах, отличающий- с я тем, что, с целью снижения количества дефектных интерферирующих частиц в вирусной популяции и повышения ее инфекционной активности, в каждом последующем цикле пассирования эмбрионы заражают вируссодержащей ал- ( лантоисной жидкостью предыдущего цикла, имеющей отрицательную и/или положительную реакцию гемагглютинации при минимальной инфекционной активности, при этом при использовании вируссодержащей аллантоисной жидкости с положительной реакцией гемагглю-
тинации цикл пассирования устанавливают в 7...10 ч, а при использовании вируссодержащей аллантоисной жидкости с отрицательной реакцией гемагглю- тинации цикл пассирования устанавливают в 18... 24 ч.
/Таблица 1



| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИННЫЙ ШТАММ ВИРУСА ГРИППА А(Н3N2)-А/8/Perth/16/2009 ДЛЯ ПРОИЗВОДСТВА ИНАКТИВИРОВАННОЙ ГРИППОЗНОЙ ВАКЦИНЫ | 2010 |
|
RU2458124C2 |
| Способ получения инактивированной гриппозной вакцины | 1991 |
|
SU1822791A1 |
| ШТАММ ВИРУСА ГРИППА А/Гонконг/1/68/162/35 (H3N2)-УНИВЕРСАЛЬНЫЙ ДОНОР ВНУТРЕННИХ ГЕНОВ ДЛЯ РЕАССОРТАНТОВ И РЕАССОРТАНТНЫЕ ШТАММЫ А/СПБ/ГК/09 (H1N1) И А/НК/Astana/6:2/2010 (H5N1), ПОЛУЧЕННЫЕ НА ЕГО ОСНОВЕ | 2011 |
|
RU2511431C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЖИВОЙ ГРИППОЗНОЙ ВАКЦИНЫ | 1995 |
|
RU2080124C1 |
| Рекомбинантный штамм вируса гриппа A/PR8-NS124-Luc и способ оценки поствакцинальных нейтрализующих антител с использованием биолюминесцентной детекции | 2019 |
|
RU2759054C2 |
| Штамм вируса гриппа A/HK/HK/6:2/2016 (H9N2) для получения инактивированных и живых гриппозных вакцин | 2018 |
|
RU2702833C1 |
| Штамм вируса гриппа A/UNL/HK/2:6/2017 (H5N8) для получения инактивированных и живых гриппозных вакцин | 2018 |
|
RU2702834C1 |
| Штамм вируса гриппа A/Shanghai/HK/6:2/2013 (H7N9) для получения инактивированных и живых гриппозных вакцин | 2017 |
|
RU2664460C1 |
| Штамм вируса гриппа А/Япония/ГК/6:2/2014 (H2N2) для получения инактивированных и живых гриппозных вакцин | 2017 |
|
RU2644670C1 |
| Рекомбинантный штамм вируса гриппа A/PR8/HK-NS80E85A, экспрессирующий фрагменты антигенов ESAT-6 и Ag85A M.tuberculosis, для получения векторной вакцины против туберкулеза | 2018 |
|
RU2678175C1 |
Изобретение относится к медицинской вирусологии, точнее к производству вирусных препаратов. Целью изобретения является снижение количества дефектных интерферирующих частиц в вирусной популяции, повышение ее инфекционной активности и улучшение тем самым качества вирусных препаратов. Для этого вируссодержащую аллантоисную жидкость каждого разведения всех циклов контролируют в реакции гемагглютинации (РГА). При этом в каждом последующем цикле пассирования развивающиеся куриные эмбрионы заражают вируссодержащей аллантоисной жидкостью (ВАЖ) с отрицательной и/или положительной РГА при минимальной инфекционной активности предшествующей заражающей дозы. Длительность циклов пассирования при этом устанавливают для проб ВАЖ с положительной РГА в 7-10 ч и проб ВАЖ с отрицательной РГА в 18-24 ч. 7 табл.
Показатель
512 256 256 32
Доза заражения
3162 316 32
Доза получения заражающегоматериала I пассажа
0,31 Число эмбрионов в которых обнаружен вирус в РГА
Обр, титр в РГА Доза заражения
0,03 Обнаружен вирус в РГА Обр. титр Доза заражения
О,003 Обнаружен
вирус в РГА Обр. титр Доза заражения
1024 512 1024 5623 562 56 5,6 0,6 0,06 0,006
О
О
О
177 18
1,8 0,2 0,02 0,002 0,0002 00000
1 0,1 0,0) 0,001 0,0001
10
(,5
0,3 0,03 0,003
Т а б л и. ц а 2
10
-л
О
О
,,U
10
Не определяется
10; 10 10
9,1 9Л
Таблицаб
512 512 512 1024
7,4V 7,6 7,6 6,7
11
1564185
lg Ю,2±0,04 7,5±0,04 ЭЙД ,„/0,2
т s Obv 576+55 480i46
ТИТГ)
7,4
4,8
12 , Таблица
7,4
4,8
| Регламент производства вакцины гриппозной инактивированной жидкой типа А, очищенной и концентрированной градиентным центрифугированием № 130-79 | |||
| Видоизменение пишущей машины для тюркско-арабского шрифта | 1923 |
|
SU25A1 |
| Коневская И.З | |||
| Пути усовершенствования технологии производства живой гриппозной вакцины Автореф | |||
| дис | |||
| на соискание ученой степени канд | |||
| биол; наук | |||
| Л, 1972, | |||
Авторы
Даты
1990-05-15—Публикация
1988-07-05—Подача