Изобретение относится к медицине, а именно к хроматографическому анализу, и может быть использовано для анализа экзогенных веществ стаминоблокаторов циметидина и ранитидина в биологических жидкостях.
Цель изобретения - повышение точности способа.
Способ осуществляется следующим образом.
Для анализа берут 1 мл плазмы, содержащей циметидин или ранитидин} добавляют 100-150 мг сухого карбоната натрия или 0,5 мл 0,001 М NaOH для создания рН в диапазоне 8,2-8,7 и 15 мл хлороформа. После 10-минутного встряхивания водную и органическую фазы разделяют центрифугированием, водную фазу удаляют, а органическую
упаривают досуха при 40°С с помощью роторного испарителя. Сухой остаток растворяют в 0,5 мл подвижной фазы и наносят аликвоту (0,05 мл) на колонку. Разделение осуществляется на колонке, заполненной силикагелем с обращенной фазой (С (8),с помощью сме- си ацетонитрил - 50 КС1 + 0,U CRjCOOH в воде в соотношении 8:92 (по объему). Количественное определение концентраций осуществляют с помощью спектро- фотометрического детектора. Детектирование проводят при длинах волн, соответствующих максимальному поглоще-1 кию: 218-222 нм для циметидина и 222- 22 нм для ранитидина. Количественное определение циметидина и ранитидина осуществляют методом калибровки. Калибровочные зависимости линейны в
СЛ
ч
СЛ
о
диапазоне концентраций 0, 1-20 мкг/мл для циметидина и 0,05-2,5 мкг/мл для ранитидина. Оба указанных диапазона концентраций шире диапазонов концент- раций циметидина и ранитидина, наблюдаемых в плазме крови больных при любом способе назначения препарата.
Минимальные обнаруживаемые с помощью предлагаемого способа концентра- Ции циметидина и ранитидина составляют 50 и 20 нг/мл соответственно. Способ достаточно прост, надежен и экономичен вследствие использования кодоступных (в том числе отечествен- ных) реактивов, позволяет без замены подвижной фазы и последующей длительной стабилизации колонки определять циметидин и ранитидин в плазме крови, что дает дополнительный экономи- ческий эффект.
Изобретение иллюстрируется следующими примерами„
Пример 1. Больной С., 37 лет, поступил в 10-е терапевтическое отде- ление 23 ГКБ с диагнозом - язвенная болезнь двенадцатиперстной кишки, Нейтронорм (циметидин фирмы Ebeve Австрия) назначали внутривенно в дозе 200 MI в 5 мл 0,9%-ного раствора хлористого натрия. Забор крови проводили из локтевой вены другой руки черес, катетер до и через 5, 10, 15, 30 мин, 1, 2, 4, 5, 6 ч после приема циметидина. Кровь центрифугировали при 1 3000 об/мин. Плазму отбирали и хранили при -20°С. К 1 мл плазмы добавляли 100 мг сухого карбоната натрия для создания рН 8,2 и 15 мл хлороформа. После 10-минугного встряхивания водную и органическую фазы разделяли центрифугированием (5 мин при 3000 об/мин), водную фазу удаляли, а органическую упаривали при досуха с помощью роторного испарителя Rotavapor R-110 (лирмы- Buchi 3 ФРГ). Сухой остаток растворяли а 0,5 мл подвижной фазы, аликво- ту (0,05 мл) наносили на колонку. Определение циметидина проводили на жидкостном хроматографе Alt-ex 110 А (США) с инжектором на 0,05 мл и колонкой (250x4,6 мм) с неподвижно фазой Spherisorb ODS 5 мкм. Подвижн фазой служила смесь ацетонитрил - 5% КС1 + 0,1% СНЭСООН в воде в соотношении 8:92 (по объему), скорость элюирования 1,5 мл/мин. Детектирование проводили с помощью спектрофото
5 0
5 о $
5
0
5
метра Hitachi 100-40 на длине волны 218 нм. Результаты приведены в табл.1.
П р и м е р 2. Больной С., поступил в 10-е терапевтическое отделение 23 ГКБ с диагнозом - язвенная болезнь двенадцатиперстной кишки. Нейтронорм (циметидин фирмы Ebewe, Австрия) назначали внутривенно в дозе 200 мг в 5 мл 0,9%-ного хлористого натрия. Забор крови проводили из локтевой вены другой руки через катетер до и через 5, 10, 15, 30 мин, 1, 2, 4, 5, 6 ч после приема циметидина. Кровь центрифугировали при 3000 об/мин. Плазму отбирали и хранили при -20°С, К 1 мл плазмы добавляли 0,5 мл 0,001 М NaOH для создания рН 8,7 и 15 мл хлороформа. После 10-минутного встряхивания водную и органическую фазы разделяли центрифугированием (5 мин при 3000 об/мин), водную фазу удаляли, а органическую упаривали при 40°С досуха с помощью роторного испарителя Rotavapor R-110 (фирмы Bu- chi, ФРГ). Сухой остаток растворяли в 0,5 мл подвижной фазы, аликвоту (0,005 мл) наносили на колонку. Определение циметидина проводили на жидкостном хроматографе Altex 110 А (США) с инжектором на мл и колонкой (250x4,6 мм) с неподвижной фазой Spheiisorb ODS 5 мкм. Подвижной фазой служила смесь ацетонитрил - 5% КС1 + 0,1% СН3СООН в воде в соотношении 8:92 (по объему); скорость элюирования 1,5 мл/мин. Детектирование проводили с помощью спектрофотометра Hitachi 100-40 на длине волны 222 нм. Результаты приведены в табл. 2.
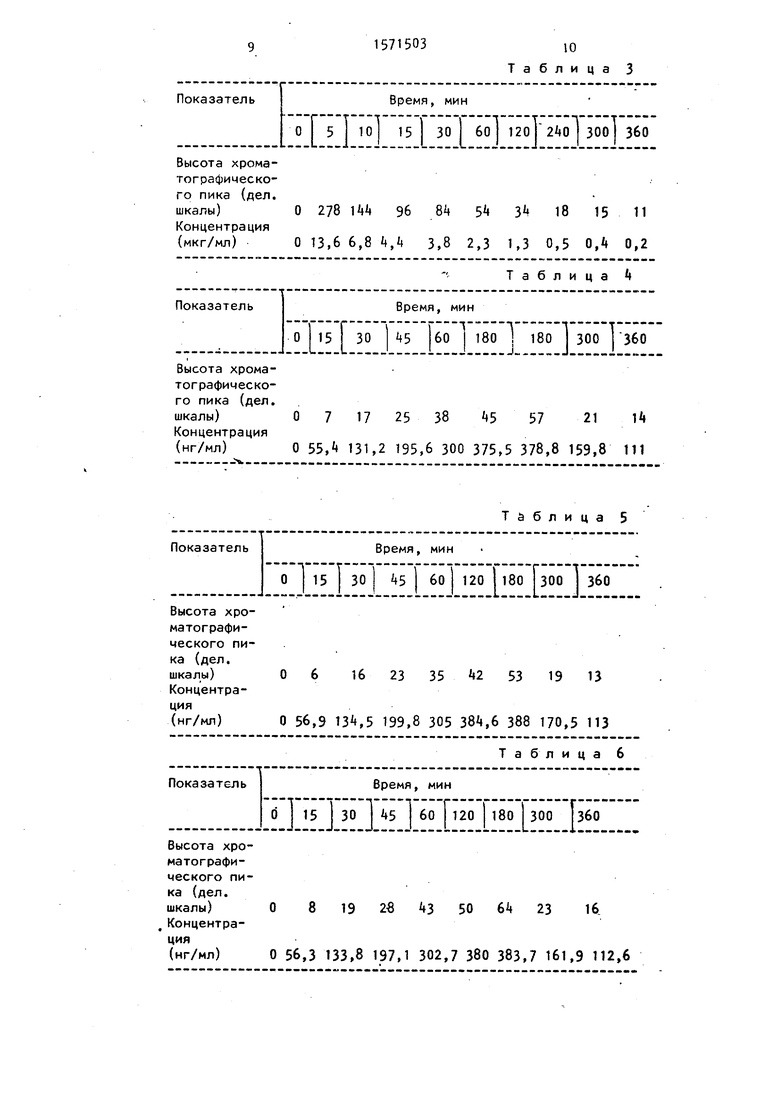
П р и м е р 3. Больной С., 37 лет, поступил в 10-е терапевтическое отделение 23 ГКБ с диагнозом - язвенная болезнь двенадцатиперстной кишки. Нейтронорм (циметидич фирмы Ebewe, Австрия) назначали внутривенно в дозе 200 мг в 5 мл 0,9%-ного раствора хлористого натрия. Забор крови проводили из локтевой вены другой руки через катетер до и через 5, Ю, 15, 30 мин, 1, 2, 4, 5, 6 ч после приема циметидина. Кровь центрифугировали при 3000 об/мин. Плазму отбирали и хранили при -20°С. К 1 мл плазмы добавляли сухой карбонат натрия до насыщения (150 мг) для создания ,5 и 15 мл хлороформа. Поеле 10-минутного встряхивания водную и органическую фазы разделяли центрифугированием (5 мин при 3000 об/мин), водную фазу удаляли, а орггничес ю упаривали при 40° Г, досуха с помощью роторного испарителя Rota-vapor R-110 (фирмы Buchi, ФРГ). Сухой остаток растворяли в 0,5 мл подвижной фазы и аликвоту СО,05 мл) наносили не колонку. Определение циметидина проводили на жидкостном хроматографе Altex 110 А (США) с инжектором на 0,05 мл и колонкой (250x4,6 мм) с неподвижной фазой Spherisorb 5 мкм. Подвижной фазой служила смесь зцето- нитрил - 5% КС1 + 0,1% СНЭСООН в воде в соотношении 8:92 (по объему); скорость элюирования 1,5 мл/мин. Детектирование проводили с помощью спектрофотометра Hitachi 100-40 на длине волны 220 нм. Результаты приведены в табл. 3.
П р и м е р 4. Больной П., 32 года поступил в 11-е терапевтическое отделение 23 ГКБ с диагнозом - язвенная болезнь двенадцатиперстной кишки. Ра- нисан (ранитидин фирмы Здравле, K)i о славия) назначали перорально в дозе 150 мг. Забор крови проводили из локтевой вены через катетер до и через 15, 30, 45 мин, 1, 2, 3, 5, 6, 7 ч после приема ранигидина. Кровь центрифугировали при 3000 об/мин. Плазму отбирали и хранили при -20 С. К 1 мл плазмы добавляли 100 мг сухого карбоната натрия для создания ,2 и 15 мл хлороформа. После 10-минутно(о встряхивания водную и органическую фазы разделяли центрифугированием (5 мин при 3000 об/мин), водную фазу удаляли, а органическую упаривали при 40°С досуха с помощью роторного испарителя Rotavapor R-110 (фирмы Wclii, ФРГ). Сухой остаток растворяли в 0,5 мл подвижной фазы, эликвоту (0,05 мл) наносили на колонку. Определение ранитидина проводили на жидкостном хроматографе Altex 110 А (США) с инжектором на 0,05 мл и колонкой (250x4,6 мл) с неподвижной фазой Spherisorb 5 мкм. Подвижной фазой служила смесь ацегонитрил - 5% КС1 + 0,1% СНЭСООН в воде в соотношении 8:92 (по обьему), скороста элюирования 1,5 мл/мин. Детектирование проводили с помощью спектрофотометра Hitachi 100-40 на длине волны 222 нм. Результаты приведены в табл.,4
O
П р и м е р 5. Больной П., 32 года, поступил в 11-е терапевтическое отделение 23 ГКБ с диагнозом - язвенная болезнь двенадцатиперстной кишки Ра- нисан (ранитидин фирмы Здравле, Югославия) назначали перорально в дозе ISO мг. Забор крови проводили из лок- певой вены через катетер до и через 15, 30, 45 мин, , 2, 3, 5, 6, 7 ч после пгиема ранитидина. Кровь центрифугировали при 3000 об/мин. Плазму отбирали и хранили при -20°С. К 1 мл плазмы добавляли 0,5 мл 0,001 М NaOH
, длД создания рН«8,7 и 15 мл хлороформа,, После 10-минутного встряхивания водную и органическую фазы разделяли цечгрифуированием (5 мин при 3000 об/1 ин), водную фазу удаляли,
0 а органическую упариззли при 40°С цогуха с помощью роторного испарителя Rotavapor K-110 (фирмы Buchi, ФРГ;. Сухой остаток растворяли в 0,5 мл подвижной фазы, аликвоту
5 (0,05 мл) наносили на колонку. Определение ранитидина проводили на жидкостном хроматографе Altex 110 А (США) с инжектором на 0,05 мл и колонкой (250x4,6 мм) с неподвижной фаQ Зой Spherisoib ODS 5 мкм. Подвижной фазой служила смесь ацетонитрил - 5% КС1 t 0,1% СН3СООН в воде в соотношении 8:92 (по объему), скорость элюирования 1,5 мл/мин. Детектирование проводили с помощью спектрофото- метра Hitachi 100-40 на длине волны 228 чм. Результаты приведены в табл. 5.
П р и м е р 6. Больной П., 32 гоQ да, в 11-е терапевтическое отделение 23 ГКЬ с диагнозом - язвенная оолезнь двенадцатиперстной кишки. Ранисзн (ранитидин фирмы Здравле, Югославия) назначали перораль5 но в дозе 150 мг. Забор крови проводили из локтевой вены через катетер до и через 15, 30, 45 мин, 1, 2, 3, 5, 6, 7ч после приема ранитидина. Кровь центрифугировали при
0 3000 об/мин. Плазму отбирали и хранили при -20 С. К 1 мл плазмы добавляли сухой карбонат натрия до насыщения (150 мг) для создания ,5 и 15 мл хлороформа. После 10-минутного встряхивания водную и органическую фазы разделяли центрифугированием (5 мин при 3000 об/мин), водную фазу удаляли, а органическую упаривали досуха при 4о°С с помощью роторного испарителя Rotavapor R-110 (фирмы Buchi, ФРГ). Сухой остаток растворяли в 0,5 мл подвижной фазы, алик- воту (0,05 мл) наносили на колонку. Определение ранитидина проводили на жидкостном хроматографе Altex 100 А (США) с инжектором на 0,05 мл и колонкой (250x4,6 мм) с неподвижной фазой Spherisorb 5 мкм. Подвижной фазой служила смесь ацетонитрил - 5% КС 4-0,1% СНдСООН в воде в соотношении 8:92 (по объему); скорость элюирования 1,5 мл/мин. Детектирование проводили с помощью спектрофото- метра Hitachi 100-40 на длине волны 225 нм. Результаты приведены в табло 6.
В табл. 7 представлены данные, обосновывающие выбор оптимальной длины волны при определении циметидина и ранитидина.
Предлагаемый способ дает возможность надежно определять концентрации двух основных типов Н гистаминобло- катеров - циметидина или ранитидина, что позволяет контролировать их клиническую эффективность с помощью фар- макокинетических исследований на доступных отечественных реактивах при повышении точности определения: в прототипе коэффициент вариации - более 6%, в предлагаемом способе - не более 3,8% (см. табл. 8),
Формула изобретения Способ определения циметидина или ранитидина в плазме крови путем экстракции образца органическим растворителем, разделения методом высокоэффективной жидкостной хроматографии на колонке, заполненной силикагелем, с обращенной фазой с последующим спектрофотометрическим определением, отличающийся тем, что, с целью повышения точности способа, рН плазмы доводят до 8,2-8,7 сухим карбонатом натрия, экстракцию проводят хлороформом, в качестве подвижной фазы используют смесь ацетонитрила с 5%-ным водным раствором хлорида калия на 0,1%-ной уксусной кислоте в объемном соотношении 8:92, спектрофотометри- ческое определение циметидина проводят при длине волны 218-222 нм, а ранитидина - при длине волны 222- 228 нм.
Таблица 1




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения циметидина в плазме крови | 1985 |
|
SU1296167A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НЕОПТЕРИНА В КРОВИ | 2006 |
|
RU2313092C1 |
| Способ определения эринита, нитросорбида и продуктов их биотрансформации в крови | 1986 |
|
SU1480819A1 |
| Способ определения кофеина в биологическом материале | 2016 |
|
RU2638789C1 |
| Способ количественного определения мебикара в биологических жидкостях | 1980 |
|
SU943571A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ДОПИНГА У ЛОШАДЕЙ | 2011 |
|
RU2489719C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ МИКРОКОЛИЧЕСТВ КЛОЗАНТЕЛА В ПЛАЗМЕ, МОЛОКЕ, ТКАНЯХ | 2007 |
|
RU2366950C2 |
| Способ получения производных гликолипидов,стимулирующих регенерацию клеток и тканей (его варианты) | 1983 |
|
SU1396958A3 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЭНАНТИОМЕРОВ ВЕРАПАМИЛА В СУБСТАНЦИЯХ, ТАБЛЕТКАХ И ОБРАЗЦАХ ПЛАЗМЫ КРОВИ МЕТОДОМ ВЭЖХ | 2008 |
|
RU2395807C1 |
| СПОСОБ ЭКСТРАКЦИИ ПЕНИЦИЛЛИНОВ ИЗ ПЛАЗМЫ КРОВИ | 2008 |
|
RU2374648C2 |
Изобретение относится к медицине, конкретно к хроматографическому анализу экзогенных веществ в биологических жидкостях, и может быть использовано для определения H2-гистаминоблокаторов циметидина или ранитидина в плазме крови. Способ заключается в том, что PH плазмы доводят до 8,2 - 8,7 сухим карбонатом натрия, экстрагируют плазму хлороформом и разделяют методом высокоэффективной жидкостной хроматографии на колонке с силикагелем с обращенной фазой. В качестве подвижной фазы используют смесь ацетонитрила с 5%-ным водным раствором хлорида калия на 0,1%-ной уксусной кислоте в объемном соотношении 8:92. Определение циметидина и ранитидина проводят спектрофотометрически при длинах волн 218 - 222 и 222 - 228 нм соответственно. Способ обеспечивает повышение точности за счет снижения коэффициента вариации почти в 2 раза. 8 табл.
Высота хро- матографичес- кого пика (дел. шкалы)
Концентрация (мкг/мл)
О 256 132 88 77 50 31 17 14 10 О 13,9 7,0 4,6 3,9 2,3 1,3 0,5 0,4 0,2
Высота хрома- тографическо- го пика (дел. шкалы) Концентрация (мкг/мл)
О 244 126 84 О 13,2 6,5 4,1
Таблица 2
74 47 30 16 13 9 3,6 2,2 1,3 0,5 0,4 0,2
Высота хроматографического пика (дел.
шкалы) 0 278 96 8 54 34 18 15 11
Концентрация
(мкг/мл) 0 13,6 6,8 Ц,Ц 3,8 2,3 1,3 0,5 О, 0,2
Высота хрома- тографического пика (дел. шкалы)
Концентрация (нг/мл)
О 7 17 25 38 45 57 21 14 О 55,4 131,2 195,6 300 375,5 378,8 159,8 111
Показатель
О | 15 I 30 45 | 60 120 1 180 300 1 360
06 16 23 35 42 53 19 13
О 56,9 134,5 199,8 305 384,6 388 170,5 113
Показатель
б 1 15 | 30 1 45 1 60 I 120 180 | 300 |ЗбО
Высота хрома то графического пика (дел. шкалы) Концентрация(нг/мл)
О 8 19 26 43 50 6k 23 16.
О 56,3 133,8 197,1 302,7 380 383,7 161,9 112,6
1571503
10 Таблица 3
Таблица 5
Время, мин
Таблица 6
Время, мин
1 2
3 4
5
6 7 8
Среднее Статистическое отклонение
Стётистичес- кая ошибка
9535ПО5811560ПО701007580657050
9534112561125811071 977480667248 9735Ю856IT 6011269 997576656648
94351115711459Ю971 967378696849
9633ПО5611257Ю8701DO7277686850
953611357ИЗ5811070 987176677147 9434109551155810872 957578677049 9435112581135711269 9бч7282666848 9334ПО551125811269 9772 8666847
,8 34,6 110,6 $6,4 113,3 58,3 110,1 70,1 97,673,2 78,366,669,048,4
1,2 0,9 1,6 1,1 1,2 1,1 1,6 1,1 1,8 1,6 2,0 1,3 1,9 1,1 0,4 0,3 0,5 0,4 0,4 0,4 0,5 0,4 0,6 0,5 0,7 0,4 0,6 0,4 Примечание: Ц- циметидин; Р - ранитидин.
Таблица 7
Таблица 8
| Fleittnan J., Torosian G., Perrin J.H | |||
| - J | |||
| Chroroatography, 1982, v | |||
| Приспособление для подачи воды в паровой котел | 1920 |
|
SU229A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
1990-06-15—Публикация
1988-04-06—Подача