Изобретение относится к пищевой промышленности.
Цель изобретения - повышение точ- ности анализа и снижение концентрации реагента.
Способ осуществляют следующим образом.
В анализируемую пробу фруктового ипи овощного сока или виноградного вина добавляют в избытке реагент - водный раствор уротропина с таким реагентом, что после прохождения реакции реагента (В) с суммой органических кислот ( )
пВ
, (1)
концентрация реагента практически не изменялась. Уротропин используют с концентрацией 0,1-0,2 моль/дм в объемном соотношении от 1 : 20 до 1 : 40.
; После перемешивания измеряют рН среды с помощью стеклянного индикаторного электрода и хлорвдсеребряного электрода сравнения. Затем добавляют небольшую, дозу (такую, чтобы можно было пренебречь разбавлением реагента) стандартного 0,4 н. раствора щавелевой кислоты, перемешивают и измеряют рНраствора.Титруемую кислотность- , в пересчете, например, на винную
.кислоту вьП1исляют по формуле
С5
о
ел
ю
16052004
0,99 и по формуле (2) вычисляют
. -1I- J л у ЕЛ. 11W l lVJi l lJfJAti iJ . Tk ..-
ст 2 2.) 2 6 (без пересчета на массовую долю) ---«.--- - ----------- - ттачггпатттлл trtj-n ттптт -л ггПпНр П.. -
пр
(10
ЬрН
О
(2)3
центрацию кислоты в пробе С
0,091 моль/дм. Ошибка определения
9,0 отн.%.
V
ст
- объем стандартного раствора щавелевой кислоты;
С ( Н„ СгО) - концентрация стан10
Пример.2о В потенциометричес- кую ячейку согласно примеру 1 вносят 20 см О,1 М раствора определяемой кислоты с С(1/2 Н2.С204)0,1 моль/дм . Измеряют рНд 6,42. Затем добавляют 0,5 см раствора щавелевой кислоты
с С(1/2 ) моль/дм
в каМ ()
V.p
дартного раствора щавелевой кислоты;
-масса эквивалента винной кислоты;
-объем анализируемой пробы;
ДрН рН , - pHg.
Преимущество уротропина как реагента обусловлено следующими причина- 20 ми,,Он является более сильным основанием bKg 1,4 ), чем ацетат-ион (рК и 5,8 10 ), что с большей на дежностью обеспечивает полноту про- измеряют рН, . Затем добавляют хождения реакции (1) и позволяет причестве стандарта. Измеряют рН - 5 5,90. .Находят ДрН 0,52 и по формуле (2) вычисляют (без пересчета на массовую долю) концентрацию кислоты в пробе Су 0,087 моль/дм. Ошибка определения 13,0 отн„%.
Пример 3. В потенциометричес- кую ячейку вносят 20 см 0,05 М раствора уротропина и 1 см анализируемой пробы раствора определяемой кислоты с С(1/2 ) 0,1 моль/дм
1 см раствора щавелеврй кислоты с С(1/2 H2.C,i.04) 0,4 моль/дм в качестве стандарта. Измеряют рН, 0,92 и по формуле (2) вычисляют (без пер.е- счета на массовую долю) концентра- цию кислоты в пробе Су; 0,055 моль/дм Ошибка определения 45 отн.%.
30
менять водные растворы уротропина с гораздо более низкой концентрацией, чем в случае ацетатной соли при удовлетворительной точности анализа.
Кроме того, ;уротропин как реактив менее гигрсюкопичен и,главное, биологически устойчив, и его раствор может храниться длительное время, что особенно важно для южных районов страны. Указанные факторы способству- 35 ют повьшению точности определения органических кислот. Верхний предел концентрации реагента (0,2 н.) определяется устранением излишнего расхода реагента, нижний предел (0,1 н.) -40 созданием, как минимум, десятикратно- . го избытка реагента при высоких содержаниях кислот (больше 20 г/дм ). .Интервал разбавления .определяется минимальным объемом реагента 20-30 см 45 и минимальным (практически без разбавления реагента) объемом дозы
1 см раствора щавелеврй кислоты с С(1/2 H2.C,i.04) 0,4 моль/дм в качестве стандарта. Измеряют рН, 0,92 и по формуле (2) вычисляют (без пер.е- счета на массовую долю) концентра- цию кислоты в пробе Су; 0,055 моль/дм Ошибка определения 45 отн.%.
Пример4о В потенциометричес- кую. ячейку вносят 20 см 0,2 М раствора уротропина и 1 см анализируемой пробы раствора определяемой кислоты с С(1/2 Н2.С2.) 0,2 моль/дм- (разбавление 20). Измеряют рН 6,44. Затем добавляют 1,0 см- раствора щавелевой кислоты с С(1/2 ) 0,4 моль/дм :в качестве стандарта. Измеряют рН2 5,95. Находят ЬрН 0,50 и по формуле (2) вы- числямт (без пересчета на массовую долю) концентрацию кислоты в пробе С.к 0,185 моль/дм. Ошибка определения 7,5 отн.%.
В потенциометри3
И р и М е р 5
0,5-1 см .. ческую ячейку вносят 20 см 0,2 М
Приме р 1. В потенциометричес- „ раствора уротропина и 2 см анализи- кую ячейку вносят 20 ,2 М раст- руемой пробы раствора определяемой
вора уротропина и 0,5 см анализируемой пробы раствора определяемой кислоты с С(1/2 Н2,) 0,1 моль/дм . Измеряют значения рН л 7,04. Затем добавляют 1,0 см- раствора щавелевой кислоты с С(1/2 .) 0,4 моль/дм в качестве стандарта. Измеряют рН 6,05. Находят йрН
кислоты с С(1/2 H2.)0,2 моль/дм (разбавление 1 : 10). Измеряют рН, 6,15. Затем добавляют 1,0 см раствора щавелевой кислоты с С(1/2 .) 0,4 моль/дм. Измеряют
рН 5,80. Находят йрН 0,35 и по формуле (2) вычисляют (без пересчета н а массову10 долю) концентрацию кислоттачггпатттлл trtj-n ттптт -л ггПпНр П.. -
3
0
центрацию кислоты в пробе С
0,091 моль/дм. Ошибка определения 9,0 отн.%.
Пример.2о В потенциометричес- кую ячейку согласно примеру 1 вносят : 20 см О,1 М раствора определяемой кислоты с С(1/2 Н2.С204)0,1 моль/дм . Измеряют рНд 6,42. Затем добавляют 0,5 см раствора щавелевой кислоты
с С(1/2 ) моль/дм
в ка20
измеряют рН, . Затем добавляют
честве стандарта. Измеряют рН - 5 5,90. .Находят ДрН 0,52 и по формуле (2) вычисляют (без пересчета на массовую долю) концентрацию кислоты в пробе Су 0,087 моль/дм. Ошибка определения 13,0 отн„%.
Пример 3. В потенциометричес- кую ячейку вносят 20 см 0,05 М раствора уротропина и 1 см анализируемой пробы раствора определяемой кислоты с С(1/2 ) 0,1 моль/дм
измеряют рН, . Затем добавляют
0
35 40 45
1 см раствора щавелеврй кислоты с С(1/2 H2.C,i.04) 0,4 моль/дм в качестве стандарта. Измеряют рН, 0,92 и по формуле (2) вычисляют (без пер.е- счета на массовую долю) концентра- цию кислоты в пробе Су; 0,055 моль/дм . Ошибка определения 45 отн.%.
Пример4о В потенциометричес- кую. ячейку вносят 20 см 0,2 М раствора уротропина и 1 см анализируемой пробы раствора определяемой кислоты с С(1/2 Н2.С2.) 0,2 моль/дм- (разбавление 20). Измеряют рН 6,44. Затем добавляют 1,0 см- раствора щавелевой кислоты с С(1/2 ) 0,4 моль/дм :в качестве стандарта. Измеряют рН2 5,95. Находят ЬрН 0,50 и по формуле (2) вы- числямт (без пересчета на массовую долю) концентрацию кислоты в пробе С.к 0,185 моль/дм. Ошибка определения 7,5 отн.%.
В потенциометри3
И р и М е р 5
ческую ячейку вносят 20 см 0,2 М
раствора уротропина и 2 см анализи- руемой пробы раствора определяемой
кислоты с С(1/2 H2.)0,2 моль/дм (разбавление 1 : 10). Измеряют рН, 6,15. Затем добавляют 1,0 см раствора щавелевой кислоты с С(1/2 .) 0,4 моль/дм. Измеряют
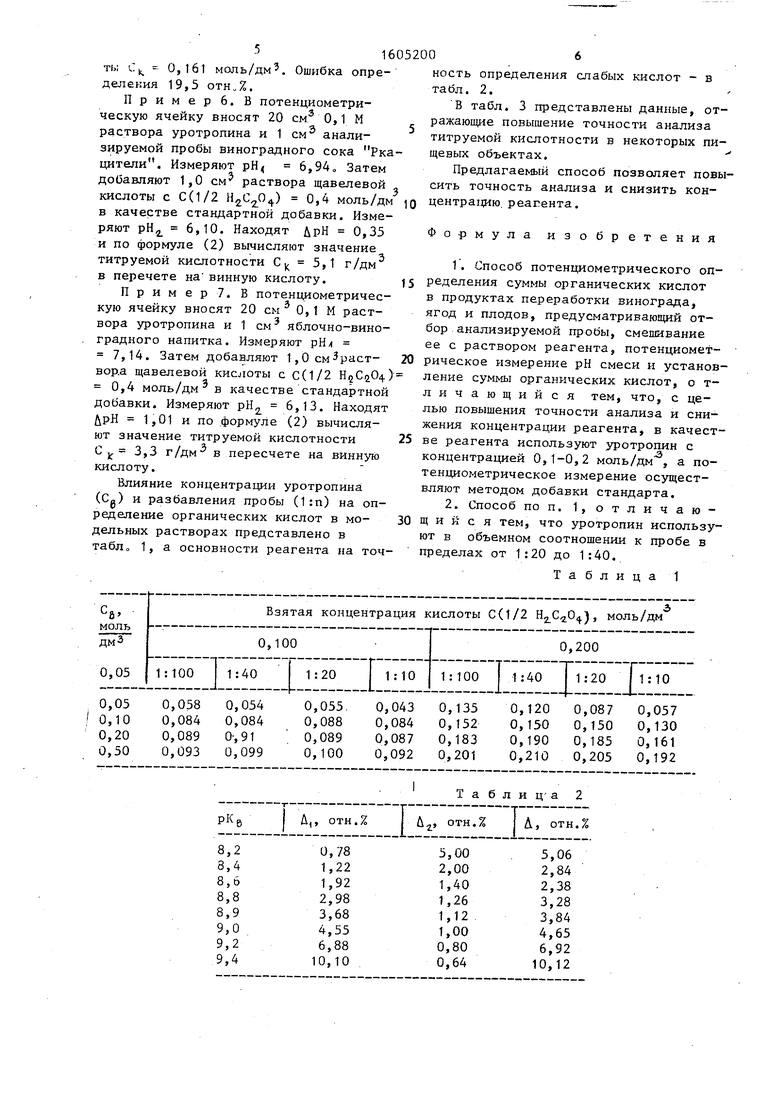
рН 5,80. Находят йрН 0,35 и по формуле (2) вычисляют (без пересчета н а массову10 долю) концентрацию кислоВзятая концентрация кислоты 0(1/2 ), моль/дм
0,100
0,200


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения общей кислотности карамели | 1991 |
|
SU1835510A1 |
| Способ определения кислотного числа масел и жиров | 1991 |
|
SU1825423A3 |
| Способ определения муравьиной щавелевой и фосфорной кислот | 1988 |
|
SU1658088A1 |
| Способ количественного определения натрий-карбоксиметилцеллюлозы | 1987 |
|
SU1503003A1 |
| Способ определения фенола в реакционной массе разложения гидроперекиси изопропилбензола производства фенола и ацетона | 1989 |
|
SU1686348A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КИСЛОТНОГО ЧИСЛА РАСТИТЕЛЬНЫХ МАСЕЛ | 1997 |
|
RU2119162C1 |
| Способ определения железа в адипиновой кислоте | 1990 |
|
SU1779289A3 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПРИМЕСНЫХ КОЛИЧЕСТВ МАЛЕИНОВОЙ, ФУМАРОВОЙ И ЩАВЕЛЕВОЙ КИСЛОТ В КРИСТАЛЛИЧЕСКОЙ ЯНТАРНОЙ КИСЛОТЕ | 1996 |
|
RU2098804C1 |
| Способ измерений массовых концентраций мышьяка, кадмия, свинца, ртути в мясных и мясосодержащих продуктах методом масс-спектрометрии с индуктивно связанной плазмой | 2020 |
|
RU2738166C1 |
| СПОСОБ ЛЮМИНЕСЦЕНТНОГО ОПРЕДЕЛЕНИЯ ТЕРБИЯ В ГОРНЫХ ПОРОДАХ | 1991 |
|
RU2007710C1 |
Изобретение относится к пищевой промышленности. Целью изобретения является повышение точности анализа и снижение концентрации реагента. В потенциометрическую ячейку вводят 1,0 мл анализируемого образца, смешивают его с водным раствором уротропина с концентрацией 01, - 2,0 моль/дм3 в объемном соотношении от 1:20 до 1:40, после перемешивания измеряют PH раствора на стандартном PH-метре со стеклянным индикаторным электродом и хлоросерябряным электродом сравнения. Затем добавляют раствор щавелевой кислоты в качестве стандарта, перемешивают и измеряют PH раствора, находят PH и на расчетной формуле определяют сумму органических кислот. 1 з.п. ф-лы, 3 табл.
°1- 1 °° I ° Г 1:20
0,05 0,10 0,20 0,50
0,058 0,084 0,089 0,093
0,054 0,084 0-,91 0,099
0,055. 0,088 0,089 0,100
0,043 0,084 0,087 0,092
0,135 0,152 0,183 0,201
0,120 0,150 0,190 0,210
0,087 0,150 0,185 0,205
0,057 0,130 0,161 0,192
РК,
(
отн.%
0,135 0,152 0,183 0,201
0,120 0,150 0,190 0,210
0,087 0,150 0,185 0,205
0,057 0,130 0,161 0,192
Таблица 2
I Л, отн.%Д, отн.%
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| М., 1961, с | |||
| Поглотительный сосуд для анализа газов | 1923 |
|
SU814A1 |
| Крешков А.П.Основы аналитической химии | |||
| М., 1965, т | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Катодная трубка Брауна | 1922 |
|
SU330A1 |
| Способ определения суммы органических кислот в продуктах переработки винограда,ягод и плодов | 1980 |
|
SU1097946A1 |
| G | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
1990-11-07—Публикация
1987-09-01—Подача