Изобретение относится к рыбной промышленности и может быть использовано для контроля за содержанием маннита в производственных растворах при его извлечении из морских водорослей.
Целью изобретения является повышение точности.
Для осуществления предлагаемого способа определенный объем производственного раствора маннита вводят в определенный объем заранее приготовленной реакционной смеси, содержащей феррицианид и ферроцианид калия. Смесь выдерживают в течение заданного времени,, регистрируют потенциал
реакционной смеси и затем вводят в нее в качестве катализатора ионы меди, вновь выдерживают заданное время и повторно регистрируют потенциал. По изменению потенциала реакционной смеси рассчитывают содержание маннита в анализируемом растворе.
Для предотвращения влияния примесей, содержащихся в произврдствен- ных растворах, таких как гликоген, крахмал, липиды, белки, нуклеиновые кислоты, альгиновые кислоты, хлорофилл, В-каротин и т.п. на результаты определения отобранную пробу производственного раствора смешивают с реакционной смесью и выдерживают в
течение 3-5 мин. За этот промежуток времени примеси успевают окислиться и не мешают в дальнейшем определению маннита,, При этом соотношение манни- та и Окислителя должно находиться в пределах 1:7 - 1:70 (моль/моль). Реакционная смесь представляет собой смесь феррицианида и ферроцианида ка- лия в соотношении 80:1 - 120:1 (моль/ /моль), растворенную в щелочи кон центрацией от О,1 до 2 М Затем в реакционную смесь в качестве катализатора вводят ионы двухвалентной меди в концентрации -10 моль/л.
Вновь выдерживают раствор при постоян ном перемешивании мин. При этом за счет реакции окисления маннита. изменяется потенциал окислительно-вое - становительной системы Fe3 /Pe2+. По изменению потенциала редокс системы рассчитывают концентрацию маннита в исследуемом растворе
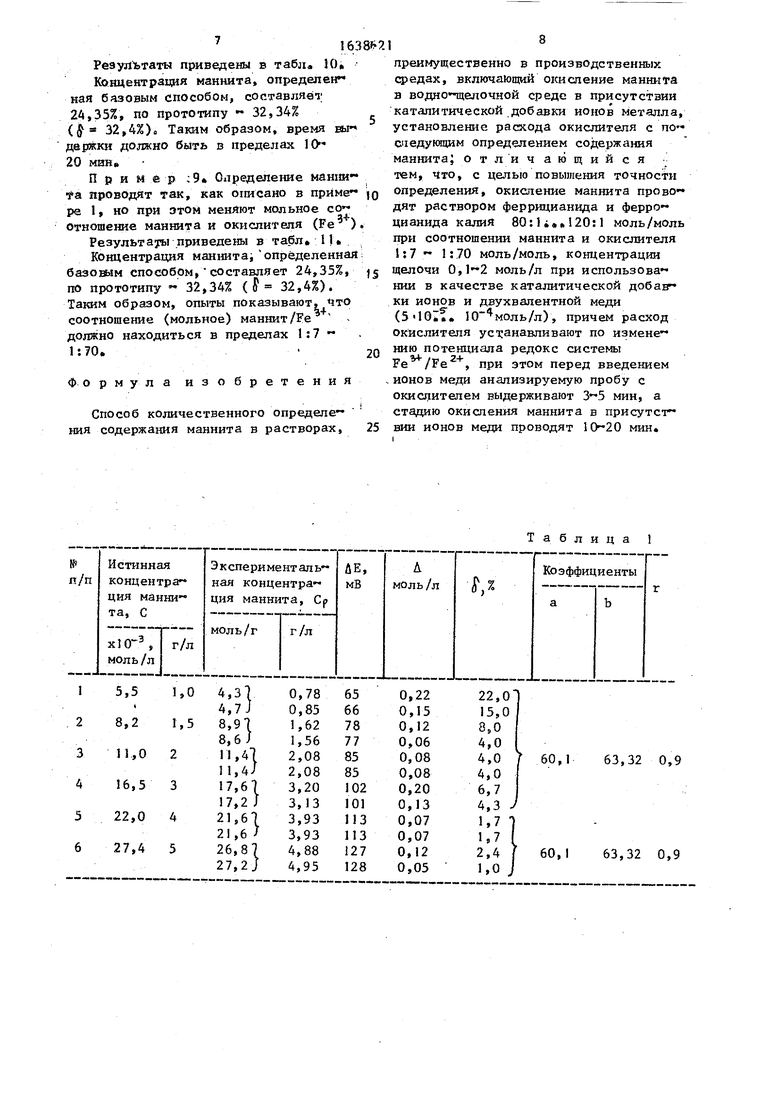
Пример 1. Для определения калибровочной зависимости между изменением показания прибора (ДЕ) (ионо- мера) и логарифмом концентрации ман- нита в растворе (lg С ман) готовят шесть растворов маннита со следукщщ- ми концентрациями: 1 г/л (5,5-10 молъ/ . /л}; 1,5 г/л (8,2 Ч 0 моль/л); 2,0 г (,0-10 3моль/л); 3,0 г/л (16,5 моль/л); 4,0 г/л . (22,0«10 3моль/л); 5,0 г/л (27,4 моль/л)«, Затем готовят ще- лочной раствор солей феррицианида ка- лия (ОХ форма) и ферроцианида калия (red-форма) с соотношением Сох:Среа 100:1 (в качестве растворителя используют NaOH концентрацией 1 моль/л) 40 мл приготовленного таким образом раствора помещают в стеклянный ста- канчик и погружают в раствор платиновый и хлорсеребряный электроды, подключенные к иономеру. Затем отби- рают 1 мл приготовленного раствора маннита концентрацией I г/л и вводят его в реакционную смесь Выдерживают раствор при постоянном перемешивании в течение 5 мин и фиксируют потен- циал смеси, равный 379±1 мВ (Е). После этого вводят в реакционный стаканчик 1 мл заранее приготовленного раствора нитрата меди с концентрацией 42 10 моль/л, снова выдержи- вают смесь в течение 10 мин, после чего фиксируют потенциал раствора, Е Ј 314±1 мВв Затем освобождают t реакционный стаканчик от прореагировавшей смеси и промывают его дистиллированной водой Повторяют эксперимент, при этом получают Е4 379±1 мВ и Ег 313+1 мВ. Рассчитывают величину Д.Е Е4-Е2 для двух параллельных измерений, которые равны соответственно 65.+1 мВ и. 66+1 мВ.
Аналогичные опыты проводят с растворами маннита других приготовленных концентраций., Полученные результаты представлены в табл 1
Методом наименьших квадратов рассчитывают коэффициенты уравнения Су|Да„ a.exp AE +Ь, величина коэффициентов а и b приведена в табя.1; кроме того, в-табл 1 приведены следующие параметры: Д, () - абсолютная ошибка определения, равная разности концентрации маннита, определенной по предлагаемому спо- собу (С), и истинней, приготовленной из навески (С); о - относитель-
ЛГ4 п - f
ная ошибка, о --- 100%; г
коэффициент кореляции
Таким образом, концентрацию маннита по предлагаемому способу можно рассчитать по уравнению
ЛАЯН
60,1-ехрйЕ + 63,32.
| Используя полученную калибровоч- ,ную зависимость, определяют содержание маннита в образцах производственных растворов, отобранных на различных стадиях процесса производства товарного маннита на Архангельском водорослевом комбинате.
Для определения содержания манни- та в водорослях (исходном сырье) отбирают навеску анализируемой пробы (56,1611 г) и проводят экстракцию дистиллированной водой (V 20 мл). Разбавляют полученный экстракт дистиллированной водой в 125 раз. 1 мл разбавленного экстракта вводят в 40 мл реакционной смеси, приготовленной как описано выше. Выдерживают раствор в течение 5 мин и фиксируют значение Е 379 тВ. Добавляют 1 мл раствора нитрата меди, выдерживают смесь 10 мин и фиксируют величину Е2 292 tnB. Изменение потенциала 4Е составляет:
АЕ Е , - Е,
87 тВ.
5
По установленнон зависимости С.ц f (ДЕ) рассчитывают с учетом предварительного разведения концент- рацию маннита в экстракте:
сман г/л а содержание маннита в образце со ставляет:
с««и-М:1-бТ Го- 100 25 50%
Ь
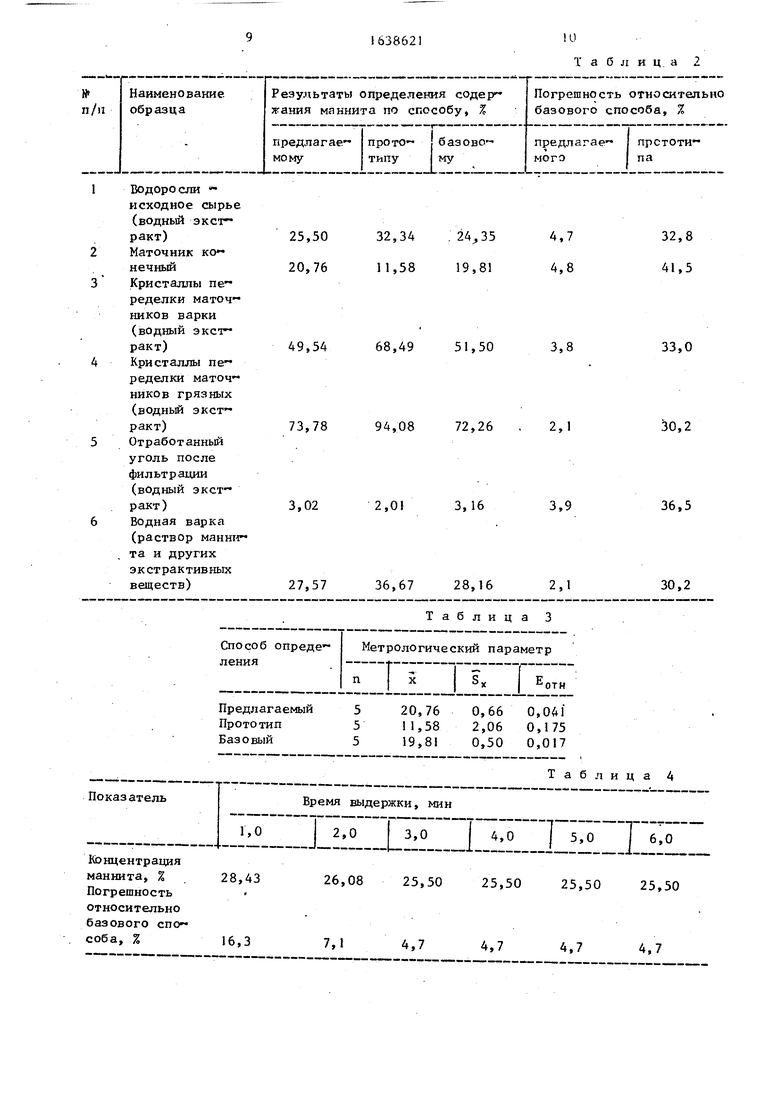
Аналогично определяют содержание маннита в других образцах Также в этих же образцах определяют содержа - ние маннита по прототипу, и по способу, принятому за базовый.
Полученные результаты сведены в табл,:2.
Из следует, что погреиг- ность определения предлагаемого способа меньше погрешности прототипа в 8-10 раз.
Для образца № 2 проведена метроло- гическая оценка всех трех способов, полученные результаты представлены в табл. 3.
Пример 2. Определение содер- жания маннита проводят так, как описано в примере 1, но при этом варьируют время выдержки раствора до введения в реакционную смесь нитрата меди.
Полученные результаты представле- ны в табл. 4.
Концентрация маннита, определенная базовым способом, составляет 24,35%, по прототипу - 32,34% (5 32,4%). Из сравнения полученных результатов видно, что оптимальное время выдержки реакционной смеси должно быть не менее 3 мин.
Пример 3. Определение манни- та проводят так, как описано в примере 1, но при этом варьируют добавку Сиг+.
Полученные результаты предстаапе- ны в табл.:5.
Концентрация маннита, определенная базовым способом, составляет 24,35%, по прототипу - 32,34% ($ 32,4%). Из сравнения полученных результатов видно, что допустимые пределы концентрации ионов Си21 в растворе 5 , наиболее предпочтительна концентрация 10 М.
-
Ь386/Iл
Пример 4. Определение манни- та проводят так, как описано в приме- ре 1 , но при -этом варьируют концент- рацию щелочи,,
Полученные результаты, представ лены в табл. 6
0
$
0
5
0
r
о
0
5
Концентрация маннита, определенная базовым способом, составляет 24,35%, по прототипу - 32,34% (о 32,4%). Таким образом, концентрация щелочи должна находиться в пределах 0,1-2 М.
Пример 5л Определение ман- нита проводят так, как описано в примере 1, но при этом используют гидроксиды различных металлов одинаковой концентрации
Полученные результаты представлены в табл. 7
По полученным результатам можно сделать вывод, что вид щелочи не оказывает на определение маннита никакого влияния.
Пример 6. Определение манни- та проводят так, как описано в примере 1, но при этом меняют концентрацию окислителя при постоянном соотношении С ох : С recj 100:1.
Полученные результаты приведены в табл. 8.
Концентрация маннита, определенная базовым способом, составляет 24,35%, по прототипу - 32,34% (Ј 32,4%). Таким образом, проведенный эксперимент показывает, что в пределах концентраций окислителя 0,01-0,1 моль/л концентрация маннита практически не меняется.
Пример 7. Определение маннита проводят так, как описано в примере 1 , но при меняют соотношение Coy/Crej при постоянной концентрации окислителя С 0)с 0,01 моль/ /л.
Полученные результаты приведены в табл. 9.
Концентрация маннита, определенная базовым способом, составляет 24,35%, по прототипу - 32,34% (Ј 32,4%). Таким образом, соотношение С ох - CPe(j должно находиться в пределах 80:1 - 120:1
Пример 8. Определение ман- нита проводят так, как описано в примере 1, но при этом меняют время выдержки раствора после введения каталитической добавки.
7163
Результаты приведены в табл« 10 Концентрация маннита, определен кая базовым способом, составляет 24,35%, по прототипу 32,34%
( 32,4%). Таким образом, время вы« держки должно быть в пределах 10 20 мин
Пример ;9 Олределение манни та проводят так, как описано в приме ре 1 но при этом меняют мольное со« отношение маннита и окислителя (Fe3 ) Результаты приведены в табл 11 Концентрация маннита, определенная базовым способом, составляет 24,35%, по прототипу 32,34% ( о 32,4%). Таким образом, опыты показывают, что соотношение (мольное) маннит/Fe должно находиться в пределах 1:7 1:70.
Формула изобретения
Способ количественного определения содержания маннита в растворах, 25
5
Q
5
0
5
I8
преимущественно в производственных средах, включающий окисление маннита в воднотцелочной среде в присутствии каталитической добавки ионов металла, установление расхода окислителя с по-« следующим определением содержания маннита; отлич ающийся тем, что, с целью повышения точности определения, окисление маннита прово дят раствором феррицианида и ферро цианида калия 80:1 120:1 моль/моль при соотношении маннита и окислителя 1:7 - 1:70 моль/моль, концентрации щелочи 0, моль/л при использова нии в качестве каталитической добавг ки ионов и двухвалентной меди (5-lOlt Ю моль/л), причем расход окислителя устанавливают по измене даю потенциала редокс системы Fe /Fez+, при этом перед введением ионов меди анализируемую пробу с окислителем выдерживают 3-5 мин, а стадию окисления маннита в присутст вии ионов меди проводят мин




Изобретение относится к рыбной промышленности и может быть использовано для контроля за содержанием маннита в производственных растворах при его извлечении из морских водорослей. Целью изобретения является повышение точности. Образец производственного раствора маннита вводят в определенный объем реакционной смеси, содержащей феррицианид и фер- роцианид калия в растворе щелочи Смесь выдерживают в течение 3-5 мин, регистрируют потенциал реакционной смеси. Затем вводят в реакционную смесь в качестве катализатора ионы меди, вновь выдерживают при постоянном перемешивании в течение 1О- 20 мин. При этом за счет реакции окис ления маннита изменяется потенциал окислительно-восстановительной системы Fe34 /Fez+. По изменению потенциала реакционной смеси рассчитывают концентрацию маннита в исследуемом растворе 11 табл. /
Таблица 1
1Водоросли - исходное сырье (водный экстракт)25,5032,3424,354,7
2Маточник конечный20,7611,5819,814,8
3Кристаллы пе- ределки маточников варки (водный экстракт)49,5468,4951,503,8
4Кристаллы переделки маточников грязных (водный экстракт)73,7894,0872,26 . 2,1
5Отработанный уголь после фильтрации (водный экстракт)3,022,013,163,9
6Водная варка (раствор маннн- та и других экстрактивных
веществ)27,5736,6728,162,1
Показатель
Концентрация маннита, % Погрешность относительно базового способа, %
Время выдержки, мин ,0 3,0| 4,0 5,0 6,0
28,4326,0825,5025,5025,5025,50
16,3
7,1
4,7
4,7
4,7
4,7
Таблица 2
32,8 41,5
33,0
30,2
36,5
30,2
Таблица 3
Таблица 4
4,7
4,7
4,7
4,7
i Показатель
2f
Концентрация ионов Си в ячейке, моль/л
10
-5
Смай 20,1
Погрешность от носительно баз о вого способа, %17,4
Показатель
Концентрация NaOH, м
МД
г/л
0,05 | 0,1 J 1J 1,5 1 2 Ј 3| 5
21,1 г 21,825,525,529,9 30,032,5
Погрешность от носительно базового способа, %13,310,54,7
4,76,423,233,5
Показатель
ьмаи Погрешность
относительно базового спо соба, %4,7
LiOH i NaOH | КОН 25,525,5 25,5
4,74,7
Показатель
ман
Концентрация рх, моль/л
0,0050 I 0,0075 I 0,010,015 | 0,02 0,1 I 0,15
27,026,225,225,525,7
Погрешность от но си тел ьно базового спо соба, %10,9
7,6
4,74,75,5
25,9 26,2
6,4 7,6
UAWH
Погрешность относительно базового спо соба, %
2f
Г |
.
26,4
28,1
8,415,4
Таблица 6
4,7
4,76,423,233,5
Таблица 7 Щелочь
4,74,7
Таблица 8
25,9 26,2
4,74,75,5
6,4 7,6
25,7
25,5
25,5
27,1
5,5
4,7
4,7
11,3
13
21,925,525,4
10,14,74,3
1638621
14
Таблица 10
25,625,526,1 28,5
5,14,77,2 17,0
| Choyksey S.P., Verraa R.Mo J | |||
| Indian Chem | |||
| Soc., 1980, v | |||
| Способ получения на волокне оливково-зеленой окраски путем образования никелевого лака азокрасителя | 1920 |
|
SU57A1 |
| МУЗЫКАЛЬНЫЙ ПРИБОР С КАТОДНЫМИ ЛАМПАМИ | 1921 |
|
SU890A1 |
Авторы
Даты
1991-03-30—Публикация
1989-01-25—Подача