1
(21)4612582/13 (22)05.12.88 (46)30.04.91. Бюл. № 16
(71)Институт питания АМН СССР
(72)Д.Б.Меламед, Б.Г.Ляпков и Т.В.Киселева
(53)543.544:637.07 (088.8)
(56)Меламед Д.Б. и др. Анализ пищевых добавок. Консерванты (обзор). Мед. реф. Ж., 1987, разд. VII, N° 8, с. 28-34.
J.Yosseleetc. Thin Layer chromatcgraphy separation of preservatives. J. Chromatogr. 1966, v. 23, N 2, p. 305-308.
(54)СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БЕНЗОЙНОЙ И-СОРБИНОВОЙ КИСЛОТ В ПИЩЕВЫХ ПРОДУКТАХ И НАПИТКАХ
(57)Изобретение относится к пищевой промышленности и может быть использовано для определения бензойной (БК) и сорбино- вой (СК) кислот в пищевых продуктах и напитках. -Цель изобретения - повышение достоверности результатов и упрощение процесса за счет обеспечения лучшего разделения пятен БК и СК. Из пробы пищевого продукта или напитка выделяют образец, содержащий БК и СК, и наносят на хрома- тографическую пластинку силуфол УФ254 точки полученного образца и стандартных растворов, содержащих смесь БК и СК. Затем одну точку образца и одну точку стандартного раствора обрабатывают
окислительной смесью (ОС), содержащей муравьиную кислоту и пероксид водорода в соотношении 1:1. Пластинку подсушивают, нагревают при 80-100°С в течение 15-20 мин, дают остыть, и проводят ТСХ в системе растворителей петролейный эфир - хлороформ - муравьиная кислота -диэтило- вый эфир 10:4:1:(0,8-1.6). Идентификацию пятен БК и СК на пластинке проводят в УФ- свете с А 254 нм, БК при обработке окислительной смесью (ОС) превращается а n-оксибензойную кислоту, Rf которой примерно второе меньше Rf БК. СК при обработке ОС образует малоновый альдегид, не поглощающий УФ-свет с А 254 нм. Его идентифицируют, опрыскивая пластинку раствором 2-тиобарбитуровой кислоты, в результате чего образуется розовое пятно. Необработанные точки дают в УФ-свете темные пятна с соответствующими Rf. На вторую пластинку наносят точки образца, стандартных растворов и холостой пробы (этилацетата). Далее точки на пластинке обрабатывают, как описано выше, и проводят ТСХ, идентифицируют пятна БК и СК, отмечают их, вырезают и элюируют этилацета- том. Измеряют оптическую плотность элюатов на спектрофотометре при А 272 и 254 нм для БК и СК соответственно и рассчитывают количество БК и СК в образце. 1 ил., 2 табл.
(Л
С
о
00 00
о




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения патулина в пищевых продуктах | 1982 |
|
SU1103146A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ N-(БЕНЗИМИДАЗОЛИЛ-2)-О-МЕТИЛКАРБАМАТА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2005 |
|
RU2300765C1 |
| Способ хроматографического определения летучих аминов и нитрозаминов | 1985 |
|
SU1259187A1 |
| Способ определения наличия афлотоксинов в и G в продуктах растительного сырья | 1980 |
|
SU928226A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ БЕНЗОКСАЗОЛОНА-2 И 6-ХЛОРБЕНЗОКСАЗОЛОНА-2 В ПРОИЗВОДСТВЕ ПЕСТИЦИДОВ, ОТНОСЯЩИХСЯ К ПРОИЗВОДНЫМ БЕНЗОКСАЗОЛОНА-2, ТОНКОСЛОЙНОЙ ХРОМАТОГРАФИЕЙ | 1991 |
|
RU2018825C1 |
| Способ определения производных бензимидазола в биологических объектах | 1983 |
|
SU1165984A1 |
| СПОСОБ ИДЕНТИФИКАЦИИ РЕЗВЕРАТРОЛА | 2008 |
|
RU2385457C1 |
| СПОСОБ ПОЛУЧЕНИЯ РОЗМАРИНОВОЙ КИСЛОТЫ | 2009 |
|
RU2402525C1 |
| Способ количественного определения дезоксиниваленола в злаках и продуктах их переработки | 1986 |
|
SU1364979A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ОСТАТОЧНЫХ КОЛИЧЕСТВ ПЕСТИЦИДА В МОЛОКЕ И МЯСЕ | 1991 |
|
RU2034295C1 |

Изобретение относится к пищевой промышленности и может быть использовано для определения бензойной и сорбиновой кислот в пищевых продуктах и напитках.
Цель изобретения - повышение достоверности результатов и упрощение процесса путем обеспечения лучшего разделения пятен бензойной и сорбиновой кислот.
Способ количественного определения бензойной (БК) и сорбиновой (СК) кислот в пищевых продуктах и напитках заключается в следующем.
Из пробы пищевого продукта или напитка выделяют образец, содержащий БК и СК, одним из известных способов, например гомогенизируют с сульфатом натрия и серной кислотой и отгоняют БК и СК с водяным паром в приемник, содержащий щелочь. Дистиллят подкисляют до рН 2-3, насыщают сульфатом натрия и экстрагируют органическим растворителем (диэтило- вый эфир, этилацетат). Экстракт сушат прокаленным сульфатом натрия. Аликвоту экстракта концентрируют и наносят несколько точек на пластинку силуфол УФ254. Рядом наносят точки разных объемов стандартного раствора, содержащего смеси БК и СК. По одному из пятен образца и стандартов обрабатывают смесью муравьиной кислоты и пероксида водорода в соотношении 1:1, подсушивают и помещают пластинку в сушильный шкаф, нагретый до 80-90°С, на 15-20 мин. Затем дают остыть и погружают в камеру тонкослойной хроматографии (ТСХ), содержащую систему растворителей петролейный эфир-хлороформ-муравьиная кислота-диэтиловый эфир 10:4:1:(0,8-1,6). Для идентификации хроматограмму рассматривают в УФ-свете с А 254 нм. Наличие темного пятна на .хроматограмме необработанной точки образца, Rr которого соответствует пятну СК, и отсутствие такого пятна на хроматограмме обработанной точки образца свидетельствует о наличии в пробе СК. Наличие темного пятна на хроматограмме необработанной точки образца, Rf которого соответствует пятну БК, исчезновение его на хроматограмме обработанной точки образца и появление на этой хроматограмме пятна с Rf, примерно втрое меньшим, чем Rf БК, доказывает наличие в пробе БК. На основании полученной хроматограм- мы оценивают примерное содержание БК и СК в пробе, сравнивая интенсивность поглощения УФ-света в образце и стандартах. На новую пластинку силуфол УФ254 наносят аликвоту концентрированного экстракта и раствора стандартов так. чтобы количества стандартов БК и СК были близки к оцененному содержанию их в экстракте. Рядом наносят холостую пробу в объеме, равном аликвоте экстракта. Холостую пробу готовят, упвривая этилацетат аналогично экстракту пробы, Чтобы не перегружать тонкий слой сорбента экстракт, раствор стандартов и холостую пробу наносят в несколько рядом стоящих точек. Пластинку хроматог- рафируют в тех же условиях, что и предыдущую, подсушивают и рассматривают в УФ-свете с Я 254 нм. Отмечают темные пятна БК и СК на хроматограмме экстракта
и стандартов, а также соответствующие по Rf хроматографические зоны холостой пробы, вырезают их и элюируют этилацетатом. На спектрофотометре измеряют оптическую плотность элюатов БК и СК хроматог- раммы экстракта относительно элюатов соответствующих хроматографических зон холостой пробы, а элюаты стандартов - относительно этилацетата, при соответствующих длинах волн (272 и 250 нм). Если концентрация БК и/или СК в пробе слишком велика, элюаты перед измерением оптической плотности следует разбавить этилзце- татом.
Содержание БК и СК в продукте или
напитке рассчитывают по формуле
К FН0 Y m
((мг/кгили мг/л).
Нет -v-t-ivr
где К- коэффициент, учитывающий полноту 0 извлечения, равный для бензойной кислоты 1,2, для сорбционной кислоты 1,25;
F - коэффициент разведения элюата перед измерением оптической плотности;
HQ- оптическая плотность опытной про- 5 бы относительно холостой, усл. ед..
Нет - оптическая платность стандарта относительно этилацетата, усл.ед.,
Y - объем экстракта, мл;
V - объем экстракта, нанесенного на 0 пластинку, мкл;
t - коэффициент концентрирования экстракта (равен 10 при упаривании части экстракта в 10 раз);
М - масса продукта, взятого на ана- 5 лиз, г;
m - количество стандарта, нанесенного на пластинку, мкг.
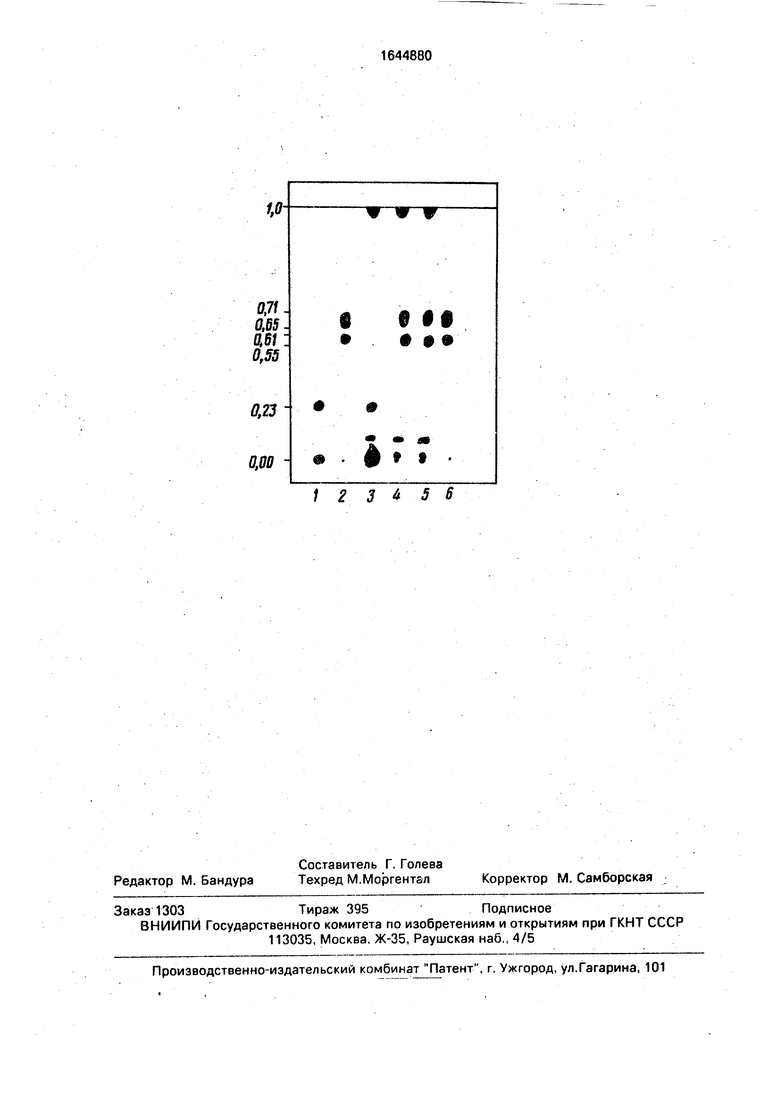
На чертеже представлена хроматограм- ма образца (точки 3, 4, 5) и стандарта без 0 (точки 2 и 6) и после (точки 1) обработки муравьиной кислотой с пероксидом водорода.
В табл. 1 приведены результаты разделения БК и СК при 22°С в испытанных системах 5 растворителей, полученных введением различных объемов диэтилового эфира в систему растворителей петролейный эфир - хлороформ- муравьиная кислота 10:4:1.
Как видно из табл. 1. введение в исход- 0 ную систему растворителей 0,8-1,6, преиму- щественно 1,0-1,2 объемных частей диэтилового эфира, позволяет четко отделить пятна БК и СК, при этом наилучшая разница между нижней границей пятна БК 5 и верхней СК (графа ARr 100 в табл. 1) наблюдается в системах с содержанием 1 и 1,2 об.ч. диэтилового эфира. При количествах эфира, больших 1,6 и меньших 0,8 об.ч., пятна в смеси практически не делятся.
При действии на пятно БК смеси муравьиной кислоты с пероксидом водорода образуется n-оксибензойная кислота, Rf которой примерно втрое меньше Rf БК.
При действии указанной смеси на пятно СК образуется малоновый альдегид, не поглощающий УФ-свет с А 254 нм.
В табл. 2 показано влияние температуры и продолжительности нагревания отработанной указанной смесью пластинки на реакцию БК и СК со смесью муравьиной кислоты с пероксидом водорода.
Пример Определение БК и СК в яблочном мармеладе.
Отвешивают 10,5 г мармелада, гомогенизируют его в ступке с 40 г N32S04 и 40 мл 1 М H2S04 и перегоняют с паром, собирая около 120 мл дистиллята а приемник, содержащий 10 мл 1 М NaOH. Половину дистиллята ПОДКИСЛЯЮТ 1 М H2S04 ДО рН 2-3,
насыщают 30 г NaaSO/i и экстрагируют 3 раза по 10 мл этилацетатз. Объединенный экстракт сушат 2 г Na2S04. 15 мг экстракта упаривают до 1,5 мл.
Раствор стандартов готовят следующим образом: 100 мг бензойной кислоты и 10 мг сорбиновой кислоты переносят в мерную колбу на 50 мл и доводят до метки этилаце- татом; концентрация бензойной кислоты в полученном растворе 2,0 мг/мл, сорбиновой кислоты 0,2 мг/мл.
На пластинку силуфол УФ254 15 х 15 см наносят (см. хроматограмму) в точки 1,2 и 6 по 1,1 и 4 мкл раствора стандартов, при этом количество БК в пятнах составляет 2,2 и 8 мкг, СК - 0,2,0,2 и 0,8 мкг соответственно. В точки 3, 4 и 5 вносят по 3,3 и 10 мкл экстракта. Точки 1 и 3 обрабатывают 4 мкл свежеприготовленной смеси равных объемов муравьиной кислоты и пероксида водорода, подсушивают теплым воздухом и помещают в сушильный шкаф, нагретый до 80°С, на 20 мин, дают остыть и погружают в камеру для ТСХ, содержащую систему растворителей: петролейный эфпр-хлоро- форм-муравьиная кислота-диэтиловый эфир 10:4:1:1,2. Пластинку рассматривают в УФ-свете с А 254 нм. На хроматограммах, полученных из точек 4 и 5, отчетливо видны пятна, по значению Rf соответствующие БК и СК. Пятна из точки 5 примерно втрое интенсивнее, чем из точки 4. При этом на хроматограммах, полученных из точек 1 и 3, пятна с Rf БК и СК отсутствуют, но появилось пятно с Rf, примерно втрое меньшим, чем Rf БК. Это свидетельствует о наличии в пробе БК и СК, Пятна БК и СК на хроматограммах хорошо отделяются от примесей и разделены, Сравнивают интенсивность поглощения УФ-света пятен стандартов и образца и ориентировочно оценивают содержание БК и СК в пятнах образца. Исходя из этой оценки, на пластинку силуфол УФ254
15 х 15 см наносят 60 мкл образца. 30 мкл раствора стандартов и 60 мкл холостой пробы (15 мл этилацетата, упаренного до 1,5 мл), Пластинку помещают в такую же систему растворителей, хроматографируют, подсушивают, вырезают зоны, соответствующие БК и СК в опытной, холостой пробах и стандартах, помещают их в пробирки, заливают 3 мл этилацетата, закрывают крышками, трясут 1-2 мин и измеряют
оптическую плотность элюантов опытной пробы относительно холостой, а стандартов - относительно этилацетата на спектрофотометре в кюветах с I 10 мм при А 272 и 250 нм для БК и СК соответственно. При
измерении оптической плотности элюата СК из опытной пробы и стандарта интенсивность поглощения очень велика (зашкаливание прибора), поэтому его разбавляют этилацетатом в 10 раз (так же разводят и
соответствующую холостую пробу).
Расчет, проведенный по формуле:
СБК 2000 К F , ,Н° . u. «mM° 2000 -1,2 х
х 1
Нет -v-t-M
0,170 -15-60
0,185 60 10 10,5
315мг/кг;
35
ССк 2000 1,25 10 х
0,105 -15-6
242 мг/кг;
0,155/ 60 10 -.10,5 показал, что в исследуемом яблочном мармеладе 315 мг/кг бензойной и 242 мг/кг
сорбиновой кислот.
П р и м е р 2. Определение бензойной и сорбиновой кислот в маргарине Особый. Отвешивают 9,8 г маргарина, интенсивно перемешивают его с 40 г N32504 и 40 мл
1 М Й2504 и перегоняют с паром, собирая 120 мл дистиллята в приемник, содержащий 10 мл 1 М NaOH. Половину дистиллята подкисляют 1 М H2S04 до рН 2-3, насыщают 30 г N32S04 и экстрагируют 3 раза по 10 мл
® этилацетата. Объединенный экстракт сушат 2 г Na2S04.10мл экстракта упаривают до 2 мл. Готовят растворы стандартов так же, как в примере 1. На пластинку силуфол УФ254 15 х 15 см наносят (см. хроматограмму) в
5 точки 1, 2 и 6 по 1,1 и 4 мкл раствора стандартов, при этом количество БК в пятнах составляет 2,2 и 8 мкг, СК 0,2, 0,2 и 0,8 мкг соответственно. В точки 3, 4 и 5 вносят по 3,3 и 10 мкл экстракта. Точки 1 и 3 обрабатевают 3 мкл смеси муравьиной кислоты и пероксида водорода, подсушивают теплым воздухом и помещают пластинку в сушильный шкаф, нагретый до 90°С, на 15 мин, охлаждают и погружают в камеру с системой растворителей: петролейный эфир-хлороформ-муравьиная кислота-диэтиловый эфир 10:4:1:0,8. Пластинку рассматривают в УФ-свете с А 254 нм. На хроматограммах, полученных из точек 4 и 5, отчетлизо видны пятна, по значению Rf соответствующие БК и СК, при этом на хроматограммах 1 и 3 пятна с Rf БК и С К отсутствуют, но появилось пятно с Rf, примерно втрое меньшим, чем Rf БК. Это свидетельствует о наличии а пробе БК и СК. Пятна БК и СК хорошо отделяются от примесей и разделены, Сравнивают ин- .тенсивность поглощения УФ-света пятен стандартов и образца. Исходя из этой оценки, на пластинку смлуфол УФ254 15 х 15 см наносят 20 мкл образца, 10 мкл раствора стандартов и 20 мкл холостой пробы (10 w, этилацетата, упаренного до 2 мл). Пластинку помещают в такую же систему растворителей, хроматографируют, подсушивают, рассматривают з УФ-свете с Я 254 нм, вырезают зоны, соответствующие БК и СК в опытной, холостой пробах и стандартах, по- мещают их в пробирки, заливают по 3 мл зтилацотата, закрывают пробкам, трясут 1-2 мин и измеряют оптическую плотность элюатов опытной пробы относительно холостой, а стандартов - относительно этилацетата на спектрофотометре в кюветах с I 10 мм при Я 272 нм и 250 нм для БК и СК соответственно.
Расчет, проведенный по указанной формуле, показал, что в исследуемом образце маргарина содержится 100С мг/кг бензойной и 13 мг/кг сорбиновей кислоты.
П р и м е р 3. Определение бензойной и сорбиновой кислот s яблочном соке.
Яблочный сок тщательно перемешивают и отмеряют 10 мл. Добавляют 5 мл 1 М НгЗСч и 40 г безводного NaaSCk. Интенсивно перемешивают и экстрагируют 3 раза по 5 мл этилацетата. Объединенный экстракт сушат 1 г безводного NaaSO/j.
На пластинку силуфол УФ254 15 х 15 см наносят (см, хроматограмму) в точки 1, 2 и б по 1,1 и 4 мкл раствора стандартов (приготовление раствора стандартов см. в примере 1), при этом количество БК в пятнах составляет 2, 2 и 8 мкг, а СК - 0,2, 0,2 и 0,8 мкг соответственно. В точки 3, 4 и 5 вносят по 6, б и 20 мкл экстракта. Точки 1 и 3 обрабатывают 5 мкл смеси муравьиной кислоты и пероксида водорода, подсушивают теплым воздухом и помещают в сушильный
шкаф, нагретый до 85°С, на 20 мин, дают остыть к погружают в камеру для ТСХ, содержащую систему растворителей: петролейный эфир-хлороформ-муравьиная
кислота-диэтиловый эфир 10:4:1:1,6. После хроматографирования пластинку рассматривают в УФ-свете с Я 254 нм, На хроматограммах, полученных из точек 4 и 5, отчетливо видны пятна, по значению соответствующиеБКиСК, При этом на хроматограммах, полученных из точек 1 и 3, пятна с Rf БК и СК отсутствуют, но появилось пятно с Rf, примерно втрое меньшим, чем Rf БК. Это свидетельствует о наличии в пробе БК и
СК. Пятна БК и СК на хроматограммах 4 и 5 разделены и хорошо отделены от примесей. Сравнивают интенсивность поглощения УФ-света пятен стандартов и образца и ори- ентирозочно оценивают содержание в них
БК и СК, С учетом результатов этой оценки на пластиьку силуфол УФ254 15 х 15 см наносят 100 мкл образца, 50 мкл раствора стандартов и 100 мкл холостой пробы (зти- лацетат). Чтобы не перегружать тонкий слой
сорбента, экстракт, раствор стандартов и холостую пробу наносят в несколько рядом стоящих точек. Пластинку помещают в такую же систему растворителей, хроматографируют, подсушивают, рассматривают в
УФ-свете с Я 254 нм, вырезают зоны, соответствующие БК и СК в опытной, холостой пробах л стандартах, помещают их в пробирки, заливают по 3 мл этилацетата. закрывают пробками, трясут 1-2 мин и измеряют
оптическую плотность элюатов опытной пробы относительно холостой, а стандартов - относительной этипацетата на спектрофотометра в кюветах с I 10 мм при Я 272 нм и 250 нм для БК и СК соответственно.
Расчет, проведенный по указанной формуле, показал, что в исследуемом образце яблочного сока содержится 132 мг/кг бензойной и 877 мг/кг сорбиновой кислоты. Надежная идентификация и определение БК достигается при ее содержании 2 мкг, а СК - 50 нг в пятне. Это находится на уровне современных методов анализа и сравнимо с чувствительностью газовых и жидкостных хроматографов.
Способ проверен на различных видах пищевых продуктов и напитков (колбаса сер- вилат, яблочный мармелад, маргарин Особый, томатный и яблочный соки и др.). Формула изобретения
Способ количественного определения бензойной и сорбиновой кислот в пищевых продуктах и напитках, включающий выделение из пробы пищевого продукта или напитка образца, содержащего бензойную и
сорбиновую кислоты, нанесение на хрома- тографическую пластинку силуфол УФ254 точек образца и стандартных растворов, разделение бензойной и сорбиновой кислот методом тонкослойной хроматографии в системе растворителей, содержащей петро- лейный эфир, хлороформ, муравьиную кислоту в соотношении 10:4:1, идентификацию пятен в УФ-свете, подтверждение наличия бензойной и сорбиновой кислот в образце, элюирование пятен указанных кислот и спектрофотометрический анализ элюатов при А 272 и 254 нм соответственно, отличающийся тем, что. с целью
повышения достоверности результатов и упрощения процесса путем обеспечения лучшего разделения пятен бензойной и сорбиновой кислот, тонкослойную хроматографию проводят в системе растворителей, содержащей дополнительно диэтиловый эфир в количестве 0,8-1.6 об.ч., а подтверждение наличия бензойной и сорбиновой кислот осуществляют путем обработки точек на
старте хроматографической пластинки смесью муравьиной кислоты с пероксидом водорода в соотношении 1:1 с последующим высушиванием и нагреванием пластинки при 80-100°С в течение 15-20 мин.
Таблица 1
Таблица 2
0,71. 0,65т:
0,55
0,00
f 2 3 Ь 5 6
f tf
99

Авторы
Даты
1991-04-30—Публикация
1988-12-05—Подача