1-(арилазохлорацетил)-3(арил)-тиомочевины, ранее не известные, могут служить исходными веществами для получения лекарственных веществ, гербицидов, фунгицидов.
Описываемый способ получения 1-(арила-зохлорацетил)-3-(арил)-тиомочевин общей формулы
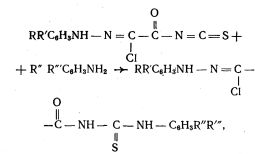
где: 1) R (при R′ и R′′=H) = Алк(С1-C5), АлкО(С1-C5), F, Cl, Br, I, SCN, CF3SO2, CH3SO2, CH3S, CH3CO, CF3, NO2; R′′′ = Алк(С1-C5), АлкО(С1-C5), F, Cl, Br, I, SCN, CF3SO2, CH3SO2, CH3S, CH3CO, CF3, CO2H, CO2C2H5, SO2NH2, SO2NHCOCH3.
2) R = R′ = Cl2, Br2, (CH3)2, (CH3O)2, (C2H5O)2; R′′′ (при R′′ = H) = Алк (C1-C5), АлкО(С1-C5), CF3SO2, CF3, CH3SO2, CH3S, F, Cl, Br, I, NO2, CO2H, SO2NH2.
3) R = CH3, R′=Cl; R′′′ (при R′′ = H) = Алк (С1-C5), АлкО(С1-C5), F, Cl, Br, I, CF3SO2, CH3SO2) CH3S, CF3, CH3CO, NO2, SO2NH2, CO2H, CO2C2H5, SO2NHCOCH3.
4) R = CH3O, R′ = Cl; R′′′ (при R′′ = H) = Алк(С1-C5), АлкО(С1-C5), F, Cl, Br, I, NO2, CF3SO2 CH3SO2, CH3CO, CO2H, CO2C2H5, SO2NH2.
5) R = NO2, R′ = Cl; R′′′ (при R′′ = H) = Алк(С1-C5), АлкО(С1-C5), F, Cl, Br, I, NO2, CF3SO2, CH3SO2, CH3S, CF3, CH3CO, SO2NH2, SO2NHCOCH3 CO2H, CO2C2H5.
6) R (при R′ = H) = Алк, АлкО, F, Cl, Br, I, NO2, CF3SO2, CH3CO, CF3, CH3SO2;
а) R′′ = R′′′ = Cl2, Br2, Алк(С1-C2), АлкО(С1-C2);
б) R′′ = OH; R′′′ = CO2H.
заключается в том, что на ароматические амины воздействуют изотиоцианатами арилазохлоруксусных кислот в среде ацетона.
Пример 1. 1-(о-метоксифенилазохлорацетил)-3(n-толил)тиомочевина. К раствору 0,5 г (0,00185 моль) изотиоцианата о-метоксифенилазохлоруксусной кислоты в 15 мл ацетона прибавляют по каплям раствор 0,3 г (0,0028 моль) n-толуидина в 8 мл ацетона. При этом наблюдается разогревание реакционной смеси. Спустя несколько минут после прибавления всего n-толуидина раствор мутнеет и выпадает осадок. Смесь выдерживают при комнатной температуре и периодическом встряхивании 5-7 час, а затем отгоняют ацетон. Остаток обрабатывают разбавленной соляной кислотой, фильтруют, промывают водой до нейтральной реакции и сушат.
Выход 0,65 г (93%); т. пл. 146-147°С (из спирта); максимум поглощения в УФ при 370 мм (в спирте).
Найдено (%): С 54,34, 54,23; Н 4.57, 4.47; S 8,65, 8.58.
Вычислено (%): С 54.17; Н 4.51; S 8.58.
Пример 2. 1-(о-метоксифенилазохлорацетил-3-(n-этоксифенил)-тиомочевина.
Получают по вышеприведенной методике. В реакцию берут 0,5 г (0,00185 моль) изотиоцианата о-метоксифенилазохлоруксусной кислоты и 0,35 г (0,0025 моль) n-фенетидина в 25 мл ацетона.
Выход 0,75 г (100%); т. пл. 140-141°С (из спирта).
Желтые мелкие иглы. Максимум поглощения в УФ при 369 мм (в спирте).
Найдено (%): С 53.32, 53.29; Н 4.73, 4.64; S 8.02, 7.99; C18H19CN4O3.
Вычислено (%): С 53.13; Н 4.70; S 7.88.
Пример 3. 1-(о-метоксифенилазохлорацетил-(-3-)-(n-хлорфенил)-тиомочевина.
Получают аналогично примерам 1 и 2. В реакцию берут 0,5 г (0,0028 моль) изотиоцианата-о-метоксифенилазохлоруксусной кислоты и 0,35 г (0,00276 моль) n-хлоранилина в 30 мл ацетона.
Выход 0,65 г (88,5%), т. пл. 154-155°С (из спирта). Желтые кристаллы. Максимум поглощения в УФ при 237, 258, 371 мм (в спирте).
Найдено (%): С 48.39, 48.35; Н 3.50, 3.42; S 8.08; C16H14Cl2N4O2.
Вычислено (%): С 48.36; Н.55; S 8.07.
Пример 4. 1-о-метоксифенилазохлорацетил-3-(n-фторфенилтиомочевина).
Получают аналогично примерам 1-3. В реакцию берут 0,5 г (0,00185 моль) изотиоцианата о-метоксифенилазохлоруксусной кислоты и 0,3 г (0,0027 моль) n-фторанилина в 25 мл ацетона.
Выход 0,6 г (84,6%); т. пл. 208-209°С (из спирта).
Найдено (%): С 50.68, 50.50; 50.47; Н 3.54; 3.61; 3.82.
Вычислено (%): С 50.46; Н 3.67. C16H14FClN4O2S.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНСЕКТИЦИДНЫЕ АРИЛПИРРОЛИДИНЫ | 2008 |
|
RU2473541C9 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСАЗОЛОВ КОНДЕНСАЦИЕЙ АРОМАТИЧЕСКИХ АЛЬДЕГИДОВ С АЛЬФА-КЕТОКСИМАМИ С ОБРАЗОВАНИЕМ N-ОКСИДОВ И ПОСЛЕДУЮЩИМ ВЗАИМОДЕЙСТВИЕМ С АКТИВИРОВАННЫМИ ПРОИЗВОДНЫМИ КИСЛОТ | 2005 |
|
RU2402537C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИМИДАЗОЛОВ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМОЙ СОЛИ | 1989 |
|
RU2028293C1 |
| НОВЫЕ КУМАРИНЫ, ИХ КАРБОКСАМИДНЫЕ ПРОИЗВОДНЫЕ, СПОСОБЫ ПОЛУЧЕНИЯ, КОМПОЗИЦИИ И ПРИМЕНЕНИЕ | 2003 |
|
RU2361870C2 |
| КВАТЕРНИЗОВАННЫЙ ПОЛИБЕНЗИМИДАЗОЛ | 2011 |
|
RU2575849C2 |
| СОЕДИНЕНИЕ | 2008 |
|
RU2505532C2 |
| СОЕДИНЕНИЯ И СПОСОБЫ ИНГИБИРОВАНИЯ ВЗАИМОДЕЙСТВИЯ БЕЛКОВ Bcl СО СВЯЗЫВАЮЩИМИ ПАРТНЕРАМИ | 2007 |
|
RU2468016C2 |
| ЛИГАНДЫ, СЕЛЕКТИВНО РАЗРУШАЮЩИЕ АНДРОГЕННЫЕ РЕЦЕПТОРЫ (SARD), И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2795431C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1,4-ДИФЕНИЛАЗЕТИДИНОНА | 2005 |
|
RU2380361C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3-ТРИФТОРМЕТИЛЬНЫХ ХАЛКОНОВ | 2009 |
|
RU2502720C2 |
Способ получения 1-(арилазохлорацетил)-3(арил)-тиомочевин общей формулы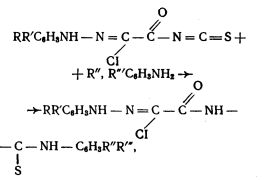
где: 1) R (при R′ и R′′ = Н) = Алк (C1 - С5), Алк О (С1 - С5), F, Cl, Br, I, SCN, CF3SO2, CH3SO2, CH3S, СН3СО, CF3, NO2; R′′′ = Алк (C1 - C5), Алк O (C1-C5), F, Cl, Br, I, SCN, CF3SO2, CH3SO2, CH3S, CH3CO, CF3, CO2H, CO2C2H5, SO2NH2, SO2NHCOCH3.
2) R = R′ = Cl2, Br2, (CH3)2 (CH3O)2, (C2H5O)2; R′′′ (при R′′ = H) = Алк (C1-C5), Алк О (С1 - C5), CF3SO2, CF3, CH3SO2, CH3S, F, Cl, Br, I, NO2, CO2H, SO2NH2.
3) R = CH2, R′ = Cl; R′′′ (при R′′ = H) = Алк (С1 - C5), Алк О (C1 - C5), F, Cl, Br, I, CF3SO2, CH3SO2, CH3S, CF3, CH3CO, NO2SO2NH2, CO2H, CO2C2H5, SO2NHCOCH3.
4) R = CH3O, R′ = Cl; R′′′ (при R′′ = H) = Алк (С1 - C5), Алк О (С1 - C5), F, Cl, Br, I, NO2, CF3SO2 CH3SO2, CH3CO, CO2H, CO2C2H5, SO2NH2.
5) R = NO2, R′ = Cl; R′′′ (при R′′ = H) = Алк (С1-C5), Алк О (С1 - C5), F, Cl, Br, I, NO2, CF3SO2 CH3SO2, CH3S, CF3, CH3CO, SO2NH2, SO2NHCOCH3 CO2H, CO2C2H5.
6) R (при R′ = H) = Алк, АлкО, F, Cl, Br, I, NO2 CF3SO2, CH3CO, CF3, CH3SO2;
а) R′′ = R′′′ = Cl2, Br2, Алк (C1 - С2), Алк О (С1 - С2);
б) R′′ = ОН; R′′ = СО2Н.
отличающийся тем, что ароматические амины обрабатывают изотиоцианатами арилазохлоруксусных кислот в среде ацетона.
Авторы
Даты
1965-02-04—Публикация
1963-08-05—Подача