Изобретение относится к ветеринарной вирусологии к клеточной биотехнологии, в частности к способу культи-- варования вируса лейкоза крупного рогатого скота (ВЛКРС ),, который может быть использован в приготовлении имму- нодиагностических и иммуноггрофилакти- ческих средств, а также при проведении разного характера вирусологических и молекулярно-иммунологических исследований.
Цель изобретения - увеличение репродукции вируса пейкоза крупного рогатого скота.
Для этого при осуществлении способа репродукции вируса лейкоза в клеточной культуре к питательной среде Игла, содержащей 10% сыворотки крупного рогатого скота, добавляют 5,6-диметилбекзимидазслил-Со-метилкобамид(метилкобаламин) г- концентрации от 0507i- 2.5- (.
П р п м ер. Для изучения стимулгг- рующен активности метилкобаламина на репрод} Ki .iTio вируса лейкоза крупного рогатого скота используют линию клеток FLK.
Перед пассажем нее культуры просматривают под микроскопом и определяют количество клеток при помощи камеры Горлова. Тп ттого клетки отделчыт. от мочослоя подогретьм до 37 С 0,25%-ным раствором трипсина, содержащим 0,025%-ньй раствор верее- на (1:1 трипсин сливают, а клетки ресуспечдкруюг Б свежей среде роста (2-3 х 10 клеток/матрас), содержащей 10% сыворотки кровч крупного ро-к|
О
ЈЛ
DO
гатого скота и антибиотики (пенициллин, 100 ед/мл, стрептомицин, 100 ед/мл). Клетки инкубируют при 37 °С. Перевивки проводят через каж- дые 5-6 дней. Из одной материнской культуры готовят несколько дочерних. Растворы метилкобаламина готовят на физиологическом растворе.; автокла- вируют при 0,5 атм в течение 30 мин и вводят в культуралънуго среду (обычно 1-2 мл) до конечных концентраций: 0,074-10 6Н; 0}}7-10 бМ; 0374. 2,5 1 11 и 5,0- . Культуры выращивают при 37°С в течение 5-6 дней.
Параллельно проводят контрольные опыты с той хе культурой по известному способу, без добавления метил кобаламипов в среду роста,
Через 5 суток культурачьпую жид- кость из всех сосудов сливают, образовавшийся монослой обрабатывают 0,25%-нмм раствором трипсина, содер- жа щим 0,025%-НЕ 1Й раствор в ер сена, разводят раствором Хенкса и подсчиты- вают количество клеток в камере Го- ряева,
В культуральной жидкости определяют вируспродуцируницую активность культуры путем измерения ревертазной активности.
Для этого культуральную жидкость 1 (обычно в объеме 20-23 мл) осветляют путем центрифугирования в течение
в сцинтилляционном счетчике SL-30.
t
Величина полученной радиоактивности характеризует ревертазную активность анализируемого аликвота вирусного лизата. Чем выше радиоактивность, тем более лизат активен в отношении ревертазы. Поскольку из литературы известно, что ревертазная активность (она определяется по величине радиоактивности) коррелирует с количеством вирусных частиц, то на основании величин радиоактивности можно высчитать и количество образовавшихся вирусных частиц в контрольных вируспродуцирую- щнх культурах и в культурах, росших в присутствии стимулятора - метилкобаламина в разных концентрациях. Данные так-ix определении приведены в таблице.
Радиоактивность контрольных вирусных лизатов принята за 100%, т.е. соответствует 39528 имп/мин. Поскольку радиоактивность з вируспродуцирую- щих культурах, росших в присутствии метилкобаламина, выше, то соответственно и процентная величина вырастает Видно, что стимуляция образования ,вирусных частиц в присутствии в среде метилкобаламина начинается уже при началы-ой концентрации 0,074-1 О М и перестает расти при концентрации 5,. Итак, наиболее эффективные концентрации метилкобаламина з пита

| название | год | авторы | номер документа |
|---|---|---|---|
| Штамм культивируемых клеток почки эмбриона коровы для культивирования вируса лейкоза крупного рогатого скота | 1989 |
|
SU1652338A1 |
| ШТАММ 8С12 ПОСТОЯННОЙ МЕЖВИДОВОЙ ГИБРИДНОЙ ЛИНИИ КЛЕТОК МЫШИ Mus. musculus И ОВЦЫ Ovis aries - ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ К ГЛИКОПРОТЕИДНОМУ АНТИГЕНУ ВИРУСА ЛЕЙКОЗА КРУПНОГО РОГАТОГО СКОТА | 2008 |
|
RU2377297C1 |
| СПОСОБ ДИАГНОСТИКИ ЛЕЙКОЗА КРУПНОГО РОГАТОГО СКОТА | 2008 |
|
RU2377962C1 |
| Штамм перевиваемых клеток легкого эмбриона крупного рогатого скота - продуцент вируса лейкоза крупного рогатого скота | 1990 |
|
SU1778185A1 |
| ШТАММ 1Н8 ПОСТОЯННОЙ ГИБРИДОМНОЙ ЛИНИИ КЛЕТОК МЫШИ Mus. Musculus - ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ К IgG ОВЦЫ | 2008 |
|
RU2377298C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИГЕНА ВИРУСА ЛЕЙКОЗА КРУПНОГО РОГАТОГО СКОТА | 1992 |
|
RU2020960C1 |
| ШТАММ 5А10 ПОСТОЯННОЙ ГИБРИДОМНОЙ ЛИНИИ КЛЕТОК МЫШИ Mus. musculus - ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ К IgG КРУПНОГО РОГАТОГО СКОТА | 2008 |
|
RU2377299C1 |
| СПОСОБ ПОДГОТОВКИ БИОМАТЕРИАЛА ДЛЯ ПЦР ДИАГНОСТИКИ ВИРУСА ЛЕЙКОЗА КРУПНОГО РОГАТОГО СКОТА (ВЛ КРС) | 2013 |
|
RU2566071C2 |
| Способ изготовления аллергена для диагностики лейкоза крупного рогатого скота | 1989 |
|
SU1734763A1 |
| ШТАММ ДИПЛОИДНЫХ КЛЕТОК ЛЕГКОГО ПЛОДА КРУПНОГО РОГАТОГО СКОТА ДЛЯ РЕПРОДУКЦИИ ВИРУСОВ | 2012 |
|
RU2515915C1 |
Изобретение относится к ветеринарной вирусологии и клеточной биотехнологии. Конкретно к способу культивирования вируса лейкоза крупного рогатого скота (ВЛКРС), который может быть использован и приготовлении им- мунодиагностических и иммунопрофилак-. тических средств, а такгсе при проведении разного рода вирусологических и молекулярно-иммунологических исследований . Цель изобретения - увеличение репродукции ВЛКРС. Для этого в культуралъную среду, содержащую среду Игла с 10% сыворотки крупного рогатого схота вводят 596-диметилбензи- мицазолил-Сс-метилкобамидк- (метилко- баламин) в концентрации от 0,074-10 до 2, что позволяет увеличить репродукцию вируса лейкоза на 30-50%. 1 та бл. -,-е о «
30 мин при 5000 об/мин при 4 С, Вирус т,- тельной среде при образовании вирусных
10
45
осаждают центрифугированием уже обработанной жидкости в течение 40 мин при 30000 об/мин при 4°С над 20%-ной сахарозой, приготовленной в 0,01 1 буфере, рН 7,5, содержащем 0,1 М NaCl и 0,001 М ЭДТА.
Собранные вирусы i00 мкл лизируют в течение 20 мин при 2°0 в 0S01 M трис-HCl буфере, рН 7,8, содержащем 0,008 Н дитиотреитол, 0,2% тритона Х-100 и проводят ревертазную реакцию. Для этого 10 мкл вирусного лизата прибавляют 90 мкл смеги, содержащей 0,05 И трио-ИГЛ бусЬер, рН 7,8, 0,002 М дитиотреитол, 0,025% тритон Х-100, ,, 0,25 ед/мл полкА-олигоТу0.(0, 0,008 ММр,СПг ч /3П/тимидинтрифосфат (74 па пробу), инкубируют 30 мин при ЗГ)°С. Ревертазную реакцию останавливают добавле| ием трпхлорукгусной кислоты до к H j4Hon концентрации 7,5%. Осадок наносят на мембранные ультрафильтры С.ыттор (диаметр пор 0,9 MiO и измеряют радиоактивность
частиц являются от 0,3/.. 10 °до 2,5 х... За пределами указанных концентраций, т.е. культивация вирусной культуры при более высоких концентрациях метилкобаламина нецелесообразна, .поскольку выход вируса не повышается, а расходы метилкобаламина повышаются, что экономически не выгодно.
Таким образом, введение метилкобаламина в питательную среду Игла с 10% сыворотки крупного рогатого скота позволяет увеличить репродукцию вируса лейкоза на 30-50% по сравнению с прототипом, а тем же самым и уменьшить материальные расходы при накоплении вирусного материала.
Формула
и з о
б р е т
и я
55
Ј. Спссоб культивирования вчтэуса лейкоза крупного рогатого скота, путем инкуб;ттвания вируспродуцирующей культуры г питательной среле Пглз с до- бавлел нем сыворотки крови крупного
тельной среде при образовании вирусных
частиц являются от 0,3/.. 10 °до 2,5 х... За пределами указанных концентраций, т.е. культивация вирусной культуры при более высоких концентрациях метилкобаламина нецелесообразна, .поскольку выход вируса не повышается, а расходы метилкобаламина повышаются, что экономически не выгодно.
Таким образом, введение метилкобаламина в питательную среду Игла с 10% сыворотки крупного рогатого скота позволяет увеличить репродукцию вируса лейкоза на 30-50% по сравнению с прототипом, а тем же самым и уменьшить материальные расходы при накоплении вирусного материала.
Формула
и з о
б р е т
и я
Ј. Спссоб культивирования вчтэуса лейкоза крупного рогатого скота, путем инкуб;ттвания вируспродуцирующей культуры г питательной среле Пглз с до- бавлел нем сыворотки крови крупного
рогатого скота, отличагощи й- с я тем, что, с целью увеличения репродукции вируса, в питательную среду дополнительно вводят 5,6-ди2, Способ по п. 1, о т л и ч a re in и и с я тем, что, с целью удешев ления, 5,6-днметиттбензимидазолил-Со метилкобамид вводят в концентрации
метилбензимидазолил-Со-метилкобамид. 0,074.,.
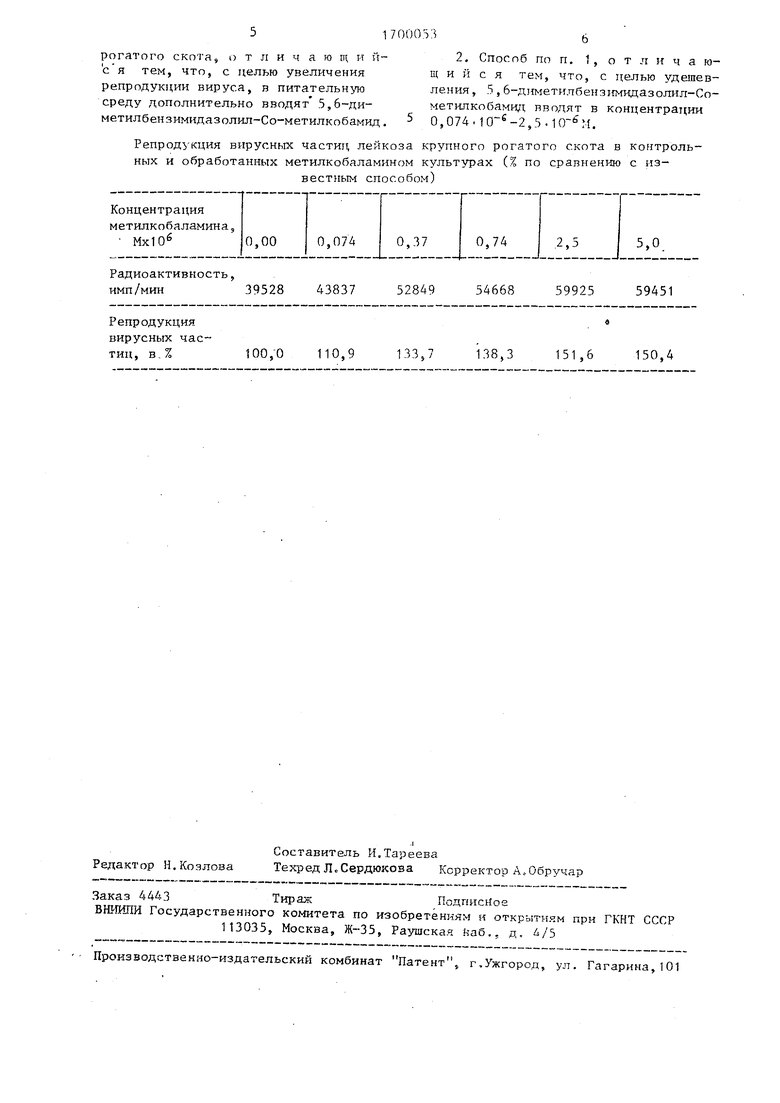
Репродукция вирусных частиц лейкоза крупного рогатого скота в контрольных и обработанных метилкобаламином культурах (% по сравнению с известным способом)
Радиоактивность, имп/мин39528
43837
Репродукция вирусных частиц, в %
100,0110,9
2, Способ по п. 1, о т л и ч a rein и и с я тем, что, с целью удешевления, 5,6-днметиттбензимидазолил-Со- метилкобамид вводят в концентрации
0,074.,.
52849 54668 59925 59451
133,7138,3151,6150,4
| Методы культивирования клеток,, Л., Наука, 1988, с | |||
| Способ очищения сернокислого глинозема от железа | 1920 |
|
SU47A1 |
| Интеграционные вирусы,, Рига, Зинатне, 1985, с | |||
| Приспособление для плетения проволочного каркаса для железобетонных пустотелых камней | 1920 |
|
SU44A1 |
Авторы
Даты
1991-12-23—Публикация
1990-02-23—Подача