Изобретение относится к способам получения а-бензиловых эфиров дикарбоновых аминокислот, конкретно а-бензиловых эфиров N-защищенных аспарагиновой и глутаминовой кислот общей формулы I
(Х-Т НСНСОгВг (,
где Х-СбНб-СНа- ОСО (Z), t BuOCO;
.2.
Соединения I используются в синтезе /3-аспартил- и у-глутамилпептидов.
Известен способ получений а-бензиловых эфиров I. Их получают этерификацией глутаминовой или аспарагиновой кислот И НгЫСНСОгН ВгЮН TsOH-H JGHCQjBrl
(СНаЬСОгНчедпСОаВг
пm
HjNCHCOzBzl
HD (CH2)ftC02H IV
с последующим селективным расщеплением дибензилового эфира III и блокированием аминогруппы 1, выход целевого продукта не превышает 40% в расчете Иа исходную аминокислоту.
По другому способу ангидриды М-защищенных дикарбоновых аминокислот подвергают взаимодействию с бензиловым спиртом в запаянной ампуле.при 100°С.
Z-ASP-OH-Z-ASP-O
.- Z-Asp-OBz + Z-AspCOB2ll-OH|
Boc-Glu-OH- Boc-Clu-O
дцгд
-- Вос-б1ц(ОВ21)-ОНДЦГА Boc-Glu-OBzl ДЦГА -Образующуюся смесь а- и у-бензиловых эфиров разделяют дробно содовой экстракцией или в виде дициклогексиламмониевых солей. Выход Z-Asp-OBzl и Boc-G u-OBzl не превышает 50%.
Недостатками указанных способов является многостадийность и низкий выход продуктов. В качестве прототипа выбран способ получения а-бензилового эфира БОК-глутаминовой кислоты 3, согласно которому к триэтиламмониевой соли БОКглутаминовой кислоты прибавляют зквимолярное количество бензилбромида. Через 10 ч продукты реакции - смесь а- и у-бензиловых эфиров переводят в этилацетат откуда дробной содовой экстракцией с последующим подкислением водного слоя и экстракцией этилацетатом выделяют 44% целевого продукта - а-бензилового эфира БОК-глутаминовой кислоты.
BzlBr
Вое- &lu- i Boc-&lu-OBzU
EtjN
-vBoc- luCOBzn- ОН
Недостатками прототипа являются длительность процесса (10 ч), неоднозначность протекания реакции, образование смеси изомерных монобензиловых эфиров и, как следствие, низкий выход целевого продукта. Кроме того, возникает необходимость разделения изомеров дробной экстракцией.
Цель изобретения - повышение выхода и упрощение способа получения а-бензиловых эфиров N-защищенных аспарагиновой и глутаминовой кислот.
Цель достигается в способе , предусматривающем взаимодействие N-эащищенных глутаминовой или аспарагиновой кислот с бензилбромидом тем, что в отличие от прототипа процесс осуществляют в присутствии эквимолярных количеств метилата натрия и краун-эфира (18 краун-6 или 15краун-5).
Указанная совокупность признаков определяет новизну изобретения.
Существенные отличия изобретения объясняются следующим.
В литературе известно использование солей карбоновых кислот для получения эфиров в присутствии краун-эфиров, которые выступают в качестве катализаторов межфазного переноса. Выбор соотношения метилата натрия и краун-эфира объясняется следующим. Максимальные выходы «-бензиловых эфиров N-защищенных дикарбоновых аминокислот наб людаются при эквимолярном соотношении исходной аминокислоты, краун-эфира и метилата натрия, изменение указанного соотношения реа
гентов приводит к уменьшению выхода (см, табл. 1). В то же время не известен способ селективного получения а-эфиров дикарбоновых кислот с краун-эфиром. При реализации предлагаемого способа не образуются
0 изомерные у-эфиры, что упрощает выделение целевых продуктов. В предлагаемом способе краун-эфир используется не как катализатор межфазного переноса, а для образования комплекса с мононатриевой
5 солью дикарбоновой аминокислоты.
Предлагаемый способ осуществляют следующим образом.
К раствору N-защищенной дикарбоновой аминокислоты в диметилформамиде
0 прибавляют аквимолярное количество метилата натрия, краун-эфира и бензилбромида. Через 2 ч обычным способом выделяют а-бензиловый эфир N-защищенной аминокислоты.
5 Изобретение иллюстрируется-следующими примерами.(
Пример1.3г (12 ммоль) БОК-глутаминовой кислоты растворяют в 7 мя ДМФА, прибавляют 0,064 г метилата натрия и
0 2,64 мл (12 ммоль) 15-краун-5. Раствор обрабаты вают 1,2 мл (12 ммоль) бензилбромида, перемешивают 2,5 ч при комнатной температуре. Прибавляют 50 мл этилацетата. промывают водой (50 мл) органический
5 слой, Этилацетатный раствор сушат, упаривают в вакууме. Получают 2,9 г (73% бензилового эфира БОК-глутаминовой кислоты,
т.пл. 93°С, « -29,7° (с 2, МеОН).
Аналогично получёны Z-Glu-OBzl, 70%(30% - лит. данные), т. пл. 96°С (95-96°
-лит. данные), -10,3° (с 1,7, уксусная кислота) (-10,4° - лит. данные).
Boc-Asp-OBzl, 68%, т.пл. 100°С (1025 104°С - лит. данные), а )° -24.6°С (-25°С
-лит. данные) (с 1,0, МеОН).
Z-Asp-OBzl, 72%,т.пл. 82°С(84°С-лит.
данные), а -8, (-9,4 - лит. данные) (с 1,2,АсОН).
Примеры 2-7, Иллюстрируют осуществление предлагаемого способа согласно примеру 1. Результаты приведены в табл.1 и 2.
Изобретение имеет следующие преимущества по сравнению с прототипом: синтез а-бензиловых эфиров N-защищенных дикар|боновых аминокислот из комплексов мононатриевых солей N-эащищенных глутаминовой и аспарагиновой кислот с краунэфирами протекает однозначно, без образования изомерных у-бензиловых эфиров, в результате увеличивается выход и упрощается процесс выделения целевых продуктов, кроме того, уменьшается время реакции.
Формула изобретения 1. Способ получения обензиловых эфиров N-защищенных дикарбоновых аминокислот формулы. .
X-MHCHCOjBzl
(СНг пСОгН
где Х-СбН5-СН2- ОСО (Z), t ВиОСО;,2.
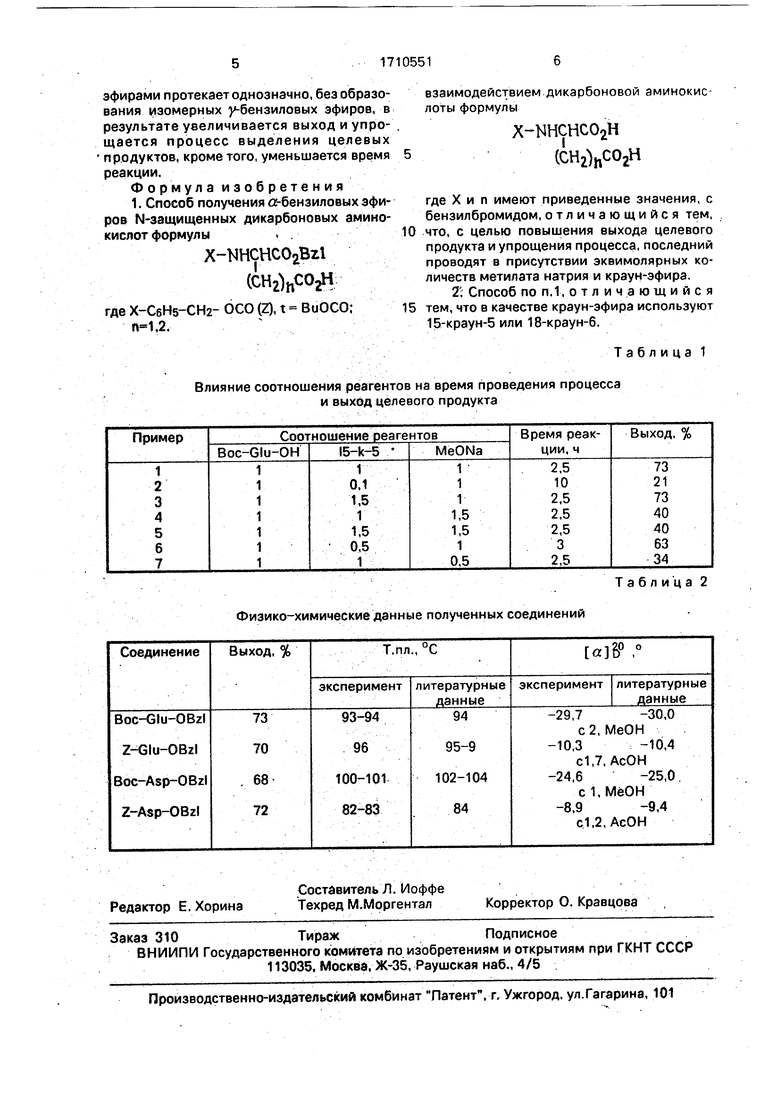
Влияние соотношения реагентов на время проведения процесса и выход целевого продукта
взаимодействием дикарбоновой аминокислоты формулы
X-NHCHCOjH
(CH2)ftC02H
где X и п имеют приведенные значения, с бензилбромидом, отличающийся тем,
10 что, с целью повышения выхода целевого продукта и упрощения процесса, последний проводят в присутствии эквимолярных количеств метилата натрия и краун-эфира. 2; Способ по П.1, о т л и ч а ю щ и и с я
15 тем, что в качестве краун-зфира используют 15-краун-5 или 18-краун-б.
Таблица 1

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения пептида Ac-His-Ala-Glu-Glu-NH | 2021 |
|
RU2767030C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕПТИДОВ, ОБЛАДАЮЩИХ ТКАНЕСПЕЦИФИЧЕСКОЙ АКТИВНОСТЬЮ, И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ | 2000 |
|
RU2161501C1 |
| ПЕПТИДЫ, ОБЛАДАЮЩИЕ ЦИТОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2011 |
|
RU2482128C1 |
| ПЕПТИД И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1994 |
|
RU2067000C1 |
| КОМБИНАЦИЯ ПЕПТИДОВ | 2009 |
|
RU2482127C2 |
| ПРОИЗВОДНЫЕ ГЕМИНА И ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, СПОСОБ ПОЛУЧЕНИЯ, ПРИМЕНЕНИЕ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2002 |
|
RU2238950C2 |
| RGD-СОДЕРЖАЩИЕ ПЕПТИДЫ | 2001 |
|
RU2214416C2 |
| АСПАРТИЛЬНЫЕ ПРОИЗВОДНЫЕ ГИСТАМИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ МОДУЛЯТОРОВ АКТИВНОСТИ ФЕРМЕНТОВ АНТИОКСИДАНТНОЙ ЗАЩИТЫ | 2005 |
|
RU2287524C1 |
| N-АЦИЛЬНЫЕ ПРОИЗВОДНЫЕ БИОГЕННЫХ АМИНОВ - МОДУЛЯТОРЫ ПЕРЕКИСНОГО ОКИСЛЕНИЯ ЛИПИДОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1994 |
|
RU2093520C1 |
| Способ получения пептидов | 1988 |
|
SU1598881A3 |
Изобретение касается эфиров аминокислот, в частности получения а-бензило- вых эфиров N-защищенных дикарбоновых аминокислот общей ф-лы X-NH- CH[(CH2)nC
Физико-химические данные полученных соединений
Таблица 2
| J.Am | |||
| Chem | |||
| Soc., 1953, 75, 4610.Pawelezak et al | |||
| Dry | |||
| Prep, and Proc | |||
| Int. | |||
| Приспособление для установки двигателя в топках с получающими возвратно-поступательное перемещение колосниками | 1917 |
|
SU1985A1 |
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
Авторы
Даты
1992-02-07—Публикация
1989-08-02—Подача