Изобретение относится к новым биологически активным соединениям, конкретно к бромистоводородной соли 4-окси-3-[N-(фенацил)бензиламино]-N-бензилбутанамида формулы I
C6H5-CO-CH2-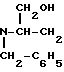 -CONH-C6H5·HBr проявляющей местноанестезирующую активность, которая в связи с этим может быть использована в медицине.
-CONH-C6H5·HBr проявляющей местноанестезирующую активность, которая в связи с этим может быть использована в медицине.
Цель изобретения - поиск новых замещенных амидов карбоновых кислот, проявляющих высокую местноанестезирующую активность.
П р и м е р 1. Бромистоводородная соль 4-окси-3-[N-(фенацил)бензиламино]-N-бензилбутанамида.
Нагревают до кипения в 50 см3 смеси этилацетата - хлороформ (2:1) 2,37 г бромистого фенацила с 3,54 г 3-бензиламино-4-окси-N-бензилбутанамида. Выпавший через сутки осадок соединения I (3,37 г, 57%) промывают на фильтре серным эфиром, т.пл. 82-84оС.
Найдено, %: C 63,5; H 5,0; N 5,5; Br 16,0.
C26H24BrN2O3.
Вычислено, %: C 63,4; H 4,9; N 5,7; Br 16,3.
ИК-спектр, см-1: 3240, 3100, 1635, 1620, 1590, 1530.
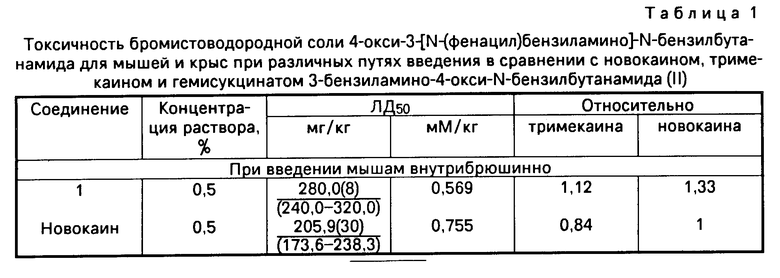
Токсичность (ЛД50) соединения I определена при однократном внутрибрюшинном, подкожном и внутривенном введениях мышам и крысам. Полученные результаты представлены в табл. 1, из которой видно, что при внутрибрюшинном введении соединение I менее токсично, чем новокаин и тримекаин, а при подкожном и внутривенном введении токсичность соединения I на уровне токсичности новокаина.
Поверхностную (терминальную) анестезию изучали в опытах на роговице глаза кролика с использованием метода Ренье. Испытания (прикосновения к роговице с помощью волоска Фрея с силой давления 50 г/мм2) начинали с третьей минуты и в последующем через каждые 5 мин (в течение 1 ч) от момента инстилляции одной или двух (с интервалом в одну минуту) капель раствора. Исследовали 0,5; 1; 2 и 5%-ные растворы, которые получали при растворении в 0,7%-ном растворе натрия хлорида при 50-55оС. Полная (100%-ная) анестезия в течение всего опыта выражалась числом 1300,0 (13 испытаний х 100 прикосновений).
Инфильтрационную анестезию исследовали в опытах на крысах с использованием интрадермального метода. Болевое раздражение анестезированного участка кожи производили с интервалами в 3 с с помощью специальной иглы, позволяющей наносить уколы всегда с одинаковой силой давления (36 г на ед. поверхности). За индекс анестезии принималось число 36 (6 испытаний х 6 уколов), которая выражалась 100%-ным обезболиванием.
Спинно-мозговую анестезию исследовали в опытах на крысах.
Растворы анестезирующих веществ готовили на 0,7%-ном растворе хлорида натрия. Результаты исследований, полученные в градуированной форме, подвергали статистической обработке, используя таблицы для ускоренной количественной оценки фармакологического эффекта. Определяли средние эффективные концентрации (ЕК50), коэффициенты относительной активности и терапевтические индексы (ЛД50/ЕК50).
Антиаритмическую активность исследовали на аконитиновой и адреналиновой моделях аритмий у наркотизированных (этаминал натрия, 40 мг/кг, внутрибрюшинно) крыс, из которых первая модель является специфической для блокаторов быстрых натриевых каналов, вторая - медленных кальциевых каналов. Рассчитывали средние эффективные дозы (ЕД50). В качестве критерия активности использовали отношение ЛД50/ЕД50, которые обозначали, как антиаритмический индекс.
П р и м е р 2. Исследование местноанестезирующей активности соединения I при терминальном методе обезболивания.
В результате изучения соединения I при терминальном методе обезболивания установлено, что соединение I по активности несколько уступает тримекаину и лидокаину и в значительной мере - дикаину (см. табл.2). В то же время следует отметить, что соединение I и тримекаин в 0,5; 1; 2 и 5%-ных концентрациях не вызывали признаков раздражающего действия на конъюнктиву глаза, тогда как от 1; 2 и 5%-ных растворов лидокаина и в большей мере дикаина отмечался выраженный эффект, характеризующийся перикорнеальной инъекцией (1%-ный раствор лидокаина), гиперемией конъюнктивы век (1%-ный раствор дикаина и 2%-ный раствор лидокаина), мигательной перепонки и склеры (2% -ный раствор дикаина и 5%-ный раствор лидокаина) в течение 30-300 мин. В части опытов под влиянием 2 и 5%-ных растворов дикаина наблюдался выраженный отек век (вплоть до выворота), длящийся более 300 мин.
П р и м е р 3. Исследование местно-анестезирующей активности соединения I при инфильтрационной анестезии.
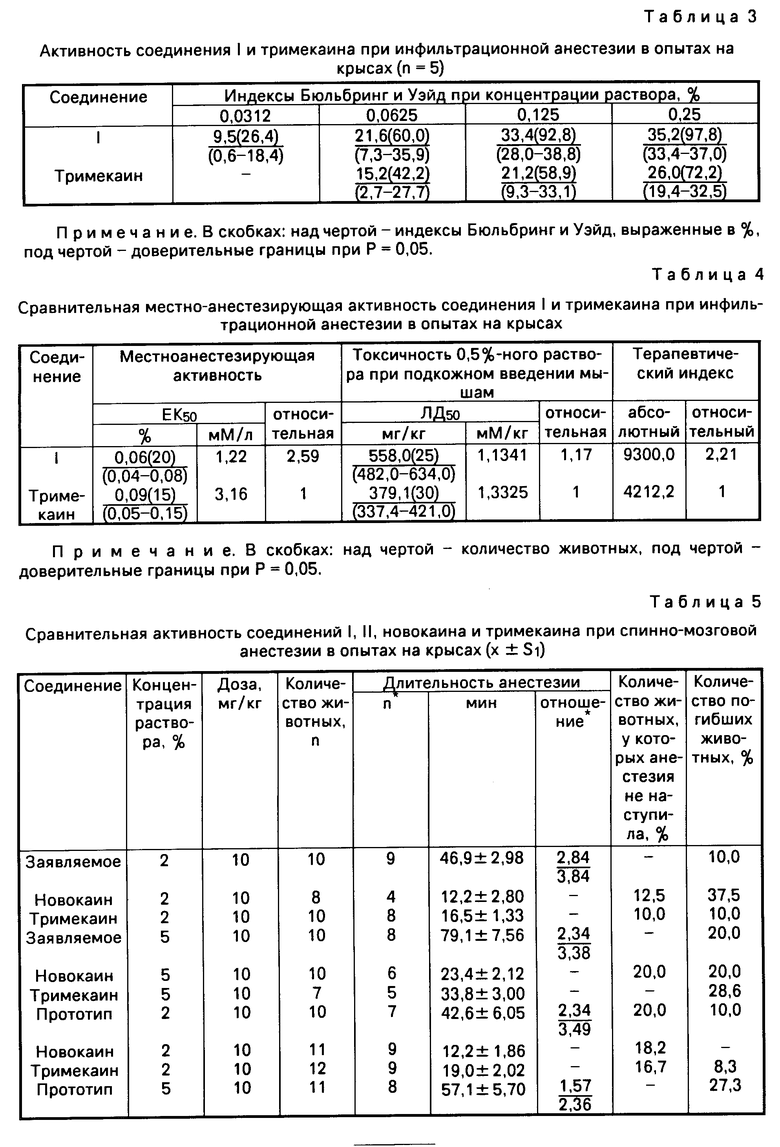
При изучении инфильтрационной анестезии, проявляемой соединением I в опытах на крысах, установлено, что минимальной эффективной концентрацией, вызывающей обезболивающее действие, является 0,0312%, тогда как для тримекаина 0,0625% (см. табл.3).
Соединение I по местно-анестезирующей активности и широте терапевтического эффекта соответственно в 2,59 и 2,21 раза превосходит тримекаин (см. табл.4).
П р и м е р 4. Исследование местно-анестезирующей активности соединения I при спинно-мозговой анестезии.
При спинно-мозговом методе обезболивания в опытах на крысах установлено, что соединение I (10 мг/кг) в 2 и 5%-ных растворах по длительности анестезии соответственно в 2,84 и 2,34 раза превосходит тримекаин в 3,84 и 3,38 раза и новокаин (см. табл.5).
П р и м е р 5. Исследование антиаритмической активности соединения I на аконитиновой модели аритмии.
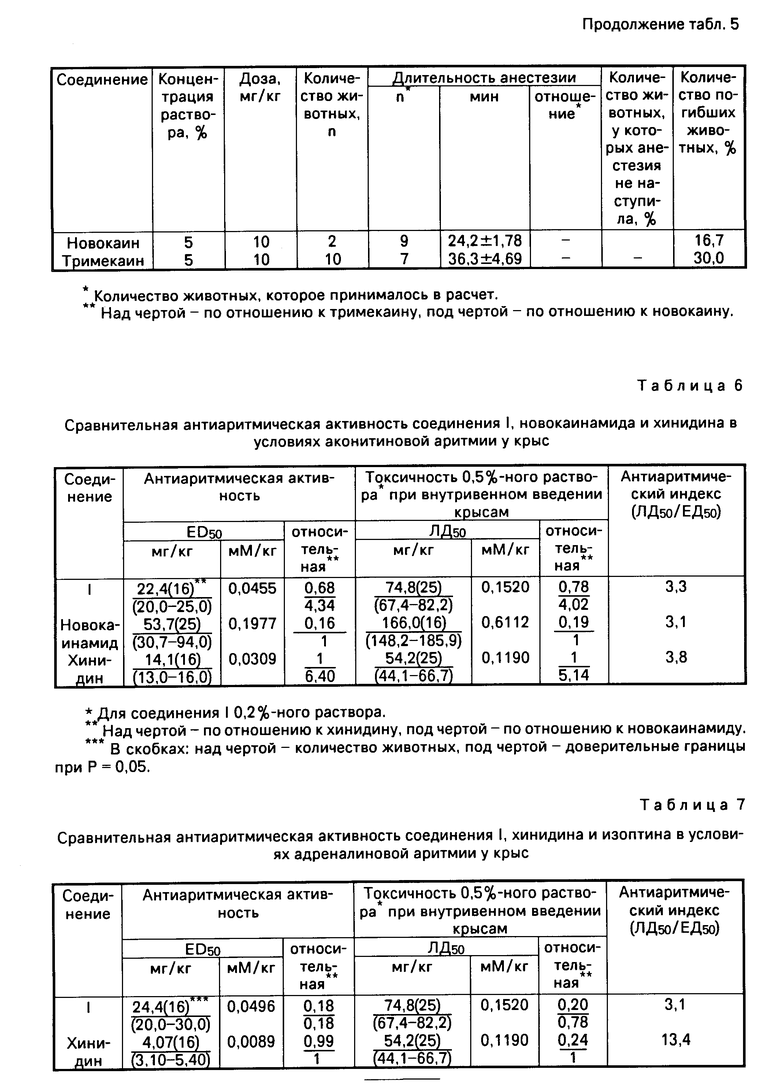
В результате исследования антиаритмических свойств соединения I выявлено, что в условиях нарушений сердечного ритма, вызванных аконитином (см. табл. 6), соединение I по активности в 4,34 раза превосходит новокаинамид, однако в 1,47 раза уступает хинидину; по широте терапевтического действия все три вещества существенно не отличаются между собой. Следует отметить, что соединение I и новокаинамид устраняли аконитиновую аритмию в течение 2-3 мин, а хинидин в течение 5-7 мин.
П р и м е р 6. Исследование антиаритмической активности соединения I на адреналиновой модели аритмии.
На адреналиновой модели аритмии соединение I по антиаритмическому действию в 5,57 и 5,64 раза уступает хинидину и изоптину соответственно, по широте терапевтического действия заявляемое соединение в 4,32 раза превосходит хинидин и сопоставимо с изоптином (см. табл.7). Учитывая специфичность аконитиновой и адреналиновой моделей аритмий, можно полагать, что соединение I проявляет свойства блокатора как натриевых, так и кальциевых каналов нервных проводников и окончаний, а также миоцитов сердца.
Таким образом, соединение I обладает выраженными местно-анестезирующими и антиаритмическими свойствами.
При терминальной анестезии соединение I по активности несколько уступает тримекаину и лидокаину, при этом в 0,5; 1; 2 и 5%-ных растворах не оказывает раздражающего действия на конъюнктиву глаза. При инфильтрационном и спинно-мозговом методах обезболивания соединение I по активности и широте терапевтического действия превосходит новокаин и тримекаин.
На аконитиновой модели аритмии заявляемое соединение по активности превосходит новокаинамид, однако уступает в этом отношении хинидину. В условиях адреналиновой аритмии соединение I менее активно, чем хинидин и изоптин.
Таким образом, заявленное соединение менее токсично (его ЛД50 290 мг/кг при внутрибрюшинном введении мышам, у прототипа ЛД50 составляет 154 мг/кг).
Сравнительная активность заявляемого соединения, прототипа (II), тримекаина и новокаина при спинно-мозговой анестезии в опытах на крысах, свидетельствует о том, что заявляемое соединение в 2 и 5%-ных растворах (10 мг/кг) превосходит по продолжительности анестезии новокаин и тримекаин в 3,84-3,38 раза и 2,84-2,34 раза соответственно, прототип же - в 3,49-2,36 раза и 2,34-1,57 раза соответственно. Очевидно, что заявляемое соединение по данному виду активности более эффективно, чем прототип.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ БЕНЗИЛАМИДА 4-ОКСИМАСЛЯНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЕ МЕСТНО-АНЕСТЕЗИРУЮЩУЮ, АНТИАРИТМИЧЕСКУЮ, АНТИАНГИАЛЬНУЮ И АНТИНЕКРОТИЧЕСКУЮ АКТИВНОСТЬ | 1988 |
|
SU1601984A1 |
| ГЕМИГЛУТАРАТ 3-БЕНЗИЛАМИНО-4-ОКСИ-N-БЕНЗИЛБУТАНАМИДА, ПРОЯВЛЯЮЩИЙ МЕСТНО-АНЕСТЕЗИРУЮЩУЮ АКТИВНОСТЬ | 1989 |
|
SU1663928A1 |
| Соли мезидидов @ -пиперидинкарбоновых кислот, обладающие местноанестезирующей, антиаритмической и антифибрилляторной активностью, и мезидиды @ -пиперидинкарбоновых кислот в качестве промежуточных продуктов для синтеза солей мезидидов @ -пиперидинкарбоновых кислот | 1983 |
|
SU1120654A1 |
| ДИГИДРОХЛОРИД 2-ТРЕТБУТИЛ-1-(3-ДИЭТИЛАМИНОПРОПИЛ)ИМИДАЗО [1,2-А]-БЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЙ МЕСТНОАНЕСТЕЗИРУЮЩИМ И АНТИАРИТМИЧЕСКИМ ДЕЙСТВИЕМ | 2000 |
|
RU2160262C1 |
| АРИЛАЛИФАТИЧЕСКИЕ АМИНОАМИДЫ БЕНЗОЙНОЙ (ЗАМЕЩЕННОЙ БЕНЗОЙНОЙ), ЦИКЛОГЕКСАН- И 1-АДАМАНТАНКАРБОНОВЫХ КИСЛОТ, ОБЛАДАЮЩИЕ АНТИАРИТМИЧЕСКОЙ, МЕСТНОАНЕСТЕЗИРУЮЩЕЙ И АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 1996 |
|
RU2130922C1 |
| ДИГИДРОХЛОРИД 1-ДИЭТИЛАМИНОПРОПИЛ-2-ФЕНИЛИМИДАЗО[1,2-А]БЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЙ МЕСТНОАНЕСТЕЗИРУЮЩИМ ДЕЙСТВИЕМ | 1999 |
|
RU2148057C1 |
| ГИДРОХЛОРИД 2- (3'-БРОМ-4'- МЕТОКСИФЕНИЛ) -3-КАРБЭТОКСИ-4- ДИМЕТИЛАМИНОМЕТИЛ-5- ОКСИБЕНЗОФУРАНА, ОБЛАДАЮЩИЙ МЕСТНОАНЕСТЕЗИРУЮЩИМ ДЕЙСТВИЕМ | 1986 |
|
SU1426050A1 |
| 1-(3-Н-БУТОКСИПРОПИЛ)-4-ГИДРОКСИПИПЕРИДИН В КАЧЕСТВЕ ПРОМЕЖУТОЧНОГО ПРОДУКТА В СИНТЕЗЕ ГИДРОХЛОРИДОВ 1-(3-Н-БУТОКСИПРОПИЛ)-4-АЦИЛОКСИПРОИЗВОДНЫХ ПИПЕРИДИНОВ, ОБЛАДАЮЩИХ МЕСТНОАНЕСТЕЗИРУЮЩЕЙ ИЛИ ПРОТИВОАРИТМИЧЕСКОЙ АКТИВНОСТЬЮ | 1991 |
|
SU1833616A3 |
| Производные 5-оксибензофурана, обладающие местноанестезирующим, противоаритмическим, противофибрилляторным, противосудорожным и противокаталептическим действием | 1982 |
|
SU1045584A1 |
| АРИЛАЛИФАТИЧЕСКИЕ АМИНОАМИДЫ ФЕНОКСИУКСУСНОЙ ИЛИ ЗАМЕЩЕННЫХ ФЕНОКСИУКСУСНЫХ КИСЛОТ, ПРОЯВЛЯЮЩИЕ АНТИАРИТМИЧЕСКУЮ, МЕСТНОАНЕСТЕЗИРУЮЩУЮ И АНАЛЬГЕТИЧЕСКУЮ АКТИВНОСТЬ | 1997 |
|
RU2128163C1 |


Изобретение касается амидов кислот, в частности бромистоводородной соли 4-окси-3-[N-фенацил)бензиламино]-N-бензилбутанамида, проявляющей местноанестезирующую активность, что может быть использовано в медицине. Цель - создание нового более активного вещества указанного класса. Синтез ведут реакцией бромистого фенацила с 3-бензиламино-4-окси-N-бензилбутанамидов в смеси этилацетата и хлороформа. Выход 57% т. пл. 82-84°С, брутто-ф-ла C26H24BrN2O3 , эффективная доза 10 мг/кг, продолжительность действия в 3,84-3,38 и 2,84-2,34 раза выше, чем у новокаина и тримекаина (при использовании 2% -ного раствора анестезирующего вещества), токсичность ЛД50 290 против 154 мг/кг для новокаинамида. В сравнении с последним продолжительность действия нового вещества в 3,49-2,36 раза выше. 7 табл.
Бромистоводородная соль 4-окси-3-[N-(фенацил)бензиламино]-N-бензилбутанамида формулы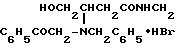 C6H5
C6H5
проявляющая местноанестезирующую активность.
| ПРОИЗВОДНЫЕ БЕНЗИЛАМИДА 4-ОКСИМАСЛЯНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЕ МЕСТНО-АНЕСТЕЗИРУЮЩУЮ, АНТИАРИТМИЧЕСКУЮ, АНТИАНГИАЛЬНУЮ И АНТИНЕКРОТИЧЕСКУЮ АКТИВНОСТЬ | 1988 |
|
SU1601984A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1994-11-15—Публикация
1989-02-13—Подача