Изобретение относится к новому биологически активному соединению/ а именно к гидрохлориду 2-(3′-бром-4′-метоксифенил)-3-карбэтокси-4-диметиламинометил-5-оксибензофура на/ обладающему местно-анестезируюзим действием/ который может найти применение в медицине.
Цель изобретения - усиление местно-анастезирующих свойств в ряду производных 4-диметиламино-5-оксибензофурана/ позволяющих исключить раздражающее действие.
Пример 1. Получение гидрохлорида 2-(3′-бром-4′-метоксифенил)-3-карбэтокси-4-диметиламинометил-5-оксибензофура на (соединение 1).
Стадия I. Получение исходного соединения -2-(3′-бром-4′-метоксифенил)-3-карбэтокси-5-оксибензофурана (соединение II).
К смеси 50 мл воды/ 30 мл толуола и 34/3 мл (0/265 моль) ацетоуксусного эфира при перемешивании и температуре 3 - 7°С прикапывают 33 %-ный водный раствор едкого натра до рН 11. Затем/ не прекращая перемешивания и охлаждения/ начинают прибавлять по каплям раствор 36/7 (0/148 моль) хлорангидрида 3-бром-4-метоксибензойной кислоты/ полученного кипячением 3-бром-4-метоксибензойной кислоты с избытком хлористого тионила в течение 3 ч с последующей отгонкой избытка хлористого тионила/ в смеси 15 мл толуола и 5 мл диметилформамида с такой скоротью/ чтобы температура реакционной массы не поднималась выше 7°С при рН 10-11. Одновременно продолжают прикапывать 33% -ный раствор едкого натра (0/35 моль).
Реакционную массу/ содержащую α-ацето-3′-бром-4′-метоксибензоилуксусный эфир/ перемешивают 1/5 ч при комнатой температуре/ 1 ч при 27-33°С и обрабатывают 8 г (0/148 моль) хлористого аммония. Смесь выдерживают 12 ч/ затем прибывляют 7 г хлористого натрия и перемешивают в течение 30 мин. Толуольный слой отделяют/ промывают насыщенным водным раствором хлористого натрия/ сушат над сульфатом магния. Толуол отгоняют. Остаток кристаллизуют из метанола.
Получают 22/8 г (51/3 %) 3′-бром-4′-метоксибензоилуксусного эфира в виде кремовых кристаллов/ растворимых в хлороформе/ бензоле/ ацетоне и не растворимых в воде. Т.пл. 50-51°С.
Найдено/ %: С 47/72; H 5,40; Br 26,26
C12H13BrO4
Вычислено/ %: С 47/86; H 4,35; Br 26,54
К смеси 22/8 г (0/076 моль)3′-бром-4′-метоксибензоилуксусного эфира/ 5/7 г хлористого цинка безводного и 0/4 мл ледяной уксусной кислоты при перемешивании и температуре 78-83°С постепенно и равномерно за 10 ч прибавляют раствор 4/11 г (0/038 моль) n-бензохинона в 20 мл хлористого метилена с одновременной отгонкой хлористого метилена из реакционной смеси. По окончании прибавления раствора хинона реакционную массу выдерживают при этой температуре 1/5 -2 ч/ охлаждают до комнатной температуры и хроматографируют на колонке с силикагелем (хлороформ)/ собирая вторую фракцию.
Получают 7 г (47 % ) 2-(3′-бром-4′-метоксифенил)-3-карбэтокси-5-оксибензофурана в виде светлокремового кристаллического вещества/ растворимого в спирте/ эфире/ хлороформе/ нерастворимого в воде. Т.пл. 153-155°С (из водного спирта).
Найдено/ %: С 55/77; H 3,99; Br 20,28 C18H15BrO5
Вычислено/ %: С 55/26; H 3,86; Br 20,43
Стадия II. Получение целевого продукта - гидрохлорида 2-(3′-бром-4′-метоксифенил)-3-карбэтокси-4-диметил-аминометил-5-оксибензофур ана (I).
Раствор 3/9 г (0/01 моль) 2-(3′-бром-4′-метоксифенил)-3-карбэтокси-5-оксибензофурана/ 0/93 мл (0/01 моль) формамина и 0/82 г (0/01 моль) гидрохлорида диметиламина в 14 мл диметилформамида при перемешивании нагревают при 100° в течение 4 ч. Растворитель отгоняют и остаток обрабатывают 30 мл ацетона. Смесь выдерживают 24 ч. Выпавший осадок отделяют и промывают на фильтре 30 мл ацетона.
Получают 2/8 г (57/8 %) гидрохлорида 2-(3′-бром-4′- метоксифенил)-3-карбэтокси-4-диметиламинометил-5-оксибензофурана в виде кристаллического вещества белого цвета/ растворимого в воде/ спирте. Т.пл. 193-194°С (с разложением/ из смеси ацетон-метанол-эфир).
Найдено/ %: С 52/24; H 4,78; N 2,96 C21H23BrClNO5
Вычислено/ % : С 52/03; H 4,78; N 2,89 Стадия III. Изучение биологической активности.
Испытания биологической активности и токсичности соединения I проводят на белых мышах/ крысах и кроликах.
Токсичность при однократном внутрибрюшинном введении исследуют на белых мышах. ЛД50 определяют по Беренсу.
Местно-анастезирующую активность при поверхностном способе анестезии исследуют на роговице глаз кроликов по Ренье.
Спинномозговую анестезию изучают в опытах на белых крысах по методу Кучерука в модификации Степанюка.
Токсичность соединения I при однократном внутрибрюшинном введении в виде 1%-ного раствора по показателю ЛД50 составляет 131/25± 5/81 мг/кг.
Изучение местно-анестезирующего действия и токсичности соединения I проводят в сравнении с известным соединением Iа - гидрохлоридом 2- фенилтиометил-3-карбоэтокси-4-диметиламинометил-5-оксибензофурана/ структурным и фармокологическим аналогом соединения I иместно-анестезирующими препаратами: дикаином/ новокаином/ тримекаином и лидокаином.
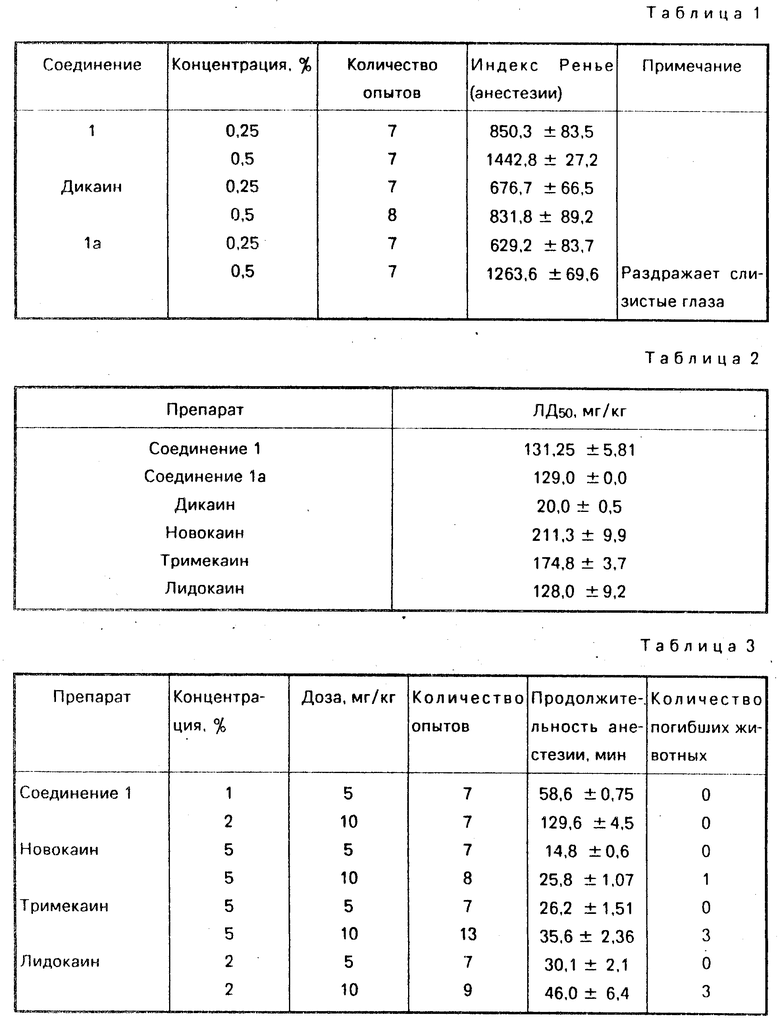
Соединение I обладает выраженной местно-анестезирующей активностью при поверхностном методе анестезии (см.табл.1).
Сравнительная активность соединения I/ дикаина и соединения Iа при поверхностной анестезии представлена в табл. 1.
Как видно из табл. 1 местно-анестезирующий эффект соединения I выше/ чем дикаина препарата/ широко применяющегося для поверхностной анестезии/ и в 6/5 раз менее токсичен/ чем дикаин (см.табл.2).
Сравнительная токсичность 1%-ных растворов соединений I/ Iа и местно-анестезирующих препаратов представлена в табл.2.
Соединение I и соединение Iа сопоставимы по местно-анестезирующему действию. Однако известное соединение Iа оказывает в 0/5%-ной концентрации раздражающее действие на слизистую облочку глаза.
При сравнительном изучении спиномозговой анестезии соединения I вышеуказанных препаратов и соединения Iа установлено/ что соединение I гораздо активнее препаратов сравнения (см.табл.3).
Сравнительная продолжительность действия соединения I/ новокаина/ тримекаина/ лидокаина при спинномозговой анестезии в опытах на крысах дана в табл.3.
Как видно из табл.3/ в дозе 5 мг/кг продолжительность болеутоляющего действия соединения I превышает продолжительность действия/ взятых в той дозе новокаина в 3/9 раза/ тримекаина - в 2/2 раза и лидокаина в 1/9 раза.
При увеличении дозы до 10 мг/кг соединение I превосходит продолжительность действия взятых также в дозе 10 мг/кг новокаина в 5 раз/ тримекаина - в 3/6 раза/ лидокаина - в 2/8 раза.
Соединение I в дозах 5 и 10 мг/кг не вызывает признаков отравления у животных. Препараты сравнения в дозе 10 мг/кг у части животных вызывают нарушение дыхания/ судороги и даже гибель отдельных особей.
Активность известного соединения Iа при спинномозговом методе местного обезболивания не исследуют/ так как оно в 0/5%-ной концентрации в опытах на роговице глаза кроликов оказывает раздражающее действие/ что является препятствием для введения соединения Iа в спинномозговой канал.
Таким образом/ соединение I при поверхностном методе обезболивания превосходит местно-анестезирующий эффект дикаина и менее токсично/ чем дикаин.
При поверхностной анестезии соединение I и соединение Iа сопоставимы по местно-анестезирующей активности/ но в отличие от последнего соединение I не оказывает раздражающего действия на слизистую оболочку глаза.
При спинномозговом способе обезболивания соединение I имеет существенные преимущества перед новокаином/ тримекаином и лидокаином как по продолжительности болеутоляющего действия/ так и по отсутствию токсического эффекта. Соединение Iа не может быть использовано пр спинномозговом способе обезболивания из-за раздражающего действия.
Таким образом соединение I обладает выраженным местно-анестезирующим действием при поверхностном и спинномозговом способах обезболивания/ превосходит действие как известных лекарственных препаратов/ так и аналога/ близкого по структуре и биологическим свойствам.
Изобретение относится к гетероциклическим соединениям, в частности к гидрохлориду 2-(3'- бром-4'- метоксифенил)- 3-карбэтокси-4- диметиламинометил- 5-оксибензофурана (ГХ), обладающему местноанестезирующим действием и может найти применение в медицине. Цель - получение более активных веществ указанного класса. Получение ГХ ведут взаимодействием 2-(3'-бром-4'- метоксифенил) -3-карбэтокси -5-оксибензофурана с формалином и гидрохлоридом диметиламина при нагревании (100°С) в диметилформамиде. Выход 57,8%. Т.пл. 193 - 194°С. Брутто формула C21H23BrCINO5 . Испытания показывают, что в дозе 5 мг/кг продолжительность болеутоляющего действия ГХ превышает действие новокаина (в той же дозе) в 3,9 раза, тримекаина - в 2,2 раза и лидокаина - 1,9 раза. 3 табл.
Гидрохлорид 2-(3'-бром-4'-метоксифенил) -3-карбэтокси-4-диметил-аминометил-5-оксибензофурана формулы
HO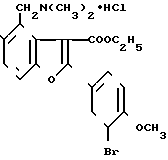
обладающий местноанестезирующим действием.
Авторы
Даты
1994-06-15—Публикация
1986-12-15—Подача