Настоящее изобретение относится к новым производным сС-пиперидинкарбоновых кислот, обладающим биологической :активностью, и промежуточным продуктам для их синтеза, которые могут. найти применение в йедицине и химико фармацевтической промышленности. Известно использование кокаина в качестве местного анестетика. Недостатком этого известного сред ства является его высокая токсичность;Известно применение новокаина в Качестве местного анестетика. Недостатки этого анестетика - его малая активность, кратковременность действия, способность вызывать аллер гические реакции. Известна применение тримекаина (гидрохлорнд мезидида диэтиламиноуксусной кислоты) в качестве местно-, анестезирующего средства. Тримекаин имеет недостаточную дпи тельность действия. Известны противоаритмические сред ства, такие как хинидин, новокаинамид (гидрохлорид R-диэтиламиноэтиламида п-аминобензойной кислоты), мар каин, лидокаин. Однако хинидин и маркаин обладают высокой токсичностью, новокаинамид сравнительно малоэффективен, лидокаин труднодоступен. Наиболее близким по структуре и биологическому действию к предложенным соединениям является пиромекаин (гидрохлор1щ мезидида N-бутилпирролидин-2-карбоновой кислоты), используемый в качестве местноанестезирующего средства. Пиромекаин имеет недостаточную длительность анестезирующего действия., Цель изобретения - новые произврд ные о4-пиперидинкарбоновой кислоты, обладающие более высокой длительностью местноанестезирующего и антиарит мического действия и большей широтой терапевтического действия, а также промежуточные продукты для синтеза этих новых производных ci-пиперидинкарбоновой кислоты. Поставленная цель достигается солями мезидидов (ki -пиперидинкарбоновых кислот общей формулы I у CHj HX R СНз н-бутил или изобутил; хлор или бром. обладающими местноанестезирующей, антиаритмической и антифибрилляторной активностью, и мезидидамиой-пиперидинкарбоновых кислот общей формулы II а j CONH где R - н-бутил или изобутил, в качестве проме.жуточных продуктов рдя синтеза солей мезидидов ci-пиперидинкарбоновых кислот. Способ получения соединений общей формулы I включает взаимодействие мезидидов с6-пиперидинкарбоновых кислот с водными или ацетоновыми растворами хлористоводородной или бромистоводородной кислоты и аналогичен известному способу. Промежуточные соединения общей формулы II получают циклизацией мезидидов oi ,СО-дигалогенкапроновых кислот при действии бутиламина или изобутиламина аналогично известной циклизации мезидидов ot ,М-дигалогенвалериановых кислот. Пример 1. Хлоргидрат мезидида N-бyтил-ci-пипepидинкapбoнoвoй кислоты (1а). 0,5 г мезидида Ы-бутил-о.-пиперидинкарбоновой кислоты растворяют при нагревании в водном растворе соляной кислоты (1 МП концентрированной соляной кислоты в 30 мл воды). К горячему раствору прибавляют .0,05 г активированного угля и смесь кипятят 5 мин. Уголь отфильтровывают. При охлаждении выпадает белый кристаллический осадок. Осадок отф шьтровывают, промывают водой и высушивают при . Выход 0,38 г (76,1%), т.пл. 248-250С (с разл.). Найдено, %: G 67,21j Н 9,13; N 8,46; С1 10,51. С, Н,, ClNgO. Вычислено, %: С 67,33; Н 9,22; N 8,27; С1 10,46. Пример 2. Хлоргидрат мезидида М-бутил-Л-пиперидинкарбоновой кислоты (1а) . К раствору 1,65 мл концентрированной соляной кислоты в 22 мл ацетона прибавляют раствор 3,25 г мезидида Н-бутил-()6-пипериди 1карбоновой кислоты в 26 мл ацетона и вьдерживают 2 ч.
51
Выпавший осадок отфильтровывают и высушивают при ЮОС. Выход 2,75 г (76,2%), т.пл. 248-250С (с разд.).
Пример 3. Бромгидрат мезидид& Ы-бутил-в4-пиперидинкар6оновой кислоты (16) .
0,5 г мезидида N-бутил-й- пиперидинкарбоновой кислоты растворяют при нагревании в водном растворе бромистоводородной кислоты (1 мл 40%-ной бромистоводородной кислоты в 20 мл воды), к горячему раствору прибавляют 0,05 г активированного угля и кипятят 5 мин. Уголь отфильтровывают. При охлаждении выпадает белый кристаллический осадок. Осадок отфильтровывают, промывают водой и высушивают при ЮОС. Выход 0,44 г (73,3%), г т.пл. 237-238С.
Найдено, %: С 59,50; Н 8,13; N 7,19; Вг 21,09.
С,Нэ, .
Вычислено, %: С 59,52; Н 8,15; N 7,30; Вг 20,84.
Пример 4. Хлоргидрат мезидида Ы-изобутил-о6-пиперидинкарбоновой кислоты (IB).
1 г мезидида Н-изобутил-о -пиперидинкарбоновойкислоты растворяют при нагревании в водном растворе соляной кислоты (4 мл концентрированной соляной кислоты и 65 мл воды). К горячему раствору добавляют 0,1 г активированного угля и смесь кипятят 5 мин. Уголь отфильтровывают, промывают водой и высушивают при 100°С. Выход 0,75 г (72%), т.пл. 244-245 0 (с разл,).
Найдено, %: С 67,49; Н 9,23; N 8,33; С1 10,32.
C qH ClNgO.
Вычислено, %: С 67,33; Н 9,22; N 8,27; С1 10,46.
Пример 5. Бромгидрат. мезидида Ы-изобутил-о -пиперидинкарбоновой кислоты (1г).
1 г мезидида Ы-изобутил-с6 Пиперидинкарбоновой кислоты растворяют при нагревании в водном растворе бромистоводородной кислоты (2 мл 40%-ной бромистоводородной кислоты в 50 мл воды), к горячему раствору прибавляют 0,1 г активированного угля и кипятят 5 мин. Уголь отфильтровывают.Приь
охлаждении выпадает белый кристаллический осадок. Осадок отфильтровывают, промывают водой и высушивают
06546
при 00°С. Выход 1 г (83,3%), т.пл 245-246 С (с разл.).
Найдено, %: С 59,08; И 5 N 7,38; Вг 20,99. С „HgtBrN G.
Вьмислено, %: С 59.,52; Н 8,15; N 7,30; Вг 20,84.
Пример 6. Мезидид N-бутил10 14-пиперидинк.арбоновой кислоты.
К 3,02 г (0,01 моль) мезидида ot ь)дихлоркапроновой кислоты прибавляют 10,95 г (0,15 моль) н-бутиламина.и реакционную смесь кипятят 5 ч. После 15 охлаждения реакционную массу вьтивают в 0,5 л воды и вьщерживают 1 сут. Кристаллическое вещество отфильтровывают, промыщ,ают водой, сушат и кристаллизуют из водного спирта. Выход 2,2 г (72,8%), т.пл. 96-98°С.
Найдено, %: С 75, Н 9,81; . N 9,24.
.
Вычислено, %: С 75,455 Н 10,00; 25 N 9,26.
Пример 7. Мезидид N-бутил с6-пипёридинкарбоновой кислоты.
К раствору 3,46, г (0,01 моль) ме30 зидида об-бром-О-хлоркапроновой кислоты в 50 МП абсолютного спирта прибавляют раствор 2,93 г (0,04 моль) нбутиламина в.25 мл абсолютного спир.та. Реакционную смесь кипятят 25 ч, JC охлаждают и выливают в 0,5 л холод- . ной воды. Выпавшее масло, при стоянии закристаллизовывается. ОсадокОтфильтровывают, промывают водой, сушат и перекристаллизовывают из 70%-ного 40 спирта. Выход 2,1 (69,5%), т. пл. 97-98 С.
П р и ме р 8. Мезидид N-бутилoL-пиперидинкарбоновой кислоты. 5 Смесь 1-3,84 г (0,04 моль) мезидида оС-бром-йЬхлоркапроновой кислоты и 50 мл н-бутиламина кипятят 5 ч. После .охлаждения к реакционной массе добав-. ляют 4,0 г (0,1 моль) мелко растер- , . 0 того едкого натра и отгоняют избыток бутиламина. К остатку при-, бавляют 50 мл воды и экстрагируют дихлорэтаном. Дихлорэтановый раствор промывают водой, упаривают. Остаток е перекристаллизовывают из 80%-ного спирта. Выход 6,5 г (54%), т.пл. 9798С, . .
Пример 9. Мезидид N-изобу- тш1-с4-пиперидинкарбоновоЙ кислоты.
Смесь 6,92 г (0,02 моль) мезидида е6-бром-М-хлоркапроновой кислоты и 25 мЛ изобутиламина кипятят 5 ч. Реакционную смесь охлаждают, прибавляют 2,8 г (0,05 моль) растертого едкого кали и отгоняют при слабом вакууме избыток изобутиламина. К остатку прибавляют 25 мл воды и экстрагируют дихлорэтаном. Дихлорэтанрвый раствор промывают водой и упаривают досуха. В остатке - .6 г маслообразного вещества, которое при стоянии закристаллизовывается. Выход 3,58 г (60%), т.пл. 101-102°С (из 80%-ного спирта).
Найдено, %: С 75,27; Н 10,10; N 9,31,
C gH5oN20.
Вычислено, %: С 75,15; Н 10,00; N 9,26.
Фармакологические исследования соединений 1а-1г проводили в сравнении с эталонными препаратами - новокаином, кокаином, тримекаином, лидокаин.ом, пиромекаином, хинидином, новoкaинa шдoм, маркаином, для чего использов,али следующие методики.
1. Поверхностная анестезия.
Изучение способности соединений вызывать поверхностную анестезию проводили на кроликах по методу Ренье. Определяли время наступления анестезии, ее глубину (вычисляли индекс Ренье) и длительность. Анестезирующее действие вещества в растворах каждой концентрации оценивали по результатам 8 опытов.
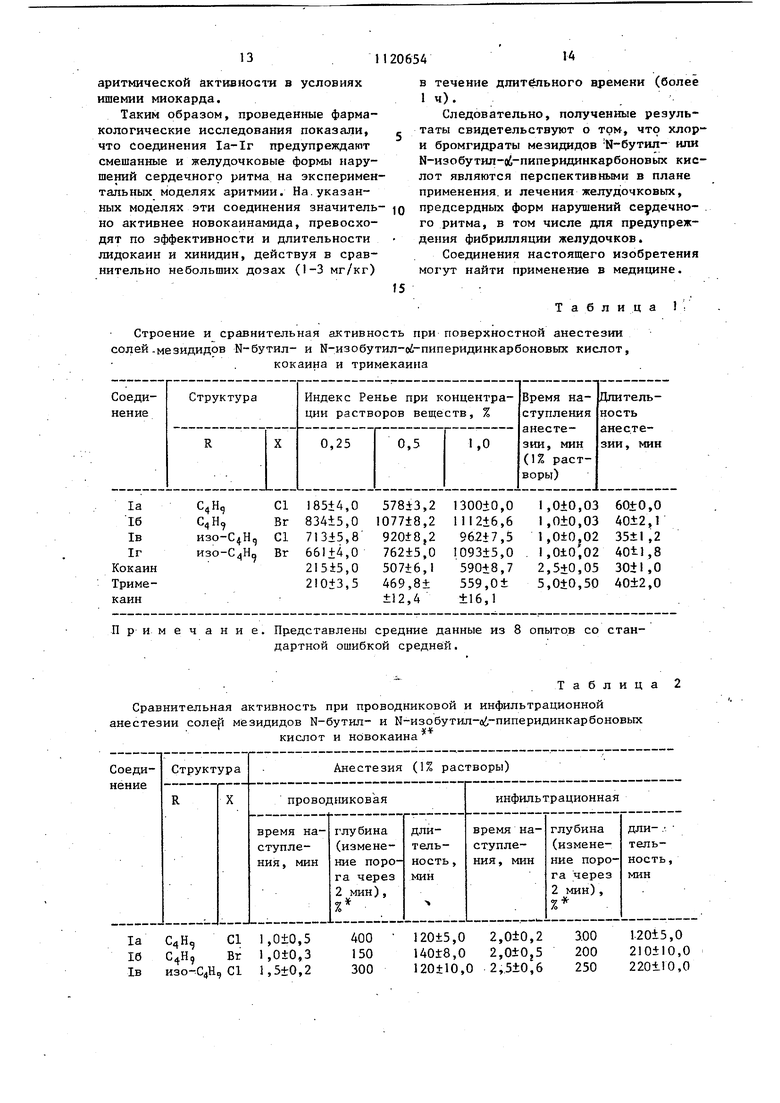
Целевые соединения la-Ir в растворах 0,25-1% концент)ации обладают активностью при поверхностной анестезии (табл. 1). Все вещества в растворах 0,5 и 1% концентрации превосходят по действию кокаин и тримекаин. Эта разница наиболее отчетливо выражена при сравнении целевых продуктов и эталонного препарата кокаина в растворах 1% концентраций. Наиболее активно соединение 1а (индекс Ренье 1300,0), которое превосходит в 2 раза кокаин и тримекаин. Время наступления поверхностной анестезии, вызванной целевыми соединениями (% растворы) - ,OiO,03 мин; эталонными препаратами: кокаином (1% раствор) 2,5±0,05 мин, тримекаином (% раствор) - 5,0±0,5 мин, т.е. при применении предлагаемых веществ анестезия наступает в 2,5-5 раз быстре.е. Дли- тельность действия, мин: соединения la 60, кокаина ЗО, тримекаина 40.
2. Проводниковая анестезия была исследована с помощью трех методов:
а)на лягушках путем воздействия раствора испытуемого препарата на обнаженгшй седалищный нерв (по Тюрку);
б)на зубах кроликов с помощью прибоQ ра злектроодонтотестера (ЭОТ-1) и в)
болевым методом. В качестве критериев активности использовали время наступления анестезии, ее глубину изменение порога электрического раз5 дражени-я и длительность обезболивания.
а) В опытах на лягушках (по. Тюрку) установлено, что целевые соединения имеют кшнимальную блокирующую нерв
0 концентрацию, равную 4,0-4,4 ммоль, т.е. такую же как новокаин и триме. каин, и несколько превосходят новокаин по времени наступления анестезии. Время наступления анестезии сое5 динений 1а 12,3±1,4 мин; 16 13,OJr ±0,8 мин; IB 14,0±1,0 мин; 1г 14,Of +0,9 мин; новокаина 14,0±0,3 мин; тримекаина 7,OtO,3 мин. Существенное различие с новокаином наблюдается
0 при определении длительности анестезирующего эффекта предлагаемых веществ: целевые соединения (1% растворы) действуют в течение 3 ч, т.е. как тримекаин, и в 3 раза длительнее,
чем новокаин.
б) В опытах на зубах кроликов целевые соединения в виде растворов 1% концентрации в дозе 4,3 мг/кг вызывают анестезию практически сразу (че0 рез 1,0-1,5 мин), на игле, новокаин - через 2 мин. Вещества 1а и 1в увеличивают порог электровозбудимости зуба кролика через 2 мин в 3-4 раза (т.е. с 20 до 60-80 В).; новокаин в
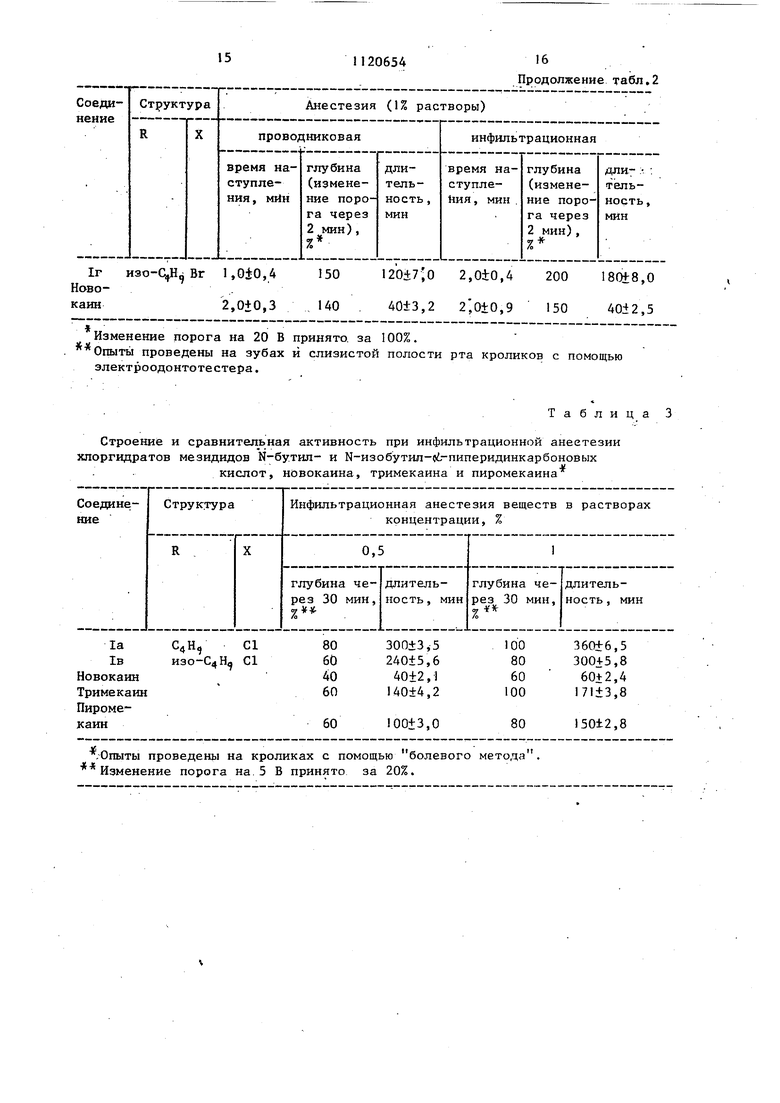
5 этих же условиях опыта - в 1,4 раза (т.е. с 20 до 28 В). Длительность действия целевых соединений (1% растворы) 120-140 мин, новокаина 40 мин, т.е. по длительности действия предлаQ гаемые. вещества превосходят новокаин в 3 раза (табл. 2).
в) При проводниковой анестезии в опытах на кроликах, проведенных болевым методом, предлагаемые соедине-
е ния 1% растворы) в дозе 5 мг/кг вызывают обезболивание через 5-6 мин, через 30 мин его глубина достигает 00%, длительность действия 7-9 ч, Пиромекаин (l% раствор) в дозе 5 мг/кг
вызывает анестезию через 12iO,5 мин, через 30 мин ее глубина з остигает 100%, длительность действия 3-3,5 ч, т.е. по длительности действия предлагаемые вещества превосходят пиромекаин в 2 раза.
3. Инфильтрационная анестезия была исследована на зубах кроликов с помощью прибора электроодонтотестеpa (ЭОТ-1) и болевым методом. В качестве критериев использовали время наступления ан1встезии, ев;глубину (изменение порога электрического раздражения) и длительность анестезии.
а)В опытах аА зубах кроликов найдено, что целевые соединения (1 % растворы) в дозе 4,5 мг/кг вызывают анестезию через 2-2,5 мин, новокаин через 2-3 мин. В э.той же дозе вещестза значительно, в 2,5-3 раза, повышают порог злектровозбудимости зуба
и действуют при этом длительно - 23,5 ч. Эталонный препарат новокаин в дозе 4,5 мг/кг вызывает повышение порога в 1,5 раза и действует всего в течение 40±2,5 мин (табл. 2).
б)В опытах на кроликах, проведенных при помощи болевого метода, установлено, что целевые соединения (1% растворы) в дозе 5 мг/кг вызывают анестезию сразу, через.30 мин ее глубина достигает 80-100%, длительность .действия 5-6 ч. Соединения 1а
и IB (0,5% растворы) в дозе 3 и 5 мг/кг вызывают анестезию через 35 .мин, глубина ее .через 30 мин достигает 60-80% и остается неизменной в течение 4-5 ч. Новокаин в этих же условиях опыта при введении в виде 0,5% раствора в дозе 5 мг/кг вызывает анестезию через 10 мин, глубина ее через 30 мин достигает 40%, длительность анестезирующего эффекта 4050 мин; тримекаин (0,5% раствор) вызы.вает анестезию практически сразу (на игле), глубина ее через 30 мин равна 60%, длительность действия . . 140 мин; пиромекаин (1% раствор) в , дозе 5 мг/кг вызывает анестезию через 15+0,9 мин, через 30 мин ее глубина достигает 80%, длительность дейстия 120-150 мин (табл. 3).
Таким образом, соединения la-Ir особенно 1а и 1в, обладают выраженной местноанестезирующей активностью при поверхностной, проводниковой и инфильтрационной анестезии, выгодно отличаясь от эталонных препаратов новокаина и кокаина быстротой наступления, глубиной и длительнос.тью действия; соединения 1а и 1в действуют в два раза длительнее тримекаика. Они относительно малотоксичны и превосходят кокаин и новокаин по широте терапевтического эффекта.
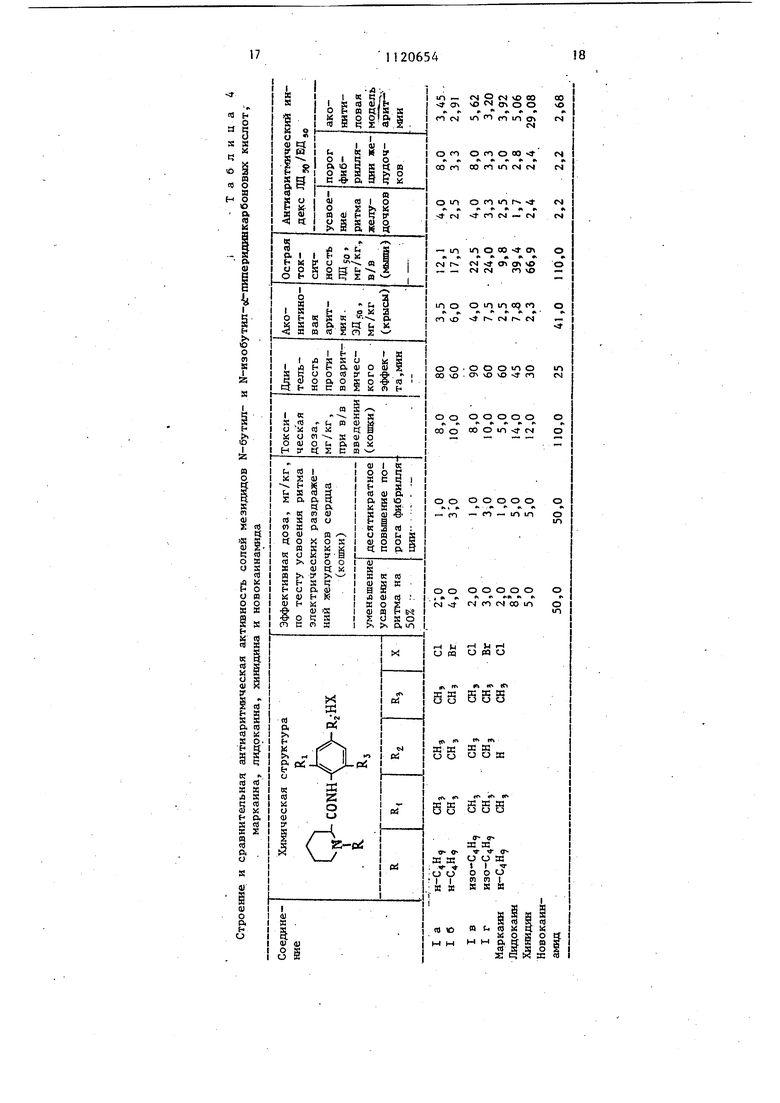
При изучении антиаритничес1;ой и антифибрилляторной активности в качестве эталонов использовали лидокаия, новокаинамид, хинидин и маркаин.
Фармакологическое исследование указанных соединений проводили иа следующих эксперимеитапьных моделях нарушений сердечного ритма; аконитинов ая модель аритмии; усвоение ритма при электрическом раздражении желудочков сердца; влияние иа порог электрической фибрилляции. Эти исследования позволили судить о противоаритмической и противофибрилляторной активности полученных соединений.
1. Смешанную форму нарушений сердечно г.о ритма, вызванных аконитином, изучали на бодрствующих крысах массой г. Аконитин вводили внутривенно (в/в) в дозе 40 мкг/кг, при этом возникали нарушения ритма смешанного характера, заканчиваю.щиеся фибрилляцией. Целевые соединения 1а1г в различных дозах вводили внухривенно за 1-3 мин до введения аконитина.
Соединения 1а-1г в дозах 3-8 мг/кг полностью купируют аритмию, вызванную аконитином.
Соединения 1а и 1в уступают в активности хийидину, но почти в 2 раза активнее лидокаина ив 12 раз - новокаинамида. Целевые .соединения обладают более длительным антиаритмическим эффектом, чем хинидин, лидокаин и нр- вокаинамид соответственно .в 3; 2 и 3,5 раза (табл. 4).
Соединения 16 и 1г в тех же дозах, что и лидокаин, предупреждают аконитиновые аритмии, но в 2 и 3 раза соответственно уступают хинидину и в 57 раз активнее новокаинамида. По длительности эффекта соединения 16 и 1г в 2 раза превосходят хинидин и лидокаин ив 2,5 раза - новокаинамид (табл. 4).
Таким образом, соединения 1а и 1в по эффективности близки к хинидину,. несколько активнее лидокаина и значительно эффективнее новокаинамида.
Соединения 16 и Ir уступают по антиаритмической активности хинидину, равноценны лидокаину и существенно активнее новокаинамида. Важным преимуществом целевых соединений по сравнению с эталонными препаратами является их более продолжительное антиаритмнческое действие.
2.Эффективность соединений 1а-1г на модели желудочковых форм аритмии сравнивали с действием эталонных препаратов . В опытах на кошках массой 3-4 кг, анестезированных нембуталом (35 мг/кг), в условиях вскрытой грудной клетки и искусственного дыхания нарушения ритма создавали электрическим раздражением желудочков сердца различной частотой, превышающей исходный ритм сердца. Через подшитые к правому или левому желудочкам биполярные электроды электрическим раздражением создавали эктопический очаг возбуждения.
Соединения 1а-1г в дозах 1 мг/кг уменьшают максимально воспроизводимую частоту навязанных возбуждений желудочков за счет увеличения эффективного рефрактерного периода. По данному тесту соединения 1а, 1в эффективнее эталонных препаратов: лидокаина - в 4 раза, хинидина - в 2,5 раза, а новокаинамида - в 25 раз.
Соединения 16 и 1г несколько активнее хинидина и превосходят по активности лидокаин в 2 раза, а новокаинамид в 10 - 15 раз.
По длительности антиаритмического эффекта целевые соединения превосходили эталонные препараты (табл. 4).
Полученные данные об уменьшении, под влиянием соединений максимально воспроизводимой частоты свидетельствуют о выраженных антиаритмических свойствах этих соединений в отно.шении желудочковых форм нарушений сердечного ритма.
3.Влияние соединений 1а-1г на порог электрической фибрилляции желудочков . В опытах на кошках создавали эктопический очаг возбуждения в желудочках миокарда в условиях, описанных в п.2 (см. выше). Порог фибрилляции желудочков определяли сканированием уязвимого периода серией из
90 прямоугольных импульсов длительностью 4 мс и следующих с частотой 50 Гц. За -порог электрической фибрилляции желудочков принимали минимальную интенсивность раздражения (ток в мА), которая вызывала фибрилляцию
желудочков.
Соединения 1а и 1в дозах 1-3 мг/кг вызывают резкое повышение порога фибрилляции желудочков в течение 6090 мин. Эти вещества в первые 1520 мин увеличивают порог фибрилляции более чем в 10 раз, превосходя значительно эталонные препараты не только по длительности, но и силе антифибрилляторного эффекта (табл. 4).
Соединения 16 и 1г также вызывают мощное и длительное повышение порога фибрилляции желудочков, превосходя по длительности эффекта лидокаин, хини0 дин и новокаинамид в 1,5-2 раза.
4.Для сравнительной оценки антиаритмической активности целевых соединений 1а-1г и эталонных препаратов вычисляли антиаритмический индекс,
5 являющийся отношением ОД g к Щ оДля модели аконитиновой аритмии ДЦ „ вычисляли по данньм острой токсичности. Результаты, представленные в табл. 4, свидетельствуют о большей
0 терапевтической широте целевьпс соединений 1а-1г по сравнению с эталонными препаратами (их антиаритмические шздексы в основном выше, чем у лидокаина, хинидина и новокаинамида).
5 Лишь на модели смешанной формы наруШЕ Ний сердечного ритма, вызванных аконитином, антиаритмические индексы целевых соединчзний несколько уступают таковому хинидина, но превосходят
0 антиаритмические индексы лидокаина и новокаинамида,
5.С целью выяснения электрофизнологического механизма действия целе5 вых соединений 1а-1г изучали их влияние на трансмембранные ионные токи миокардиальных клеток трабекулы предсердия лягушки в условиях двойного сахарозного мостика методом фиксации
Q потенциала. Целевые соединения 1а-1г вызывают подавление быстрого входящего, блокируемого тетродотоксином, натриевого тока, следовательно, могут быть отнесены к I-и группе- антиарит- мических веществ с хинидино-подобным эффектом. Их более выраженное влияние на быстрый входящий натриевый ток в деполяризованных волокнах может свидетельствовать об их высокой антиаритмической активности в условиях ишемии миокарда.
Таким образом, проведенные фармакологические исследования показали, что соединения 1а-1г предупретвдают смешанные и желудочковые формы нарушений сердечного ритма на экспериментальных моделях аритмии. На.указанных моделях эти соединения значительно активнее новокаинамида, превосходят по эффективности и длительности лидокаин и хинидин, действуя в сравнительно небольших дозах (1-3 мг/кг)
Строение и сравнительная активность при поверхностной анестезии солей.мезидидов N-бутил- и N-изoбyтил-oi-пипepидинкapбoнoвыx кислот,
кокаина и тримекаина
в течение длительного времени (более 1 ч).
Следовательно, полученные результаты свидетельствуют о том, что хлори бромгидраты мезидидов Ы-бутил- или Ы-изобутил-ой-пиперидинкарбоновых кислот являются перспективными в плане применения, и лечения желудочковых, предсердных форм нарушений сердечного ритма, в том числе для предупреждения фибрилляции желудочков.
Соединения настоящего изобретения могут найти применение в медицине.
Таблица 1





| название | год | авторы | номер документа |
|---|---|---|---|
| Гидрохлорид мезидида N-(5-оксиадамантил-2)- @ -пирролидинкарбоновой кислоты, обладающий местно-анестезирующей активностью | 1985 |
|
SU1336499A1 |
| ПРОИЗВОДНЫЕ БЕНЗИЛАМИДА 4-ОКСИМАСЛЯНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЕ МЕСТНО-АНЕСТЕЗИРУЮЩУЮ, АНТИАРИТМИЧЕСКУЮ, АНТИАНГИАЛЬНУЮ И АНТИНЕКРОТИЧЕСКУЮ АКТИВНОСТЬ | 1988 |
|
SU1601984A1 |
| Хлоргидраты ариламидов @ -гексаметилениминокарбоновых кислот, обладающие местоанестезирующей активностью, и ариламиды @ -гексаметилениминокарбоновых кислот в качестве промежуточных соединений для их синтеза | 1987 |
|
SU1528773A1 |
| БРОМИСТОВОДОРОДНАЯ СОЛЬ 4-ОКСИ-3[N-(ФЕНАЦИЛ)БЕНЗИЛАМИНО- N - БЕНЗИЛБУТАНАМИДА, ПРОЯВЛЯЮЩАЯ МЕСТНО-АНЕСТЕЗИРУЮЩУЮ АКТИВНОСТЬ | 1989 |
|
SU1713242A1 |
| АНТИАРИТМИЧЕСКОЕ СРЕДСТВО | 1983 |
|
RU2068261C1 |
| ДИЦИКЛОГЕКСИЛАМИДЫ N-ЗАМЕЩЕННЫХ α-АМИНОКАРБОНОВЫХ КИСЛОТ, ОБЛАДАЮЩИЕ АНТИАРИТМИЧЕСКОЙ И АНТИФИБРИЛЛЯТОРНОЙ АКТИВНОСТЬЮ | 1994 |
|
RU2114821C1 |
| АРИЛАЛИФАТИЧЕСКИЕ АМИНОАМИДЫ БЕНЗОЙНОЙ (ЗАМЕЩЕННОЙ БЕНЗОЙНОЙ), ЦИКЛОГЕКСАН- И 1-АДАМАНТАНКАРБОНОВЫХ КИСЛОТ, ОБЛАДАЮЩИЕ АНТИАРИТМИЧЕСКОЙ, МЕСТНОАНЕСТЕЗИРУЮЩЕЙ И АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 1996 |
|
RU2130922C1 |
| ДИГИДРОХЛОРИД 1-ДИЭТИЛАМИНОПРОПИЛ-2-ФЕНИЛИМИДАЗО[1,2-А]БЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЙ МЕСТНОАНЕСТЕЗИРУЮЩИМ ДЕЙСТВИЕМ | 1999 |
|
RU2148057C1 |
| ПРОИЗВОДНЫЕ 2-МЕРКАПТОБЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЕ ПРОТИВОИШЕМИЧЕСКОЙ, АНТИАРИТМИЧЕСКОЙ И ПРОТИВОФИБРИЛЛЯТОРНОЙ АКТИВНОСТЬЮ | 1995 |
|
RU2136667C1 |
| КОМПОЗИЦИЯ АМИНОКИСЛОТ С МИКРОЭЛЕМЕНТАМИ, ОБЛАДАЮЩАЯ ПРОТИВОАРИТМИЧЕСКОЙ АКТИВНОСТЬЮ | 1999 |
|
RU2173553C2 |
1. Соли .мезидидов -пиперидинкарбоновых кислот общей формулы а СН,- НХ CONH -N I R где R - н-бутил или изобутил; X - хлор или бром, обладающие местноанестезирующей, антиаритмической и антифибрилляторной активностью. 2. Мезидиды о(.-пиперидинкарбоновых кислот общей формулы CL К) CONH ®) R з СП где R - н-бутил или изобутил, 4 в качестве промежуточных продуктов для синтеза солей мезидидов о6-пиперидинкарбоновых кислот. 
Примечание.
Сравнительная активность при проводниковой и инфильтрационной анестезии соле|1 мезидидов N-бутил- и Ы-изобутил-а -пиперидинкарбоновых
кислот и новокаина
. Т а б л и ц а 2 Представлены средние данные из 8 опытов со стандартной ошибкой средней. 1г изо-О Вг I,OiO,4150 Ново-. 120i7;o 2,0±0,4 200 180t8,0
| Машковский М.Д | |||
| Лекарственные средства | |||
| - М.: Медицина, 1978, ч | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Видоизменение прибора с двумя приемами для рассматривания проекционные увеличенных и удаленных от зрителя стереограмм | 1919 |
|
SU28A1 |
| Там же, с | |||
| РЕЛЬСОВАЯ ПЕДАЛЬ | 1920 |
|
SU289A1 |
| Там же, с | |||
| УСТРОЙСТВО ПАРОПЕРЕГРЕВАТЕЛЯ | 1920 |
|
SU295A1 |
| Там же, с | |||
| Разборное колесо | 1921 |
|
SU370A1 |
| Там же, с | |||
| Электромагнитный счетчик электрических замыканий | 1921 |
|
SU372A1 |
| Chapin.J.C | |||
| et al | |||
| Lidocaine, Bupivacaine, Etidocaine and Epinephrine - induced Arryhythmias during Halothane anesthesia in Dogs - Anesthesiology, 1980, V | |||
| Устройство для устранения мешающего действия зажигательной электрической системы двигателей внутреннего сгорания на радиоприем | 1922 |
|
SU52A1 |
| Прибор для равномерного смешения зерна и одновременного отбирания нескольких одинаковых по объему проб | 1921 |
|
SU23A1 |
| Машковский М.Д | |||
| Лекарственные средства..- М., Медицина | |||
| Чугунный экономайзер с вертикально-расположенными трубами с поперечными ребрами | 1911 |
|
SU1978A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| РЕЛЬСОВАЯ ПЕДАЛЬ | 1920 |
|
SU290A1 |
| 0 |
|
SU202955A1 | |
Авторы
Даты
1990-06-23—Публикация
1983-01-27—Подача