Изобретение относится к биотехнологии,-в частности к микробиологической промышленности, и может быть использовано в производстве высокоактивных ферментных препаратов для приготовления лекарственных средств.
Наиболее близким к предлагаемому по технической сущности и достигаемому результату является способ, в котором продуцент гиалуронидазы - штамм Streptomyces actinocidus 77 - выращивали глубинным способом, культуральную жидкость концентрировали вакуум-выпариванием при 40- 60°С и рН 7,5-8,5, фермент выделяли осаждением из культуральной жидкости 3-4 объемами этилового спирта. В результате получали препарат гиалуронидазы с активностью 450-800 МЕ/г (колоримерический метод) и удельной активностью 7-10 МЕ/мг белка.
Недостатками данного технического ре-
шения являются низкая активность и степень чистоты гиалуронидазы.
Цель изобретения - повышение активности и степени чистоты гиалуронидазы.
Штамм Streptomyces actinocidus 77 выращивают глубинным способом на питательной среде определенного состава, фильтрат культуральной жидкости подкисляют 2N соляной кислотой до рН 4,4-4,6, осветляют центрифугированием или фильтрацией и сорбируют на карбоксильном катионите КМ-2п (40-60 объемов на объем сорбента) со скоростью 50-100 мл/ч/см2, сорбент промывают 0,01 М ацетатным буфером рН 4,4-4,6, гиалуронидазу десорбируют щелочными растворами, затем элюат обесцвечивают активированным углем в концентрации 1,0-1,5% при перемешивании и уголь отделяют. Десорбцию можно провоXJ Ю СО
ю
дить либо в статических условиях при рН 8,5-8,7, либо в динамике растворами щелочи, аммиака или раствором фосфорнокислого натрия двузамещенного.
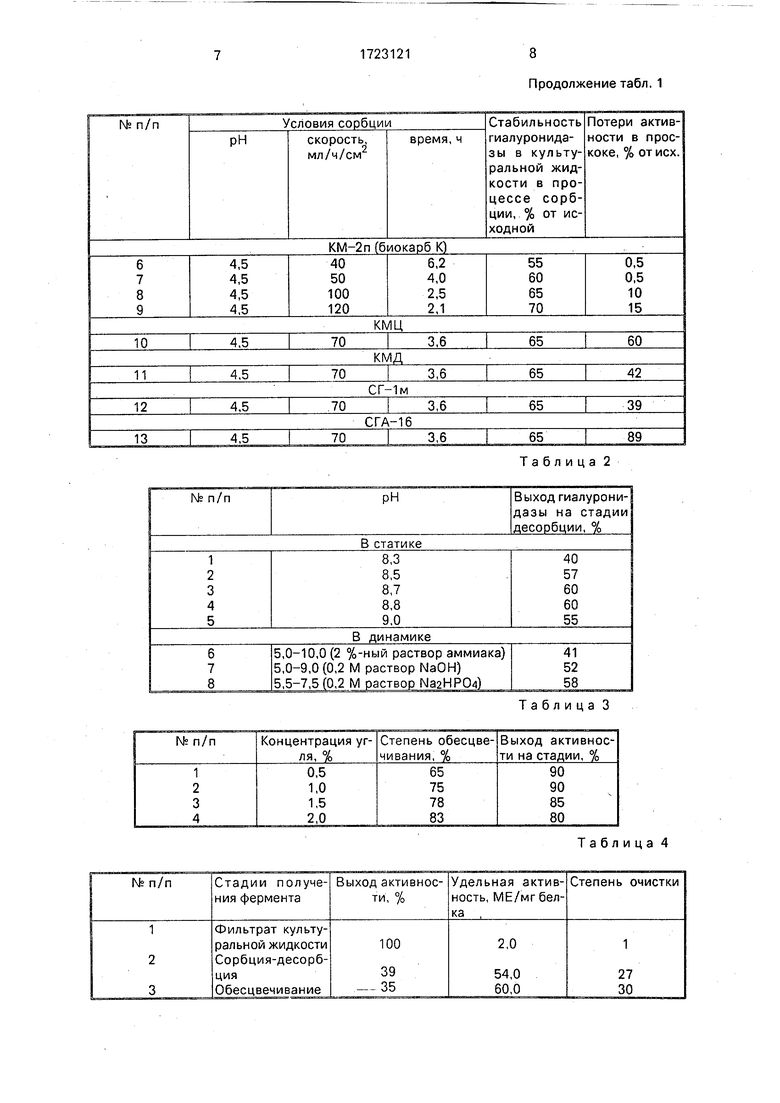
В табл, 1 представлены данные по подбору условий сорбции гиалуронидазы из 1 л фильтрата культуральной жидкости на колонке с карбоксильным катионитом Ш-2п объемом 20 мл (Ф 1,1 см, I 5 см). Для сравнения приведены данные по сорбции гиалуронидазы на колонке тех же размеров с карбоксиметилцеллюлозой (КМЦ) и некоторых других карбоксильных катионитах.
Из табл. 1 следует, что из пяти испытанных карбоксильных катионитов только КМ- 2п практически полностью сорбировал гиалуронидазу. Сорбцию фильтрата культуральной жидкости на катионите необходимо проводить в интервале рН 4,4-4,6, при этом на стадии подкисления гиалуронидаз- ная активность сохраняется на 60-70%, при снижении рН до 4,2 гиалуронидаза инакти- вируется сильнее и активность сохраняется лишь на 50%. При увеличении рН до 4,8 количество фермента в проскоке достигает 15%, что уменьшает выход фермента.
Важное значение имеет скорость сорбции фильтрата культуральной жидкости на катионите. Оптимальным является интервал 50-100 мл/ч/см . При уменьшении скорости ферментный раствор при кислых значениях рН (4,5) длительное время сорбируется на колонку, что приводит к снижению стабильности гиалуронидазы. В результате увеличения скорости сорбции пропорционально повышается выход фермента в проскоке и соответственно снижается количество гиалуронидазы в элюате.
Гиалуронидазу десорбируют различными щелочными растворами в статических условиях в воду путем сдвига рН или в динамических условиях путем пропускания различных элюентов через колонку с сорбентом.
Данные по подбору условий десорбции приведены в табл. 2 (сорбцию фермента проводили в оптимальных условиях; рН 4,5, скорость 70 мл/ч/см ).
Из табл. 2 следует, что десорбцию гиалуронидазы в статических условиях необходимо проводить при рН выше 8,5, при этом выход на стадии составлял 55-60%. Увеличение рН выше 8,8 приводило к элюции большого количества балластных белков, что вызывало уменьшение удельной активности в конечных препаратах (см. табл. 5).
В табл. 3 приведены экспериментальные данные по подбору условий обесцвечивания растворов гиалуронидазы активированным углем.
Результаты опытов свидетельствуют о том, что при концентрации угля 1,0-1,5% происходит обесцвечивание раствора гиалуронидазы на 75-78% при сохранении активности на стадии до 85-90%. При снижении концентрации угля в растворе остается значительное количество пигментов, что отрицательно влияет на качество препаратов. Увеличение концентрации угля до
0 2,0% приводит к снижению выхода гиалуронидазы на стадии обесцвечивания.
Схема получения гиалуронидазы по предлагаемому способу представлена в табл. 4.
5 Как видно из табл. 4, предлагаемая схема позволяет получить гиалуронидазу высокой степени очистки с удельной активностью 60 МЕ/мг белка и общим выходом фермента 35%,
0 Пример (по прототипу). Продуцент гиалуронидазы Streptomyces actinocidus 77 выращивали в ферментере емкостью 250 л (заполнение 180 л) на среде, содержащей 3% гидролизата БВК, 0,8% сульфата аммо5 ния, 0,1 % «аНРСм. Аэрация в процессе культивирования дробная: первые 12 ч роста - 9 м /ч, затем до конца культивирования 27 м /ч, рН в начале культивирования 6,8, время выращивания 56 ч. По окончании
0 выращивания мицелий отделяют центрифугированием, фильтрат культуральной жидкости (150 л) упаривали в 10 раз. К концентрату добавляли 4 объема охлажденного этилового спирта, осадок отделяли на
5 нутч-фильтре и лиофилизировали. Получали препарат гиалуронидазы с активностью 450 МЕ/г и удельной активностью 8 МЕ/мг белка.
П р и м е р 1. Продуцент гиалуронидазы
0 выращивали на той же питательной среде, в теж же условиях, что и в примере по прототипу, мицелий отделяли центрифугированием. Получали 150 л фильтрата культуральной жидкости с активностью 13 МЕ/мл и удель5 ной активностью 2,0 МЕ/мг белка. Фильтрат подкисляли 2N соляной кислотой до рН 4,5 и сорбировали на колонку (d 12 см, I 28 см) с 3,0 л карбоксильного катионита КМ- 2п кислотного гидролиза (биокарб К), урав0 повешенного 0,01 М ацетатным буфером рН 4,5. Скорость сорбции - 70 мл/ч/см2, время сорбции 19 ч. Катионит после сорбции переносили в емкость с мешалкой, дважды (по 3 л) отмывали 0,01 М ацетатным буфером рН
5 4,5. Гиалуронидазу десорбировали с катионита в статических условиях 7,5 л дистиллированной воды путем доведения рН до значения 8,7 раствором 2 М едкого натрия. Перемешивали смесь 15 мин, элюат отфильтровывали через капроновую ткань, затем
проводили повторную десорбцию фермента в тех же условиях. Элюаты объединяли. Выход активности на стадии сорбции-десорбции составил 39%, активность 55 МЕ/млчК 15л элюата добавляли 150 гактивированно- го угля марки Б и перемешивали 30 мин. Уголь отделяли центрифугированием при 5000 об/мин 30 мин. Ферментный раствор упаривали под вакуумом при 30°С до активности в растворе 130 МЕ/мл. Получили 3,5 л раствора, общий выход на стадии 92%. Удельная активность 60 МЕ/мг белка, общий выход на схеме 39%, степень очистки 30 раз.
П р и м е р 2. Стадии получения и очист- ки гиалуронидазы до стадии десорбции проводили аналогично примеру 1. Десорбцию с катионита проводили непосредственно на колонке в динамических условиях, используя 0,2 М раствор N32HP04. Элюирование производили со скоростью 14 мл/ч/см2. Фракции с гиалуронидазой объединяли. Объем элюата - 30 л, рН -7,5. Выход активности на стадии сорбции - десорбции составил 38%. Активность 28 МЕ/мл. К 30 л элюата добавили 360 г активированного угля, перемешивали 30 мин и уголь отделяли. Ферментный раствор обессоливали и концентрировали ультрафильтрацией. Объем полученного концентрата 5,2 л, активность 131 МЕ/мл. Удельная активность 70 МЕ/мг белка, общий выход 34%, степень очистки 35.
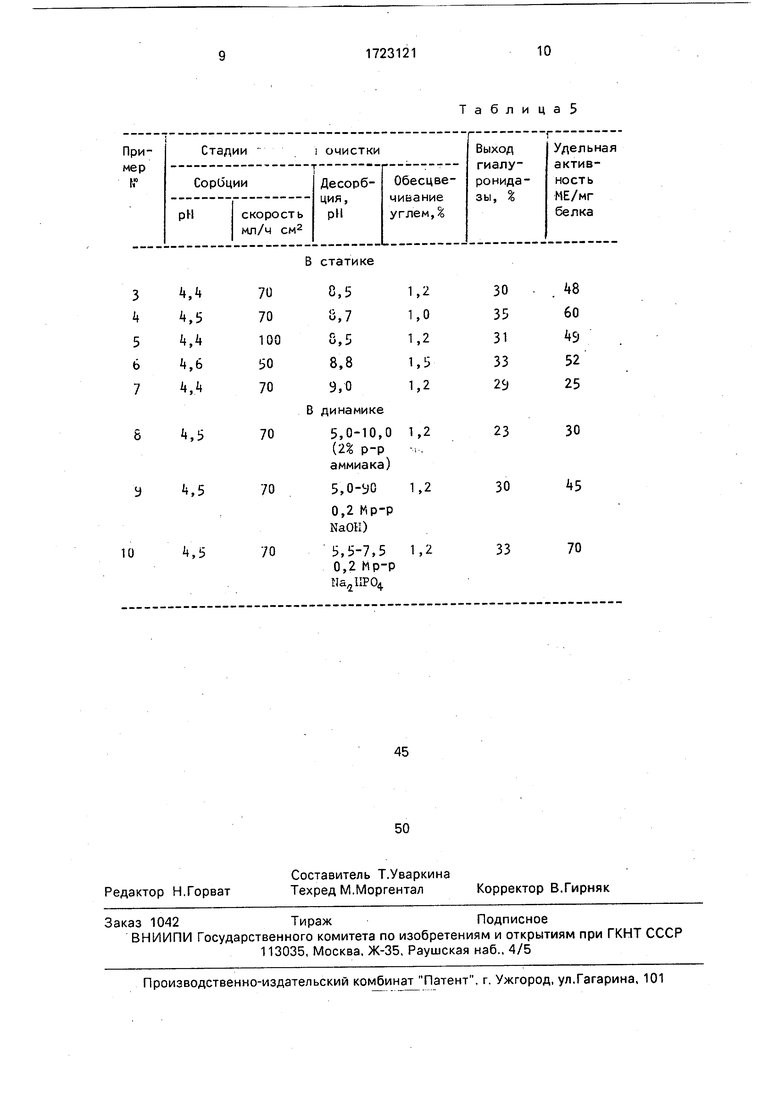
Примеры 3-10. Продуцент гиалуронидазы выращивали как в примере 1, мице- лий отделяли центрифугированием. Условия сорбции и десорбции представлены в табл. 5.
Из табл. 5 следует, что десорбцию гиалуронидазы в статических условиях необхо- димо проводить при рН 8,5-8,8, при этом
выход фермента составляет 31-35%, а удельная активность достигается 49-60 МЕ/мг белка (примеры 4-6). Увеличение рН при десорбции больше 9,0 приводит к значительному снижению удельной активности в препарате. Наилучшие результаты по десорбции гиалуронидазы в динамике получены при использовании 0,2 М раствора форсфорнокислого натрия двузамещенно- го, при этом удельная активность достигает 70 МЕ/мг белка (пример 10). Таким образом, предлагаемый способ позволяет получать фермент с высокой степенью очистки. По сравнению с примером-прототипом удельная активность гиалуронидазы выше в 7-9 раз (примеры 4, 10).
Формула изобретения
1.Способ получения гиалуронидазы. предусматривающий глубинное выращивание продуцента Streptomyces actinocidus 77, отделение мицелия, выделение фермента из полученной культуральной жидкости и очистку, отличающийся тем, что, с целью повышения активности и степени чистоты гиалуронидазы, культуральную жидкость подкисляют до рН 4,4-4,6, а очистку фермента ведут сорбцией через колонку с карбоксильным катионитом КМ-2п кислотного гидролиза со скоростью 50-100 мл/ч/см и десорбцией с катионита щелочными растворами, полученный элюат обесцвечивают активированным углем в концентрации 1,0-1,5% при перемешивании.
2.Способ по п.1, о т л и ч а ю щ и и с я тем, что фермент десорбируют с катионита в статических условиях при рН 8,5-8,8.
3.Способ по п.1,отличающийся тем, что фермент десорбируют промыванием катионита в колонке 0,2 М N32HP04.


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ БАКТЕРИАЛЬНОГО ВНЕКЛЕТОЧНОГО ЛЕКТИНА | 1991 |
|
RU2027763C1 |
| ШТАММ STREPTOMYCES GRISEOCARNEUS SUBSP. BLEOMYCINI ВКПМ-S1086 - ПРОДУЦЕНТ БЛЕОМИЦЕТИНА И СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА БЛЕОМИЦЕТИНА | 2007 |
|
RU2358008C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЦЕЛЛОБИАЗ | 1984 |
|
SU1274297A1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНЕЙ СОЕДИНИТЕЛЬНОЙ ТКАНИ | 1992 |
|
RU2005488C1 |
| ШТАММ AMYCOLATOPSIS ORIENTALIS SUBSP. EREMOMYCINI ВКПМ-S892 - ПРОДУЦЕНТ АНТИБИОТИКА ЭРЕМОМИЦИНА И СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА ЭРЕМОМИЦИНА | 1997 |
|
RU2110578C1 |
| Способ получения ферментного препарата @ -галактозидазы | 1979 |
|
SU891776A1 |
| ШТАММ STREPTOALLOTEICHUS CREMEUS SUBSP. TOBRAMYCINI ВКПМ S-1084 - ПРОДУЦЕНТ АПРАМИЦИНА И СПОСОБ ПОЛУЧЕНИЯ АПРАМИЦИНА | 2007 |
|
RU2392311C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТИЛОЗИНА | 1993 |
|
RU2108392C1 |
| Способвыделения фермента тромболитического действия | 1975 |
|
SU584034A1 |
| СПОСОБ ПОЛУЧЕНИЯ РИСТОМИЦИНА Д | 1970 |
|
SU268596A1 |
Изобретение относится к биотехнологии, в частности к микробиологической промышленности, и может быть использовано в производстве высокоактивных ферментных препаратов для приготовления лекарст- венных средств. Цель изобретения - повышение активности и степени чистоты гиалуронидазы. Способ заключается в том, что штамм Streptomyces actinocidus 77 выращивают глубинным способом, фильтрат культуральной жидкости подкисляют до рН 4,4-4,6, осветляют и сорбируют на карбоксильном катионите КМ-2п. Сорбент промывают и гиалуронидазу десорбируют щелочными растворами, затем элюат обесцвечивают активированным углем при перемешивании и уголь отделяют. Удельная активность продукта 60 МЕ/мг, степень очистки 30. 2 з.п. ф-лы, 5.табл.
Таблица 1
Продолжение табл. 1
Таблица 2
Таблица 3
Таблица 4
Таблица5
| Авторское свидетельство СССР № 974816, кл | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
1992-03-30—Публикация
1990-01-19—Подача