Изобретение относится к медицинской промышленности, и касается нового штамма-продуцента антибактериального антибиотика эремомицина, из группы полициклических гликопептидов (далбагептидов) и способа получения эремомицина сульфата.
Антибактериальный антибиотик эремомицин (в зарубежных фармакопеях не описан) является представителем группы антибиотиков-гликопептидов, к которой относится применяемый в медицинской практике антибиотик ванкомицин (Vancocin. HCI, USA). Антибиотики гликопептидной группы эффективны при лечении заболеваний, вызванных различными стафилококками, включая метициллинрезистентные штаммы, а также при лечении псевдомембранозного колита, возбудителем которого является анаэроб Clostridium difficile. Эремомицин превосходит ванкомицин по антибактериальной активности: его химиотерапевтическая эффективность в 2-4 раза выше чем у ванкомицина: он в 3,5 раз менее токсичен чем ванкомицин, и в отличие от ванкомицина эремомицин не обладает местно раздражающим действием и поэтому может вводиться не только внутривенно, но к внутримышечно.
Известен штамм Nocardia orientalis (ИНА-238) продуцент антибиотика эремомицина [1]. Недостатком данного штамма является низкий уровень содержания антибиотика в культуральной жидкости (не более 150 мг эремомицина на 1 л культуральной жидкости).
Сущность изобретения состоит в том, что получен новый штамм- продуцент эремомицина в результате многоступенчатого мутагенного воздействия этиленимина, нитрозоэтилбиурета, метилнитрозогуанидина, гамма лучей60 на исходный штамм N 238 с последующим отбором мутантов на средах, содержащих стрептомицин и ванкомицин в качестве селективных агентов.
Полученный новый штамм депонирован в коллекции культур НИИгенетика под номером ВКМП-S892.
Штамм ВКМП-S892 обладает повышенной продуктивностью эремомицина (1800 мг в 1 л КЖ) и характеризуется следующими культурально- морфологическими и физиологическими признаками.
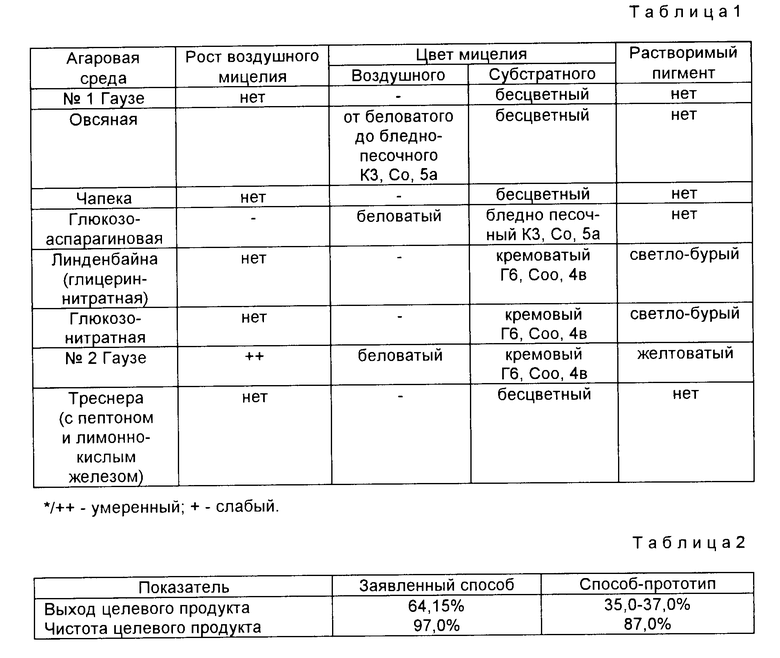
Культурально-морфологические признаки штамма ВКПМ-S892. Температура 28oC; длительность выращивания 7-21 сутки; Споровый посевной материал с 10-дневной культуры штамма, выращенной на глюкозоаспарагиновом агаре или N 2 Гаузе. Цвет определен по таблице Бондарцева и Праузера (табл.1):
Микробиологические признаки. Гифы воздушного мицелия прямые или извилистые, распадающиеся на элементы различной длины; поверхность спор гладкая.
Физиолого-биохимические свойства. Аэроб растет при 24-37oC, оптимум 28oC. Желатину разжижает. Молоко пептонизирует. Крахмал гидролизует. Сахарозу инвертирует. На клетчатке не растет. Восстанавливает нитраты до нитритов. Меланоиды не образует при росте на среде Треснера с лимонно- кислым железом.
Отношение к углеводам: хорошо использует фруктозу, арабинозу, маннит, глюкозу, умеренно - лактозу, инозит, галактозу, рамнозу, ксилозу; не использует раффинозу.
Антагонистические свойства. Продуцируемый Amycolatopsis orientalis subsp. eremomycini ВКМП- S892 антибиотик эремомицин подавляет рост грамположительных бактерий Staphylococcus aureus, Bacillus mycoides. Micrococcus luteus и не действует на грамотрицательные бактерии Escherichia coli, Comamonas terigena, Providencia stuaztis.
Отношение к специфическим вирулентным фагам, вызывающим лизис культуры Amycolatopsis orientalis; штамм ВКПМ-S892 - фагоустойчивый, лизиса в процессе ферментации не происходит.
Штамм поясняется следующим примером.
Пример 1. Споровым материалом с мицелием культуры Amycolatopsis orientalis subsp. eremomycini ВКПМ-S892, выращенной в течение 10-14 сут. на агаровой среде N 2 Гаузе, засевают питательную среду (100 мл в колбах Эрленмейера, объемом 750 мл) и выращивают 24-36 ч. при 28oC на качалке при 220-240 об/мин. Состав посевной среды, %:
Глицерин - 2,0
Соевая мука - 0,5
Магний сернокислый - 0,01
Натрий хлористый - 0,3
Вода - Водопроводная
Выросшим мицелием в количестве 3-5% засевают питательную среду (100 мл в колбах Эрленмейера, объемом 750 мл) следующего состава, %:
Глицерин - 0,3
Соевая мука - 0,5
Калий азотнокислый - 0,3
Натрий хлористый - 0,3
Мел - 0,3
Магний сернокислый - 0,01
Вода - Водопроводная
Ферментацию проводят на качалке при 220-240 об/мин, 28oC в течение 120-144 ч. Антибиотическую активность культуральной жидкости определяют методом диффузии в агар с использованием тест-культуры - Bacillus subtilis ATCC 6633. Содержание эремомицина в культуральной жидкости продуцента к концу ферментации составляет 1800 мкг/мл.
Преимуществом заявленного штамма по сравнению с прототипом является более высокое содержание антибиотика эремомицина в культуральной жидкости, а именно, в штамме-прототипе 150 мкг/мл, в заявленном штамме 1800 мкг/мл.
Известен способ получения эремомицина на основе штамма ИНА-238. Этот способ основан на выделении эремомицина из культуральной жидкости, полученной в результате биосинтеза штамма-продуцента N 238, на сорбенте Амберлит XAD-2 с последующей элюцией смесью ацетон-н.- бутанол-вода (1:1:1) при pH 3,0. Органические растворители удаляют в вакууме и антибиотик осаждают из водного концентрата ацетоном. Дальнейшая очистка проводится на карбоксильном катионите КБ-2 (NH
Известный способ имеет ряд недостатков. Использование в процессе выделения взрывоопасных растворителей (ацетон, н.-бутанол) на стадии элюции антибиотика с сорбента и двух стадий осаждения затрудняет воспроизведение способа в условиях производства. Более того, выделение эремомицина в виде основания, а не в форме сульфата, который является водорастворимым и более устойчивым, в сочетании с низким выходом целевого продукта (35,0-37,0%) от содержания в нативном растворе, низкая чистота препарата (не выше 87%) также являются недостатками способа-прототипа. Используемый сорбент имеет низкую сорбционную емкость и избирательность, является дорогостоящим.
Сущность изобретения состоит в том, что эремомицин выделяют из нативного раствора заявленного штамма ВКПМ-S892 сорбцией на карбоксильной смоле КБ-2 в солевой форме при pH 6,5. Сорбент загружают в хроматографическую колонку из расчета 400±50 мг антибиотика на 1 г сухого или 5,0±0,5 мл влажного катионита. Колонку промывают водой и антибиотик десорбируют 0,5 н. раствором аммиака. Элюат с колонки нейтрализуют 40%-ным раствором серной кислоты до pH 6,9. Нейтральный элюат обеззоливают с помощью ионита КУ-2-20 (H+, нейтрализуют ионитом ЭДЭ- 10П до pH 5,0±0,5 и пропускают через колонку, заполненную сорбентом ПТФЭ. Сорбент ПТФЭ берут из расчета 4,5-5,0 г на 1,0 г эремомицина. Вытеснение эремомицина с ПТФЭ-колонки осуществляют дистиллированной водой. Фильтрат и водные промывки с колонки объединяют и концентрируют в вакууме до содержания эремомицина 120-140 мг/мл и кристаллизуют из 20%-ного этилового спирта.
Выход очищенного кристаллического препарата эремомицина сульфата от содержания в нативном растворе составляет 60,0-65,0%, чистота целевого продукта 97,0% (метод ВЭЖХ).
Сорбент ПТФЭ способствует практически полному устранению сопутствующих целевому продукту примесей - минорных компонентов, пигментов, продуктов белкового характера и др.
Эремомицин сульфат, полученный заявленным способом, представляет собой белый кристаллический порошок, легко растворимый в воде и практически нерастворимый в органических растворителях. Брутто-формула: C73H89N10ClO26H2SO4. Мол. масса 1656 а.е.м.
УФ-спектр: λmax (0,01 н. HCl) нм (E
ИК-спектр (KBr), λmax, см-1: 3350, 1650, 1500, 1200-100;
[α]
Использование одинарного катионирования и нового сорбента ПТФЭ считаем существенными, поскольку именно они приводят к повышению выхода целевого продукта и улучшению его качества.
Преимущества эремомицина по сравнению с антибиотиками данного класса представлены в материалах [2-5].
Способ поясняется следующим примером:
Пример 2. 12 л КЖ, подкисленной соляной кислотой до pH 6,5, отделяют от мицелия и нативный раствор (10 л), содержащий 18 г эремомицина пропускают через колонку, заполненную 250 мл катионита КБ- 2 (Na+) со скоростью 1,0±0,1 мл/см2/мин. Колонку промывают водой и антибиотик десорбируют 0,5 н. раствором аммиака. Элюат с колонки (300 мл), содержащий 14,58 г эремомицина, нейтрализуют 40%-ным раствором серной кислоты до pH 6,9±0,1, обрабатывают катионитом КУ-2-20 (H+) для удаления солей и с помощью анионита ЭДЭ-10П (OH-) доводят до pH 5,0±0,5. Обессоленный элюат пропускают через колонку, заполненную 220 мл (72 г) сорбента ПТФЭ, со скоростью 1,0+0,1 мл/см2/мин. Антибиотик вытесняют с колонки дистиллированной водой, фракции, содержащие очищенный антибиотик, объединяют и концентрируют в вакууме при 35,0-37,0oC до содержания эремомицина 120-140 мг/мл. Из полученного концентрата эремомицин кристаллизуют в форме сульфата при добавлении 20,0%-ного этилового спирта. Получают 11,0-11,5 г эремомицина сульфата. Выход целевого продукта от содержания в нативном растворе составляет 64,15%. Преимущества заявленного способа представлены в табл.2.
Таким образом, заявленное решение позволяет получить антибиотик с высокой степенью чистоты и высоким выходом. При этом способ является более экономичным, позволяет использовать отечественные сорбенты и упростить технологический процесс.
Литература:
1. SU, авторское свидетельство, 1475150 A1, C 12 C N 1/00, 1997.
2. Gause G.F., Brazhnikova M.G., Lomakina N.N., Berdnikova T.F., Fedorova G.B., Tokareva N.L., Borisova V.N., Batta G.Y., J. of Antibiotics, 42, 1790-1799 (1989).
3. Гаузе Г.Ф., Бражникова М.Г., Лайко А.В., Свешникова М.А, Преображенская Т. П. , Федорова Г. Б. и др. Эремомицин - новый антибиотик из группы циклических гликопептидов. - Антибиотики и медицинская биотехнология, 32, N 8. 571-575 (1987).
4. Филиппосьянц С.Т., Шевнюк Л.А. Экспериментальное изучение гистаминосвобождающих свойств эремомицина. - Антибиотики и химиотерапия, 34, N3, 209-212 (1989).
5. Бухман В.М., Катруха Г.С., Бердникова Т.Ф., Федорова Г.Б., Филиппосьянц С. Т. , Дудник Ю. В. Новый высокоактивный гликопептидный антибиотик - эремомицин. - Тезисы докладов II Российского национального конгресса "Человек и лекарство. - М.: 10-15 апреля 1995 г., с.179.
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ Amycolatopsis orientalis ВКПМ-Ас-807-ПРОДУЦЕНТ ЭРЕМОМИЦИНА | 2007 |
|
RU2352631C2 |
| Штамм Amycolatopsis umgeniensis - продуцент антибиотика эремомицина | 2018 |
|
RU2689699C1 |
| Штамм Amycolatopsis orientalis - продуцент антибиотика диметилванкомицина и способ получения антибиотика | 2016 |
|
RU2633511C1 |
| АНТИБИОТИК "ЭРЕМОМИЦИН" И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1981 |
|
SU1475150A1 |
| ШТАММ Amycolatopsis orientalis - ПРОДУЦЕНТ АНТИБИОТИКА ЭРЕМОМИЦИНА И СПОСОБ ПОЛУЧЕНИЯ ЭРЕМОМИЦИНА | 2016 |
|
RU2621866C1 |
| ШТАММ STREPTOMYCES GRISEOCARNEUS SUBSP. BLEOMYCINI ВКПМ-S1086 - ПРОДУЦЕНТ БЛЕОМИЦЕТИНА И СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА БЛЕОМИЦЕТИНА | 2007 |
|
RU2358008C2 |
| ШТАММ Streptomyces griseocarneus subsp. bleomycini ВКПМ-S887 - ПРОДУЦЕНТ БЛЕОМИЦИНА A И СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА БЛЕОМИЦИНА A | 2007 |
|
RU2355758C2 |
| ШТАММ STREPTOALLOTEICHUS CREMEUS SUBSP. TOBRAMYCINI ВКПМ S-1084 - ПРОДУЦЕНТ АПРАМИЦИНА И СПОСОБ ПОЛУЧЕНИЯ АПРАМИЦИНА | 2007 |
|
RU2392311C2 |
| ШТАММ Nonomuraea roseoviolacea subsp. carminata (Actinomadura carminata) - ПРОДУЦЕНТ АНТИБИОТИКА КАРМИНОМИЦИНА И СПОСОБ ПОЛУЧЕНИЯ КАРМИНОМИЦИНА | 2007 |
|
RU2355757C2 |
| ШТАММ AMYCOLATOPSIS FRUCTIFERI SUBSP. RISTOMYCINI - ПРОДУЦЕНТ АНТИБИОТИКА РИСТОМИЦИНА | 2008 |
|
RU2392325C2 |
Использование: в медицинской промышленности, в частности в биотехнологии. Получен штамм Amycolatopsis orientalis subsp. eremomycini ВКПМ-S892 - продуцент антибиотика эремомицина. Штамм используется в качестве продуцента в способе получения эремомицина. После биосинтеза штамма проводят сорбцию антибиотика на карбоксильном катионите КБ-2 в солевой форме и элюируют раствором аммиака. Затем элюат нейтрализуют, обеззоливают, пропускают через сорбент ПТФЭ. Эремомицин с сорбента вытесняют водой, концентрируют в вакууме до содержания 120 - 140 мг/мл и кристаллизуют в форме сульфата. 2 с п. ф-лы. 2 табл.
| RU, авторское свидетельство, 1475150, кл | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
1998-05-10—Публикация
1997-06-18—Подача