Изобретение относится к аналитической химии, в частности к газохроматогра- фическим методам анализа микропримесей органических веществ в газах.
Цель изобретения - повышение точности и стабильности результатов анализа во времени за счет исключения влияния растворителя на разделительные свойства хроматографической колонки.
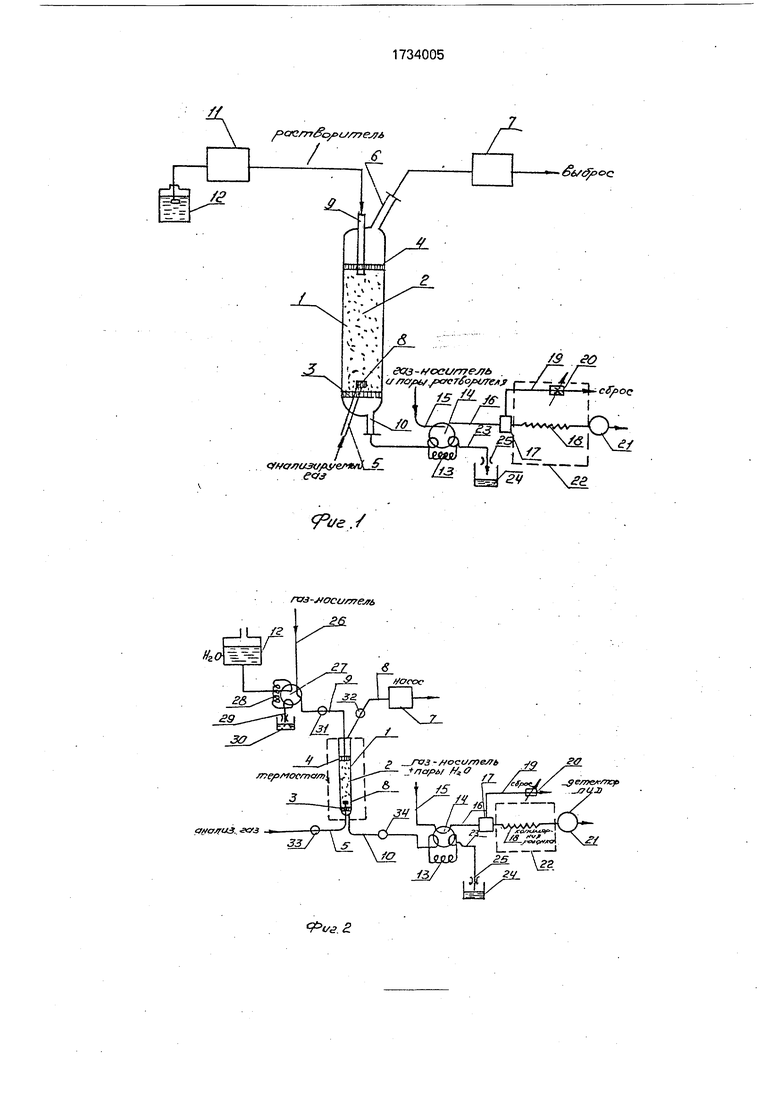
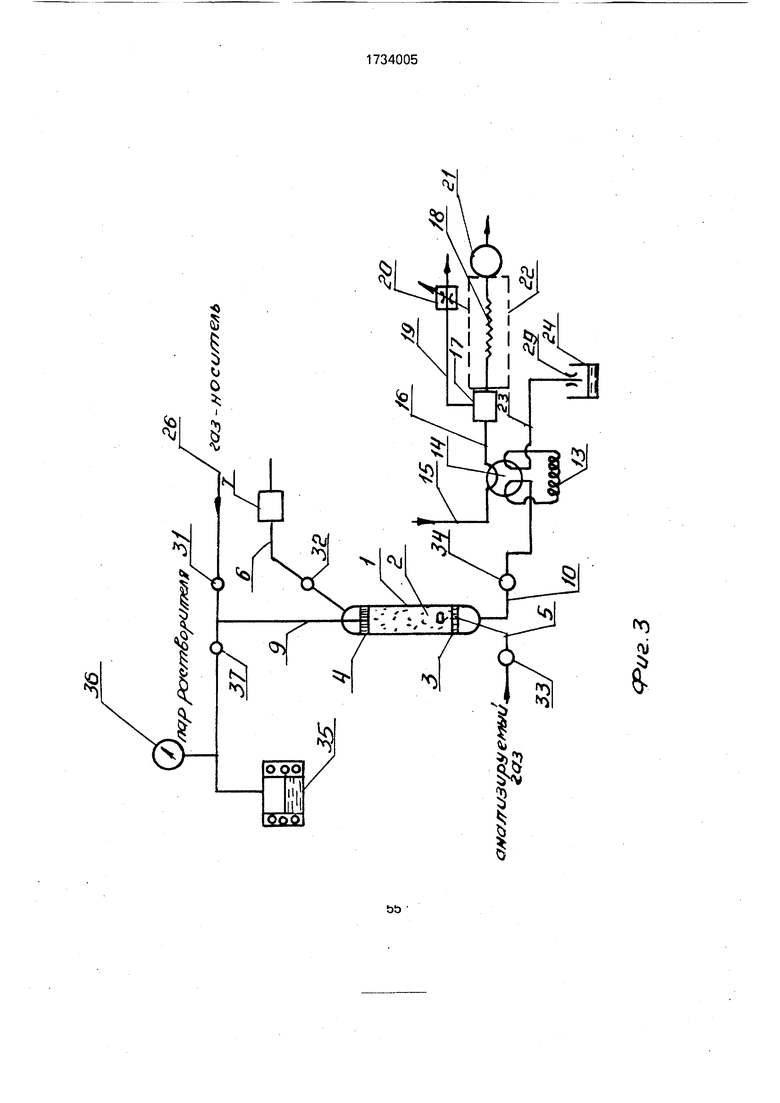
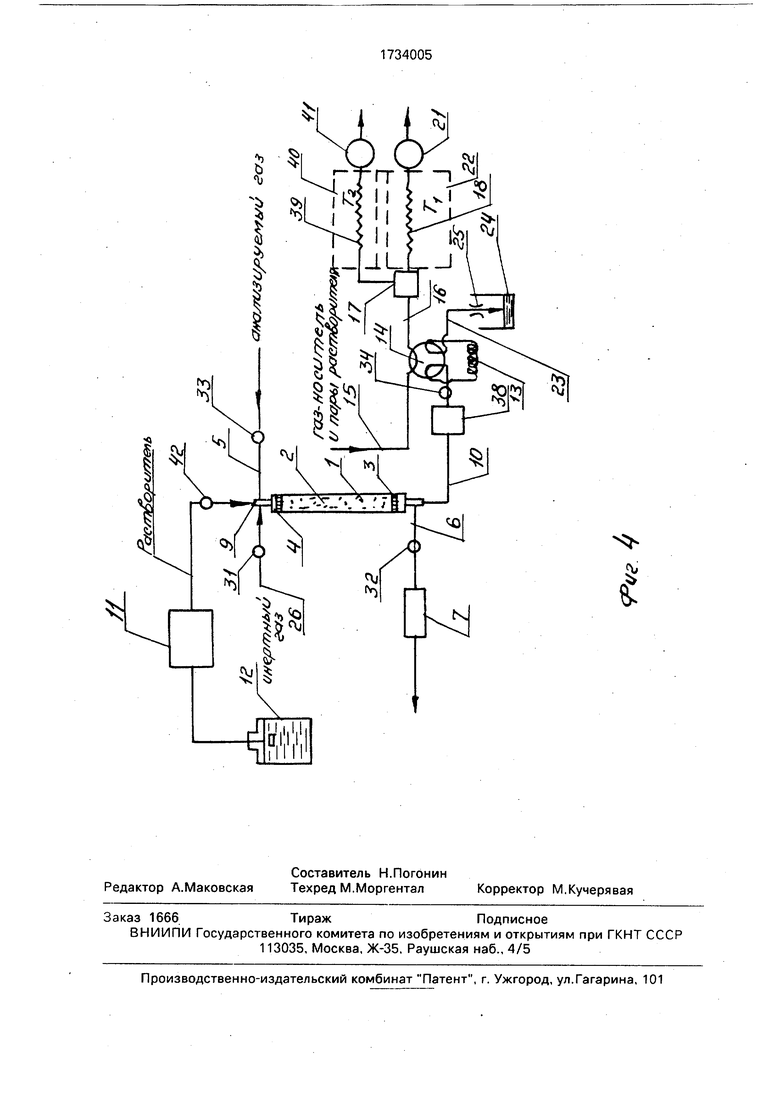
На фиг. 1 изображена схема устройства для осуществления способа с концентрированием микропримесей в режиме противо- точной экстракции; на фиг. 2 - то же, с концентрированием микропримесёй в слое частиц адсорбента и экстракцией жидких растворителей; на фиг. 3 - то же, с концентрированием микропримесей на слое частиц
адсорбента и экстракцией паром растворителя; на фиг. 4-тоже, с концентрированием примесей на слое частиц адсорбента и экстракцией их в режиме жидкостной хроматографии.
Наиболее простой вариант выполнения устройства для осуществления способа изображен на фиг, 1. Устройство содержит концентратор 1 микропримесей, выполненный в виде трубки, заполненной частицами 2 из инертного материала (например, стеклянных шариков диаметром 0,1-0,2 мм), которые уложены на пористом фильтре 3 укрепленном в основании концентратора 1. Сверху на слой частиц 2 из инертного материала уложен второй пористый фильтр 4. Концентратор 1 имеет два патрубка 5 и 6 для
-N
со
-N О О
ел
подвода и вывода анализируемого газа, причем патрубок 6 соединен с входом побудителя 7 расхода анализируемого газа. На конце патрубка 5, размещенном в слое частиц 2 инертного материала, заключен фильтр 8 из пористого материала, который проницаем для газа, но непроницаем для жидкости. Концентратор 1 снабжен также патрубками 9 и 10 для подачи и отвода потока растворителя и соединен с выходом насоса 11 для подачи растворителя, вход которого соединен с емкостью 12с растворителем. В качестве насоса 11 может быть использован насос перистальтического типа с регулируемой производительностью (скорость подачи растворителя должна регулироваться в диапазоне 0,04-5,0 мл/мин). Патрубок 10 соединен с дозированным объемом 13 крана-дозатора 14, который имеет также каналы 15 и 16 для подвода и вывода подвижной газопаровой фазы, подаваемой через испаритель 17 и капиллярную трубку 18, служащую разделительной хроматогра- фической колонкой. В качестве крана-дозатора 14 может быть использован кран штокового типа с калиброванным дозировочным объемом, выполненным непосредственно в штоке крана (объем 0,5-2,0 мкл), В качестве капиллярной трубки 18 может быть использована капиллярная трубка из нержавеющей стали с внутренним диаметром 0,5 мм. Испаритель 17 может быть снабжен линией 19 для сброса части потока подвижной фазы в атмосферу, в которой установлен регулируемый дроссель 20, служащий для регулирования коэффициента деления потока подвижной фазы между линией 19 сброса и капиллярной трубкой 18. На выходе капиллярной трубки 18 установлен детектор 21, например пламенно-ионизационный детектор. Газопаровая подвижная фаза, подаваемая по каналу 15 через кран-дозатор 14 в испаритель 17, образуется путем насыщения инертного газа- носителя (Не, На, N2,-Str и др.) парами того же растворителя, который подается в концентратор 1. Насыщение газа-носителя парами растворителя осуществляется с применением барботера (не показан), устанавливаемого в термостате 22, где помещена капиллярная трубка 18, служащая разделительной хроматографической колонкой. Кран-дозатор 14 имеет также патрубок 23 для слива избытка растворителя при заполнении дозировочного объема 13. Избыток растворителя сливают в емкость 24 через регулируемый дроссель 25.
Устройство для осуществления предлагаемого способа по описанному выше варианту работает следующим образом.
Перед началом процесса анализа через капиллярную трубку 18 пропускают по каналам 15 и 16 через кран-дозатор 14 и испаритель 17 поток газопаровой смеси,
образованный путем барботирования потока чистого газа-носителя, например N2, через слой растворителя, например дистиллированной воды, в барботере (не показан), установленном в термостате 22 хро0 матографической колонки. Температуру термостата 22 поддерживают ниже температуры кипения растворителя. Температуру воды поддерживают в диапазоне 60-90°С. Часть потока газопаровой смеси после ис5 парителя 17 может сбрасываться в атмосферу по линии 19 для сброса. При этом коэффициент деления потока на выходе испарителя между капиллярной трубкой 18 и линией 19 для сброса регулируется с по0 мощью регулируемого дросселя 20, установ- ленного в линии 19. Температуру испарителя 17 и детектора 21 поддерживают выше температуры испарения анализируемых микропримесей в растворителе.
5 Далее подготавливают к работе концентратор 1. С этой целью запускают насос 11, который нагнетает растворитель из емкости 12 по патрубку 9 в концентратор 1, где растворитель, фильтруясь через слой частиц 2
0 из инертного материала (например, стеклянные шарики диаметром 0,2-0,5 мм), стекает в нижнюю часть концентратора 2, проходит через пористый фильтр 3 и через патрубок 1.0 выводится из концентратора в
5 дозировочный объем 13 крана-дозатора 14, а из него по патрубку 23 через регулируемый дроссель 25 - в емкость 24 для сбора растворителя. Скорость потока растворителя через концентратор 1 составляет 0,01-0,1
0 мл/мин, При этом верхняя часть концентратора 1 над фильтром 4 должна быть свободной от растворителя, образуя газовое пространство, заполненное воздухом. С этой целью фильтр 4 должен быть выполнен
5 из пористого материала, проницаемого для газа, но непроницаемого для растворителя, а нижний конец патрубка 9 должен быть установлен под фильтром 4. Затем включают насос 7, с помощью которого в верхней
0 части концентратора 1 создается разрежение, под действием которого анализируемый газ (воздух) через патрубок 5 и фильтр 8 барботируется через слой частиц 2 инертного материала, смоченных растворителем,
5 и через патрубок 6 и насос 7 сбрасывается в атмосферу. При этом осуществляется непрерывный противоточный контакт мелких пузырьков газа со стекающим вниз по слою частиц 2 концентратора 1 растворителем, обусловливающий переход микропримесей
анализируемого газа, растворимых в данном растворителе (экстракцию), в жидкую фазу с одновременным их концентрированием в жидкой фазе. Жидкий экстракт выводится из концентратора 1 по сливному патрубку 10 в кран-дозатор 14, заполняя его дозировочный объем 13. Периодически с помощью крана-дозатора 14 осуществляется ввод дозировочного количества обогащенного в концентраторе 1 экстракта (пробы) в поток газа паровой подвижной фазы, поступающий в испаритель 17, где осуществляется испарение пробы, пары которой поступают в потоке газопаровой подвижной фазы в капиллярную трубку 18, где происходит хроматографическое разделение анализируемых микропримесей. Поскольку проба экстракта в качестве основного компонента содержит тот же растворитель, который используется для образования газопаровой подвижной фазы и конденсированной псевдонеподвижной фазы в капиллярной трубке 18, то ввод пробы сопровождается некоторым увеличением толщины пленки неподвижной жидкой фазы на входе капиллярной трубки 18, что приводит к дополнительному эффекту сжатия полосы анализируемых микропримесей на начальном участке капиллярной трубки 18 и способствует повышению эффективности капиллярной хроматографической колонки, каковой является капиллярная трубка 18. Этот эффект воспроизводимо повторяется при вводе каждой последующей пробы экстракта, при этом разделительная способность капиллярной колонки с конденсированной псевдонеподвижной фазой не изменяется от анализа к анализу, так как происходит постоянное обновление пленки неподвижной жидкой фазы на внутренних стенках капиллярной трубки 18. Разделенные в капиллярной трубке 18 анализируемые микропримеси детектируют на ее выходе с помощью детектора 21. В качестве растворителя используют дистиллированную воду, которая применяется и как экстрагент в концентраторе 1, и как составная часть газопаровой подвижной фазы, подаваемой в капиллярную трубку 18, где она образует пленку конденсата, служащую псевдонеподвижной жидкой фазо й. Наиболее подхо- дящим детектором для детектирования анализируемых органических микропримесей является пламенно-ионизационный детектор. Могут быть использованы и селективные высокочувствительные детекторы, например пламенно-фотометрический и термоионный.
Описанный вариант выполнения устройства для осуществления способа (фиг. 1)
может в соответствии со способом работать и в режиме периодического концентрирования микропримесей в концентраторе 1. С этой целью насос 11 для подачи растворителя в концентратор 1 включают на время, достаточное для заполнения растворителем пространства между фильтрами 4 и 3 (пространство между частицами 2 насадки концентратора 1) и нижней его части, включая
дозировочный объем 13 крана-дозатора 14. Затем подачу растворителя в концентратор 1 прекращают, отключая насос 11, и начинают подачу в концентратор 1 анализируемого газа, включая насос 1. При прохождении
мелких пузырьков анализируемого газа через слой частиц 2 насадки концентратора 1 происходит поглощение анализируемых микропримесей в объем растворителя между фильтрами 3 и 4. После пропускания через слой частиц 2 насадки концентратора определенного объема анализируемого газа подачу его в концентратор 1 прекращают, отключая насос 7. Затем вновь на определенное время включают насос 11 для подачи
свежей порции растворителя в концентратор 1, которая вытесняет ранее содержащийся в концентраторе 1 растворитель, обогащенный анализируемыми микропримесями, в дозировочный объем 13 крана-дозатора 14, с помощью которого осуществляют отбор и ввод проб экстракта в поток газопаровой подвижной фазы, поступающей в испаритель 17 газового хроматографа. Затем процесс концентрирования
повторяют в описанной выше последовательности. В этом варианте осуществления способа частицы 2 насадки концентратора могут представлять собой частицы адсорбента, который активно участвует в накоплении микропримесей в концентраторе 1 при продувании слоя частиц 2 насадки анализируемым газом.
Вариант устройства для осуществления предлагаемого способа, изображенный на фиг. 2, отличается от описанного тем, что вместо насоса 11 для прокачки растворителя используют линию 26 сжатого газа-носителя, в которой установлен кран-дозатор 27, дозировочный объем 28 которого непосредственно соединен с емкостью 12 с растворителем. Сливной патрубок крана-дозатора 27 снабжен регулируемым дросселем 29 и установлен над емкостью 30 для сбора излиш- ков растворителя. В патрубках 9, 6, 5 и 10, соединенных с концентратором, установлены управляемые запорные клапаны 31, 32, 33 и 34 соответственно. При этом концентратор 1 заполнен частицами 2 селективного адсорбента для поглощения (адсорбции)
анализируемых микропримесей из анализируемого газа.
Данный вариант устройства в своей хроматографической части работает аналогично устройству, изображенному на фиг, 1. Отличие заключается в работе концентратора 1, в котором осуществляются периодические процессы концентрирования микропримесей в слое частиц 2 адсорбента и экстракции их из слоя частиц 2 сорбента дозированным количеством растворителя. На этапе концентрирования микропримесей в слое частиц 2 адсорбента клапаны 31 и 34 закрыты, а клапаны 32 и 33 открыты, включен насос 7, который прокачивает че- рез слой частиц 2 адсорбента определенный объем анализируемого газа до момента, предшествующего проскоку легких микропримесей анализируемого газа через слой частиц 2 адсорбента. В качестве адсорбента могут быть использованы сили- кагель, активированный уголь, полимерный адсорбент типа тенакса и др. Затем клапаны 32 и 33 закрывают и открывают клапаны 31 и 34. С помощью потока сжатого газа-носи- теля и крана-дозатора 27 осуществляют ввод дозированного количества растворителя в концентратор 1. Порция растворите- ля, введенного в концентратор 1, перемещается в виде пробки по слою час- тиц 2 адсорбента, экстрагируя из него скон- центрированные микропримеси, а полученный экстракт поступает в дозировочный объем 13 крана-дозатора 14, заполняя его. Затем с помощью крана-дозатора 14 осуществляется ввод дозированного количества экстракта в поток газопаровой подвижной фазы, подаваемый в испаритель 17 газового хроматографа, где осуществляются хроматографическое разделение микро- примесей и детектирование их. Экстракция микропримесей из слоя частиц 2 адсорбента может осуществляться многократно с дозированием экстракта в систему газового хроматографа, пока детектор 21 незафикси- рует отсутствие микропримесей в экстракте. После этого при открытых клапанах 31 и 34 и закрытых клапанах 32 и 33 осуществляют продувку концентратора 1 потоком газа- носителя со сбросом его через дозировочный объем 13 и сливной патрубок 23 крана-дозатора 14 в атмосферу. Затем процессы концентрирования и экстракции микропримесей осуществляют вновь в описанной выше последовательности. Вариант устройства для осуществления предлагаемого способа, изображенного на фиг. 3, отличается от устройства, изображенного на фиг, 2, тем, что вместо емкости 12с растворителем и крана-дозатора 27 для ввода дозированного объема растворителя в поток газа-носителя используют парогенератор 35, на выходе которого установлены манометр 36 для контроля давления пара в парогенераторе и управляемый запорный клапан 37, через который выход парогенератора 35 сообщается с патрубком 9 для подвода паров растворителя или потока газа-носителя в концентратор 1. Данный вариантустройствавсвоейхроматографической части работает аналогично устройствам, изображенным на фиг. 1 и 2. Отличие заключается в работе концентратора, в котором осуществляются периодические процессы концентрирования микропримесей в слое частиц 2 адсорбента и экстракция их из слоя частиц адсорбента дозированным количеством пара растворителя, поступающим из парогенератора 35. На этапе концентрирования микропримесей на слое частиц 2 адсорбента клапаны 37, 31 и 34 закрыты, а клапаны 33 и 32 открыты, включен насос 7, который прокачивают через слой частиц 2 адсорбента определенный объем анализируемого газа до момента, предшествующего проскоку легких микропримесей анализируемого газа через слой частиц адсорбента в концентраторе 1. В этот момент в парогенераторе 35 под действием высокой температуры формируется необходимое давление пара, находящегося в равновесии с жидким растворителем. Затем останавливают насос 7, закрывают клапаны 33 и 32 и открывают клапаны 37 и 34. Поток пара растворителя с выхода парогенератора 35 под действием перепада давления поступает по линии 9 в слой частиц 2 адсорбента в концентраторе 1, осуществляя быструю и эффективную экстракцию сконцентрированных микропримесей. Процесс экстракции сопровождается процессом конденсации паров растворителя в концентраторе, что контролируется по показаниям манометра 36 и времени дозировки. Затем закрывают клапан 37 и открывают клапан 31, подавая в верхнюю часть концентратора
1по линии 9 поток сжатого газа-носителя, Поток сжатого газа-носителя выдавливает сконденсированный растворитель, обогащенный экстрагированными из слоя частиц
2адсорбента микропримесями, в дозировочный объем 13 крана-дозатора 14, заполняя его. Затем с помощью крана-дозатора 14 осуществляется ввод дозированного количества экстракта в поток газопаровой подвижной фазы,подаваемый в испаритель 17 газового хроматографа, где осуществляется хроматографическое разделение микропримесей и детектирование их, Экстракция микропримесей из слоя частиц адсорбента
может осуществляться порциями пара растворителя многократно с дозированием экстракта в систему газового хроматографа, пока детектор 21 не зафиксирует отсутствие микропримесей в экстракте. После этого при открытых клапанах 31 и 34 и закрытых клапанах 37,32 и 33 осуществляют продувку концентратора 1 потоком газа-носителя со сбросом его через дозированный объем 13 и сливной патрубок 23 крана-дозатора 14 в атмосферу. Затем процессы концентрирования и экстракции микропримесей потока пара растворителя повторяют вновь в описанной выше последовательности.
Вариант выполнения устройства для осуществления предлагаемого способа, изображенный на фиг. 4, отличается от описанных выше тем, что концентратор 1 выполнен в виде хроматографической колонки для жидкостно-адсорбционной хроматографии, в выходном патрубке 10 которой установлен детектор 38 для жидкостной хроматографии, например УФ-фотометр, выход которого через клапан 34 соединен с дозировочным объемом 13 крана-дозатора 14. При этом патрубок 9 для подачи растворителя в концентратор 1 соединен с линиями 5 и 26 для подвода анализируемого газа и газа-носителя соответственно, в которых установлены управляемые запорные клапаны 31 и 33. Патрубок 6 для отвода анализируемого газа соединен с нижней частью концентратора 1, и в нем установлены насос 7 для прокачки анализируемого газа и управляемый запорный клапан 32. Газохрома- тографическая часть устройства дополнена еще одной хроматографической колонкой 39, установленной в отдельном термостате 40 и снабженной своим детектором 41. В качестве дополнительной хроматографической колонки 39 предпочтительно использовать капиллярную хроматографическую колонку, внутренние стенки которой покрыты тонкой пленкой малолетучей неподвижной жидкой фазы. Дополнительная колонка 39 может быть установлена в любом из описанных выше устройств (фиг. 1-3) вместо линии 19 для сброса части потока газопаровой подвижной фазы из испарителя 17 в атмосферу для идентификации анализируемых микропримесей. На выходе насоса 11 в линии подачи растворителя установлен запорный клапан 42.
Данный вариант устройства работает следующим образом.
В момент времени, предшествующий концентрированию микропримесей, клапаны 42, 33 и 32 закрыты, а клапаны 31 и 34 открыты и поток газа-носителя, подаваемый в концентратор 11, проходит через слой частиц 2 адсорбента, освобождая его от паров растворителя и выдувая их по линии 10 через детектор 38 и кран-дозатор 14 в атмосферу. В это время газопаровая подвижная
фаза, образованная путем насыщения газа- носителя парами растворителя в барботере (не показан), по линии 15 через кран-дозатор 14 поступает в испаритель 17 газового хроматографа, где делится на две части. Од0 на часть газопаровой подвижной фазы поступает в капиллярную трубку 18, где образует тонкую пленку конденсата на внутренних стенках капилляра, служащую в качестве неподвижной жидкой фазы. Вторая
5 часть газопаровой подвижной фазы поступает в дополнительную капиллярную хроматографическую колонку 39, температуру которой с помощью термостата 40 поддерживает выше температуры кипения раство0 рителя, так что в этой колонке газопаровая фаза используется только как подвижная фаза для переноса анализируемых микропримесей от входа колонки к выходу. После продувки концентратора 1 потоком инерт5 ного газа-носителя клапаны 31 и 34 запирают, оставляя запертым также клапан 42, открывают клапаны 33 и 32 и включают насос, осуществляющий прокачку заданного объема анализируемого газа через слой ча0 стиц 2 адсорбента в концентраторе 1. В процессе прокачивания заданного объема анализируемого газа через слой частиц 2 адсорбента в концентраторе 1 происходит концентрирование микропримесных компо5 нентов на слое частиц адсорбента и частичное их разделение в режиме фронтального обогащения. Затем останавливают насос 7, закрывают клапаны 32 и 33, оставляя закрытым клапан 31, и открывают клапаны 42 и 34,
0 запуская одновременно насос 11 для прокачки растворителя через слой частиц адсорбента в концентраторе 1 в том же направлении, в котором до этого осуществлялась прокачка анализируемого газа. По5 ток растворителя, фильтруясь через слой частиц адсорбента в концентраторе 1, осуществляет экстракцию адсорбированных микропримесей и одновременное разделение их на отдельные фракции, которые в
0 потоке растворителя последовательно выходят из концентратора 1 и по патрубку поступают в детектор 38, а из него - в дозировочный объем 13 крана-дозатора 14. По сигналу детектора выбранная фракция
5 сконцентрированных микропримесей с помощью крана-дозатора 14 переводится в поток газопаровой фазы, направляемый в испаритель 17 газового хроматографа. Испаренные анализируемые микропримеси делятся на две части и вместе с соответствующими частями газопаровой подвижной фазы поступают в хроматографические колонки 18 и 39, где осуществляются их хро- матографическое разделение на различных по своему составу неподвижные жидкие фазы и детектирование на отдельных детекторах 21 и 41. При этом определяется не только количественный состав анализируемых микропримесей, но и их качественный состав по различию времен удерживания одних и тех же компонентов на различных колонках.
Пример 1. Анализу подвергали модельную смесь газа-носителя (N2), насыщен- ного парами органических веществ, с концентрацией анализируемых компонентов на уровне % (объемных). В качестве концентратора использовали U-образную стеклянную трубку длиной 30 см и внутренним диаметром 5 мм, заполненную стеклянными шариками диаметром 0,2-0,3 мм. В качестве растворителя использовали дистиллированную воду, которую заливали в U-образную трубку, заполняя пространство между стеклянными шариками. Анализируемый газ (газ-носитель, насыщенный парами анализируемых веществ) пропускали через концентратор при скорости потока 30 мл/мин в течение 20 мин. Затем воду из концентратора сливали в ампулу и подвергали хроматографическому анализу. Для проведения анализов использовали капиллярный газовый хроматограф Биохром 1, в котором в качестве капиллярной хроматографической колонки использовали пустую капиллярную трубку из нержавеющей стали длиной 6,5 м и внутренним диаметром 0,47 мм. Система ввода пробы представляла собой испаритель, снабженный делителем потока подвижной фазы. В качестве детектора использовали пламенно-ионизационный детектор. В качестве газа-носителя использовали гелий из баллона, который насыщали парами воды в барботере, устанавливаемом непосредственно в термостате колонки перед испарителем. Скорость потока подвижной фазы в капиллярной трубке составляла 0,6 мл/мин, а в линии сброса из испарителя - 60 мл/мин, т.е. коэффициент деления потока на входе в капиллярную трубку составлял 1:100. Температуру капиллярной трубки, служащей хроматографической колонкой, и барботера поддерживали равной 80°С. Температуру испарителя поддерживали равной 180°С, а детектора - 140°С.
Ввод пробы в испаритель осуществляли с помощью медицинского шприца. Объем
пробы составлял 100 мкл. В этих условиях было обеспечено полное разделение анализируемых веществ.
Формула изобретения
1. Способ хроматографического анализа микропримесей в газе, при котором мик- ропримесиконцентрируют с
использованием растворителя в качестве экстрагента с последующим разделением
паров экстракта на хроматографической колонке и детектированием разделенных компонентов экстракта, отличающийся тем, что, с целью повышения точности и стабильности результатов анализа во времени за счет исключения влияния растворителя на разделительные свойства хроматографической колонки, разделение паров экстракта осуществляют в капиллярной трубке в потоке газопаровой подвижной
фазы, образованной путем насыщения газа- носителя парами растворителя, используемого для экстракции микропримесей, находящимся в контакте с пленкой конденсата этого растворителя на внутренних
стенках капиллярной трубки, при этом температуру трубки поддерживают ниже температуры испарения растворителя, а детектирование осуществляют с применением детектора, нечувствительного к парам
растворителя.
2.Способ по п. 1,отличающийся тем, что концентрирование микропримесей осуществляют в режиме непрерывной про- тивоточной экстракции, проводимой в слое
насадки из частиц инертного материала, через который пропускают анализируемый газ, а противотоком к нему - поток растворителя, причем из непрерывного потока растворителя, обогащенного анализируемыми микропримесями, периодически отбирают дозированное количество экстракта, который испаряют и вводят в потоке газопаровой подвижной фазы в капиллярную трубку.
3,Способ по п.1,отличающийся тем, что концентрирование микропримесей осуществляют путем пропускания заданного объема анализируемого газа через слой
частиц адсорбента с последующей экстракцией из слоя частиц адсорбента сконцентрированных микропримесей дозированным объемом растворителя, причем порции обогащенного микропримесями растворителя
многократно вводят в виде пара в газопаровой поток подвижной фазы, подаваемый в капиллярную трубку.
rr.
&xtr 3a/aЈ- 0 // «JoLtf-02 of-4&ausnzoH- ГЛУ с
e& fnifo/io
{Ј/jOU/J0fi/ &f
т





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ газохроматографического анализа микропримесей веществ в газе и устройство для его реализации | 2018 |
|
RU2694436C1 |
| Устройство для термодесорбции сконцентрированных примесей из концентратора в хроматографическую колонку | 1983 |
|
SU1122969A1 |
| СПОСОБ АНАЛИЗА ПРИМЕСЕЙ МАЛОЛЕТУЧИХ ПОЛЯРНЫХ ВЕЩЕСТВ В ЖИДКИХ СРЕДАХ | 2018 |
|
RU2698476C1 |
| Газовый хроматограф | 1989 |
|
SU1689844A1 |
| Устройство подготовки пробы для анализа примесей малолетучих полярных веществ в жидких средах | 2018 |
|
RU2697575C1 |
| Способ твердофазного концентрирования комбинации водорастворимых летучих и нелетучих пластовых индикаторов | 2019 |
|
RU2720656C1 |
| Способ газохроматографического ана-лизА МиКРОпРиМЕСЕй ВЕщЕСТВ B ВОздуХЕ | 1979 |
|
SU842576A1 |
| Устройство для анализа примесей в водороде | 1978 |
|
SU767641A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СООТВЕТСТВИЯ ХРОМАТОГРАФИЧЕСКИХ ПИКОВ ОДНОМУ И ТОМУ ЖЕ КОМПОНЕНТУ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2014 |
|
RU2556759C1 |
| Способ хроматографического анализа примесей газов в водороде и устройство для его осуществления | 1987 |
|
SU1408360A1 |
Изобретение относится к аналитической химии, в частности к газохроматогра- фическим методам анализа микропримесей органических веществ в газах. Цель изобретения - повышение точности и стабильности результатов анализа во времени за счет исключения влияния растворителя на разделительные свойства хроматографической колонки. В способе хроматографического анализа микропримесей в газе микропримеси концентрируют с использованием растворителя в качестве экстрагента с последующим разделением паров экстракта на хроматографической колонке и детектированием разделенных компонентов экстракта. Разделение паров экстракта осуществляется в капиллярной трубке в потоке газопаровой подвижной фазы, образованной путем насыщения газа-носителя парами растворителя, используемого для экстракции микропримесей, находящихся в контакте с пленкой конденсата этого растворителя на внутренних стенках капиллярной трубки, при этом температуру трубки поддерживают ниже температуры испарения растворителя. 2 з.п. ф-лы, 4 ил. (/ С
W3 // oo/f-eoj
ЛЈГШЈ Н&
О
si
вSJ.
3 6.
| Справочник по физико-химическим методам исследования объектов окружающей среды | |||
| Под ред | |||
| Г.И | |||
| Арановича | |||
| - Л.: Судостроение, 1979, с | |||
| Говорящий кинематограф | 1920 |
|
SU111A1 |
| То же, с | |||
| Прялка для изготовления крученой нити | 1920 |
|
SU112A1 |
Авторы
Даты
1992-05-15—Публикация
1987-07-29—Подача