да, в течение 1,5 мин. После гибридизации и отмывания клеток от полиэтиленгликоля, клетки высевают в 96-луночные панели по 1 105спленоцитов в лунку. Для культивирования и селекции гибридом используют среду IMDM (модифицированная Iskove s среда Дульбекко) с добавлением 10% эмбриональной телячьи сыворотки (ЭТС), 10 М гипоксантина, 4 М аминоптерина и 1,6 М тимидина. Гибриды-продуценты клонируют один раз методом конечных разведений, высевая по 1 клетке на лунку, содержащую клеток селезенки. После клонирования практически 100% субклонов продуцируют МКА к ра-ФНО. Продукция антител сохраняется как минимум в течение 15 пассажей в культуре. Штамм получил условное обозначение ЮРМ.Он хранится в ЭТС с добавлением 10% диметилсульфок- сида в жидком азоте. Штамм продуцирует МКА G2a изотипа, обладающие специфичностью к а-ФНО человека, Секреция моно- клональных антител на 3-4 день культивирования составляет 100-125 мкг/мл культуральной среды.
Использование штамма иллюстрируется следующими примерами.
Пример 1. Гибридные клетки помещают в стеклянный флакон объемом 50 мл по клеток в 5 мл среды IMDM с 10% ЭТС, 2мМ L-глютамина, 100 мкг/мл пенициллина и стрептомицина, 0,05 мМ меркап- тоэтанола. Клетки культивируют 2-3 дня при 37°С в атмосфере 5% С02. МКА выделяют из полученного супернатанта аффинной хроматографией на колонке с иммобилизиро- ванным рекомбинантным белком A St. aureus Cowan I и используют в иммунофер- ментном анализе (ИФА). ра-ФНО, р/Ј-ФНО и бычий сывороточный альбумин (БСА) в количестве 0,3 мкг в 100 мкл 0,1 М карбонатного буфера (рН 9,5) вносят в 96-луночные микроплаты и оставляют на ночь при 4°С. Отмывают водопроводной водой и вносят 1 мкг МКА в 100 мкл 0,1 М фосфатного буфера (рН 7,4), содержащего 0,15 М NaCI, 1 % БСА (ФСБ-БСА). Инкубируют в течение 1 ч на встряхивателе. После отмывания инкубируют с меченными пероксидазой к иммуноглобулинам мыши антителами в разведении 1:2000 на ФСБ-БСА в течение 1 ч. Ферментную реакцию проводят в течение 10 мин. Раствор субстрата представляет собой 0,1 М цитратный буфер (рН 4,7) с 0,6 мг/мл ортофенилендиамина гидрохлорида и 0,01% перекиси водорода. Реакцию останавливают через 10 мин 1М серной кислотой и учитывают на спектрофотометре с
вертикальным лучом при длине волны 492 нм.
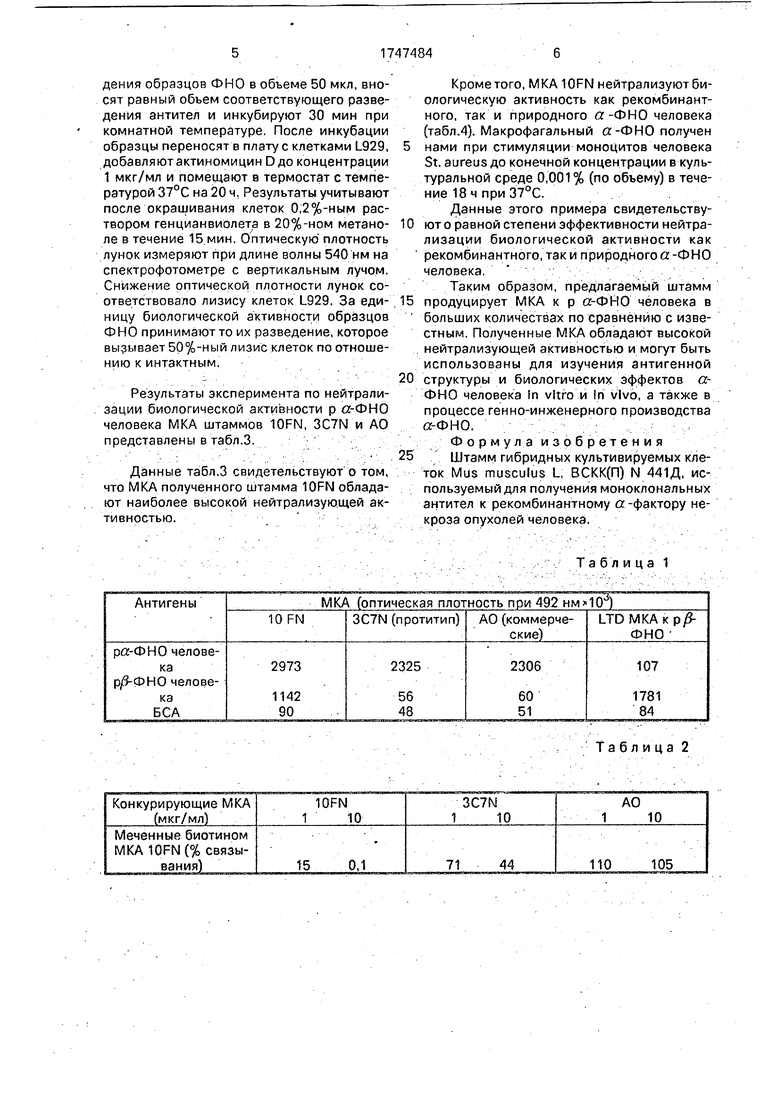
Результаты эксперимента по изучению специфичности связывания МКА, продуци руемого клетками штамма 10FN, с антигенами, иммобилизированными на пластике, представлены в табл.1.
Результаты исследований свидетельствуют о более высокой специфичности МКА,
продуцируемых клетками штамма 10FN по сравнению с прототипом, и подтверждают возможность применения данных МКА для определения ра-ФНО человека с помощью иммуноферментного анализа.
П р и м е р 2. Меченные биотином МКА используют в конкурентном ИФА с адсорбированным на твердой фазе р а-ФНО человека в присутствии двух концентраций немеченных антител.
На 96-луночной полистироловой плате для ИФА адсорбируют ра-ФНО (2 мкг/мл) в 100 мкл 0,1М бикарбонатного буфера (рН 9,5) в течение ночи при +4°С. Неспецифическое связывание блокируют раствором
ФСБ-БСА. После каждой инкубации плату пятикратно отмывают ФСБ, содержащим 0,01% Твина 20. Разведенные раствором ФСБ-БСА биотинированные МКА смешивают с различными-концентрациями немеченных антител. Смесь добавляют в лунки и инкубируют в течение 1 ч при комнатной температуре на встряхивателе. После отмывания добавляют конъюгированную с ави- дином пероксидазу (разведение 1:2000 на
ФСБ-БСА) и инкубируют в течение 1 ч. Затем плату отмывают и проводят ферментную реакцию в течение 10 мин, как указано. Результаты исследований представлены в табл.2.
Результаты, представленные в табл.2, свидетельствуют о том, что МКА 10FN в некоторой степени подавляют связывание МКА 3C7N с р а-ФНО человека, адсорбированным на пластике, и не препятствуют взаимодействию с антигеном МКА АО. Таким образом, МКА штамма tOFN и 3C7N распознают неидентичные, частично перекрывающиеся эпитопы. Эпитопы, распознаваемые МКА 10FN и АО, различны,
П р и м е р 3. Биологическую активность различных образцов ФНО определяют по лизису клеток мышиной фибробластоидной линии L929 в присутствии актиномицина D. Накануне теста клетки L929 рассевают по
50л 10 -на лунку в плоскодонные 96-луночные микроплаты в минимальной среде, модифицированной Дульбекко (ДМЕМ) с 5% ЭТС, глютамином, пенициллином и стрептомицином. В отдельной плате готовят разведения образцов ФИО в объеме 50 мкл, вносят равный объем соответствующего разведения антител и инкубируют 30 мин при комнатной температуре. После инкубации образцы переносят в плату с клетками L929, добавляютактиномицинОдо концентрации 1 мкг/мл и помещают в термостат с температурой 37°С на 20 ч. Результаты учитывают после окрашивания клеток 0,2%-ным раствором генцианвиолета в 20%-ном метаноле в течение 15 мин. Оптическую плотность лунок измеряют при длине волны 540 нм на спектрофотометре с вертикальным лучом. Снижение оптической плотности лунок соответствовало лизису клеток L929. За единицу биологической активности образцов ФИО принимают то их разведение, которое вызывает 50%-ный лизис клеток по отношению к интактным.
Результаты эксперимента по нейтрализации биологической активности р «-ФНО человека МКА штаммов 10FN, 3C7N и АО представлены в табл.3.
Данные табл.3 свидетельствуют о том, что МКА полученного штамма 10FN обладают наиболее высокой нейтрализующей активностью.
Кроме того, МКА 10FN нейтрализуют биологическую активность как рекомбинант- ного, так и природного or-ФНО человека (табл.4). Макрофагальный а-ФИО получен
нами при стимуляции моноцитов человека St. aureus до конечной концентрации в куль- туральной среде 0,001 % (по объему) в течение 18ч при37°С.
Данные этого примера свидетельству0 ют о равной степени эффективности нейтра- лизации биологической активности как рекомбинантного.таки природного с-ФИО человека.
Таким образом, предлагаемый штамм
5 продуцирует МКА к р а-ФНО человека в больших количествах по сравнению с известным. Полученные МКА обладают высокой нейтрализующей активностью и могут быть использованы для изучения антигенной
0 структуры и биологических эффектов а- ФНО человека In vitro и fn vivo, а также в процессе генно-инженерного производства а-ФНО.
Формула изобретения
5 Штамм гибридных культивируемых клеток Mus musculus L ВСКК(П) N 441Д, используемый для получения моноклональНых антител к рекомбинантному ее -фактору некроза опухолей человека.


| название | год | авторы | номер документа |
|---|---|---|---|
| Штамм гибридных культивируемых клеток животных MUS мUSсULUS - продуцент моноклонального антитела, нейтрализующего биологическую активность человеческого фактора некроза опухолей-альфа | 1987 |
|
SU1521776A1 |
| Штамм гибридных культивируемых клеток животных MUS мUSсULUS-продуцент моноклонального антитела к фактору некроза опухолей-альфа человека | 1987 |
|
SU1507791A1 |
| Штамм гибридных культивируемых клеток животных MUS мUSсULUS L - продуцент моноклонального антитела к пирофосфатазе ЕSснеVIнIа coLI | 1990 |
|
SU1712412A1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS L. CCHFV Vd-3-ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА 3H6/F2 К ВИРУСУ КРЫМ-КОНГО ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ | 2013 |
|
RU2528869C1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS L. CCHFV Vd-2-ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА 1E2/E5 К ВИРУСУ КРЫМ-КОНГО ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ | 2013 |
|
RU2528868C1 |
| Штамм гибридных культивируемых клеток животных MUS мUSсULUS - продуцент моноклональных антител к фактору некроза опухоли @ человека | 1988 |
|
SU1585329A1 |
| Штамм гибридных культивируемых клеток животных MUS мUSсULUS - продуцент моноклонального антитела к фактору некроза опухолей - альфа человека | 1987 |
|
SU1530638A1 |
| ШТАММ КУЛЬТИВИРУЕМЫХ ГИБРИДНЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS L. CCHFV VD-1-ПРОДУЦЕНТ МОНОКЛОНАЛЬНОГО АНТИТЕЛА 4G/B К ВИРУСУ КРЫМ-КОНГО ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКИ | 2013 |
|
RU2535982C1 |
| Штамм культивируемых гибридных клеток животных МUSмUSсULUS L - продуцент моноклональных антител против В-лимфоцитов крупного рогатого скота | 1988 |
|
SU1645295A1 |
| ШТАММ ГИБРИДНЫХ КУЛЬТИВИРУЕМЫХ КЛЕТОК ЖИВОТНЫХ mus musculus α-ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ, СПЕЦИФИЧНЫХ К ГРАНУЛОЦИТАРНОМУ КОЛОНИЕСТИМУЛИРУЮЩЕМУ ФАКТОРУ (GCSF) ЧЕЛОВЕКА | 2013 |
|
RU2542381C2 |

Таблица 1
Таблица 2
)-выражена в ME p а-ФНО человека, нейтрализуемых 1 мкг Jq G
)-активность макрофагального а-ФНО человека составляет 235 ME/мл
) концентрация р-а-ФНО человека составляет Юнг/мл, что соответствует 750 МЕ/мл
Таблица 3
Таблица 4
Авторы
Даты
1992-07-15—Публикация
1991-01-28—Подача