Изобретение относится к получению сплавов из цветных металлов, а именно к производству медно-бериллиевых сплавов с применением при плавке специальных средств для рафинирования и окисления расплава.
Известны способы получения искусственных силикатов в виде шлаков, содержащих окислы металлов. Такие шлаки образуются вследствие растворения окислов металлов в силикатном флюсе, например в стекле. Такие флюсы обычно применяются для защиты расплава от окисления и его рафинирования (Авт. св. СССР N 1046315, кл. C 22 C 1/06, 1983, патент ФРГ N 2246723, кл. C 22 C 1/06, 1973 и др.). Полученные таким образом шлаки в своем составе имеют низкое содержание металлов и представляют поэтому промышленные отходы.
При плавке грязной медно-бериллиевой шихты под флюсом из стеклянного боя и ведением в расплав рафинирующей добавки в виде кремния (авт.св. СССР N 1431347, кл. С 22 С 1/06, 1987) содержание бериллия в искусственном силикате становится уже значительным, однако этот способ не обеспечивает заданного химического состава силиката из-за невозможности управления процессом рафинирования расплава.
Целью изобретения является полная безотходность технологии для утилизации различных ломов и отходов медно-бериллиевых бронз. Благодаря этому способу полученные слитки можно использовать для производства промышленной продукции или товаров народного потребления, а силикатные шлаки как сырье для повторного извлечения бериллия либо производства силикатных изделий, так как оксид бериллия в силикате обеспечивает ему высокий коэффициент светопреломления, что обеспечивает высокое качество таких товаров.
Сущность предлагаемого способа получения медно-бериллиевых сплавов и шлаков состоит в том, что подбором состава шихты и плавкой ее в индукционной или тигельной печи под флюсом из стеклянного боя и рафинирующей добавки на поверхность расплава в виде кусков кристаллического кремния получают шлак, состоящий из силиката бериллия заданного состава. Для ускорения процесса шлакообразования расплав продувается кислородсодержащим газом. С целью обеспечения нужной окраски силиката бериллия в расплав вводятся микродобавки элементов, окислы которых окрашивают стекла в различные цвета. К таким элементам относятся хром, никель, кобальт, железо, редкоземельные элементы и т. д.
В природе известно более 20 минералов бериллия в виде окислов, причем их большая часть представляет собой силикаты. В промышленном отношении наиболее важными из них являются фенакит и берилл, которые служат основным сырьем для производства бериллия. Кроме того, окрашенные природные минералы бериллия образуют большую группу драгоценных камней.
Если представить состав минералов бериллия в форме окислов, то нетрудно заметить, что их состав подобен обычным силикатным стеклам. Фенакит (2ВеO˙SiO2), берилл (3BeO˙Al2O3˙6SiO2), бертрандит (ВеO˙BaO˙2SiO2)
и другие природные силикаты бериллия состоят из окислов, растворенных в кремнеземе. Если растворяют окись бериллия в стекле, то получают искусственный силикат, подобный природным минералам бериллия. Процесс растворения окислов металлов в стекле можно показать с точки зрения "дырочной" проводимости полупроводников.
Обычное стекло представляет собой переохлажденную жидкость, кристаллизация в которой не успела произойти из-за быстрого нарастания вязкости при охлаждении. Вследствие этого оно обладает некоторым запасом внутренней химической энергии, которая начинает проявляться при нагревании. С повышением температуры вязкость стекла уменьшается, а химическая энергия возрастает. Это проявляется в способности стекла растворять в себе окислы металлов (2, 3).
Основу любого силиката в том числе и стекла составляют кремнийкислородные тетраэдры SiO40, образующие сложные цепные, плоские и объемные структуры, которые при нагревании дисоcoциируют с образованием активных радикалов кремнезема SiO31+,SiO22+,SiO23+. В местах обрыва ковалентных связей образуются положительно заряженные "дырки", которые представляют собой обнаженные, не занятые кислородом атомы кремния в активном кремнеземе. В зависимости от сродства к кислороду, эти атомы кремния способны либо восстанавливать металл из окисла, либо присоединять к себе поляризованные диполи через кислород окисла.
В результате термического разложения стекла увеличивается свободная энергия Гиббса, которая равна (4)
E 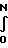 U·
U· 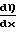 ·dx
·dx
где N число "дырок";
U энергия "дыркообразования";
η- степень порядка;
х переменное число "дырок".
Степень порядка равна
η 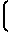 1-e
1-e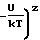
где К газовая постоянная;
Т абсолютная температура;
Z координационное число решетки.
Переменное число "дырок" определяется по формуле
х=N(η1/2-1).
"Дырки" в стекле создают положительное электрическое поле, под действием которого происходит поляризация диполей окислов металлов, всплывающих на поверхность расплава. Поляризованные диполи создают двойной электрический слой, состоящий из положительно заряженных концов диполей из металла, направленных в сторону расплава, и отрицательных концов из кислорода, направленных в сторону стеклянного флюса.
Максимальное значение напряженности электрического поля, создаваемого поляризованными диполями составит (4)
Eo= 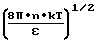 где n число диполей на единицу поверхности;
где n число диполей на единицу поверхности;
ε- диэлектрическая постоянная.
Если теперь приравнять свободную энергию Гиббса и значение напряженности электрического поля, создаваемого поляризованными диполями окислов металлов, то получим условие равновесия между флюсом и окислами металлов (шлаком) на поверхности расплава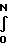 U·
U· 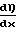 ·dx
·dx 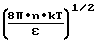
Отсюда минимальное число диполей на единицу поверхности расплава
n 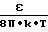
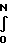 U2·
U2· 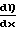 ·dx
·dx
При наличии на поверхности расплава двойного электрического слоя, состоящего из флюса и окислов металлов в шкале, по аналогии с полупроводником имеются две валентных зоны: зона проводимости, состоящая из положительно заряженных "дырок", и валентная зона, состоящая из отрицательных концов диполей окислов металлов. Как и в полупроводнике, здесь существует и запрещенная зона, величина которой зависит от свойств и состояния флюса. Из физики полупроводников известно, что изолятор становится полупроводниковым только тогда, когда ширина запрещенной зоны по своей величине не менее 4 эВ. Ширина запрещенной зоны (5) равна
ΔЕ=Е2-Е1, где Е2 напряженность поля в зоне проводимости, Е2=Е;
Е1 напряженность поля в валентной зоне, Е1=Ео.
Тогда условие растворимости окислов металлов в силикатах следующее
ΔE 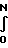 U·
U· 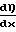 ·dx-
·dx-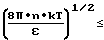 4эВ
4эВ
В результате "дырочной" проводимости поляризованные окислы заполняют "дырки", в которых кремний присоединяет к себе атом металла через кислород окисла. Способность изоляторов становиться полупроводниками при нагревании, видимо, объясняется образованием в них "дырок", нейтрализуемых электронами.
При нейтрализации активного кремнезема, например, в форме SiO22+ двумя молекулами окиси бериллия BeO1- образуется фенакит 2ВеO˙SiO2 и стекло снова становится изолятором, а вследствие исчезновения электрического поля в зоне проводимости, происходит располяризация диполей окислов металлов в шлаке. Чтобы флюс снова сделать полупроводником, нужно образовать новые дырки, повысив температуру расплава. Другим эффективным способом образования "дырок" является введением кремния на поверхность расплава.
Легко восстанавливая окислы меди и окисляясь, кремний образует активный кремнезем, "дырки", которые находятся непосредственно в слое окислов. Окислы металлов, которые не восстанавливаются кремнием, например, бериллий, под действием молекул активного кремнезема поляризуются, вступают в ковалентную связь и образуют молекулы фенакита. Если в шихту, состоящую из бериллиевой лигатуры, добавить алюминий и продуть расплав, то в шлаке будет образовываться берилл (Be3Al2Si6O8).
В результате химических реакций в поверхностном слое расплава по окислению кремния и "связывания" поляризованных диполей окислов металлов между флюсом и расплавом идет процесс стеклообразования, в результате которого новое стекло (силикат бериллия), наращивается на нижнюю поверхность силикатного флюса. Для увеличения скорости процесса стеклообразования, расплав окисляется кислородом или воздухом, которые можно вводить в расплав всеми известными способами.
Примером практического выполнения способа получения медно-бериллиевых сплавов и шлаков может служить плавка различной шихты медно-бериллиевой бронзы БрБ-2 в соответствии с технологической инструкцией ТИ 1-2-82 "Плавка и отливка плоских слитков бериллиевой бронзы на установке полунепрерывного литья".
Всего было выполнено 150 плавок, которые позволили определить дозировку флюса и кремния при работе на индукционной печи ИЛК-1,6, а также выяснить некоторые закономерности образования искусственного силиката бериллия.
По технологической инструкции процесса плавки шихты и отливки слитков проходил при 1180-1200оС. Шихта представляла собой грязные возвратные лома из мелких деталей приборов, сечки и обрезков тонких лент с значительным содержанием машинного масла и посторонних включений. После загрузки шихты на ее поверхность засыпался стеклянный бой в количестве 30 кг, а после расплавления шихты под флюс вводился кремний весом 2,5 кг. Технологический цикл получения слитка составлял 60 мин. Общий вес шлака составил 48 кг, а после отделения сплесов и корольков бронзы 41 кг. Таким образом, увеличение веса силикатного флюса после плавки получилось равным 11 кг.
Полученный силикат бериллия представляет собой неоднородную массу, состоящую из прозрачного стекла со стороны верхней части печи и с оранжевой окраской разных оттенков со стороны расплава. Содержание бериллия в прозрачном силикате составляет 0,12 и окрашенном 1,65% Меняется и содержание железа: от 0,04 до 0,25% в оранжевом силикате. Полученный силикат бериллия легко измельчается, что позволяет вести его механическую обработку. Ручная сортировка силиката по цвету определила содержание окрашенной части в количестве 18 кг или около 50% от общего веса силиката. Прозрачную его часть в количестве 23 кг можно использовать повторно в качестве флюса, а окрашенную для производства силикатных изделий.
В опытных плавках окислителем шихты служило машинное масло, а окрашивающим элементом железо. Окисление расплава кислородсодержащим газом с использованием подшихтовки расплава медно-бериллиевой лигатурой по мере выгорания бериллия, позволит практически беспредельно увеличивать его содержание в силикате, а использование других красящих элементов или их сочетаний получать силикаты разного цвета.
Предлагаемый способ получения медно-бериллиевых сплавов и шлаков представляет собой безотходную технологию, которая позволяет утилизировать различные лома и отходы медно-бериллиевых сплавов. Это даст не только высокий экономический, но и экологический эффект.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОИЗВОДСТВА КОЛОКОЛОВ | 1992 |
|
RU2064520C1 |
| СПОСОБ ПЕРЕРАБОТКИ БЕРИЛЛИЙСОДЕРЖАЩИХ ОТХОДОВ | 2014 |
|
RU2558588C1 |
| Флюс для плавки бериллиевой бронзы | 1983 |
|
SU1129261A1 |
| Способ переработки медных и медно-цинковых сульфидных концентратов | 1982 |
|
SU1312115A1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ БЕРИЛЛИЯ ИЗ БЕРИЛЛИЙСОДЕРЖАЩИХ КОНЦЕНТРАТОВ | 1996 |
|
RU2107742C1 |
| СПОСОБ РАФИНИРОВАНИЯ МЕДИ И СПЛАВОВ НА МЕДНОЙ ОСНОВЕ | 2000 |
|
RU2185455C1 |
| Способ плавки сульфидно-кремнистой медной руды | 1982 |
|
SU1036778A1 |
| СПОСОБ ОГНЕВОГО РАФИНИРОВАНИЯ МЕДИ | 2009 |
|
RU2391420C1 |
| СПОСОБ ПЕРЕРАБОТКИ БЕРТРАНДИТ-ФЕНАКИТ-ФЛЮОРИТОВЫХ КОНЦЕНТРАТОВ | 2006 |
|
RU2324653C2 |
| СПОСОБ ПЕРЕРАБОТКИ БЕРИЛЛИЙСОДЕРЖАЩИХ КОНЦЕНТРАТОВ | 2006 |
|
RU2309122C2 |
Изобретение относится к получению сплава из цветных металлов, конкретно к производству медно-бериллиевых сплавов с применением при плавке специальных средств для рафинирования и окисления расплава. Цель изобретения получение в шлаке силикатов бериллия. Плавку шихты под флюсом из стеклянного боя и с рафинирующей добавкой в виде кускового кристаллического кремния ведут с продувкой расплава кислородсодержащим газом, причем в качестве газа может использоваться воздух. Для получения нижнего цвета силиката бериллия в шихту вводятся микродобавки элементов, например хром, никель, окислы которых кобальт, железо и др. окрашивают стекла в различные цвета. Использование изобретения позволяет получить до 50% силикатного шлака, содержащего 1,65% бериллия.
| Авторское свидетельство СССР N 1431347, кл | |||
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
Авторы
Даты
1995-10-27—Публикация
1990-04-27—Подача