Изобретение относится к улучшенному способу получения 1,4-дихлоразопро- изводных диарилбутадиена-1,3 общей Формулы I
где при R - H, X-N, Ri-H, СНз, ОСНз, С, N(CH3)2, СеН5;
при R - Ri-СНз. ОСНз, М(СНз)2. CI, X-N;
приР-СбНб, R1-H.X-CH; которые используются в качестве полупродуктов синтеза люминофоров, сцинтиллято- ров и лазерных красителей, относящихся к группе диарилпроизводных, оксазола, окса- диазола, имидазола и триазола.
Известен способ получения бис-(а-хлор- бензилиден)гидразина, заключающийся во взаимодействиидибензаилгидразина с PCI5 при нагревании сухой смеси реагентов при температуре 110-130°С. После охлаждения
реакционную смесь экстрагируют зфиром, эфирный слой обрабатывают льдом для разложения избытка PCIs и образующегося , затем промывают раствором №НСОз. После отгонки эфира получали целевой продукт с выходом не превышающим 60%.
Недостатком известного способа является заниженный выход продукта реакции.
Наиболее близким к описываемому является способ получения 1,4-дихлора- зопроизводных диарилбугадиена-1,3 заключающийся во взаимодействии диароилгидразина с PCIs при нагревании до 110-120°С в о-дихлорбензоле.
К недостаткам указанного способа относятся довольно низкий выход и значительная загрязненность целевого продукта, что требует увеличения количества стадий очистки, на каждой из которых неизбежны потери. Кроме того, соединения несимметnvwAt
Xj
о
00 СЛ 00 00
ричного строения () по данному способу получить не удается.
Целью настоящего изобретения является обеспечение возможности получения соединений как симметричного () так и несммметричногб (R/Ri) строения, а также повышение выхода и чистоты целевого продукта.
Поставленная цель ДОсТй гается тем, что
ппм лгм ЛПЯЪМнЬ S/f. ta №-ЯППМЛЯМ /|НПЯНЙдиароилгидразйнЈ| и л й М-ароиламиноаце- тофеноны общей формулы
5 i
(o)iN-x-cto)-( ,
где R, R , X - как указано выше, подвергают взаимодействию с SOCI2 или С20лС12 в среде SOCia или С 02С12,ззятыу в количестве, | .}е°опиакк ем 1ческое в t 10 рез при 50-80°С до прекращения выделения i чзообразных продуктов с последующим удалением остатка непрореагировавшего хлорирующего агента под вакуумом до получения целевого продукта в кристаллическом состоянии.
Пример 1 0.01 моль (2,4 г) дибен- зоиггидразина смешивают с 10 мл (0,139 моль ,7-кратный избыток) тионилхлорида. Смесь чэгревают в колбе с обратным холодильником и кипятят при температуре 75°С до прекращения выделения хлоро- водорода и сернистого газа, на что т ре буется время 15 мин Затем избыток тионилхлорица удаляют под вакуумом при температуре бани 30-50°С до получения продукта в кристаллическом виде Получено 2,7 г(97 4%) 1 4-дифенил-2,3-ди- азо-1,4-дихлорбу тадиена- , 3 с температурой плавления 123-124°С
Пример 2 0,01 моля (2,4 г) дибензо Ш1гидразина смешивают с 7 мл (0,1 МОЛР, 5 кратный избыток) тионилхлорида Смесь нагревают в колбе с обратным холодильником при 80°С до прекращения выделения хлороводорода и сернистого газа, на чго требуется время 15 мин Затем избыток тионилхлорида удаляют под вакуумом при температуре бани 40-50°С до получения продукта в кристаллическом состоянии Получено 2,6 г (96 2%) 1,4-дифенил-2 3 диа- зо-1,4-дихлорбутадиена-1,3 с температурой плавления 123-124°С.
Пример 3 0,01 моля (2,4 г) дибен- зоилгидразина смешивают с 15 мл (0,2 моля, 10-кратный избыток) тионипхлори- да Смесь нагревают в колбе с обратным холодильником при температуре 60°С до прекращения выделения хлороводорода и сернистого газа, на что требуется время 30 мин Затем избыток тионилхлорида
удаляют под вакуумом при температуре бани 40-50°С до получения продукта в кристаллическом состоянии. Получено 2,65 г (96,9%) 1,4-дифенил-2,3-диазо-1,4-дихлорбутадиена-1,3 с температурой плавления 123-124°С.
Пример 4. 0,01 моля (2,7 г) 1-бензо- ил-2-анизоилгидразина смешивают с 10 мл (0,139 моля, 7-кратный избыток) тионилхло0 рида. Смесь нагревают в колбе с обратным холодильником и кипятят при температуре 75°С до прекращения выделения хлороводорода и сернистого газа, на что требуется время 20 мин. Затем избытоктионилхлори5 да удаляют под вакуумом при температуре бани 40-50°С до получения продукта в кристаллическом виде. Получено 3,0 г (97,7%) 1-фенил-4-анизил-2,3-диазо-1,4-дихлорбут- ,,3 с температурой плавления 1150 116°С.
Пример 5. 0,01 моля (3,9 г) N-бензо- иламиноацетофенона смешивают с 12 мл (0,14 мел 7-крагный избыток) оксалилхло- рида. Смесь нагревают в колбе с обратным
5 холодильником и кипятят при 65°С до прекращения выделения хлороводорода, углекислого газа и окиси углерода, на что требуется время 30 мин. Затем избыток ок- салилхпорида удаляют под вакуумом при
0 температуре бани 40-50°С до получения продукта в кристаллическом виде. Получено 2,63 г (95,2%) 1,4-дифенил-2-азо-1,4 дихлор- бутадиена-1,3 с температурой плавления 146-147°С.
5 Пример 6 0,01 моля (3,16 г) 1-бензо- ил-2-(4-фенил бен зоил гидразин а) смешивают с 17 мл (0,2 моля, 10-кратный избыток) оксалилхлорида. Смесь нагревают в колбе с обратным холодильником и кипятят при
0 80°С до прекращения выделения хлороводорода, углекислого газа и окиси углерода, на что требуется время 25 мин. Затем избыток оксалилхлорида удаляют под вакуумом при температуре бани 40-50°С до получения
Ь продукта в кристаллическом виде Получено 3,45 г (97,7%) 1-фен1 л-4-бифенилил-2 3-диа- зо-1 4-дихлорб/тадиена-1,3 с температурой ПЛРВГСНИЯ 182-183°С
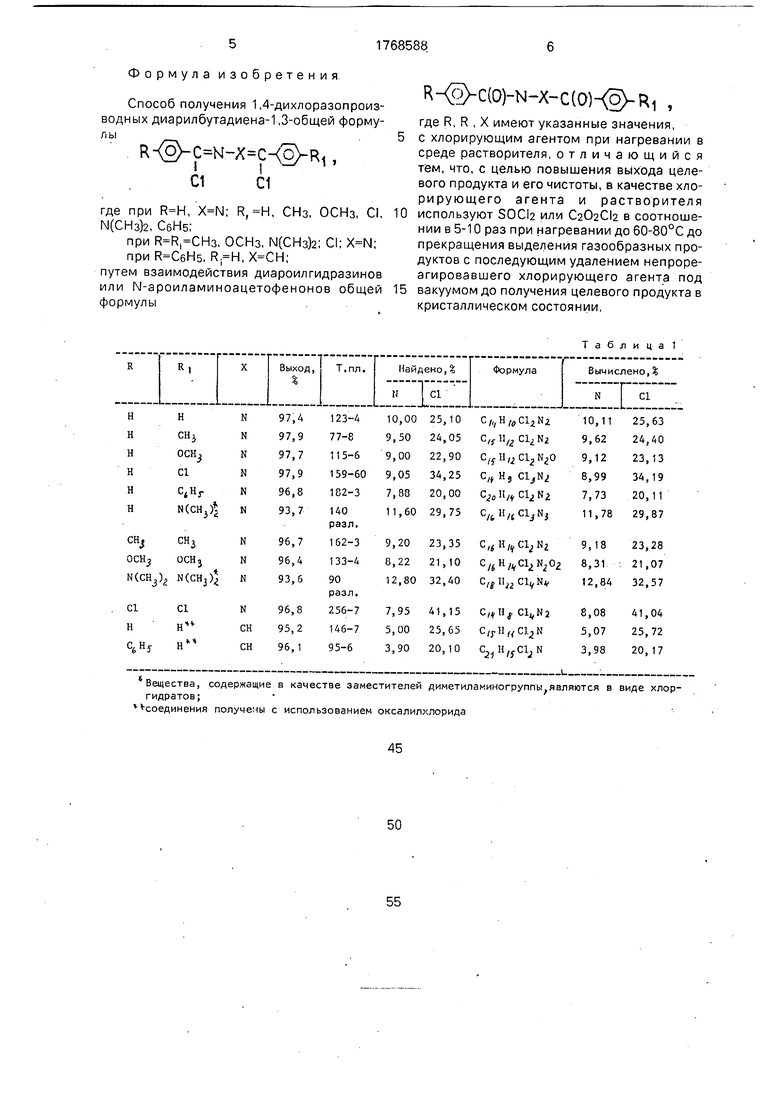
Другие соединения получаются анало0 гично Полученные вещества представляют собой светло-желтые кристаллы, обладающие резким запахом и дымящие во влажном воздухе Характеристики полученных веществ приведены в табл.1.
5Качество продукта определялось методом ТСХ на пластинках Silufo UV-254 (злюечт - хлороформ). Содержание основного вещества не менее 99,5%.
В табл 2 приведены ИК-спектры впервые полученных соединений.
Формула изобретения
Способ получения 1,4-дихлоразопроиз- водных диарилбутадиена-1,3-общей формулы
RX2), С1С1
где при , R, H, СН3, ОСНз, CI, М(СНз)2, C6H5;
при ,CH3, ОСНз, N(CH3)2; CI;
при , RpH, путем взаимодействия диароилгидразинов или 1 1-ароиламиноацетофенонов общей формулы
0
5
(0)-N-X-C(0) ,
где R, R , X имеют указанные значения, с хлорирующим агентом при нагревании в среде растворителя, отличающийся тем, что, с целью повышения выхода целевого продукта и его чистоты, в качестве хлорирующего агента и растворителя используют SOCI2 или CaOaCIa в соотношении в 5-10 раз при нагревании до 60-80°С до прекращения выделения газообразных продуктов с последующим удалением непрореагировавшего хлорирующего агента под вакуумом до получения целевого продукта в кристаллическом состоянии,


| название | год | авторы | номер документа |
|---|---|---|---|
| Твердый каталитический компонент для полимеризации олефинов и катализатор полимеризации олефинов | 1989 |
|
SU1836384A3 |
| Способ получения поли-N-хлорированных бициклических мочевин | 1989 |
|
SU1675300A1 |
| ДИАМИДЫ 4,7-ДИЗАМЕЩЕННЫХ 1,10-ФЕНАНТРОЛИН-2,9-ДИКАРБОНОВЫХ КИСЛОТ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ЭКСТРАКЦИОННАЯ СМЕСЬ НА ИХ ОСНОВЕ | 2014 |
|
RU2601554C2 |
| Способ получения аминопроизводных 1,2-дифенил-1,1,2.2-тетрафторэтана | 1971 |
|
SU497766A3 |
| Способ получения органовинил(гидрид)циклосилоксанов | 1973 |
|
SU457706A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2 КАРБАМИД- ,3-ОКСИБЕНЗОФУРАНА | 1972 |
|
SU332626A1 |
| Способ получения органических изоцианатов | 1974 |
|
SU550381A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПЕРФТОРМЕТАКРИЛОВОй КИСЛОТЫГ.. асЁСО^сзнАЯ,ГЛаТ1^0-Т;1ШВШБИЕ-Л^'О:Т:- | 1973 |
|
SU379567A1 |
| Способ получения вицинально-замещенных 3-гидроксиламинопиридинов | 1990 |
|
SU1745721A1 |
| Способ получения производных бензиламина или их солей | 1973 |
|
SU571188A3 |
Сущность изобретения: продукт 1,4- дихлоразопроизводные диарилбутадиен- 1,3 ф-лы 1 )(ci), где при R H, X N; , СНз, ОСНз, CI М(СНз)2: СбН5 при R R СНз ОСНз, М(СН3)2, CI, X N; при R СбН5, Ri H, X CH. Реагент 1- RH((0)-N-X-C(0), , где R, R , X - как указано выше Реагент 2. SOCI2 или C2C2CI2. Условия реакции: в среде SOCI2 или C202CI2 при 60-80°С 2 табл
Вещества, содержащие в качестве заместителей диметиламиногруппы;являются в
гидратов; соединения получены с использованием оксалилхлорида
Т а б л и ц а 1
виде хлорТаблица 2
| R Stolbe, i Pract.Chem., 1906, b.73, стр 288 Патент Великобритании N 970480, кл | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
1992-10-15—Публикация
1989-10-31—Подача